更新于:2023-12-10

Imeik Technology Development Co., Ltd.
更新于:2023-12-10
概览
标签
其他疾病
毒素
关联
1
项与 爱美客技术发展股份有限公司 相关的药物作用机制 SNAP抑制剂 |
原研机构 |
非在研适应症- |
最高研发阶段临床3期 |
首次获批国家/地区- |
首次获批日期- |
1
项与 爱美客技术发展股份有限公司 相关的临床试验多中心、双盲、随机、平行、阳性对照的Ⅲ期试验,评价注射用A型肉毒毒素HUTOX相较于BOTOX®在中度至重度眉间纹受试者中的有效性和安全性
主要目的:评价在中国的中至重度眉间纹成年受试者中,使用试验药品 Huons BioPharma Co., Ltd.生产的注射用A型肉毒毒素(HUTOX)在注射后4周 的最大皱眉时眉间纹改善率是否非劣于对照药品BOTOX ®
开始日期- |
申办/合作机构  爱美客技术发展股份有限公司 爱美客技术发展股份有限公司 [+1] |
100 项与 爱美客技术发展股份有限公司 相关的临床结果
登录后查看更多信息
0 项与 爱美客技术发展股份有限公司 相关的专利(医药)
登录后查看更多信息
87
项与 爱美客技术发展股份有限公司 相关的新闻(医药)2023-12-04
·创鉴汇
▎药明康德内容团队编辑据创鉴汇不完全统计,上周(11月27日至12月3日)全球大健康领域共披露融资事件27起,总额超27亿元。按照金额划分,亿元及以上融资9起,潜在最高融资额来自圣因生物的超8000万美元A+轮融资。按照已披露的融资轮次划分,早期融资(B轮以前)15起,中后期融资(B轮及以后)3起。生物制药领域共12家公司获融资,其中6家来自中国,涉及药物类型包含RNAi疗法、多肽药物、基因编辑药物等。#01圣因生物完成超8000万美元A+轮融资关键词:RNAi疗法最新融资:超8000万美元A+轮本轮投资机构:北极光创投(Northern Light Venture Capital)、启明创投(Qiming Venture Partners )、上海生物医药基金(Shanghai Healthcare Capital)、深圳市创新投资集团(Shenzhen Capital Group)、腾讯投资、元生创投(YuanBio Venture Capital)等近日,圣因生物(SanegeneBio)宣布完成超八千万美元(近6亿元人民币)的A+轮融资,本次募集资金将主要用于加速公司针对心血管及代谢性疾病、免疫介导性疾病等药物管线的IND申报和临床试验,以及推进肝外递送平台的建设和药物开发。圣因生物成立于2021年,致力于开发新型RNAi疗法。成立之初便迅速建立了核酸药物化学修饰平台和肝内肝外递送技术平台,并基于LEAD(Ligand and Enhancer Assisted Delivery)平台布局多款药物管线,治疗领域覆盖心脑血管及代谢疾病、免疫介导性疾病、神经系统疾病等。其中,用于治疗高胆固醇血症的1类新药SGB-3403已在中澳两地进入临床试验阶段,1款产品已递交澳洲IND申请,2款产品处于IND-enabling阶段,其他管线也同步推进中。#02质肽生物完成近2亿元B+轮融资关键词:重组蛋白质药物最新融资:近2亿元B+轮本轮投资机构:爱美客、成都科创投、嘉远基金、晋成基金、蓝驰创投(BlueRun Ventures)、中美绿色基金11月27日,质肽生物宣布完成近2亿元人民币B+轮融资。据悉,本轮融资募集资金将主要用于推动质肽生物创新药和生物类似药相关管线的临床试验进度。质肽生物成立于2018年,专注于依托大肠杆菌技术平台开发重组蛋白质药物。据新闻稿介绍,该公司产品管线已达10条以上,围绕GLP-1靶点在代谢病领域中的适应症进行研发。其中,该公司研发的新型超长效GLP-1受体激动剂ZT002已在澳洲完成针对成人2型糖尿病血糖控制适应症的1期临床研究,并已经在中国获得成人2型糖尿病血糖控制、成人肥胖或者超重患者的减重治疗以及阿尔茨海默病三大适应症的临床许可。ZT002为GLP-1类似物分子,通过分子设计优化拥有较长的半衰期,有望实现每月仅需注射1次,可极大降低给药频次,有效提高患者的依从性,减轻患者因频繁注射带来的痛苦。#03尧唐生物完成超亿元A+轮融资关键词:基因编辑药物最新融资:超亿元A+轮本轮投资机构:德诚资本(Decheng Capital)、广州产投资本(Guangzhou Industrial Investment and Capital)、华方资本11月30日,尧唐生物宣布完成超亿元人民币A+轮融资,自去年8月完成超亿元人民币A轮融资后,该公司再次斩获超亿元融资。至此,尧唐生物A轮系列融资近3亿元。尧唐生物专注于结合mRNA体内递送技术和基因编辑技术,通过对CRISPR、碱基编辑和其他新一代基因编辑工具的持续开发和优化,对新一代mRNA生产平台和脂质纳米载体组装工艺的创新型改进,致力于开发针对遗传性疾病和心血管疾病的体内基因编辑药物。目前,尧唐生物首个体内基因编辑药物管线YOLT-201已经完成毒理药理研究,已经于近期向中国国家药监局(NMPA)递交了YOLT-201的IND申报文件,有望开启基于mRNA-LNP递送的体内基因编辑药物的注册临床试验。#04恒赛生物完成亿元级A轮融资关键词:树突细胞疫苗最新融资:亿元级A轮本轮投资机构:富汇创投、凯骑康盈、勤智资本(Triwise CAPITAL)11月27日,恒赛生物(KOUSAI)发布新闻稿称,继去年完成数千万融资后,今年再次完成亿元级A轮融资。恒赛生物成立于2018年,致力于树突细胞疫苗(DC疫苗)研发与产业化。该公司已构建Eco-DCVax平台,旨在打破产业化技术壁垒、开发全球创新的安全高效、给药便利的高品质DC疫苗产品。恒赛生物开发的治疗性树突细胞疫苗,有望为复发/难治性肿瘤、慢性病毒感染、自身免疫性疾病等临床亟需有效治疗手段的疾病提供治疗新途径、新策略。目前,该公司已和多家海内外科研机构和三甲医院建立稳定的合作关系,正在进行中美双报,开展临床研究和技术合作,以全面验证DC疫苗的临床安全性和有效性。#05动肽医药完成800万美元种子轮融资关键词:多肽药物最新融资:800万美元种子轮本轮投资机构:成为资本(Chengwei Capital)12月1日,动肽医药(Perpetual Medicines)宣布已完成800万美元的种子轮融资,以推进高度整合的计算设计-自动化合成多肽药物发现平台。动肽医药是一家基于高度整合的计算设计-自动化合成平台的多肽药物研发公司,旨在构建下一代多肽药物发现引擎。公司的平台结合了尖端计算物理方法和下一代人工智能技术的预测能力,与先进的合成化学相结合,以探索广阔未开发的多肽化学空间。该平台旨在解决以往难以成药的靶点和疾病领域,加速发现过程,并提高多肽候选药物质量。目前,动肽医药在中国上海和美国波士顿均设有运营机构。读者们请星标⭐创鉴汇,第一时间收到推送免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。版权说明:本文由药明康德内容团队根据公开资料整理编辑,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转发/复制至其他平台。转发授权请在「创鉴汇」微信公众号留言联系我们。更多数据内容推荐点击“在看”,分享创鉴汇健康新动态
临床申请临床1期基因疗法
2023-11-30
·今日头条
本期看点
① 奥赛康药业启动ASKB589注射液胃癌3期临床
② 默沙东抗生素头孢洛生他唑巴坦钠在华申报上市
③ 质肽生物完成近2亿元B+轮融资
④ Alladapt食物过敏药ADP101获FDA快速通道认定
⑤ Sosei Heptares重新获得IBD药物GSK4381406所有权
⑥ 淇嘉科技完成首轮融资
① 奥赛康药业启动ASKB589注射液胃癌3期临床
作者:医药观澜
解读:orchid
来源:医药观澜
发布日期:2023-11-28
■ 内容要点
近日,中国药物临床试验登记与信息公示平台官网显示,奥赛康药业已经启动ASKB589注射液的3期临床研究。此次研究旨在评价ASKB589注射液联合化疗及PD-1抑制剂,
一线治疗CLDN18.2阳性、不可切除的局部晚期复发性或转移性胃及胃食管交界处腺癌患者有效性和安全性问题。
该研究的主要终点指标为独立中心审评委员会评估的无进展生存期,主要研究者为北京大学肿瘤医院沈琳教授,拟在中国入组780人。
研究显示,50%-80%的胃癌患者和60%的胰腺癌患者肿瘤细胞中存在CLDN18.2高表达现象,这使得CLDN18.2成为消化道肿瘤靶向治疗的理想靶点。
ASKB589注射液是抗体依赖细胞介导毒作用(ADCC)增强型的第二代抗CLDN18.2人源化单克隆抗体。该产品对CLDN18.2的亲和力和特异性更高,能转化为更强的ADCC和补体依赖的细胞毒性作用。在2期临床研究中,该产品经研究者确认的疾病控制率达95.8%。
原文链接:
https://mp.weixin.qq.com/s/1yDe1nxA8WM_3we6G9Ektw
② 默沙东抗生素头孢洛生他唑巴坦钠在华申报上市
作者:医药魔方
解读:orchid
来源:医药魔方Info
发布日期:2023-11-27
■ 内容要点
11月27日,国家药品监督管理局药品审评中心网站显示,默沙东抗生素二联复方注射用头孢洛生他唑巴坦钠在华申报上市。
根据临床试验进展,推测此次申报的适应证为腹腔感染。
注射用头孢洛生他唑巴坦钠复方(研发代号:MK-7625A)于2014年12月首次在美国获批上市,商品名为Zerbaxa,用于联合甲硝唑治疗指定易感微生物引起的复杂性腹腔感染和复杂性尿路感染(包括肾盂肾炎)。后来,其适应证又扩大至医院获得性细菌性肺炎和呼吸机相关性细菌性肺炎。
该药物治疗复杂性腹腔感染的中国3期临床研究结果显示,头孢洛生他唑巴坦钠复方联合甲硝唑对比美罗培南组患者的临床治愈率,分别为95.2%和93.1%,达到了非劣效性标准。此外,在次要终点的微生物学应答指标方面,该复方组也显示出了治疗优势(应答率94.4% vs 93.2%)。
原文链接:
https://mp.weixin.qq.com/s/JPjvQuxJeTNgMaQ8Tkowjg
③ 质肽生物完成近2亿元B+轮融资
作者:质肽生物
解读:Richard
来源: 易凯资本
发布日期:2023-11-27
■ 内容要点
近日,北京质肽生物宣布完成近2亿元人民币B+轮融资,领投方为爱美客和中美绿色基金,其它主要投资方还包括嘉远基金、成都科创投和蓝驰创投等。
资金将主要用于推进质肽生物仿制药和创新药相关管线的临床试验进展。
质肽生物成立于2018年,专注于依托大肠杆菌技术平台来开发重组蛋白质药物。质肽生物围绕胰高血糖素样肽-1(GLP-1)靶点在代谢病领域中的主要适应证进行了全方位布局,产品管线已达10条以上。
目前,质肽生物的核心管线均有重大临床进展突破。其自主研发的新型超长效GLP-1受体激动剂ZT002,已在澳洲完成针对成人2型糖尿病血糖控制的1期临床研究。在国内,ZT002陆续于2023年上半年取得了成人2型糖尿病血糖控制、成人肥胖或者超重患者的减重治疗,以及阿尔茨海默病的临床许可。
原文链接:
https://mp.weixin.qq.com/s/g3YZOm7-JYvURHXgU_rTNA
④ Alladapt食物过敏药ADP101获FDA快速通道认定
作者:Alladapt Immunotherapeutics
解读:orchid
来源:Biospace
发布日期:2023-11-22
■ 内容要点
11月22日,生物制药公司Alladapt Immunotherapeutics宣布,旗下治疗多种食物过敏的口服免疫疗法(OIT)ADP101获得FDA快速通道资格认定。
ADP101成为开发速度最快的OIT药物。
目前,FDA尚未批准针对多种食物过敏的OIT药物。一项过去为期12个月的调查研究显示,93%过敏患者表现为对多种食物过敏,仅有6.6%患者为花生单一致敏。ADP101可用于4-17岁儿童15种常见食物过敏症状治疗,包括杏仁、腰果、鸡蛋、鳕鱼、牛奶、榛子、花生、山核桃、开心果、鲑鱼、芝麻、虾、大豆、核桃和小麦。
1/2期临床Harmony研究结果显示,ADP101表现出剂量依赖性,并具有良好的安全性和耐受性,患者使用ADP101后出现有临床意义的脱敏反应。目前,Alladapt Immunotherapeutics公司正在进行Encore开放标签扩展研究,以评估ADP101长期使用治疗单一和多种食物过敏患者症状。
原文链接:
https://www.biospace.com/article/releases/alladapt-immunotherapeutics-receives-fda-fast-track-designation-for-adp101-for-the-treatment-of-mono-and-multi-food-allergies/
⑤ Sosei Heptares重新获得IBD药物GSK4381406所有权
作者:Sosei Heptares
解读:Richard
来源:Sosei Heptares官网
发布日期:2023-11-24
■ 内容要点
11月24日,日本生物制药公司Sosei Heptares对外表示,经过与葛兰素史克(GSK)公司商议后,
GSK公司决定放弃炎症性肠病(IBD)药物GSK4381406所有权,而Sosei Heptares公司则重新获得该药物所有权。
GSK公司表示在重新审视了自身免疫产品线开发前景以及面临的挑战后,决定降低GSK4381406药物的优先权并终止其开发。因此,此次退货并不涉及GSK4381406药物的安全性问题或其临床前研究等可靠性问题。
GSK4381406是一款口服GPR35激动剂,由Sosei Heptares公司使用结构指导的药物设计平台开发而来,于2020年授权给GSK公司。临床前数据表明,GSK4381406可以改善屏障功能并减少胃肠道内脏疼痛。目前,该药物已在英国获批1期临床,后续Sosei Heptares公司将独自承担开发任务。
原文链接:
https://soseiheptares.com/news/897/129/Sosei-Heptares-to-Regain-Full-Ownership-of-GSK4381406-a-Clinic-ready-First-in-Class-Oral-GPR35-Agonist-for-Inflammatory-Bowel-Disease.html
⑥ 淇嘉科技完成首轮融资
作者:动脉网
解读:Richard
来源:探针资本
发布日期:2023-11-27
■ 内容要点
近期,淇嘉科技(苏州)有限公司完成由讯飞创投独家领投的数千万元人民币首轮融资。
资金将用于淇嘉科技人仿生微器官技术平台建设与商业转化。
淇嘉科技创立于2022年,是一家仿生微器官平台公司。淇嘉科技以“开发更真实的微器官服务人类健康”为使命,致力于解决临床前药物评价模型不足、类器官再生修复效率低等行业痛点。
凭借自身国际首创的iPS谱系共分化技术,淇嘉科技实现了传统类器官模型在谱系-结构-功能上的全面拓展。目前,淇嘉科学团队已完成人源呼吸消化道仿生微器官系统的开发,可提供人源十二指肠、结直肠、肺脏和肝脏等仿生微器官标准化的产品和定制化服务。
原文链接:
https://mp.weixin.qq.com/s/f00f66ys17y0gbTLHYyx4w
临床3期临床2期申请上市上市批准
2023-11-27
·生物谷
1、质肽生物完成2亿元B+轮融资,爱美客、中美绿色基金领投质肽生物于近日完成近2亿元人民币B+轮融资。领投方为爱美客、中 美绿色基金,其他投资方包括嘉远基金、成都科创投、晋成基金等,老股东蓝驰创投持续加码。易凯资本任独家财务顾问。质肽生物成立于2018年,主要从事重组蛋白质药物开发。公司两款核心产品,司美格鲁肽生物类似药ZT001和一款自研的超长效GLP-1月制剂ZT002均已在澳洲完成I期临床,其中ZT002的第三项适应症已于今年8月获中国国家药监局药审中心批准启动,用于治疗阿尔兹海默症。2、淇嘉科技完成数千万天使轮融资,讯飞创投领投淇嘉科技(苏州)有限公司(简称:淇嘉科技)于近期正式完成数千万元人民币天使轮融资。本轮融资由讯飞创投独家领投,探针资本担任独家财务顾问。所募集资金将用于人仿生微器官技术平台建设与商业转化。淇嘉科技创立于2022年,由葛啸虎博士发起并联合吴迪博士和万飞先生共同创立,是一家仿生微器官平台公司。淇嘉科技以“开发更真实的微器官服务人类健康”为使命,致力于解决临床前药物评价模型不足、类器官再生修复效率低等行业痛点。3、赛福凯尔获数千万元Pre-A轮融资,聚焦肿瘤电场治疗2023年11月27日,赛福凯尔完成约数千万元Pre-A轮融资,由普华资本领投。据悉,赛福凯尔将会在2023年12月份启动新一轮融资。这轮资金除了用于持续研发产品技术外,还会围绕前期积累的多条“TTF+”管线开展真人临床试验,团队也在积极接触国内产业化合作方一起进行电场技术应用的持续探索和商业化落地。4、牛肉和牛奶中的营养物质有望对抗多种癌症一系列实验和动物研究发现,牛羊等反刍动物的肉类和乳制品中含有一种长链脂肪酸——反式青霉烯酸(TVA),可促进对某些类型癌细胞的破坏。进一步研究表明,它可用于辅助现有的癌症治疗。相关研究11月22日发表于《自然》。5、基金委通报 2023 第二批不端行为处理结果,涉及山东大学、北理工等高校学者11 月 24 日,国家自然科学基金委员会公布了2023 年第二批不端行为案件处理结果。案件涉及来自滨州医学院、山东大学、山东第一医科大学、北京理工大学、华中科技大学、南昌大学、广州医科大学等二十余所高校、医院、公司的 24 名学者,主要涉及委托第三方完成实验或代写论文,买卖项目申请书、未经同意使用他人署名、擅自标注他人基金项目、抄袭剽窃他人申请书内容、个人信息造假、向评审专家实施请托等问题。基金委对涉案个人处以取消国家自然科学基金项目申请和参与申请资格 3~7 年,追回已拨资金等处罚。6、WHO:中国出现儿童肺炎聚集或和“免疫落差”现象有关11月26日下午3点,国家卫生健康委召开新闻发布会,介绍冬季呼吸道疾病防治有关情况。国家卫生健康委新闻发言人、宣传司副司长米锋表示,监测显示,近期呼吸道感染性疾病以流感为主。此外,还有鼻病毒、肺炎支原体、呼吸道合胞病毒、腺病毒等引起。中国疾控中心免疫规划首席专家王华庆则表示在不同年龄段,除了流感以外还有其他病原的分布,比如说1~4岁儿童,除了流感以外,还有引起普通感冒的鼻病毒,也占到一定的比例。5~14岁人群除了流感以外,支原体也占了一定的比例,还有引起普通感冒的腺病毒存在。15~59岁,除了流感病毒以外,也有鼻病毒,还有新冠病毒病原被分离出来。60岁以上的人群,人偏肺病毒(human metapneumovirus, HMPV)也是引起普通流感症状的病毒。此外还有,普通的冠状病毒在60岁以上人群当中占的比例也比较大。所以在最近呼吸道疾病流行的季节,是有多种病原共同存在的。本文仅用于学术分享,转载请注明出处。若有侵权,请联系微信:bioonSir 删除或修改!
100 项与 爱美客技术发展股份有限公司 相关的药物交易
登录后查看更多信息
100 项与 爱美客技术发展股份有限公司 相关的转化医学
登录后查看更多信息
管线布局
2024年05月03日管线快照
管线布局中药物为当前组织机构及其子机构作为药物机构进行统计,早期临床1期并入临床1期,临床1/2期并入临床2期,临床2/3期并入临床3期
临床3期
1
登录后查看更多信息
当前项目
| 药物(靶点) | 适应症 | 全球最高研发状态 |
|---|---|---|
A型肉毒毒素(Aquavit Pharmaceuticals/Huons) ( ) | 鼻唇沟皱纹 更多 | 临床3期 |
登录后查看更多信息
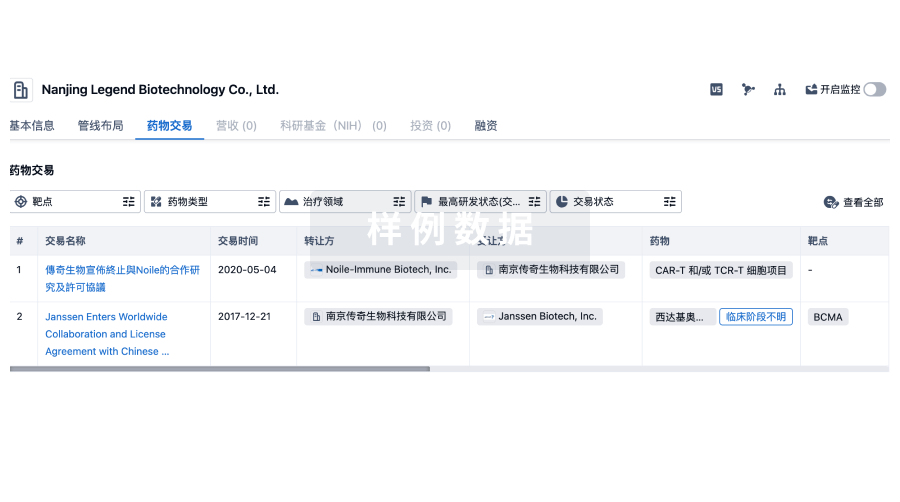
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
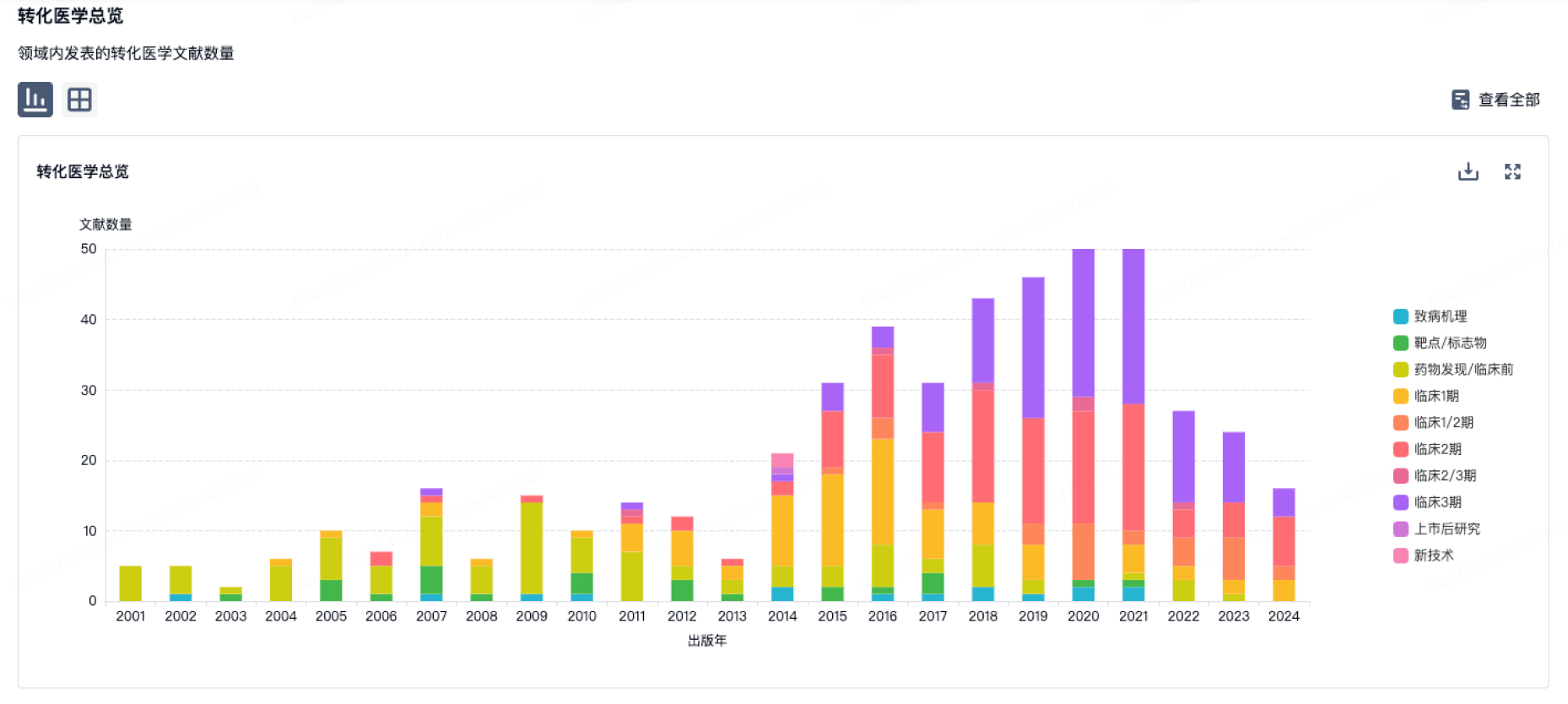
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
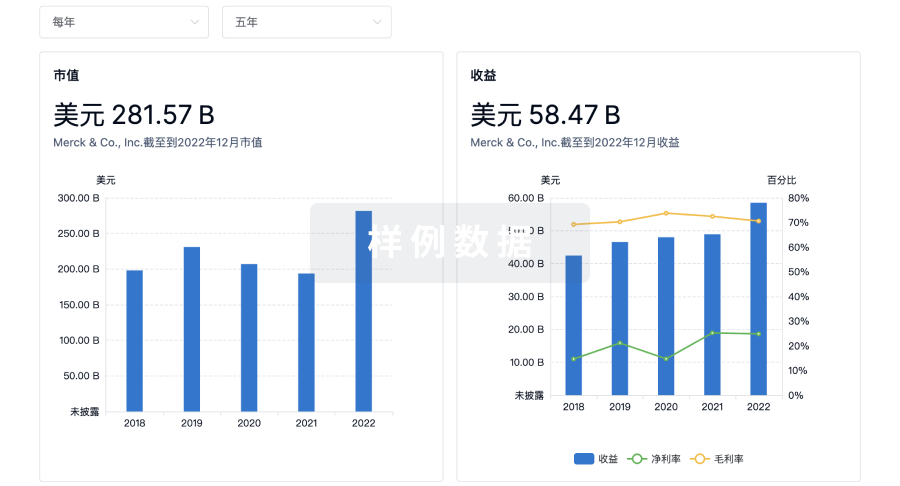
营收
使用 Synapse 探索超过 36 万个组织的财务状况。
登录
或
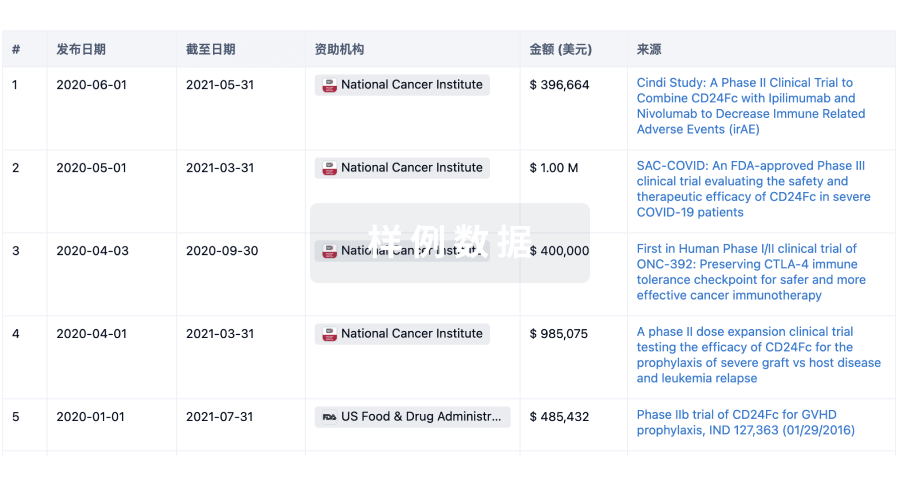
科研基金(NIH)
访问超过 200 万项资助和基金信息,以提升您的研究之旅。
登录
或
投资
深入了解从初创企业到成熟企业的最新公司投资动态。
登录
或
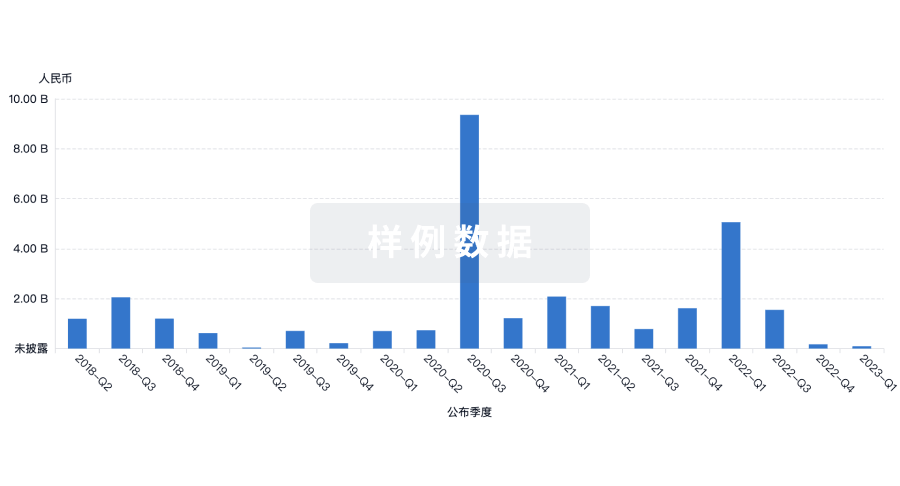
融资
发掘融资趋势以验证和推进您的投资机会。
登录
或
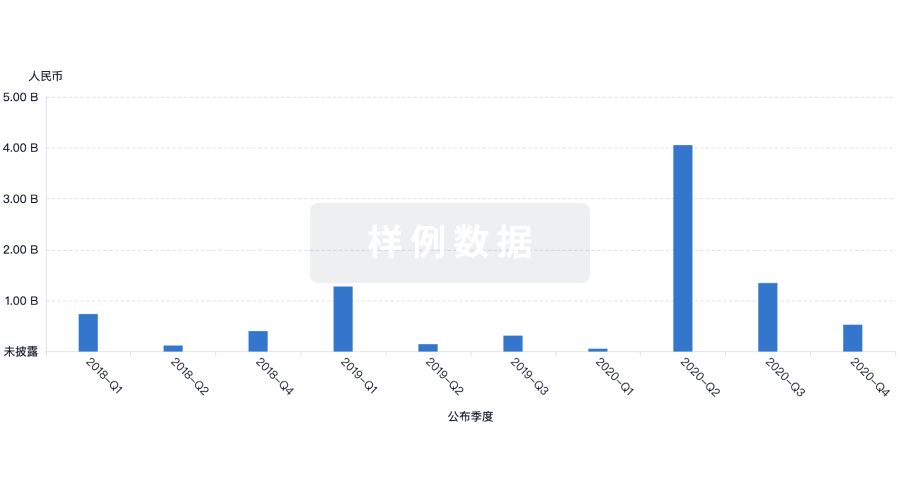
标准版
¥16800
元/账号/年
新药情报库 | 省钱又好用!
立即使用
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用

