预约演示
更新于:2025-05-07
DLL3 x CD47
更新于:2025-05-07
关联
1
项与 DLL3 x CD47 相关的药物作用机制 CD47抑制剂 [+1] |
在研机构 |
非在研适应症- |
最高研发阶段临床2期 |
首次获批国家/地区- |
首次获批日期1800-01-20 |
2
项与 DLL3 x CD47 相关的临床试验CTR20242720
一项评价PT217治疗表达DLL3的晚期难治性癌症受试者的开放标签、剂量递增和扩展的I期临床研究。
评估PT217在晚期实体瘤受试者中的安全性和耐受性,通过剂量递增评估PT217在晚期实体瘤中的限制毒性的发生情况,并确定最大耐受剂量(如达到),以及Ⅱ期推荐剂量。评估PT217在晚期实体瘤受试者中的药代动力学特征、免疫原性、细胞因子水平及初步的抗肿瘤活性。
开始日期2024-08-26 |
申办/合作机构 |
NCT05652686
An Open-label, Multicenter, Dose Escalation, and Dose Expansion Phase 1/2 Study with Peluntamig (PT217) Followed by a Key ChemotherapY And/or Checkpoint Inhibitor ComBination in Patients with NeuRoendocrIne Carcinomas That Are Known to Be DLL3 ExpressinG CancErs (SKYBRIDGE)
This is a first-in-human, Phase 1/2, open-label, dose escalation, dose expansion and combination study designed to evaluate the safety, tolerability, pharmacokinetics, pharmacodynamics, and preliminary efficacy of Peluntamig (PT217) as a monotherapy and in combination with chemotherapy.
开始日期2023-09-05 |
申办/合作机构 |
100 项与 DLL3 x CD47 相关的临床结果
登录后查看更多信息
100 项与 DLL3 x CD47 相关的转化医学
登录后查看更多信息
0 项与 DLL3 x CD47 相关的专利(医药)
登录后查看更多信息
105
项与 DLL3 x CD47 相关的新闻(医药)2025-04-22
·医药笔记
▎Armstrong近期,DLL4/VEGF双抗ES104(Tovecimig)在胆道癌的关键性临床试验中取得成功,达到主要终点,有望成为胆道癌二线治疗的新标准,为这一高度未满足的临床领域带来新的希望。胆道癌是一种高度恶性的消化系统肿瘤,具有进展快、诊断晚、预后差等特点。全球胆道癌发病率约为3/10万,根据最新的GLOBOCAN数据,全球胆道系统相关癌症的新发病例总数大约为 27–29 万例/年,且呈逐年上升趋势。在中国,胆道癌发病率明显高于欧美地区,每年新增胆道癌患者约为55,700人【1】。大多数胆道癌患者确诊时已处于晚期,当前标准治疗手段对其控制效果有限。一线治疗以免疫联合化疗为主,客观缓解率不足30%,虽然免疫检查点抑制剂能够改善生存,但整体获益仍有限;70-80%的患者在一线治疗失败后会进入二线治疗阶段。二线治疗中,仅有FOLFOX化疗方案作为标准,其客观缓解率仅5%,中位生存期约为半年;真正具有明确靶点突变可使用靶向治疗的患者仅占比不超过20%。因此,二线晚期胆道癌二线治疗尤其缺乏有效手段,亟需机制新颖、疗效确切的新型药物。在ES104的胆道癌关键性临床试验中,Compass采取随机、对照设计,入组168例晚期胆道癌患者,主要终点为ORR,关键次要终点包括PFS、OS、DOR等。ES104联合紫杉醇治疗组相比于紫杉醇对照组,ORR分别为17.1%、5.3%,p值为0.031,ORR提高到3倍以上,展示出优异疗效。两组BOR为PD的比例差异显著,紫杉醇组42.1%的患者其最佳疗效为疾病进展,而ES104联合治疗组仅16.2%的患者为疾病进展,提示PFS曲线在治疗早期即已出现分离,预示着PFS将获得显著获益。此外,ES104更早的2期单臂研究中,BTC二线或三线的患者经ES104联合紫杉醇治疗后中位PFS和中位OS分别达到9.4个月和12.5个月,远超化疗PFS 3-4个月,OS半年的历史数据。从瀑布图上可以看到,联合治疗组有4名患者达到100%缩瘤,靶病灶完全消退,获益明显。在疗效显著提高的情况下,ES104安全性表现也与已获批的同类药物类似。ES104有望成为全球胆道癌二线治疗的标准疗法。Stifel在其近期的研究报告中指出,Tovecimig当前在客观缓解率方面已取得统计学显著性,这一结果使得后续对无进展生存期数据的正式统计分析成为可能。在当前缺乏有效治疗选择的疾病背景下,结合Tovecimig在疾病进展数据中表现出的差异性优势等方面的评估,Stifel将Tovecimig在二线胆道癌适应症中的成功概率(POS)由原先的75%上调至85%。适应症拓展方面,ES104在结直肠癌单药临床试验中也显示出积极的临床获益。ES104在胆道癌、结直肠癌的临床进展,其意义远超本身,意味着DLL4/VEGF有望成为新一代的血管抑制基石药物,对于胃癌、胶质母细胞瘤、肝癌、卵巢癌、肾癌等多个瘤种都有拓展可能。在血管抑制方面,最经典的治疗方案包括贝伐珠单抗、小分子VEGF受体抑制剂等,虽已广泛应用于多种肿瘤治疗中,但其疗效常因耐药性而受限。更重要的是,血管抑制这一机制也开始取得迭代突破。ES104采用对称的2+2设计,靶向DLL4和VEGF两个关键血管生成通路,其中,DLL4-Notch1 通路被认为是VEGF单抗产生耐药的关键机制。通过同步阻断这两大路径,ES104有望克服传统血管抑制疗法的局限性,成为血管生成抑制领域的新一代“基石”药物。DLL4/VEGF双抗的成功,也提示我们新的抗体药物形式近年来快速发展,PD-1/VEGF为代表的肿瘤免疫双抗,EGFR/cMET为代表的TAA双抗,DLL3/CD3为代表的实体瘤TCE,DXd-ADC为代表的三代ADC取得一系列临床突破。以双抗为例,多款TCE、PD-1/VEGF双抗、自免双抗密集完成高额出海授权交易,新的赛道如MCE(Myeloid Cell Engager),也出现科望医药PD-L1/SIRPα双抗更创新的双抗新药。双抗本质上是不同靶点作用机制的有机组合,肿瘤免疫、TAA靶向、血管抑制等为肿瘤治疗中最重要的几类机制。PD-1/VEGF双抗的成功正是源于肿瘤免疫与血管抑制机制的有效结合,也引起了整个行业的广泛关注和布局。在双抗领域的布局,科望医药走在了更前沿,其拥有DLL4/VEGF双抗ES104的大中华区权益,正积极推进胆道癌在大中华区的商业化进程,同时布局多个瘤种的临床探索。此外,其自主研发的MCE包括多款基于BiME平台的双抗、两款TL1A/X双抗等,将持续加热双抗赛道。总结默沙东和BMS的PD-1+小分子VEGF抑制剂 ,康方生物PD-1/VEGF双抗一再验证了免疫治疗+血管抑制的应用前景,免疫治疗、血管抑制、化疗、放疗成为肿瘤治疗的最重要基石。免疫治疗的迭代主要是新靶点组合,化疗的迭代主要是ADC,放疗的迭代主要是靶向核药。相比之下,血管抑制的迭代仍有很大空间,DLL4/VEGF双抗有望成为血管抑制的新一代基石药物,后续可以与化疗、ADC、免疫治疗多种治疗机制开展联合治疗的探索,不断扩展其临床应用空间。参考文献[1] Zheng R, Zhang S, Zeng H, et al. Cancer incidence and mortality in China, 2016. J Natl Cancer Cent 2022;2:1-9.Armstrong技术全梳理系列GPRC5D靶点全梳理;CD40靶点全梳理;CD47靶点全梳理;补体靶向药物技术全梳理;补体药物:眼科治疗的重要方向;Claudin 6靶点全梳理;Claudin 18.2靶点全梳理;靶点冷暖,行业自知;中国大分子新药研发格局;被炮轰的“me too”;佐剂百年史;胰岛素百年传奇;CUSBEA:风雨四十载;中国新药研发的焦虑;中国生物医药企业的研发竞争;中国双抗竞争格局;中国ADC竞争格局;中国双抗技术全梳理;中国ADC技术全梳理;Ambrx技术全梳理;Vir Biotech技术全梳理;Immune-Onc技术全梳理;亘喜生物技术全梳理;康哲药业技术全梳理;科济药业技术全梳理;恺佧生物技术全梳理;同宜医药技术全梳理;百奥赛图技术全梳理;腾盛博药技术全梳理;创胜集团技术全梳理;永泰生物技术全梳理;中国抗体技术全梳理;德琪医药技术全梳理;德琪医药技术全梳理2.0;和铂医药技术全梳理;荣昌生物技术全梳理;再鼎医药技术全梳理;药明生物技术全梳理;恒瑞医药技术全梳理;豪森药业技术全梳理;正大天晴技术全梳理;吉凯基因技术全梳理;基石药业技术全梳理;百济神州技术全梳理;百济神州技术全梳理第2版;信达生物技术全梳理;信达生物技术全梳理第2版;中山康方技术全梳理;复宏汉霖技术全梳理;先声药业技术全梳理;君实生物技术全梳理;嘉和生物技术全梳理;志道生物技术全梳理;道尔生物技术全梳理;尚健生物技术全梳理;康宁杰瑞技术全梳理;科望医药技术全梳理;科望医药技术全梳理2.0;岸迈生物技术全梳理;礼进生物技术全梳理;康桥资本技术全梳理;余国良的抗体药布局;荃信生物技术全梳理;安源医药技术全梳理;三生国健技术全梳理;仁会生物技术全梳理;乐普生物技术全梳理;同润生物技术全梳理;宜明昂科技术全梳理;派格生物技术全梳理;迈威生物技术全梳理;Momenta技术全梳理;NGM技术全梳理;普米斯生物技术全梳理;普米斯生物技术全梳理2.0;三叶草生物技术全梳理;贝达药业抗体药全梳理;泽璟制药抗体药全梳理;恒瑞医药抗体药全梳理;齐鲁制药抗体药全梳理;石药集团抗体药全梳理;豪森药业抗体药全梳理;华海药业抗体药全梳理;科伦药业抗体药全梳理;百奥泰技术全梳理;凡恩世技术全梳理。
临床2期临床结果
2025-04-12
·医药笔记
▎Armstrong2025年4月11日,安进宣布DLL3/CD3双抗在三期临床中达到OS主要终点,相比于化疗对照组显著延长mOS。安进将在即将召开的医学会议上汇报DeLLphi-304的详细数据。2024年5月,Tarlatamab凭借二期临床DeLLphi-301的数据获得FDA加速批准,99例患者ORR为40%,其中CR为2%,mDoR为9.7个月。Tarlatamab在安进HLE-BiTE技术平台上构建,也是首个在常见实体瘤取得突破的CD3双抗。总结很长时间内,CAR-T细胞疗法、CD3双抗的成功应用都局限在血液瘤,但这种局面正在快速打破。CAR-T仍然在路上,TIL已经获批治疗黑色素瘤,DLL3/CD3双抗获批治疗小细胞肺癌并在验证性三期临床获得成功。与此同时,自免也在快速成为CAR-T及其他细胞疗法、CD3双抗厮杀的又一条热门赛道。为您推荐: 项目:北京大学医疗产业投融资领军人才研修班 学制:1年,累计144课时。 时间:正在报名中,即将开班。(点击上方链接了解详情)Armstrong技术全梳理系列GPRC5D靶点全梳理;CD40靶点全梳理;CD47靶点全梳理;补体靶向药物技术全梳理;补体药物:眼科治疗的重要方向;Claudin 6靶点全梳理;Claudin 18.2靶点全梳理;靶点冷暖,行业自知;中国大分子新药研发格局;被炮轰的“me too”;佐剂百年史;胰岛素百年传奇;CUSBEA:风雨四十载;中国新药研发的焦虑;中国生物医药企业的研发竞争;中国双抗竞争格局;中国ADC竞争格局;中国双抗技术全梳理;中国ADC技术全梳理;Ambrx技术全梳理;Vir Biotech技术全梳理;Immune-Onc技术全梳理;亘喜生物技术全梳理;康哲药业技术全梳理;科济药业技术全梳理;恺佧生物技术全梳理;同宜医药技术全梳理;百奥赛图技术全梳理;腾盛博药技术全梳理;创胜集团技术全梳理;永泰生物技术全梳理;中国抗体技术全梳理;德琪医药技术全梳理;德琪医药技术全梳理2.0;和铂医药技术全梳理;荣昌生物技术全梳理;再鼎医药技术全梳理;药明生物技术全梳理;恒瑞医药技术全梳理;豪森药业技术全梳理;正大天晴技术全梳理;吉凯基因技术全梳理;基石药业技术全梳理;百济神州技术全梳理;百济神州技术全梳理第2版;信达生物技术全梳理;信达生物技术全梳理第2版;中山康方技术全梳理;复宏汉霖技术全梳理;先声药业技术全梳理;君实生物技术全梳理;嘉和生物技术全梳理;志道生物技术全梳理;道尔生物技术全梳理;尚健生物技术全梳理;康宁杰瑞技术全梳理;科望医药技术全梳理;科望医药技术全梳理2.0;岸迈生物技术全梳理;礼进生物技术全梳理;康桥资本技术全梳理;余国良的抗体药布局;荃信生物技术全梳理;安源医药技术全梳理;三生国健技术全梳理;仁会生物技术全梳理;乐普生物技术全梳理;同润生物技术全梳理;宜明昂科技术全梳理;派格生物技术全梳理;迈威生物技术全梳理;Momenta技术全梳理;NGM技术全梳理;普米斯生物技术全梳理;普米斯生物技术全梳理2.0;三叶草生物技术全梳理;贝达药业抗体药全梳理;泽璟制药抗体药全梳理;恒瑞医药抗体药全梳理;齐鲁制药抗体药全梳理;石药集团抗体药全梳理;豪森药业抗体药全梳理;华海药业抗体药全梳理;科伦药业抗体药全梳理;百奥泰技术全梳理;凡恩世技术全梳理。
细胞疗法免疫疗法临床1期抗体药物偶联物临床2期
2025-04-08
·癌度
癌度临床试验病友交流群(点击)一、新药快讯1、 国产双特异性抗体药PT217获批临床,治疗实体瘤2025年4月7日,DLL3和CD47双特异性抗体药PT217已获得中国国家药品监督管理局药品审评中心(CDE)批准开展2期联合治疗临床试验,该药将会与化疗或PD-L1抑制剂联合治疗小细胞肺癌和其他神经内分泌癌,包括前列腺神经内分泌癌的安全性和治疗效果。2、新疗法PIPAC-MMC联合化疗,治疗肠癌显示积极疗效2025年美国外科肿瘤学会年会上,一项一期临床试验公布研究结果,新疗法PIPAC-MMC联合全身化疗,在一部分无法手术切除的结直肠癌和阑尾癌腹膜转移患者中,展现出积极的疗效和良好的耐受性。PIPAC-MMC是一种治疗癌症腹膜转移的新型局部化疗方法,19名患者中1名患者病灶全消失,2名患者病灶缩小30%以上,12名患者病情稳定。3、新药SON-1010治疗晚期肉瘤展现较好安全性和初步疗效最近,公布的一项临床试验结果表明,前沿药SON-1010治疗晚期肉瘤,包括平滑肌肉瘤或脂肪肉瘤,显示出良好的安全性和初步疗效。晚期肉瘤患者中,SON-1010联合化疗药曲贝替定,未发现任何意料之外的安全性。SON-1010单药治疗的6名患者,5名患者治疗4个月病情稳定,SON-1010剂量递增阶段的24名患者,13名表现出临床获益的迹象。二、新药快讯1、沈琳教授科研成果,NOTCH1基因状态对晚期食管鳞癌疗效预测2025年4月3日,北京大学肿瘤医院沈琳教授在《临床肿瘤学杂志》发表了一篇研究,基于一项三期临床试验结果,揭示了NOTCH1基因突变在晚期或转移性食管鳞癌接受PD-1单抗治疗的价值,在22%的携带NOTCH1基因突变的患者中,免疫治疗药物中位总生存时间是18.4个月,而化疗组的中位总生存时间是5.3个月,NOTCH1突变或有助于筛选可能从抗PD-1治疗中获益的患者。
临床3期临床2期免疫疗法临床结果
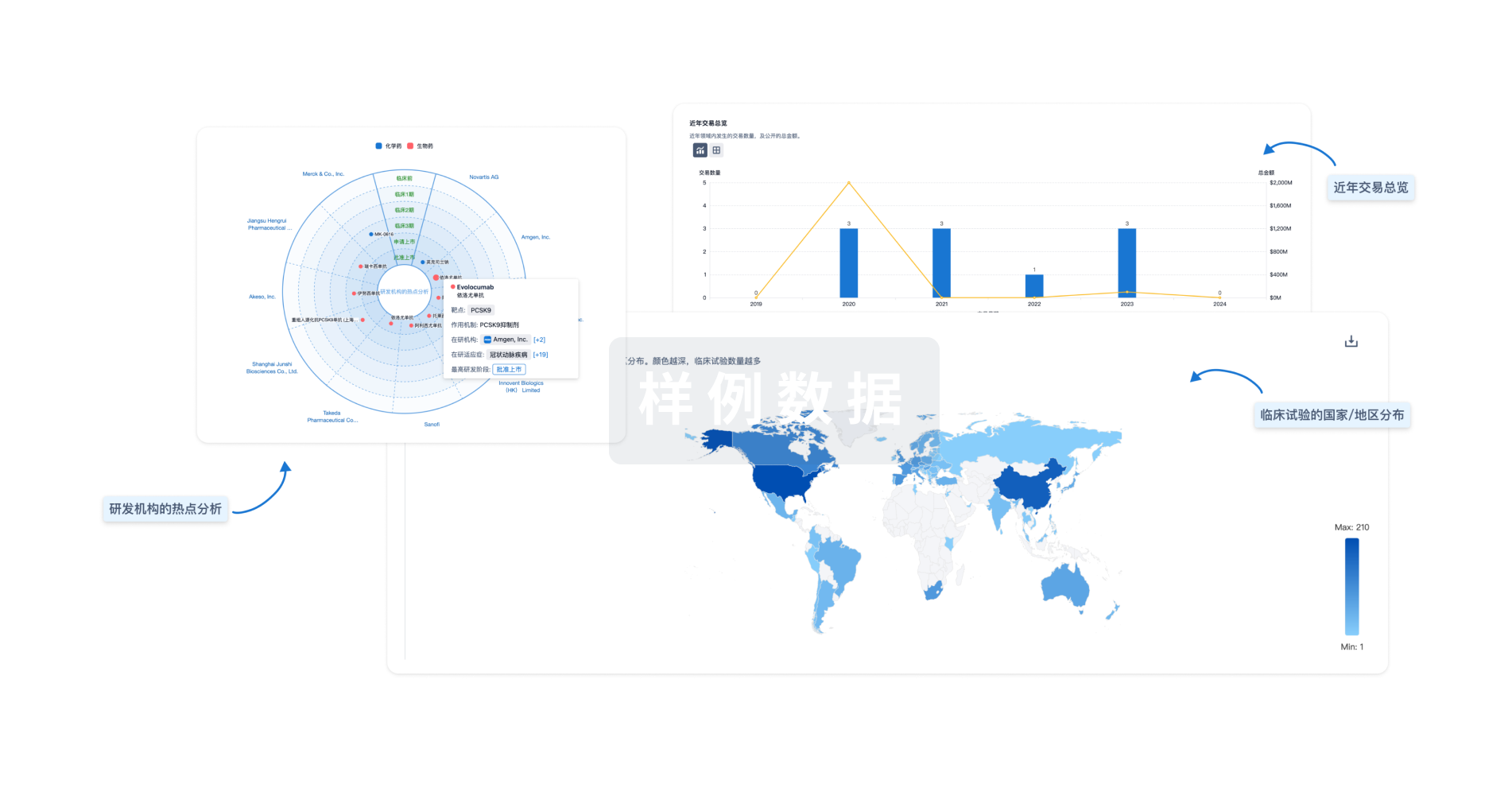
分析
对领域进行一次全面的分析。
登录
或
生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用
