预约演示
更新于:2025-05-07
替格瑞洛
更新于:2025-05-07
基本信息
别名- |
简介- |
关联
1
项与 替格瑞洛 相关的药物靶点 |
作用机制 替格瑞洛抑制剂 |
原研机构 |
非在研适应症- |
最高研发阶段申请上市 |
首次获批国家/地区- |
首次获批日期1800-01-20 |
6
项与 替格瑞洛 相关的临床试验CTR20213065
一项对于接受替格瑞洛治疗后出现失控大出血/危及生命的出血或需要紧急手术/有创性操作的患者使用 PB2452 的 3 期、多中心、开放性、单臂研究
主要目的:使用 VerifyNow™ PRUTest™ (VerifyNow™, 2016) 血小板反应检测,证明对接受替格瑞洛治疗后出现失控大出血/危及生命的出血或者需要紧急手术/有创操作的患者,开始静脉输注 PB2452 后,替格瑞洛的抗血小板作用能够得到逆转;证明对接受替格瑞洛治疗后出现失控大出血/危及生命的出血或者需要紧急手术/有创性操作的患者给予 PB2452 后,PB2452 对达到有效止血的作用
次要目的:通过 PRU 以及使用血管扩张刺激磷蛋白 (VASP) 试验测定血小板反应活性指数 (PRI),证明对接受替格瑞洛治疗后出现失控大出血/危及生命的出血或者需要紧急手术/有创性操作的患者,静脉输注 PB2452 后,替格瑞洛的抗血小板作用能够得到逆转
其他预设目的:评估所有招募患者接受 PB2452 的临床结局;评估经静脉给予的 PB2452、替格瑞洛和替格瑞洛活性代谢物 (TAM) 的药代动力学 (PK) 特征;评估替格瑞洛逆转对 P-选择素及可选的其他血小板功能相关生物标志物的作用
安全性目的:评估 PB2452 对接受替格瑞洛治疗的患者的安全性、耐受性和免疫原性。
开始日期2022-11-04 |
申办/合作机构 |
CTR20212626
在中国健康志愿者中评估 PB2452 (Bentracimab) 联合和不联合替格瑞洛预治疗的安全性、耐受性、药代动力学和药效学的一项 1 期、随机、双盲、安慰剂对照、单剂量递增研究
本研究的主要目的是针对中国受试者评估以渐增型单一剂量方式经静脉 (IV) 给予 PB2452(伴或不伴替格瑞洛)的安全性和耐受性,此外通过 VerifyNow P2Y12 测定法测量 P2Y12 反应单位 (PRU),评估 PB2452 单次剂量递增给药对替格瑞洛抗血小板活性的影响。
开始日期2021-12-20 |
申办/合作机构 |
NCT04286438
A Phase 3, Multicenter, Open-Label, Single-Arm Study of Bentracimab (PB2452) in Ticagrelor-Treated Patients With Uncontrolled Major or Life-Threatening Bleeding or Requiring Urgent Surgery or Invasive Procedure (REVERSE-IT Trial)
This is a multi-center, open-label, prospective single-arm study of reversal of the antiplatelet effects of ticagrelor with bentracimab (PB2452) in patients who present with uncontrolled major or life-threatening bleeding or who require urgent surgery or invasive procedure.
At least 200 patients will be enrolled from approximately 200 centers in North America, Europe, and Asia-Pacific regions, including mainland China. Patients with reported use of ticagrelor within the prior 3 days who require urgent ticagrelor reversal will be eligible for enrollment. These populations will be enrolled based on separate inclusion criteria.
At least 200 patients will be enrolled from approximately 200 centers in North America, Europe, and Asia-Pacific regions, including mainland China. Patients with reported use of ticagrelor within the prior 3 days who require urgent ticagrelor reversal will be eligible for enrollment. These populations will be enrolled based on separate inclusion criteria.
开始日期2020-07-15 |
申办/合作机构 |
100 项与 替格瑞洛 相关的临床结果
登录后查看更多信息
100 项与 替格瑞洛 相关的转化医学
登录后查看更多信息
0 项与 替格瑞洛 相关的专利(医药)
登录后查看更多信息
3
项与 替格瑞洛 相关的新闻(医药)2025-01-17
摘要:抗体治疗药物的商业开发是一项全球性事业,涉及数千家生物制药公司和支持服务组织。迄今为止,他们的共同努力已经导致了超过200种上市的抗体治疗药物和近1400种正在进行临床研究评估的试验产品候选物,这些产品作为治疗各种疾病的治疗手段。在此,我们讨论了2024年期间发生的抗体治疗药物开发的关键事件,并预测可能在2025年发生的与晚期临床管线相关的关键事件。特别是,我们报告了2024年至少在一个国家或地区获得首次批准的21种抗体治疗药物,包括双特异性抗体tarlatamab (IMDELLTRA®)、zanidatamab (Ziihera®)、zenocutuzumab (BIZENGRI®)、odronextamab (Ordspono®)、ivonescimab (依達方®)和抗体-药物偶联物(ADC) sacituzumab tirumotecan (佳泰萊®)。我们还讨论了截至2024年12月9日我们最后一次更新时,至少有一个监管机构正在审查市场申请的30种试验性抗体治疗药物,包括ADCs datopotamab deruxtecan、telisotuzumab vedotin、patritumab deruxtecan、trastuzumab botidotin、becotatug vedotin和trastuzumab rezetecan。在我们纳入晚期管线的178种抗体治疗药物中,我们总结了18种可能在2025年底提交市场申请的关键数据,例如双特异性或多特异性抗体denecimig、sonelokimab、erfonrilimab和anbenitamab。报告了双特异性抗体和ADC等抗体格式的开发和批准的关键趋势,以及这些抗体格式的临床阶段转换和全球批准成功率。
1.引言
自2010年以来,“值得关注的抗体”系列文章每年都会更新抗体治疗药物的商业临床开发和市场批准情况。每份报告都关注三个类别,这些类别由分子的开发阶段定义:1)晚期临床管线(即处于关键性2期、2/3期或3期研究中的分子);2)正在接受监管机构审查市场申请的试验性抗体治疗药物;以及3)在过去一个日历年中首次获得市场批准的抗体治疗药物。对于处于晚期临床研究中的抗体治疗药物,由于过去16年中数量大幅增加(从2010年的“值得关注的抗体”中报告的26种增加到本报告中的178种),我们现在仅对那些可能很快提交市场申请的晚期抗体治疗药物提供最新开发情况的总结,这些信息是根据开发这些分子的公司公开披露的信息得出的。为了便于趋势分析,抗体学会还收集处于临床开发早期阶段的抗体治疗药物的数据。这些管线数据已被纳入“值得关注的抗体”文章中报告的抗体治疗药物开发趋势和批准成功率的多项分析中。例如,我们之前曾报告非典型格式的抗体在晚期研究中的比例增加,这些非典型格式旨在增强分子的生物学活性。在此,我们分析了不同抗体格式的趋势和成功率,根据以下标准对分子进行分类:1)特异性(即单特异性或双特异性/多特异性);2)缀合状态(即抗体-药物缀合物(ADC,此处限于与细胞毒性药物缀合的抗体)、放射免疫治疗(包括放射免疫缀合物(RIC)和抗体螯合物缀合物),以及免疫缀合物(即不属于ADC或放射免疫治疗组的抗体缀合物,或由抗体与非免疫球蛋白衍生的蛋白结构域融合而成的缀合物);以及3)组成(即单一分子或混合物)。在我们的分析中,每个分子仅被代表一次,并根据修改对分子性质的改变程度进行分类。因此,ADC组包括双特异性ADC,放射免疫治疗组包括双特异性放射免疫治疗药物,免疫缀合物组包括免疫缀合物混合物。目前市场上大多数重组单克隆抗体是典型的裸单特异性抗体,但自2019年以来,ADC、双特异性抗体、免疫缀合物和抗体混合物的批准数量有所增加(图1a)。这些非典型格式约占2024年(截至11月)批准的抗体产品的25%,以及目前正处于监管审查中的试验性抗体治疗药物的30%(图1a)。这一趋势可能是由于进入临床研究的非典型格式抗体数量增加,特别是ADC、双特异性抗体和免疫缀合物(图1b)。我们的分析显示,自2010年以来,进入临床研究的非典型格式抗体治疗药物数量稳步增加,自2021年以来,这些抗体每年约占进入临床研究抗体的50%(图1b)。
图1. 抗体形式的趋势。(a) 按一般分子类别分层的抗体治疗药物在任何国家的首次批准趋势以及目前处于监管审查中的抗体。(b) 按一般分子类别分层的抗体治疗药物的首次人体研究趋势。2024年的数据截至2024年12月7日。分子仅计算一次,并分类为:裸单特异性(典型形式);抗体 - 药物偶联物(ADC)(与细胞毒性药物偶联时,包括双特异性ADC);双特异性/多特异性(裸);免疫偶联物(与分子(不包括细胞毒性药物、放射性同位素和螯合剂)偶联的抗体;或与非免疫球蛋白衍生的蛋白域融合,包括免疫偶联物混合物);混合物;放射免疫治疗(包括放射免疫偶联物(RIC)和抗体螯合剂偶联物)。
我们还评估了不同格式抗体的临床阶段转换和全球成功率的差异(图2)。我们分析了2000-2019年进入临床研究的1373种抗体队列,根据上述一般分子类别进行分层,并将每个分子分配到其最先进开发阶段,选择九个可能的开发阶段之一(1期、2期或3期临床研究;监管审查;批准;所有开发在1期、2期、3期或监管审查期间终止)。我们评估了全球成功率,定义为在任何国家的首次市场批准;后续补充批准未包含在计算中。最终结果(即批准或所有开发终止)已知的比例为裸单特异性抗体的67%,ADC的76%,双特异性/多特异性抗体的61%,免疫缀合物的73%,混合物的79%,以及放射免疫治疗组的73%。应注意,随着仍在开发中的分子的最终结果在未来确定,这些比率可能会有所不同。
图2. 不同抗体形式的临床阶段转换和全球成功率。2000-2019年进入临床研究的抗体治疗药物的临床阶段转换和全球批准成功率,按分子类别分层。红色条形,裸单特异性抗体。橙色条形,抗体药物偶联物(ADC)。黄色条形,双特异性/多特异性抗体。浅绿色条形,免疫偶联物。深绿色条形,抗体混合物。粉色条形,用于放射免疫治疗的抗体(包括放射性免疫偶联物和抗体螯合剂偶联物)。所包括的队列仅限于由商业公司赞助的临床研究中的新型抗体治疗药物;生物类似药被排除在外。对于裸单特异性抗体,最终结果(批准或终止)已知的占67%;对于ADC,占76%;对于双特异性/多特异性抗体,占61%;对于免疫偶联物,占73%;对于混合物,占79%;对于放射免疫治疗组,占73%。处于1/2期研究的单克隆抗体被归类为2期;推进到2/3期的单克隆抗体被归类为3期。包括在全球范围内进行的从1期到2期和从2期到3期临床研究之间的转换。全球批准指的是在任何国家或地区首次获批;不包括任何类型的补充批准。单步转换率是通过将从给定阶段转换到下一阶段的抗体治疗药物数量除以在计算时转换和在该阶段终止的数量之和来计算的。从1期到批准的比率是通过将四个相关的单步转换率相乘得出的。数据截至2024年12月7日。
对于大多数格式,阶段转换率显示出药物开发的典型整体模式,即2期到3期转换率最低,市场申请提交到批准转换率最高。然而,ADC和放射免疫治疗格式是例外。对于ADC组,1期到2期转换率最低,这与第一代ADC报告的增加的毒性一致。放射免疫治疗组也有一个低的1期到2期转换率,与其他组相比最低,可能是因为RIC报告的毒性。此外,由于唯一过渡到监管审查的RIC,碘-131 omburtamab的开发被终止,该组的市场申请提交到批准转换率为0%。我们的分析显示,不同抗体格式的全球批准成功率差异很大(0-32%)。放射免疫治疗组目前的成功率最低(0%)。应注意,尽管两种RIC,碘-131 tositumomab(Bexxar)和钇-90 ibritumomab tiuxetan(Zevalin)获得了市场批准,但这两个分子首次进入临床研究的时间都远远早于2000年,因此未包含在我们的成功率分析中。有趣的是,尽管RIC的成功率很低,但我们观察到,在2015-2019年和2020-2024年期间,进入临床研究的放射免疫治疗抗体数量比前一个5年期间(2010-2014年)有所增加,尽管数量很少,即在这些期间都不到10个。这一新兴趋势可能与RIC技术的进步和下一代同位素载荷的使用有关,如阿尔法发射体(锕-225、钍-227、硼-10),它们具有短的组织穿透范围和高线性能量转移,有潜力实现更有针对性的递送,减少对周围健康组织的损害。免疫缀合物的批准成功率最低(14%)。该组包括各种在结构和作用机制方面具有非常不同特征的抗体分子,包括免疫细胞因子、免疫毒素、双特异性免疫缀合物、非典型ADC和PEG化抗体。由于异质性和包含的分子数量少,按其子类别分层的分子分析可能无法得出有意义的结果。随着2020-2024年期间进入临床研究的免疫缀合物数量不断增加,我们预计未来将能够进行此类分析。ADC组的全球批准成功率为20%,低于典型(即裸的、单特异性)抗体(30%)和双特异性/多特异性抗体(32%)(图2)。由于我们的数据限于2000-2019年进入临床研究的抗体治疗药物,ADC组包括大量第一代分子,这些分子存在毒性问题。其设计的进步产生了下一代ADC,在结构、连接子和载荷方面有所改进。在按载荷类型分层的ADC组的初步分析中,我们发现包含拓扑异构酶I抑制剂的ADC的成功率高于包含微管抑制剂或DNA结合剂的ADC(数据未显示)。虽然我们分析的数据中包含的基于拓扑异构酶I抑制剂的ADC不到十几个,但目前早期管线中几乎有100个这样的ADC。我们期待在未来报告这些ADC的成功率。作为一组,双特异性抗体和多特异性抗体的批准成功率最高(32%)。有趣的是,按治疗领域分层,即癌症和非癌症适应症,用于癌症的双特异性/多特异性抗体的成功率(35%)明显高于用于非癌症适应症的抗体(23%)(补充图S1)。这一结果可能部分是由于T细胞参与的双特异性抗体的成功,表明成功不仅取决于格式,还取决于靶点和作用机制,突出了抗体治疗药物开发的复杂性。在本“值得关注的抗体”系列文章的其余部分中,我们提供了截至12月4日2024年首次获得批准的21种抗体治疗药物的详细信息,以及正在考虑市场申请的30种产品候选物。我们还讨论了预计到2025年底进入监管审查的18种试验性抗体治疗药物。由于这些分子的信息量很大,下面的总结中仅引用了2024年1月至11月期间公开发布的出版物和其他披露信息。
2.2024年在任何国家首次获批的抗体治疗药物
截至12月4日,2024年共有21种抗体治疗药物在至少一个国家或地区获得首次批准(表1)。其中一些药物在2024年随后又在其他更多国家或地区获批。在21种获批产品中,大多数在中国获批,其中9/21(43%)在美国或欧盟获批。11种(55%)获批用于非癌症适应症,而10种获批用于癌症。获批产品的关键细节在以下摘要中提供,其顺序与表1中相同。
3.2024年在美国或欧盟首次获批的市场许可
3.1.Donanemab(礼来公司)
Donanemab(Kisunla™,donanemab-azbt,LY3002813)是一种人源化IgG1κ单克隆抗体,设计用于靶向Aβ(p3–42),这是一种在聚集的淀粉样斑块中发现的淀粉样β的焦谷氨酸变体。美国食品药品监督管理局(FDA)授予donanemab突破性治疗指定,用于治疗阿尔茨海默病。2024年7月2日,美国食品药品监督管理局(FDA)批准Kisunla™(donanemab-azbt)用于治疗早期症状性阿尔茨海默病的成人,包括那些有轻度认知障碍(MCI)或轻度痴呆以及确认的淀粉样病理的患者。推荐剂量为KISUNLA每4周(Q4W)700毫克,连续三剂,然后每4周1400毫克,通过约30分钟的静脉(IV)输注给药。一旦淀粉样斑块清除,就有证据支持停止Kisunla™治疗。2024年9月和10月,礼来公司分别宣布Kisunla™在日本和英国获得批准。欧洲药品管理局(EMA)于2023年8月开始评估donanemab的市场申请;截至2024年11月,该申请仍在评估中。这些批准得到了关键的3期TRAILBLAZER-ALZ 2试验(NCT04437511)的结果支持。该试验涉及1736名早期症状性阿尔茨海默病患者,他们有淀粉样蛋白和低至中等或高tau病理。参与者随机按1:1的比例分配,接受静脉donanemab(前3剂为700毫克,之后为1400毫克)(n = 860)或安慰剂(n = 874)每4周一次,持续72周。该研究的主要结果是从基线到76周的综合阿尔茨海默病评定量表(iADRS)的变化。结果显示,donanemab根据iADRS显著减缓了认知和功能衰退22%。值得注意的是,某些亚组患者获得了更大的益处。例如,在tau水平低至中等的患者(n = 1182)中,donanemab治疗在iADRS上减缓了衰退35%。2024年10月29日,礼来公司宣布3期b TRAILBLAZER-ALZ 6(NCT05738486)研究的积极结果,显示在接受稍微修改剂量的donanemab治疗的参与者中,在24周主要终点时淀粉样蛋白相关成像异常伴水肿/积液(ARIA-E)有所减少。礼来公司正在与全球监管机构就研究结果进行讨论,并计划提交潜在的Kisunla™标签更新申请。礼来公司正在进行多项donanemab的临床试验,包括TRAILBLAZER-ALZ 3,该试验专注于降低患有临床前期阿尔茨海默病个体发展为症状性阿尔茨海默病的风险,以及TRAILBLAZER-ALZ 5,这是一项针对早期症状性阿尔茨海默病的注册试验,目前正在中国、韩国、台湾及其他地区招募参与者。
3.2.Axatilimab(Syndax Pharmaceuticals)
Axatilimab(Niktimvo,axatilimab-csfr,SNDX-6352,UCB6352,INCA034176)是一种人源化、铰链稳定(S228P)的IgG4κ抗体,靶向在单核细胞和巨噬细胞中表达的集落刺激因子1受体(CSF-1 R)。UCB于2016年授予Syndax axatilimab的全球独家开发许可。2021年,Syndax和Incyte就axatilimab在慢性移植物抗宿主病(cGVHD)及任何未来适应症的全球独家共同开发和共同商业化许可协议达成一致。Niktimvo将由Incyte和Syndax Pharmaceuticals在美国共同商业化。Incyte拥有在美国以外地区对Niktimvo的独家商业化权利。Axatilimab被FDA授予用于治疗cGVHD患者的孤儿药指定。2024年8月14日,FDA批准axatilimab-csfr(Niktimvo)用于治疗在至少两种先前系统治疗失败后患有cGVHD的成人和体重至少40公斤的儿童患者。Niktimvo的推荐剂量为每2周(Q2W)0.3毫克/公斤(最大35毫克),在体重40公斤及以上的成人和儿童患者中通过30分钟的静脉输注给药。Axatilimab是首个获得市场批准的抗CSF-1 R抗体。FDA的批准基于关键的2期AGAVE-201研究(NCT04710576)的结果,该研究评估了3种剂量水平的Niktimvo在总共241名接受至少两种先前系统治疗的难治性cGVHD成人和儿童患者中的安全性和有效性。患者通过静脉输注每2周0.3毫克/公斤(0.3-毫克剂量组)、每2周1毫克/公斤或每4周3毫克/公斤给药。Niktimvo的疗效基于第7周期第1天的总缓解率。在所有接受Niktimvo的队列中均达到了主要终点。在接受批准剂量0.3毫克/公斤Q2W的Niktimvo治疗的患者中(n = 80),74%在治疗的前6个月内实现了总缓解率,中位反应时间为1.5个月。
3.3.Marstacimab(辉瑞公司)
Marstacimab(HYMPAVZI™,marstacimab-hncq,PF-06741086)是一种人IgG1λ抗体,靶向组织因子途径抑制剂的Kunitz 2结构域。该靶点是一种天然抗凝蛋白,防止血栓形成。Marstacimab正在开发作为一种预防措施,以预防或减少血友病患者的出血频率,被FDA授予快速通道指定,用于预防或减少有抑制剂的A型血友病或有抑制剂的B型血友病患者的出血发作频率,以及被FDA授予用于有或没有抑制剂的A型和B型血友病患者的孤儿药指定。EMA已授予marstacimab用于治疗血友病的孤儿药产品指定。Marstacimab在2024年在美国和欧盟均获批用于血友病。2024年10月11日,FDA批准HYMPAVZI™(marstacimab-hncq)用于治疗无抑制剂的A型或B型血友病成人和青少年。HYMPAVZI的推荐剂量包括300毫克的负荷剂量(两次150毫克皮下注射),1周后每周同一天皮下(SC)注射150毫克维持剂量,一天中的任何时间均可。该批准基于3期BASIS试验(NCT03938792)的结果,该试验表明与常规预防和按需治疗相比有显著的出血减少。在研究中,HYMPAVZI在无抑制剂的A型或B型血友病患者中,在12个月的积极治疗期后,与常规预防和按需治疗相比,分别将治疗出血的年化出血率降低了35%和92%。HYMPAVZI的安全性概况与1/2期结果一致。HYMPAVZI是首个每周一次皮下预防治疗,适用于患有B型血友病的合格人群,也是首个通过预填充笔或注射器给药的治疗,适用于患有A型或B型血友病的合格人群。欧洲委员会于2024年11月批准marstacimab用于12岁及以上体重至少35公斤的严重A型血友病(先天性因子VIII [FVIII]缺乏,FVIII < 1%)无FVIII抑制剂或严重B型血友病(先天性因子IX [FIX]缺乏,FIX < 1%)无FIX抑制剂患者的出血发作常规预防。欧盟的市场授权也基于关键的3期BASIS研究的结果。
3.4.Crovalimab(中外制药、基因泰克、F. 霍夫曼 - 拉罗氏有限公司)
Crovalimab(‘派圣凯®,PiaSky,crovalimab-akkz,SKY59,RG6107,RO7112689)是一种补体C5抑制、人源化IgG1κ抗体,经过M428L/N434A修饰以增强在酸性pH下对新生儿Fc受体的亲和力,从而延长其血浆半衰期。由中外制药开发的crovalimab缺乏效应子功能,旨在治疗阵发性夜间血红蛋白尿症(PNH)。利用中外制药的循环抗体®技术开发的crovalimab被设计为反复结合其抗原,允许以低剂量、每4周皮下注射一次(Q4W)的方式实现持续的补体抑制。与现有抗体药物不同,crovalimab靶向C5上的不同表位,为具有特定C5基因突变的PNH患者提供了潜在的替代治疗。2024年2月6日,皮下注射crovalimab在中国首次获批,用于治疗未接受过补体抑制剂治疗的12岁及以上青少年和成人PNH患者。该批准基于在PNH患者中进行的3期COMMODORE 2(NCT04434092)和COMMODORE 3(NCT04654468)研究的积极结果。Crovalimab随后于2024年3月在日本获批,用于治疗既往未治疗和既往已治疗的PNH患者,该批准基于3期COMMODORE 1(NCT04432584)和COMMODORE 2研究的积极结果,以及分别于2024年6月和8月在美国和欧盟获批。全球3期COMMODORE 1和2研究评估了crovalimab与eculizumab在PNH患者中的疗效和安全性。COMMODORE 1关注C5抑制剂经验患者,而COMMODORE 2涉及未接受过补体抑制剂治疗的患者。COMMODORE 1评估了crovalimab的安全性、药代动力学(PK)、药效学(PD)和探索性疗效。该研究的数据支持crovalimab的有利效益 - 风险概况,突出了皮下给药的便利性,以及自我给药的选择。COMMODORE 2研究的数据表明,每4周一次的皮下注射crovalimab在控制疾病方面不劣于每2周一次的静脉注射eculizumab,对于先前未接受过C5抑制剂的患者,安全性相当。COMMODORE 3是一项在中国进行的多中心、单臂试验,评估了crovalimab在C5抑制剂初治PNH患者(n = 51)中的疗效。患者接受了基于体重的剂量方案,包括初始负荷阶段(第1天和第4天静脉注射,从第2天开始每周皮下注射)和从第5周开始的每4周一次的维持皮下注射。对于有临床益处的患者,治疗延长超过24周。溶血控制和输血避免(TA)这两个共同主要终点均达到:78.7%实现了溶血控制(第5 - 25周),输血避免率从治疗前的0.0%增加到治疗后的51.0%(p < .0001)。
3.5.Zolbetuximab(安斯泰来制药公司)
Zolbetuximab(VYLOY,zolbetuximab-clzb)是一种嵌合IgG1κ抗体,靶向Claudin 18.2(CLDN18.2),最初由Ganymed Pharmaceuticals AG开发。安斯泰来于2016年收购了Ganymed。CLDN18.2是胃上皮的紧密连接分子,在恶性转化期间肿瘤细胞表面变得可接近。该蛋白还在其他癌症中异位表达,包括胰腺癌。CLDN18.2已成为癌症免疫治疗的有吸引力靶点,目前临床研究中有超过40种抗CLDN18.2抗体,包括一些双特异性和抗体药物偶联物(ADC)格式。2024年3月26日,日本厚生劳动省(MHLW)批准VYLOY™(zolbetuximab)用于CLDN18.2阳性、不可切除、晚期或复发性胃癌患者。Zolbetuximab随后分别于2024年8月、9月和10月在英国、欧盟和美国获批用于未治疗的CLDN18.2阳性、人表皮生长因子受体2(HER2)阴性不可切除晚期胃或胃食管连接部(G/GEJ)腺癌。Zolbetuximab是首个获批上市的抗CLDN18.2抗体。这些市场批准基于3期SPOTLIGHT(NCT03504397)和GLOW临床试验(NCT03653507)的数据。这两项试验均为随机(1:1)、双盲、多中心试验,包括CLDN18.2阳性、HER2阴性、局部晚期不可切除或转移性G/GEJ腺癌患者。SPOTLIGHT试验包括565名患者,随机分配接受zolbetuximab(800 mg/m²负荷剂量静脉注射,随后每3周600 mg/m²一次(Q3W)加上mFOLFOX6化疗(283名患者)或安慰剂加mFOLFOX6(282名患者)。GLOW研究评估了zolbetuximab加卡培他滨和奥沙利铂作为507名患者的一线治疗。在SPOTLIGHT研究中,zolbetuximab-clzb/化疗组的中位无进展生存期(PFS)为10.6个月(95% CI:8.9, 12.5),安慰剂/化疗组为8.7个月(95% CI:8.2, 10.3)(风险比[HR] 0.751 [95% CI:0.598, 0.942];单侧p值 = .0066)。中位总生存期(OS)分别为18.2个月(95% CI:16.4, 22.9)和15.5个月(95% CI:13.5, 16.5)(HR 0.750 [95% CI:0.601, 0.936];单侧p值 = .0053)。在GLOW研究中,zolbetuximab-clzb/化疗组的中位PFS为8.2个月(95% CI:7.5, 8.8),安慰剂/化疗组为6.8个月(95% CI:6.1, 8.1)(HR 0.687 [95% CI:0.544, 0.866];单侧p值 = .0007)。中位OS分别为14.4个月(95% CI:12.3, 16.5)和12.2个月(95% CI:10.3, 13.7)(HR 0.771 [95% CI:0.615, 0.965];单侧p值 = 0.0118)。
3.6.Tarlatamab(安进公司)
Tarlatamab(IMDELLTRA™,tarlatamab-dlle,AMG 757)是由安进公司开发的延长半衰期的抗Delta样配体3(DLL3)×抗CD3双特异性T细胞接合抗体。它结合肿瘤细胞上的DLL3和T细胞上的CD3,激活T细胞靶向并杀死表达DLL3的小细胞肺癌(SCLC)细胞。2024年5月16日,美国食品药品监督管理局(FDA)授予IMDELLTRA™(tarlatamab-dlle)加速批准,用于治疗成人广泛期(ES)SCLC患者,这些患者在接受铂类化疗后疾病进展。Tarlatamab是首个获批上市的靶向DLL3的抗体。该批准基于临床试验中观察到的有希望的响应率和响应持续时间(DoR)。该批准得到了2期DeLLphi-301(NCT04471727)试验的结果支持,该试验评估了IMDELLTRA在先前接受过两种或更多治疗方案失败的患者中的疗效,这些患者接受了10 mg Q2W剂量方案。研究发现,此剂量的IMDELLTRA(n = 99)显示出显著的客观响应率(ORR)40%(95% CI:31, 51)和中位DoR 9.7个月(CI:2.7, 20.7+)。中位OS为14.3个月,最终生存数据仍在等待中。安全性概况可控,细胞因子释放综合征(CRS)是最常见的不良事件。2024年9月,安进公司展示了DeLLphi-301 2期研究的扩展随访数据,显示IMDELLTRA在先前接受过铂类化疗的ES-SCLC患者中具有持续的抗癌活性和可控的安全性概况。Tarlatamab正在多项研究中进行调查,包括DeLLphi-303(NCT05361395),一项1b期研究,调查tarlatamab与标准治疗(SOC)在一线ES-SCLC中的联合应用;DeLLphi-304(NCT05740566),一项随机3期试验,比较tarlatamab单药治疗与SOC化疗在SCLC二线治疗中的疗效;DeLLphi-305(NCT06211036),一项随机3期试验,比较tarlatamab与durvalumab联合应用与单独durvalumab作为ES-SCLC一线维持治疗的疗效;DeLLphi-306(NCT06117774),一项随机安慰剂对照3期试验,评估tarlatamab在局限期SCLC患者接受同步放化疗后的疗效;以及DeLLpro-300,一项1b期研究,评估tarlatamab在原发性或治疗相关神经内分泌前列腺癌中的应用。
3.7.Zanidatamab(百济神州、Jazz Pharmaceuticals Plc、Zymeworks Inc)
Zanidatamab(ZW25)是一种人源化、双特异性、双特异性IgGκ,由半抗体(Fab-h-CH2-CH3 × scFv-h-CH2-CH3)组成,靶向HER2的两个非重叠表位。2022年,Zymeworks将美国、欧洲、日本和所有其他地区(除Zymeworks之前许可的亚太地区)的开发和商业化权利授权给Jazz Pharmaceuticals。百济神州于2018年获得了Zanidatamab在亚洲(除日本外)、澳大利亚和新西兰的独家开发和商业化权利。美国食品药品监督管理局(FDA)授予Zanidatamab突破性治疗指定,用于先前治疗过的HER2基因扩增BTC患者,快速通道指定,用于Zanidatamab单药治疗难治性BTC,以及孤儿药指定,用于难治性BTC。2024年11月20日,Jazz Pharmaceuticals宣布FDA授予Ziihera®(zanidatamab-hrii)50 mg/mL注射液加速批准,用于治疗先前治疗过、不可切除或转移性HER2阳性(IHC 3+)胆管癌(BTC)成人,该诊断由FDA批准的测试确定。一项确认性、随机3期试验(HERIZON-BTC -302;NCT06282575)正在评估zanidatamab与SOC治疗联合应用与SOC治疗单独应用在HER2阳性BTC患者一线治疗中的疗效,该试验于2024年7月启动,目前正在招募患者。该批准部分基于zanidatamab在HER2扩增、不可切除、局部晚期或转移性BTC患者中的单臂、2b期试验(HERIZON-BTC-01;NCT04466891)的结果,这些患者在先前基于吉西他滨的治疗中疾病进展。患者(n = 87)接受zanidatamab 20 mg/kg静脉注射Q2W。患者根据HER2免疫组化(IHC)评分分为队列:队列1(IHC 2+或3+;HER2阳性)和队列2(IHC 0或1+)。主要终点是队列1中经独立中央审查(ICR)评估的确认客观响应率。中位随访时间为12.4个月(四分位间距9.4–17.2)。队列1中33名患者(41.3%(95% CI 30.4–52.8))观察到确认客观响应,但队列中HER2低表达患者未观察到响应。Zanidatamab作为BTC治疗的市场申请也已提交至欧盟和中国。百济神州预计NMPA将在2025年下半年批准zanidatamab作为HER2+ BTC的二线治疗。除了BTC,zanidatamab还在3期研究中作为HER2+乳腺癌(NCT06435429)和胃癌(NCT05152147)的治疗进行评估。
3.8.Zenocutuzumab(Merus N.V.)
Zenocutuzumab(MCLA-128)是一种人源化、ADCC增强的双特异性IgG1κ抗体,同时靶向生长因子受体HER2和HER3,从而阻断由HER3与其配体neuregulin 1(NRG1)或NRG1融合蛋白结合引起的信号传导。该抗体由Merus开发,用于治疗携带NRG1基因融合(NRG1+癌症)的实体瘤患者,这些患者通常对传统系统治疗反应不佳。美国食品药品监督管理局(FDA)授予Zenocutuzumab突破性治疗指定,用于治疗先前系统治疗后疾病进展或没有满意替代治疗选择的晚期不可切除或转移性NRG1+胰腺癌患者,以及快速通道指定,用于治疗在SOC治疗后进展的转移性NRG1+癌症患者和孤儿药指定,用于治疗胰腺癌患者。2024年12月4日,Merus N.V.宣布FDA批准BIZENGRI®(zenocutuzumab-zbco)作为治疗成人胰腺腺癌或NSCLC的药物,这些患者为晚期不可切除或转移性,并携带NRG1基因融合,且在接受先前系统治疗后疾病进展。该批准基于开放标签1/2期eNRGy试验(NCT02912949)的数据,该试验评估了zenocutuzumab单药治疗在NRG1+ NSCLC、PDAC和其他实体瘤中的安全性和抗肿瘤活性。该研究包括三个患者队列:1)NRG1+ NSCLC,2)NRG1+ PDAC,和3)其他NRG1+实体瘤。在eNRGy研究的剂量扩展期间,参与者接受每2周一次的750 mg zenocutuzumab静脉输注。响应率使用RECIST v1.1由盲法ICR评估。NRG1+ NSCLC(n = 64)和NRG1+ PDAC(n = 30)队列的ORR分别为33%(95% CI,22%–46%)和40%(95% CI,23%–59%),NRG1+ NSCLC队列的中位DOR为7.4个月(95% CI,4.0–16.6),NRG1+ PDAC队列的中位DOR范围为3.7个月至16.6个月。
3.9.Odronextamab(Regeneron Pharmaceuticals, Inc)
Odronextamab(Ordspono™,REGN1979)是一种人源、铰链稳定、抗CD20×CD3双特异性IgG4κ抗体。Fc区域经过工程改造(E233P, F234V, L235A, G236del),以减少效应子功能。Regeneron的VelocImmune®技术和Veloci-Bi®平台被用来创建该抗体,该公司正在开发该抗体用于治疗复发/难治性B细胞NHL,包括FL和DLBCL。Odronextamab获得了FDA的快速通道指定,以及FDA和EMA分别授予的用于治疗滤泡性淋巴瘤(FL)和弥漫性大B细胞淋巴瘤(DLBCL)患者的孤儿药和孤儿药产品指定。Regeneron在美国和欧盟提交了用于FL和DLBCL的odronextamab的市场申请。基于EMA的积极意见,欧洲委员会于2024年8月批准odronextamab用于治疗接受过两线或更多系统治疗的成人复发/难治性(R/R)FL或R/R DLBCL。该批准得到了1期ELM-1(NCT02290951)和关键2期ELM-2(NCT03888105)试验的结果支持,这些试验表明odronextamab在成人R/R FL或R/R DLBCL中具有强大、持久的响应率和可接受的安全性概况。在ELM-2研究中入组的R/R FL患者(n = 128)中,ORR为80%;其中73%达到完全响应,中位DoR为25个月。在嵌合抗原受体T细胞疗法初治的R/R DLBCL患者中入组的ELM-2(n = 127)研究中,ORR为52%,其中31%达到CR。在完全响应者中,中位DoR为18个月。2024年3月,美国食品药品监督管理局(FDA)对odronextamab在R/R FL和R/R DLBCL的生物制品许可申请(BLAs)发出完全回应函(CRLs),每种都是在两线或更多系统治疗后。唯一可批准性问题涉及确认性试验的入组状态。Regeneron正在赞助OLYMPIA项目中淋巴瘤患者的多项3期odronextamab试验。FDA要求这些试验包括剂量寻找和确认性部分。虽然剂量寻找部分的入组已经开始,但CRLs表明这些试验的确认性部分应该正在进行中,并且在重新提交之前应同意完成的时间表。截至2024年11月初,Regeneron尚未公开披露这些时间表的更新。
4.2024年仅在中国或俄罗斯首次获得市场批准
4.1.马佐雷维单抗、扎莫雷维单抗(Synermore Biologics Co. Ltd.)
马佐雷维单抗和扎莫雷维单抗(克瑞毕®,SYN-023)是两种人源化IgG1κ抗体CTB-011和CTB-012的1:1混合物,它们结合狂犬病外膜糖蛋白的非重叠表位。2024年6月,中国的国家药品监督管理局(NMPA)批准了马佐雷维单抗和扎莫雷维单抗的混合物用于狂犬病的暴露后预防治疗。在一项随机的3期研究(NCT04644484)中,将马佐雷维单抗和扎莫雷维单抗混合物与人狂犬病免疫球蛋白(HRIG)进行了比较,作为对成人3类狂犬病暴露风险的暴露后预防。该研究在中国进行,共招募了1000名参与者,他们接受了中国许可的狂犬病疫苗,并与干预措施(即研究性抗体混合物或对照剂HRIG)联合使用。干预措施通过直接注入伤口进行,如无法实现,则通过皮下(SC)或肌肉(IM)注射。2期NCT03961555临床研究的结果最近也已报告,该研究同样评估了马佐雷维单抗和扎莫雷维单抗混合物的效果,研究设计与NCT04644484研究类似。NCT03961555研究招募了448名参与者,他们被随机分配在潜在狂犬病暴露后的54小时内接受0.3 mg/kg SYN023或0.133 mL/kg HRIG以及狂犬病疫苗。结果显示,马佐雷维单抗和扎莫雷维单抗混合物与狂犬病疫苗(RabAvert/Rabipur)的抗狂犬病免疫反应不劣于HRIG和疫苗。在任何患者中均未发生可能/确诊的狂犬病病例,马佐雷维单抗和扎莫雷维单抗混合物的安全性可接受。
4.2.夫那奇珠单抗(江苏恒瑞医药股份有限公司)
夫那奇珠单抗(SHR-1314,夫那奇珠单抗,安达静®)是一种人源化IgG1κ单克隆抗体,它结合IL-17A,这是一种在多种自身免疫性疾病相关的炎症过程中起关键作用的细胞因子。2024年8月20日,夫那奇珠单抗被NMPA批准用于治疗适合系统治疗或光疗的中度至重度斑块型银屑病成人患者。夫那奇珠单抗的批准基于一项多中心、随机、双盲、平行、安慰剂对照的3期临床研究(SHR-1314-301)。共招募了690名中度至重度斑块型银屑病成人患者,并以2:1的比例随机分配到夫那奇珠单抗组(240 mg Q2W随后240 mg Q4W)或安慰剂组(第12周转为夫那奇珠单抗240 mg治疗,第12、14、16周Q2W给药,此后Q4W)。共同主要终点是第12周达到银屑病面积和严重程度指数90(PASI 90)的受试者比例和第12周达到静态医生全球评估(sPGA)评分0/1的受试者比例。关键次要终点包括第12周达到PASI 75/PASI 100的受试者比例和sPGA评分为0的受试者比例。在第12周,夫那奇珠单抗组的PASI 90应答率为76.8%,而安慰剂组为0.9%。同样,夫那奇珠单抗组的sPGA 0/1应答率为71.8%,而安慰剂组为0.4%。其他关键指标也显示出显著差异:PASI 75为93.6%对4.0%,PASI 100达到36.6%对0.0%,sPGA 0的应答率为38.2%对0.0%。夫那奇珠单抗组的疗效在第52周得以维持,PASI 100和sPGA 0的应答率分别达到63.1%和63.3%。夫那奇珠单抗的临床反应起效迅速,PASI的平均百分比降低在第2周就超过了50%。到第4周,56.6%的参与者已经实现了PASI 75应答。在12周诱导期内,接受夫那奇珠单抗治疗的受试者与接受安慰剂的受试者在不良反应的发生率和严重程度上相似。
4.3.赛立奇单抗(重庆智翔金泰生物制药股份有限公司)
赛立奇单抗(GR1501,赛立奇单抗,金立希®)是一种针对白细胞介素-17A(IL-17A)的人源、铰链稳定的IgG4κ抗体,IL-17A是一种涉及多种免疫介导炎症疾病的细胞因子。2024年8月27日,智翔金泰宣布赛立奇单抗已获得NMPA的市场授权,用于治疗适合系统治疗或光疗的中度至重度斑块型银屑病成人患者。2024年1月,赛立奇单抗用于放射学轴性脊柱关节炎的NDA被NMPA接受。赛立奇单抗的批准基于一项针对中度至重度斑块型银屑病患者的随机、双盲、安慰剂对照、多中心3期临床研究(CTR20210246/ChiCTR2100043223)。患者被随机分配到200 mg赛立奇单抗皮下注射Q2W(n = 281)或安慰剂(n = 139)进行前12周的治疗,随后治疗方案延长至赛立奇单抗Q4W再进行40周。到第12周,赛立奇单抗组90.7%的参与者从基线至少改善了75%,而安慰剂组为8.6%。此外,治疗组74.4%的患者在第12周达到皮肤清晰或几乎清晰(PGA 0/1),而安慰剂组为3.6%。主要终点成功达到。此外,次要临床终点也得以实现,第12周的PASI 90应答率为74.4%。PASI 75/90和PGA 0/1应答维持至第52周,显示出显著且持久的疗效。
4.4.康悦达(凯美博生技股份有限公司)
康悦达(康悦达®,Kangyueda,CM310)是由凯美博生技开发的一种人源化、铰链稳定的IgG4κ单克隆抗体,靶向白细胞介素-4受体α(IL-4 Rα),阻断IL-4和IL-13信号传导,最终减少2型炎症。2024年9月12日,凯美博生技宣布NMPA已批准康悦达用于治疗中度至重度特应性皮炎。凯美博还正在寻求补充批准。2024年6月,康悦达用于治疗慢性鼻窦炎伴鼻息肉(CRSwNP)的NDA被NMPA接受并授予优先审评。2024年4月,NMPA接受了康悦达针对季节性过敏性鼻炎的NDA。凯美博还与石药集团合作,在中国开发和商业化康悦达,用于治疗中度至重度哮喘、慢性阻塞性肺病和其他呼吸系统疾病。NMPA的批准基于一项多中心、随机、双盲、安慰剂对照的3期确证性临床研究(CM310AD005)的结果。该试验评估了康悦达在中度至重度特应性皮炎患者中的疗效、安全性、药代动力学/药效学(PK/PD)和免疫原性。共500名合格患者以1:1的比例随机分配到接受康悦达(600–300 mg Q2W)或安慰剂。共同主要终点是治疗第16周时达到湿疹面积和严重程度指数改善≥75%(EASI-75)的受试者比例和IGA评分为0或1且从基线降低≥2分的受试者比例。结果显示,经过16周的康悦达治疗后,达到EASI-75的受试者比例达到66.9%,而44.2%的受试者IGA评分为0或1且从基线降低≥2分,均超过了安慰剂组(分别为25.8%和16.1%),两者差异均有统计学意义(p < 0.0001)。两个共同主要终点均成功达成。在维持治疗期的第52周,康悦达组的EASI-75达成率为92.5%,从安慰剂转为康悦达的为88.7%。达到IGA评分为0或1且从基线降低≥2分的比例分别为67.3%和64.2%。
4.5.伊喜宁(Akeso Biopharma, Inc.)
伊喜宁(AK102,伊喜宁®)是由Akeso Biopharma, Inc.和AD Pharmaceuticals联合开发的一种人源抗PCSK9 IgG1λ单克隆抗体治疗高胆固醇血症。2024年9月,NMPA批准伊喜宁用于治疗原发性高胆固醇血症和混合型高脂血症以及杂合子家族性高胆固醇血症(HeFH)。批准基于四项随机关键研究的结果,包括三项评估伊喜宁与安慰剂对比治疗原发性高胆固醇血症和混合型高脂血症的研究(CTR20212815(450 mg Q4W剂量),CTR20213363(450 mg或600 mg Q6W剂量),CTR20212466(450 mg Q4W或150 mg Q2W))和一项治疗HeFH的研究(CTR20191935(450 mg Q4W,300 mg Q4W,或150 mg Q2W剂量))。伊喜宁的疗效结果在不同研究和不同适应症人群中均一致,显示伊喜宁可显著降低从基线的低密度脂蛋白胆固醇(LDL-C)水平,每个剂量周期的最大降低超过65%。3期CTR20212466研究(NCT05255094)的结果显示,伊喜宁在中国患者中具有显著的LDL-C降低效果,这些患者接受了450 mg Q4W或150 mg Q2W剂量。
4.6.昂戈瑞西单抗(上海君实生物医药科技股份有限公司)
昂戈瑞西单抗(JS002,昂戈瑞西单抗,君适达®)是由君实生物开发的一种人源化、铰链稳定的抗PCSK9 IgG4κ单克隆抗体。2024年10月11日,它获得了NMPA的批准,用于治疗原发性高胆固醇血症和混合型血脂异常(与他汀类药物联合使用)。此外,目前还有两个sNDAs正在NMPA审查中。这些包括一个用于治疗杂合子家族性高胆固醇血症的,以及另一个用于对他汀类药物不耐受或禁忌的原发性高胆固醇血症和混合型血脂异常患者(作为单一药物)的。批准主要基于两项关键的3期临床试验,均为多中心、随机、双盲和安慰剂对照:JS002–003(NCT04781114)和JS002–006(NCT05532800)。JS002–003研究评估了皮下注射昂戈瑞西单抗治疗中国原发性高胆固醇血症和混合型血脂异常的疗效和安全性,共招募了806名参与者。该试验结果显示,以150 mg Q2W或300 mg Q4W剂量皮下注射昂戈瑞西单抗,可显著降低LDL胆固醇水平——与安慰剂相比超过60%。这些降低在52周治疗期内得以维持。此外,昂戈瑞西单抗还显著改善了其他脂质指标,包括非HDL胆固醇、载脂蛋白B(ApoB)和总胆固醇。昂戈瑞西单抗的安全性良好,在研究期间未出现新的安全性问题。JS002–006研究旨在评估通过两种不同的皮下注射装置——预填充注射器和自动注射器——给药昂戈瑞西单抗治疗原发性高胆固醇血症和混合型血脂异常的疗效和安全性。该试验共招募了255名参与者。研究发现,两种昂戈瑞西单抗给药方式均显示出显著的降脂效果。在150 mg Q2W剂量治疗12周后,预填充注射器组的LDL胆固醇水平降低了72.7%,自动注射器组降低了71.1%,与安慰剂相比,均显示出良好的安全性。
4.7.恩朗苏拜单抗(石药集团有限公司)
恩朗苏拜单抗(SG001,恩舒幸®)是一种人源、铰链稳定的抗PD-1 IgG4κ单克隆抗体,阻断PD-1通路,使免疫细胞能更有效地靶向和摧毁癌细胞。恩朗苏拜单抗最初由杭州尚健生物技术有限公司开发。2018年11月,尚健生物与石药集团达成战略协作,共同开发恩朗苏拜单抗。2024年6月,恩朗苏拜单抗获NMPA有条件批准上市,用于治疗既往接受过铂类化疗失败、PD-L1表达阳性(联合阳性评分CPS≥1)的复发或转移性宫颈癌患者。恩朗苏拜单抗的批准主要基于一项关键的2期临床试验(NCT04886700)数据,该试验在晚期宫颈癌治疗中显示出显著的客观缓解率(ORR)改善。在这项多中心、单臂、开放标签的研究中,共纳入107名宫颈癌患者,每名患者接受240 mg恩朗苏拜单抗Q2W治疗,最大治疗时长24个月,或直至疾病进展、不可耐受的毒性或其他研究终止标准出现。试验结果显示,经独立影像审查委员会评估,ORR为29%,其中2名患者达到完全缓解,29名患者部分缓解。中位缓解持续时间(DoR)为16.6个月。此外,恩朗苏拜单抗展现出良好的安全性。一项正在进行的3期临床试验(NCT05715840/CTR20230132)正在评估恩朗苏拜单抗联合铂类化疗、有或无贝伐珠单抗,作为复发或转移性宫颈癌患者的一线治疗,这些患者PD-L1表达阳性(CPS≥1)。此外,还有数项其他临床研究正在进行中,以探索恩朗苏拜单抗与纳米药物、抗体药物、抗体药物偶联物(ADCs)和小分子疗法联合治疗各种实体瘤的潜力。
4.8.齐倍安(齐鲁普吉声生物治疗有限公司)
齐倍安是齐鲁普吉声生物治疗有限公司开发的两种单克隆抗体混合物PSB205(也称QL1706)的组成部分,分别为抗PD-1的伊帕洛利单抗和抗CTLA-4的图沃纳利单抗。该混合物由单一细胞系通过公司的专有MabPair技术生产。伊帕洛利单抗是一种铰链稳定的IgG4单克隆抗体,而图沃纳利单抗是一种IgG1单克隆抗体,其重链和轻链均带有突变,以确保正确链的高效配对。2024年9月,NMPA授予PSB205加速批准,用于治疗复发或转移性宫颈癌。批准基于齐鲁药业在中国开展的关键、单臂2期DUBHE-C-206研究(NCT05557565)的结果,该研究包括148名对免疫检查点抑制剂无经验、复发或转移性宫颈癌患者,这些患者既往接受过一线铂类化疗,有或无贝伐珠单抗。患者接受伊帕洛利单抗和图沃纳利单抗5.0 mg/kg静脉注射Q3W。研究的主要终点是由独立审查委员会(IRC)评估的ORR,评估期长达2年。ORR为33.8%,疾病控制率(DCR)为64.9%,中位无进展生存期(PFS)为5.4个月。一项正在进行的随机、双盲、安慰剂对照3期试验(NCT05446883),评估伊帕洛利单抗和图沃纳利单抗联合化疗作为持续性、复发性或转移性宫颈癌的一线治疗,预计在2024年9月完成。伊帕洛利单抗和图沃纳利单抗混合物还在研究作为鼻咽癌(NPC)和非小细胞肺癌(NSCLC)的治疗。在NPC中,一项单臂2期研究(NCT05576272)的结果最近报告,该研究涉及29名患者,他们接受QL1706(5 mg/kg静脉注射)联合化疗(吉西他滨和顺铂)。主要终点是安全性和耐受性,次要终点包括ORR、PFS和总生存期(OS)。中位随访时间为15.5个月,中位ORR和PFS分别为82.1%和12.5个月,而中位OS尚未达到。在NSCLC中,一项开放标签、多队列2期研究(NCT05329025)的结果最近报告,该研究评估了QL1706联合贝伐珠单抗、紫杉醇或培美曲塞以及卡铂在91名晚期表皮生长因子受体(EGFR)野生型(60名患者)和EGFR突变(31名患者)NSCLC患者中的疗效和安全性。所有药物均在每周期第1天Q3W静脉注射,QL1706剂量为5 mg/kg。对于EGFR野生型NSCLC患者,ORR为45%,中位PFS为6.8个月。在经EGFR酪氨酸激酶抑制剂(TKI)治疗后进展的EGFR突变NSCLC患者中,ORR为54.8%,中位PFS为8.5个月。
4.9.安奈韦(中国生物制药有限公司)
安奈韦(Andewei, TQB2450)是由中国生物制药有限公司子公司正大天晴药业开发的一种人源化抗PD-L1 IgG1κ单克隆抗体,其Fc段经过工程改造以降低效应功能(D265A)。2024年4月29日,安奈韦获NMPA批准与安罗替尼、卡铂和依托泊苷联合用于ES-SCLC的一线治疗,该批准基于随机、双盲、安慰剂对照、多中心3期ETER701(NCT04234607)试验的结果。研究比较了安奈韦和安罗替尼联合依托泊苷/卡铂(EC;n = 246)、安慰剂/安罗替尼联合EC(n = 245)或双安慰剂/EC单独(n = 247)。安奈韦(1,200 mg静脉注射)在每个21天周期的第1天给药。安奈韦和安罗替尼联合EC治疗组的中位总生存期(OS)显著改善(19.3个月),与化疗单独(依托泊苷/卡铂)组(OS 11.9个月;风险比HR 0.61,p < 0.05)相比,而安罗替尼联合EC的OS改善在统计学上不显著(13.3与11.9个月;HR 0.86;p = 0.1723)。与EC单独组相比,安奈韦和安罗替尼联合EC组的中位IRC评估的PFS显著更长(6.9个月(95% CI 6.2–8.3)与4.2个月(95% CI 4.17–4.24);HR 0.32(95% CI 0.26–0.41);p < 0.0001),安罗替尼联合EC组也是如此(5.6个月(95% CI 5.6–6.8)与4.2个月(95% CI 4.17–4.24);HR 0.44(95% CI 0.36–0.55);p < 0.0001)。截至2024年7月,NMPA正在审查安奈韦针对两个额外适应症的上市申请:1)与安罗替尼联合用于治疗复发或转移性子宫内膜癌,这些患者既往接受过一线或二线化疗方案,但治疗失败或不耐受;2)与安罗替尼联合用于晚期不可切除或转移性肾细胞癌的一线治疗。安奈韦还在进行其他适应症的3期临床试验评估,包括NSCLC放疗和化疗后的维持治疗以及一线NSCLC。
4.10.依达方(康方生物、Summit Therapeutics)
依达方®是一种四价、双特异性抗体,靶向PD-1和人血管内皮生长因子(VEGF),经过工程改造以降低效应功能(L234A, L235A)。通过靶向这两种抗原,该分子将癌症免疫疗法与抗血管生成机制相结合。康方生物已将依达方在包括美国、加拿大、欧洲、日本、拉丁美洲、非洲和中东等特定地区的开发和商业化权利独家授权给Summit Therapeutics。迄今为止,依达方的晚期临床研究主要集中在NSCLC适应症上。NMPA已授予依达方三项突破性治疗认定,用于在不同环境和患者人群中治疗NSCLC。2024年5月,NMPA批准依达方与化疗联合用于治疗经EGFR TKIs治疗后进展的EGFR突变局部晚期或转移性非鳞状NSCLC患者。依达方是首个获得上市批准的靶向PD-1和VEGF组合的抗体。批准基于在中国进行的随机、双盲3期hARMONi-A研究(AK112–301, NCT05184712, CTR20213079)的结果。患者按1:1随机分配接受静脉注射依达方(20 mg/kg)联合培美曲塞(500 mg/m2)和卡铂(AUC 5)(n = 161)或静脉注射安慰剂联合化疗(n = 161)Q3W,共四个周期。主要终点是由IRC根据实体肿瘤疗效评价标准(RECIST)v1.1在意向治疗(ITT)人群中评估的PFS。中位随访时间为7.89个月。依达方组的中位PFS为7.1(95% CI, 5.9–8.7)个月,而安慰剂组为4.8(95% CI, 4.2–5.6)个月(差异,2.3个月;HR, 0.46 [95% CI, 0.34–0.62]; p < 0.001)。依达方组的ORR为50.6%(95% CI, 42.6%–58.6%),而安慰剂组为35.4%(95% CI, 28.0%–43.3%)(差异,15.6% [95% CI, 5.3%–26.0%]; p = 0.006)。2024年7月,康方生物向NMPA提交了依达方单药用于一线治疗PD-L1阳性(PD-L1 TPS ≥ 1%)局部晚期或转移性NSCLC的补充生物制品许可申请。补充BLA基于3期hARMONi-2(AK112–303, NCT05499390)研究的结果,该研究评估了依达方与抗PD-1帕博利珠单抗(Keytruda®)相比,作为一线治疗晚期NSCLC患者的疗效和安全性,这些患者的肿瘤PD-L1表达阳性(TPS≥1%)。患者(总计n = 398)随机分配接受选定剂量的静脉注射依达方或200 mg Q3W静脉注射帕博利珠单抗。研究的主要终点是由IRRC根据RECIST v1评估的PFS。2024年9月报告了HARMONi-2研究预设中期分析数据的积极顶层结果。在ITT人群中,依达方组的中位PFS为11.14个月,而帕博利珠单抗组为5.82个月,依达方组的ORR为50.0%,而帕博利珠单抗组为38.5%。此外,在亚组分析中,依达方在年龄、性别、PD-L1表达、组织学类型以及肝或脑转移的存在等因素上均优于帕博利珠单抗。
4.11.Sacituzumab Tirumotecan(四川科伦制药有限公司,Merck & Co.)
Sacituzumab tirumotecan (佳泰萊®, SKB264, MK-2870) 是一种人源化 IgG1κ 抗体药物偶联物(ADC),靶向 TROP2,携带专有的细胞毒性、belotecan 衍生物载荷。该 ADC 的平均药物抗体比(DAR)为 7.4,包含一个水解连接子,能够实现细胞外 pH 敏感性裂解和细胞内酶促裂解以释放膜通透性载荷。2022 年,科伦药业将 sacituzumab tirumotecan 在大中华区(包括中国大陆、香港、澳门和台湾)以外地区的开发权授予了默沙东公司。Sacituzumab tirumotecan 已获得国家药品监督管理局(NMPA)的三项突破性疗法认定:1)局部晚期或转移性三阴性乳腺癌(TNBC);2)局部晚期或转移性 HR 阳性和 HER2− 乳腺癌,且已接受至少二线系统治疗;3)局部晚期或转移性 EGFR 突变 NSCLC,且 EGFR-TKI 治疗失败。
2024 年 11 月 21 日,NMPA 批准 sacituzumab tirumotecan 在中国上市,用于治疗不可切除的局部晚期或转移性 TNBC 成人患者,这些患者已接受至少两种先前的系统治疗,其中至少一种是针对晚期或转移性疾病的治疗。该批准基于 Phase 3 OptiTROP-Breast01 研究的积极结果。
Phase 3 OptiTROP-Breast01 研究(NCT05347134)的结果最近报告称,sacituzumab tirumotecan 单药治疗在无进展生存期(PFS)和总生存期(OS)方面显示出统计学上显著和临床意义的益处,优于化疗。在这项研究中,局部复发或转移性 TNBC 患者,之前接受过两种或更多治疗,包括至少一种针对转移性疾病的治疗,被随机分配(1:1)到实验组(n = 130)和对照组(n = 133),按先前治疗线数(2–3 vs. >3)分层。然后比较了 sacituzumab tirumotecan(5 mg/kg,每 28 天周期的第 1 天和第 15 天静脉注射)与对照组(医生选择的化疗药物,包括艾日布林、长春瑞滨、卡培他滨或吉西他滨)的效果。主要终点是由盲法独立中心审查(ICR)评估的无进展生存期(PFS)。TROP2 表达通过免疫组化(IHC)使用半定量 H 评分方法确定。基于中期分析(数据截止日期:2023 年 6 月 21 日),主要终点 PFS 达到,进展或死亡风险降低 69%(HR 0.31;95% CI,0.22 至 0.45;p < 0.00001)。由盲法 ICR 评估的中位 PFS 分别为 sacituzumab tirumotecan 组 5.7 个月(95% CI,4.3 至 7.2)和化疗组 2.3 个月(95% CI,1.6 至 2.7),6 个月时的 PFS 分别为 43.4% 和 11.1%。在 TROP2 H 评分 >200 的患者亚组中,中位 PFS 分别为 SKB264 组 5.8 个月和化疗组 1.9 个月(HR 0.28;95% CI,0.17 至 0.48)。由盲法 ICR 评估的客观反应率分别为 SKB264 组 43.8% 和化疗组 12.8%。
目前,NMPA 正在审查两项补充营销申请。2024 年 8 月,NMPA 接受了 sacituzumab tirumotecan 用于治疗局部晚期或转移性 EGFR 突变 NSCLC 患者的营销申请,这些患者在 EGFR-TKI 治疗和铂类化疗后失败。2024 年 10 月,NMPA 又接受了一项针对局部晚期或转移性 EGFR 突变 NSCLC 成人患者的治疗申请,这些患者在 EGFR-TKI 治疗后病情进展。
sacituzumab tirumotecan 用于治疗局部晚期或转移性 EGFR 突变 NSCLC 患者的营销申请,这些患者在 EGFR-TKI 和铂类化疗治疗后失败,是基于 OptiTROP-Lung03 研究的结果。这项随机、关键性临床研究评估了 sacituzumab tirumotecan 单药治疗(5 mg/kg,每两周静脉注射一次)与多西他赛相比,用于治疗 EGFR-TKI 治疗和铂类化疗后失败的局部晚期或转移性 EGFR 突变 NSCLC 患者。在预先指定的分析中,sacituzumab tirumotecan 单药治疗在客观反应率(ORR)和无进展生存期(PFS)方面显示出统计学上显著和临床意义的改善,优于多西他赛。
默沙东已启动了 10 项 Phase 3 临床试验,评估 sacituzumab tirumotecan。其中五项研究正在招募 NSCLC 患者(NCT06074588、NCT06170788、NCT06312137、NCT06305754 和 NCT06422143),另外分别招募子宫内膜癌(NCT06132958)、HR+/HER2− 不可切除的局部晚期或转移性乳腺癌(NCT06312176)、宫颈癌(NCT06459180)、TNBC(NCT06393374)和胃食管癌(NCT06356311)患者的研究各一项。
4.12.Seniprutug (BIOCAD)
Seniprutug(Tribuvia®,BCD-180)是由 BIOCAD 和来自皮罗戈夫俄罗斯国家研究医科大学的科学家共同开发的人源化抗 T 细胞受体 Vbeta9 IgG1 单克隆抗体。2024 年 4 月,俄罗斯联邦卫生部注册了 seniprutug(Tribuvia®),用于治疗放射学轴性脊柱关节炎(axSpA)患者。Seniprutug 是首个获得市场批准的针对 TCR Vbeta9 的抗体。
在 5 臂 Phase 3 LEVENTA 研究(NCT06333210)中,比较了固定剂量的 seniprutug 与阿达木单抗和安慰剂在活动性 axSpA 患者中的效果。该研究在白俄罗斯和俄罗斯联邦进行,包括 HLA-B27+ 的放射学 axSpA 和非放射学 axSpA 患者,这些患者对先前的非甾体抗炎药(NSAIDs)治疗无反应,未接受生物疾病修饰抗风湿药物(bDMARDs)或靶向合成疾病修饰抗风湿药物(tsDMARDs),以及那些在 bDMARDs 和/或 tsDMARDs 上疗效不足和/或失去疗效的患者。研究组的干预措施为:1)静脉注射 seniprutug;2)静脉注射安慰剂;3)静脉注射 seniprutug + 皮下注射安慰剂;4)静脉注射 + 皮下注射安慰剂;5)静脉注射安慰剂 + 皮下注射阿达木单抗。主要结果指标是在第 24 周时,bDMARDs 和 tsDMARDs 初治患者以及 bDMARDs 和/或 tsDMARDs 经治患者中达到 ASAS40 的受试者比例。ASAS40(脊柱关节炎评估 40%)反应定义为在设计用于评估 axSpA 严重程度的评分系统中四个领域中的三个领域改善 ≥ 40%。
在 Phase 2 ELEFTA 研究(NCT05445076)中,seniprutug 显示出优于安慰剂的效果,该研究评估了两种剂量的 seniprutug 与安慰剂相比,在活动性放射学 axSpA 患者中的效果。研究包括 HLA-B27+ 的放射学 axSpA 患者,这些患者对先前的 NSAIDs 治疗无反应,未接受生物治疗或 tDMARDs。共 260 名患者被随机分配到三个组,分别接受 5 mg/kg 或 7 mg/kg 剂量的 seniprutug 或安慰剂。Seniprutug 在第 0、12、36 周给药。安慰剂组的患者在第 24 周转为 5 mg/kg 剂量的 seniprutug,并在第 36 周继续治疗。主要结果指标是在第 24 周时达到 ASAS40 的受试者比例。在第 24 周时,接受 7 mg/kg 和 5 mg/kg 剂量 seniprutug 的患者中达到 ASAS40 的比例分别为 51.4% 和 40.8%,而安慰剂组为 24%(p = 0.0012 和 p = 0.0417,分别)。Seniprutug 治疗的耐受性被认为是可接受的。
5.抗体疗法接受首次监管审查
截至 2024 年 12 月 9 日我们的最后一次更新,我们确定了 30 种研究性(即在任何国家均未获批准上市)抗体治疗药物,其营销申请(包括在美国提交的生物制品许可申请(BLAs)、在欧盟提交的营销授权申请以及在中国提交的新药申请(NDAs))正在至少一个监管机构进行审查(表 2)。其中,13 项申请正在美国或欧盟进行审查,可能还包括其他国家,而 17 项申请仅在中国进行审查。16 项申请针对非癌症适应症,而 14 项针对癌症。这些分子的相关细节如下总结,按其在表 2 中出现的顺序。
5.1.具有营销应用综述的抗体:非癌症适应症
Bentracimab (SFJ Pharmaceuticals, SERB Pharmaceuticals)
Bentracimab (PB2452; formerly MEDI2452) 是一种人源抗体 Fab 片段,能够与并中和 Brilinta®/Brilique® (ticagrelor),从而逆转 ticagrelor 及其活性代谢产物的抗血小板效应。Ticagrelor 是一种口服 P2Y12 血小板抑制剂,其产品标签中包含有关出血风险的黑框警告。美国食品药品监督管理局(FDA)和欧洲药品管理局(EMA)分别授予了 bentracimab 突破性疗法和 PRIME 指定。SERB Pharmaceuticals 从 SFJ Pharmaceuticals 获得了 bentracimab 在美国的独家权利。FDA 接受了 bentracimab 的生物制品许可申请(BLA),并进行了优先审查,目标行动日期定在 2025 年第一季度。
BLA 提交基于单臂、开放标签的 Phase 3 REVERSE-IT 试验(NCT04286438)的结果,该试验评估了 bentracimab 在需要紧急手术或其他侵入性程序或出现大出血的 ticagrelor 治疗患者中的效果。中期分析表明,bentracimab 在 5 到 10 分钟内逆转了 ticagrelor 的抗血小板效应,并且这种效应持续超过 24 小时。BLA 还包括了 REVERSE-IT 试验数据的计划第二次中期分析的结果。
Garadacimab (CSL Ltd.)
Garadacimab (CSL312) 是一种铰链稳定的、人源抗因子 XIIa IgG4λ 抗体,开发用于治疗遗传性血管性水肿(HAE)。Garadacimab 异常长的 CDR-H3 结合 FXIIa 的 beta 链,从而抑制其蛋白水解活性以及随后的促凝血和促炎途径的激活。Garadacimab 获得了美国和欧盟分别针对遗传性血管性水肿的孤儿药和孤儿药产品指定。
Garadacimab 作为每月一次、自动注射器给药的预防性治疗 HAE 的营销申请正在欧盟、美国、日本和加拿大进行审查。这些申请包括来自 Phase 2、关键 Phase 3 和开放标签扩展研究的数据,这些数据表明 garadacimab 能够提供对 HAE 发作的持久保护,并且具有适合长期使用的安全性特征。CSL 预计在 2025 年上半年在欧盟、美国和日本获得 garadacimab 用于 HAE 的批准。
Nipocalimab (Johnson & Johnson)
Nipocalimab (JNJ-80202135, M281) 是一种人源无糖基化 IgG1λ 单克隆抗体,靶向新生儿 Fc 受体(FcRn),这是一种负责调节血液中 IgG 抗体水平的蛋白。如临床前模型所示,阻断 FcRn 的 nipocalimab 增加循环中的 IgG 抗体水平,从而减少自身免疫疾病中的免疫系统过度活跃。Johnson & Johnson 正在开发 nipocalimab 用于治疗由病理性 IgG 抗体驱动的疾病,如全身性重症肌无力(gMG)和胎儿及新生儿溶血病(HDFN)。
Nipocalimab 获得了美国针对 gMG 和 HDFN 的快速通道和孤儿药指定,美国针对 HDFN 的突破性疗法指定,以及欧盟针对 HDFN 的孤儿药产品指定。该药物还有针对温抗体自身免疫性溶血性贫血、胎儿新生儿同种免疫性血小板减少症和慢性炎症性脱髓鞘多发性神经病的额外监管机构指定。Johnson & Johnson 已向 FDA 和 EMA 提交了 nipocalimab 用于治疗 gMG 患者的营销申请。
营销申请提交基于双盲安慰剂对照的 Phase 3 Vivacity-MG3 试验(NCT04951622)的积极数据。在这项研究中,153 名对持续的标准治疗(SOC)反应不足(重症肌无力日常生活活动(MG-ADL)评分 ≥6)的血清阳性成人 gMG 患者以 1:1 的比例随机分配到接受 nipocalimab(30 mg/kg 静脉注射负荷剂量,随后每两周 15 mg/kg)加当前 SOC 或安慰剂加当前 SOC。研究结果显示,在接受 nipocalimab 的抗体阳性成人患者中,24 周内持续疾病控制。在双盲阶段,31.2%(24/77)接受 nipocalimab 的患者和 13.2%(10/76)安慰剂组患者达到了预先指定的最小症状表达终点,定义为 MG-ADL 总分为 0 或 1。
正在进行的后期临床研究还在评估 nipocalimab 在以下方面的疗效和安全性:1)患有 gMG 的儿童(Phase 2/3 NCT05265273 研究);2)有 HDFN 风险的孕妇(Phase 3 AZALEA 试验(NCT05912517));3)患有温抗体自身免疫性溶血性贫血的患者(Phase 2/3 ENERGY 研究(NCT04119050));4)患有慢性炎症性脱髓鞘多发性神经病的成人(Phase 2/3 NCT05327114 研究);5)有胎儿和新生儿同种免疫性血小板减少症风险的孕妇(Phase 3 FREESIA1 研究(NCT06449651))。截至 2024 年 11 月,这些研究正在招募参与者。
Vilobelimab (InflaRx N.V.)
Vilobelimab (Gohibic),一种嵌合 IgG4κ 抗体,通过结合补体系统的一个组分补体 C5a 来阻断补体系统介导的炎症反应。InflaRx N.V. 正在开发 vilobelimab 用于治疗由 SARS-CoV-2 引起的脓毒症急性呼吸窘迫综合征(ARDS)和溃疡性坏疽性脓皮病,这些疾病中 C5a 信号传导起着关键作用。Vilobelimab 获得了 FDA 的快速通道和孤儿药指定,以及 EMA 的孤儿药产品指定,用于治疗溃疡性坏疽性脓皮病。
2023 年 8 月,EMA 开始评估 vilobelimab 的营销申请。2024 年 11 月 14 日,EMA 的人用药品委员会采纳了积极意见,推荐批准 Gohibic 用于治疗接受系统性皮质类固醇治疗的 SARSCoV2 引起的急性呼吸窘迫综合征(ARDS)的成人。欧洲委员会的决定通常在采纳意见后 67 天内发布。
申请包括了 Phase 2/3 PANAMO 试验(n = 368;NCT04333420)的结果,该试验评估了 vilobelimab 加标准治疗(SOC)与安慰剂加 SOC 用于治疗 COVID-19 相关的严重肺炎。SOC 包括同时使用的皮质类固醇(97%)和抗凝血剂(98%),以及免疫调节剂(约 20%),主要是托珠单抗而非巴瑞克替尼。对在 vilobelimab 加 SOC 和安慰剂加 SOC 组中接受托珠单抗治疗的 61 名患者的事后亚组分析表明,vilobelimab 和托珠单抗的联合使用可能在这些危重 ARDS 患者中产生协同生存益处。
Sipavibart (AstraZeneca)
Sipavibart (AZD3152) 是一种人源 IgG1λ 抗体,靶向 SARS-CoV-2 的刺突蛋白。Sipavibart 源自 SARS-CoV-2 感染后患者的 B 细胞,经过优化以减少 Fc 效应功能(L234F, L235E, P331S),从而最小化抗体依赖性感染增强的风险,并延长半衰期(M252Y, S254T, T256E)。AstraZeneca 于 2022 年 5 月从 RQ Biotechnology 获得了 sipavibart 的许可。AstraZeneca 向 EMA 提交了 sipavibart 用于免疫受损患者 COVID-19 的暴露前预防的营销申请。EMA 的评估于 2024 年 6 月开始,该申请被接受进行加速评估程序。AstraZeneca 还在日本提交了 sipavibart 用于免疫受损患者 COVID-19 的暴露前预防的营销申请。
营销申请包括了 Phase 1/3 SUPERNOVA 试验(NCT05648110)的数据,该试验比较了 sipavibart 与 tixagevimab/cilgavimab (EVUSHELD) 或安慰剂在预防免疫受损患者群体中 COVID-19 的效果。该研究包括一个开放标签的 Phase 2 子研究,以评估 AZD3152 用于 COVID-19 暴露前预防的安全性、药代动力学(PK)和中和活性。AZD3152 在 SUPERNOVA 试验的第 1 天和第 181 天作为 300 mg 剂量进行肌肉注射。总共 1,669/3,335 名参与者接受了 sipavibart,1,666/3,335 名参与者接受了比较剂。试验的高级别积极结果显示,与对照组(tixagevimab/cilgavimab 或安慰剂)相比,sipavibart 在免疫受损患者群体中显著降低了有症状 COVID-19 的发生率。该试验达到了两个双重主要终点:1)由任何 SARS-CoV-2 变体引起的有症状 COVID-19 的相对风险降低;2)由不含有 F456L 突变的 SARS-CoV-2 变体引起的感染的相对风险降低。
Clesrovimab(Merck Sharp & Dohme LLC (MSD))
Clesrovimab(MK-1654)是由默克公司(MSD)开发的一种人源单克隆IgG1κ抗体,用于预防呼吸道合胞病毒(RSV)感染,特别是在婴儿和老年人等脆弱人群中。其作用机制是通过靶向病毒的F蛋白来中和RSV,F蛋白对于病毒进入宿主细胞至关重要。引入YTE突变(M252Y,S254T,T256E)延长了其半衰期,从而允许在每个RSV季节仅需给药一次。欧洲药品管理局(EMA)于2024年11月28日开始评估Clesrovimab的市场申请。2024年10月,默克宣布了其双盲、随机的2b/3期临床试验(MK-1654-004,NCT04767373)的积极顶线结果,该试验比较了单剂量105毫克Clesrovimab肌肉注射与安慰剂在3632名健康的早产儿和足月儿中的安全性和有效性。所有预设终点均达到。与安慰剂相比,通过第150天(5个月)后剂量的RSV相关医疗就诊的下呼吸道感染发生率降低,这是主要疗效终点,降低了60.4%(95% CI:44.1,71.9,p < 0.001)。此外,RSV相关住院(次要终点)和RSV相关下呼吸道感染住院(三级终点)在给予Clesrovimab的参与者中与安慰剂相比,分别降低了84.2%(95% CI:66.6,92.6,p < 0.001)和90.9%(95% CI:76.2,96.5)。默克正在评估肌肉注射Clesrovimab与肌肉注射Palivizumab在增加RSV疾病风险的婴儿和儿童中的效果,这是3期MK-1654-007试验(NCT04938830)。估计有1000名参与者参加了这项研究,该研究处于活跃状态,但截至2024年10月不再招募。该研究的主要完成日期为2025年4月。
Narsoplimab(Omeros Corporation)
Narsoplimab(OMS721)是一种人源抗甘露聚糖结合凝集素相关丝氨酸蛋白酶-2(MASP-2)抗体。靶标是补体系统凝集素途径的效应酶。美国食品药品监督管理局(FDA)授予Narsoplimab突破性疗法认定,用于治疗高风险造血干细胞移植相关血栓性微血管病(TA-TMA)患者,并授予孤儿药认定,用于预防补体介导的TMAs和治疗TA-TMA。Narsoplimab也被欧盟认定为治疗造血干细胞移植的孤儿药。Omeros Corporation的滚动提交Narsoplimab治疗TA-TMA的生物制剂许可申请(BLA)于2020年底完成。在收到FDA关于BLA问题的完整回应函(CRL)后,Omeros与机构进行了持续讨论,涉及:1)评估已有的临床试验数据、来自外部来源的历史对照人群现有数据、Narsoplimab扩展访问(即同情使用)计划的数据以及针对Narsoplimab作用机制的数据的分析计划;以及2)FDA对BLA重新提交的要求。公司已修订并重新提交了统计分析计划,FDA现已对分析计划提出了额外建议。在数据准备完成后,如果主要和次要疗效分析的结果支持重新提交,公司计划尽快完成并重新提交BLA。76 此外,公司计划在2025年上半年向EMA提交市场申请。Omeros的临床管线还包括OMS1029,这是一种长效、下一代MASP-2抑制剂,正在1期研究中评估,以及Zaltenibart(OMS906),这是一种抗MASP-3抗体,在PNH患者中进行2期研究。Omeros计划在2024年底前启动Zaltenibart在PNH的3期项目。
Recaticimab(江苏恒瑞医药股份有限公司)
Recaticimab(SHR-1209,瑞卡西单抗)是一种长效、人源化IgG1κ单克隆抗体,选择性靶向PCSK9。Fc区域发生了突变(M252Y,S254T,T256E),以延长抗体的血清半衰期。2023年6月,恒瑞宣布Recaticimab的NDA被国家药品监督管理局(NMPA)接受。该提交基于三项多中心、随机、双盲、安慰剂对照的3期临床试验(SHR-1209-301,SHR-1209-302和SHR-1209-303),每项试验研究不同的适应症。SHR-1209-301研究(REMAIN-1,NCT04849000)评估了SHR-1209作为单药治疗非家族性高胆固醇血症和混合型高脂血症患者的疗效和安全性。主要终点测量了从基线到第12周的150毫克Q4W和450毫克Q12W剂量方案,以及到第16周的300毫克Q8W的LDL-C百分比变化。共有703名患者随机接受Recaticimab剂量为150毫克Q4W(n = 157),300毫克Q8W(n = 156),或每12周450毫克(n = 155),或安慰剂(n = 78,79和78,分别)。Recaticimab进一步降低了患者的LDL-C水平,与安慰剂相比,实现了150毫克Q4W降低49.6%(95% CI:44.2%–54.9%),300毫克Q8W降低52.8%(95% CI:48.3%–57.2%)和450毫克Q12W降低45.0%(95% CI:41.0%–49.0%)的降低(所有比较p < 0.0001)。Recaticimab的安全性与安慰剂相当。经过12或16周的治疗后,接受Recaticimab治疗的患者继续至第24周,而最初接受安慰剂的患者则转换为Recaticimab,遵循相同的剂量方案。24周的Recaticimab方案和安慰剂后的12或8周Recaticimab治疗均显示出持续的疗效。SHR-1209-302研究(REMAIN-2,NCT04885218)考察了SHR-1209作为非家族性高胆固醇血症(非FH)和混合型高脂血症患者的附加疗法的疗效和安全性,共招募了689名参与者。患者随机接受Recaticimab(150毫克Q4W,300毫克Q8W和450毫克Q12W)或安慰剂48周。主要疗效终点被定义为从基线到第24周计算的LDL-C水平的百分比变化。结果显示,与安慰剂相比,Recaticimab显著且呈剂量依赖性地降低了LDL-C水平,相应剂量的治疗差异分别为−62.2%,−59.7%和−53.4%。在第24周,85.8%到94.5%接受Recaticimab治疗的患者达到了LDL-C目标水平,并且这些降低在整个48周试验期间得以维持。SHR-1209-303研究评估了SHR-1209与其他降脂疗法联合用于杂合子家族性高胆固醇血症患者的疗效和安全性。共有143名患者随机接受Recaticimab(n = 95)或安慰剂(n = 48)。到第12周,Recaticimab组显示出平均LDL-C降低54.4%(95% CI:−57.9%到−50.8%),而安慰剂组降低4.5%(95% CI:−9.4%到0.3%)。治疗差异为−49.8%(95% CI:−55.8%到−43.9%;p < 0.0001),显示出Recaticimab的显著影响。
Suciraslimab(SinoMab BioScience Limited)
Suciraslimab(SM03,舒西利单抗)是由SinoMab BioScience开发的抗CD22 IgG1κ嵌合抗体,用于治疗类风湿关节炎。Suciraslimab特异性结合CD22的构象表位,促进CD22从顺式配体向反式配体结合的转变,反式配体结合的CD22可以抑制BCR引发的针对自身细胞的免疫反应。80 2023年9月,NMPA接受了Suciraslimab治疗类风湿关节炎的BLA,并且截至2024年6月,正处于最终审查阶段。SinoMab计划进一步开发Suciraslimab,用于治疗系统性红斑狼疮(SLE)、由阿尔茨海默病引起的轻度认知障碍(MCI)以及阿尔茨海默病。81
TNM002(珠海泰诺麦博生物技术有限公司)
TNM002是一种人源单克隆抗体,靶向破伤风神经毒素(TeNT),为预防或治疗破伤风提供了一种新的治疗方法。通过Trinomab的专有HitmAb®技术平台开发,TNM002通过结合TeNT毒素,中和其对神经系统的影响,并设计为肌肉注射给药。2023年12月6日,Trinomab宣布TNM002的NDA被NMPA接受,并被授予优先审查,用于紧急破伤风预防。82
一项多中心、随机、双盲、平行、阳性对照的3期临床试验(CTR20223067/NCT05664750)评估了TNM002肌肉注射与人破伤风免疫球蛋白(HTIG)作为破伤风预防的疗效。主要终点是给药后与基线相比破伤风中和抗体滴度的增加。TNM002实现了保护性水平的抗破伤风抗体,无论是在疗效还是抗体持续时间上都优于标准250 IU HTIG。TNM002显示出良好的安全性、耐受性和低免疫原性,在1至3期试验中不良事件率与安慰剂或HTIG相当。
Gensci-048(长春金赛药业股份有限公司)
Gensci-048(genakumab,金纳单抗)是一种人源化单克隆抗体,靶向白细胞介素-1β(IL-1β)途径。IL-1β是一种关键的促炎细胞因子,在各种炎症性疾病中发挥作用。通过特异性阻断IL-1β与其受体的结合,genakumab可以抑制炎症。2024年4月,GenSci宣布genakumab的市场申请已被NMPA接受,用于治疗急性痛风性关节炎。Genakumab也在进行其他适应症的临床研究,如系统性幼年特发性关节炎和间质性肺病。GenSci进行了一项前瞻性、随机、多中心、活性对照的3期研究(GUARD-1,CTR20223136),涉及中国成年痛风发作患者,包括48周治疗期后跟12周安全性随访。患者随机(1:1)接受单剂量genakumab 200毫克皮下注射(n = 157)或betamethasone 7毫克肌肉注射(n = 156),在间隔>2周的新发作情况下按需重新给药。研究表明genakumab有效降低了疼痛并延迟了新发作与betamethasone相比。共同主要终点包括基线时最受影响关节的疼痛强度变化,使用0–100毫米视觉模拟量表(VAS)在治疗后72小时评估,以及12周内首次新痛风发作的时间。Genakumab在降低72小时疼痛强度方面与betamethasone相比显示出非劣效性,全分析集的疼痛评分平均差异为−3.32毫米(95% CI:−7.56到0.91),方案遵循集为−2.21毫米(95% CI:−6.49到2.07)。此外,genakumab显著延长了首次新痛风发作的中位时间与betamethasone相比,betamethasone的中位时间为45天(genakumab的数据无法估计)。
IBI311(信达生物制药有限公司)
IBI311是由信达生物开发的一种重组抗胰岛素样生长因子1受体(IGF-1R)抗体,用于治疗甲状腺眼病(TED)。通过结合IGF-1R,这是一种在TED患者的眶周成纤维细胞(OFs)、B细胞和T细胞中过表达的受体,IBI311阻断IGF-1R信号传导,减少炎症途径的激活。这一作用有助于减少与OF激活相关的透明质酸和其他糖胺聚糖的产生,缓解如眼球突出、复视和眼睑肿胀等症状。2024年5月,NMPA接受了IBI311用于TED治疗的NDA。该NDA的接受基于一项多中心、随机、双盲、安慰剂对照的2/3期临床研究RESTORE-1(CTR20223393)的积极结果。3期结果显示,主要终点成功达到,表明与安慰剂相比,接受IBI311治疗的患者在眼球突出、疾病活动度和生活质量方面有显著改善。在第24周,研究眼中从基线减少≥2毫米眼球突出且对侧眼未出现≥2毫米恶化的眼球突出的参与者比例在IBI311组显著高于安慰剂组。接受IBI311和安慰剂的应答率分别为85.8%和3.8%,显示出显著差异81.9%(95% CI:69.8%至93.9%,p < 0.0001)。IBI311在关键次要终点方面也显示出与安慰剂相比的显著改善,如总体应答率(研究眼中从基线减少≥2毫米眼球突出且临床活动评分改善≥2的受试者百分比)、临床活动评分(CAS)为0或1的受试者百分比,以及研究眼中从基线的眼球突出平均变化。IBI311的整体安全性良好,未报告严重不良事件。
巴托利单抗(Harbour BioMed (Guangzhou) Co. Ltd., Roivant sciences Ltd., HanAll Biopharma)
巴托利单抗(HBM9161, IMVT-1401)是一种人源IgG1λ抗FcRn单克隆抗体,Fc区域经过工程改造以降低效应功能(L234A, L235A),最初由HanAll Biopharma开发,用于治疗IgG介导的自身免疫疾病,包括全身性重症肌无力(gMG)和格雷夫斯病。HanAll Biopharma将巴托利单抗授权给Harbour Biomed,后者随后与CSPC集团的全资子公司NBP Pharma达成协议,共同开发巴托利单抗在中国大陆、香港、澳门和台湾地区的应用。HanAll还将巴托利单抗的开发权授权给Roivant Sciences,用于北美、拉丁美洲、瑞士、北非以及欧盟、英国和中东地区的开发。巴托利单抗获得了NMPA授予的突破性疗法认定,用于治疗成人重症肌无力患者。2023年6月,Harbour BioMed向NMPA提交了用于治疗gMG的市场申请,然后在2024年6月补充了额外的安全性数据重新提交申请。87 该提交基于在中国进行的一项安慰剂对照的3期研究(NCT05039190)的积极结果,显示每周皮下注射巴托利单抗(680毫克剂量)在gMG的主要和次要终点方面均显示出疗效。接受抗体检测的患者(n = 131)接受了安慰剂或每周皮下注射巴托利单抗(680毫克剂量)。每个治疗周期包括一个5周的治疗期,患者接受六剂安慰剂或药物,随后是一个4周的观察期(总共9周)。在接受安慰剂的患者中,抗体阳性患者第一个周期中持续重症肌无力日常生活活动量表(MG-ADL)改善的比率为31.3%(64中的20),而巴托利单抗组的MG-ADL改善为58.2%(67中的39)(比值比,3.45;95% CI,1.62–7.35;p = .001)。Roivant Sciences的子公司Immunovant优先开发了IMVT-1402,这是一种下一代抗FcRn抗体,由于其独特的FcRn结合方式,可能具有更有利的整体治疗特性,避免了由巴托利单抗引起的白蛋白减少和随后胆固醇水平的增加。尽管如此,Immunovant目前正在进行巴托利单抗在gMG患者(NCT05403541)、甲状腺眼病(NCT05524571, NCT05517421, NCT05517447)的3期研究,以及在慢性炎症性脱髓鞘性多发性神经病(NCT05581199)和格雷夫斯病(NCT05907668)的2期研究。
依若奇单抗(Akeso Biopharma, Inc.)
依若奇单抗(AK101)是由Akeso Biopharma开发的一种人源抗IL-12/23p40 IgG1κ单克隆抗体。通过靶向IL-12和IL-23共有的p40亚基,依若奇单抗抑制这些细胞因子的信号传导,这些细胞因子参与炎症反应。依若奇单抗正在开发用于治疗中度至重度斑块型银屑病。NMPA正在审查2023年中期提交的依若奇单抗用于治疗中度至重度斑块型银屑病的市场申请。依若奇单抗的长期安全性和疗效在中国中度至重度斑块型银屑病患者中进行了单臂3期研究(CTR20220206)评估。该研究包括三组:1)在先前的16周双盲、安慰剂对照研究(CTR20212660)中接受依若奇单抗治疗的患者在第16周继续接受依若奇单抗135毫克治疗,随后每12周进行维持治疗并随访至第52周;2)先前研究中安慰剂组的患者在本研究的第16周/第20周接受依若奇单抗135毫克治疗,随后每12周进行维持治疗并随访至第52周;3)直接参与本研究的患者在第0周/第4周接受依若奇单抗135毫克治疗,随后每12周进行维持治疗并随访至第52周。如2024年在阿姆斯特丹举行的欧洲皮肤科和性病学会大会上报道,89 第1组在第16周的银屑病面积和严重程度指数(PASI75)和静态医生全球评估(sPGA)0/1反应率分别为80.5%和66.0%。第1组患者的PASI75和sPGA0/1反应率一直维持至第52周。在第16周转换为依若奇单抗后,第2组患者的PASI评分下降。第32周的PASI75和sPGA0/1反应率分别为81.4%和71.1%,反应率维持至第52周。第3组在第16周的PASI75和sPGA0/1反应率分别为69.5%和59.1%,与第1组的结果一致。
Picankibart(信达生物制药有限公司)
Picankibart(IBI112)是由信达生物制药有限公司开发的一种抗IL-23p19 IgG1κ单克隆抗体,用于治疗银屑病或其他自身免疫疾病患者。该分子中和IL-23的p19亚基,从而阻止IL-23与细胞表面受体结合及其随后的下游信号传导,阻断IL-23诱导的IL-17产生。Picankibart的Fc区域经过YTE突变(M252Y, S254T, T256E)工程改造以延长半衰期。2024年9月,信达生物制药有限公司宣布,用于治疗中度至重度斑块型银屑病的Picankibart的NDA被NMPA接受。90
NDA的接受基于随机、双盲、安慰剂对照的3期CLEAR-1研究(NCT05645627)的积极结果,该研究评估了IBI112在不同剂量方案中治疗中度至重度斑块型银屑病受试者的疗效和安全性。该试验共招募了500名患者,他们被随机(1:2:2比例)分配接受安慰剂或Picankibart 200毫克Q4W在第0周、第4周和第8周,随后每12周200毫克或100毫克。研究的主要终点是第16周时从基线银屑病面积和严重程度指数得分改善超过90%(PASI 90)的患者百分比和第16周时静态医生全球评估(sPGA)得分为清晰(0)或几乎清晰(1)的患者百分比。两个主要终点均成功达到,与接受安慰剂的患者相比,接受Picankibart的患者实现PASI 90和sPGA 0或1的比例显著更高(PASI 90为80.3%对比2.0%和sPGA 0/1为93.5%对比13.1%,两者p < 0.0001)。Picankibart还显示出良好的安全性,并达到了所有关键次要终点,通过一年维持了高水平的皮肤清除。
SSGJ-608(三生国健药业(上海)股份有限公司,3SBio Inc.)
SSGJ-608(608)是一种人源化单克隆抗体,靶向IL-17A,由3SBio和三生国健药业(上海)有限公司开发,用于治疗自身免疫和炎症疾病患者。3SBio于2024年11月向NMPA提交了SSGJ-608用于中度至重度斑块型银屑病的NDA。在中国中度至重度斑块型银屑病患者中进行的3期SSGJ-608-PsO-III-01研究(NCT05536726)已成功达到所有主要和次要终点。该随机、双盲、安慰剂对照、平行组SSGJ-608-PsO-III-01研究评估了两种剂量方案的SSGJ-608与安慰剂在中国中度至重度斑块型银屑病参与者中的效果。参与者接受:1)SSGJ-608 160毫克在第0周 + 80毫克Q2W(6个周期)+ 在维持期间80毫克Q4W,2)SSGJ-608 160毫克Q4W(3个周期)+ 在维持期间160毫克Q8W,或在预定时间点接受安慰剂以维持盲法。该研究包括一个诱导剂量期,剂量为12周,主要终点在12周时测量,随后是一个随机、双盲、40周的维持剂量期。在维持剂量期,评估了反应/缓解的维持以及治疗后的复发。银屑病面积和严重程度指数(PASI)75在第12周时表明,接受160毫克Q4W + 160毫克方案的患者中有95.1%,接受160毫克Q4W方案的患者中有93.4%实现了≥75%的改善。12周的主要疗效数据显示了快速反应率和疗效优势。在维持治疗期间,608的剂量间隔延长至Q4W或Q8W,疗效保持在高水平。SSGJ-608还在强直性脊柱炎和非放射学轴性脊柱炎患者中进行临床研究。
5.2.正在审查的具有市场应用的抗体:癌症适应症
Cosibelimab(Checkpoint Therapeutics, Inc.)
Cosibelimab(CK-301)是一种人IgG1λ抗体,它结合免疫检查点PD-L1,从而抑制其与受体PD-1的相互作用。这种阻断消除了PD-L1对抗肿瘤T细胞的抑制效应,恢复细胞毒性T细胞反应。此外,cosibelimab的功能性Fc域可能诱导对肿瘤细胞的抗体依赖性细胞毒性(ADCC)和补体依赖性细胞毒性(CDC)。Checkpoint Therapeutics正在开发cosibelimab作为皮肤鳞状细胞癌(cSCC)的治疗方法。该公司于2023年1月宣布,他们已向FDA提交了一份生物制品许可申请(BLA),以批准cosibelimab用于治疗转移性或局部晚期cSCC患者。2023年12月,公司宣布FDA对cosibelimab BLA发出了一封完全回应函(CRL),指出在对Checkpoint的第三方合同制造组织进行多赞助方检查期间出现的检查发现,作为重新提交中需解决的批准问题。Checkpoint于2024年7月重新提交了其cosibelimab BLA,该BLA已被FDA接受。FDA对BLA采取行动的目标日期为2024年12月28日。Checkpoint预计将在全球包括欧洲在内的其他市场进行额外的潜在提交。
Datopotamab deruxtecan(AstraZeneca,第一三共株式会社)
Datopotamab deruxtecan(Dato-DXD)是一种抗滋养层细胞表面抗原2(TROP2)抗体药物偶联物(ADC),正在开发用于治疗乳腺癌和肺癌。有效载荷是一种拓扑异构酶I抑制剂,通过可切割的连接子与人源化IgG1κ抗体结合。第一三共在日本拥有此ADC的独家权利,但与AstraZeneca达成协议,共同开发和商业化datopotamab deruxtecan在世界其他地区。2024年3月,欧洲药品管理局(EMA)开始评估datopotamab deruxtecan的两项市场申请,用于两种类型的癌症。一项申请是用于治疗成年患者,这些患者患有不可切除或转移性激素受体(HR)阳性、HER2阴性(IHC 0,IHC 1+或IHC 2+/ISH-)乳腺癌,他们已对内分泌治疗产生进展且不适合内分泌治疗,并接受了至少一种额外的系统治疗。另一项申请是用于治疗成年患者,这些患者患有局部晚期或转移性非鳞状非小细胞肺癌(NSCLC),需要在先前治疗后进行系统治疗。截至2024年12月初,这两项申请仍在EMA的评估中。同样在2024年3月,第一三共向日本的厚生劳动省(MHLW)提交了datopotamab deruxtecan的市场申请,用于治疗成年患者,这些患者患有HR阳性、HER2阴性(IHC 0,IHC 1+或IHC 2+/ISH-)不可切除或复发性乳腺癌,且之前接受过化疗。该提交基于第三阶段TROPION-Breast01(NCT05104866)临床试验的结果。2024年4月,AstraZeneca宣布FDA接受了datopotamab deruxtecan的BLA,用于治疗成年患者,这些患者患有不可切除或转移性HR阳性、HER2阴性(IHC 0,IHC 1+或IHC 2+/ISH-)乳腺癌,且之前接受过不可切除或转移性疾病系统的治疗。该BLA基于第三阶段TROPION-Breast01试验的结果。FDA对BLA采取行动的目标日期为2025年1月29日。2024年11月,第一三共和AstraZeneca宣布他们向FDA提交了datopotamab deruxtecan的BLA,申请加速批准用于治疗成年患者,这些患者患有局部晚期或转移性EGFR突变NSCLC,且之前接受过包括EGFR靶向治疗在内的系统治疗。该BLA包括来自三项临床研究的汇总分析:1)第二阶段TROPION-Lung05,第三阶段TROPION-Lung01,以及3)第一阶段TROPION-PanTumor01。同时,公司宣布之前提交的基于第三阶段TROPION-Lung01试验结果的非鳞状NSCLC的BLA已自愿撤回。第三阶段TROPION-Lung01(NCT04656652)试验的随机、开放标签结果最近已报告。患者在本研究中接受datopotamab deruxtecan 6 mg/kg(n = 299)或docetaxel 75 mg/m2(n = 305)Q3W治疗。双重主要终点为PFS和OS。接受datopotamab deruxtecan治疗的患者与接受docetaxel治疗的患者相比,中位PFS分别为4.4个月(95% CI,4.2至5.6)和3.7个月(95% CI,2.9至4.2)(HR,0.75(95% CI,0.62至0.91);p = 0.004)。中位OS结果在数值上倾向于datopotamab deruxtecan,与docetaxel相比(12.9对比11.8个月),但未达到统计学显著性(HR 0.94;95%置信区间[CI] 0.78–1.14;p = 0.530)。在非鳞状NSCLC的预设亚组患者中,中位PFS分别为5.5对比3.6个月(HR,0.63(95% CI,0.51至0.79)),datopotamab deruxtecan与docetaxel相比OS改善了2.3个月(14.6对比12.3个月;HR 0.84;95% CI 0.68–1.05)。在鳞状NSCLC患者中,中位PFS分别为2.8对比3.9个月(HR,1.41(95% CI,0.95至2.08)),中位OS分别为7.6对比9.4个月(HR,1.32(95% CI,0.91至1.92))。AstraZeneca和第一三共正在评估datopotamab deruxtecan在多个额外的第三阶段研究中用于NSCLC患者。Datopotamab deruxtecan在第三阶段TROPION-Breast01试验(NCT05104866)中的结果与研究者选择的化疗相比,在HR阳性/HER2阴性(HR+/HER2–)乳腺癌患者中显示了PFS的统计学显著和临床意义的改善,但未在不可切除或转移性HR阳性、HER2低或阴性(IHC 0,IHC 1+或IHC 2+/ISH-)乳腺癌患者的最终OS分析中达到统计学显著性,这些患者之前接受过内分泌治疗和至少一种系统治疗。AstraZeneca和第一三共还在第三阶段TROPION-Breast02、TROPION-Breast03、TROPION-Breast04和TROPION-Breast05试验中评估datopotamab deruxtecan单独使用和与免疫治疗联合使用在三阴性或HR低、HER2阴性乳腺癌患者中的应用。
Telisotuzumab vedotin(AbbVie)
Telisotuzumab vedotin(Teliso-V,ABBV-399)是一种ADC,由人源化IgG1κ抗体组成,该抗体针对cMET,通过可切割的缬氨酸-瓜氨酸连接子与单甲基奥瑞他汀E(MMAE)结合。cMet过表达在各种肿瘤类型中均有发现,与不良预后相关。抗体部分hz224G11最初由Pierre Fabre发现,并由AbbVie作为裸分子(ABT-700)开发。FDA授予Teliso-V突破性疗法认定,用于治疗晚期/转移性EGFR野生型、NSCLC患者,这些患者c-Met过表达水平高,疾病在铂类治疗期间或之后进展。2024年9月,AbbVie宣布向FDA提交了Teliso-V的BLA,申请批准其作为单药治疗之前接受过治疗的cMet过表达、EGFR野生型局部晚期或转移性NSCLC患者。该BLA由第二阶段LUMINOSITY试验的数据支持,将在肿瘤学卓越中心实时肿瘤学审查计划下进行评估。第二阶段LUMINOSITY试验(M14–239,NCT03539536)的开放标签、单臂结果最近已报告,该试验旨在识别NSCLC人群中过表达c-Met最适合在二线或三线设置中接受Teliso-V单药治疗,然后扩大组别以评估所选人群中的疗效。Teliso-V(1.9 mg/kg)通过IV输注Q2W给予172名患者,直至疾病进展、不可耐受的毒性或其他研究终止标准满足。该研究的主要终点,由ICR确定的ORR为28.6%(95% CI,21.7至36.2;c-Met高,34.6%[95% CI,24.2至46.2];c-Met中等,22.9%[95% CI,14.4至33.4])。中位DoR为8.3个月(95% CI,5.6至11.3;c-Met高,9.0[95% CI,4.2至13.0];c-Met中等:7.2[95% CI,5.3至11.5]),中位OS为14.5个月(95% CI,9.9至16.6;c-Met高,14.6[95% CI,9.2至25.6];c-Met中等,14.2[95% CI,9.6至16.6]),中位PFS为5.7个月(95% CI,4.6至6.9;c-Met高,5.5[95% CI,4.1至8.3];c-Met中等:6.0[95% CI,4.5至8.1])。AbbVie正在赞助正在进行的随机第三阶段TeliMET NSCLC-01试验(NCT04928846),该试验正在评估Teliso-V与docetaxel在之前接受过治疗的cMET过表达、EGFR野生型、局部晚期/转移性非鳞状NSCLC受试者中的效果。预计698名参与者将接受IV Teliso-V Q2W或docetaxel Q3W治疗,直至满足研究药物终止标准。该研究的主要完成日期为2028年3月。
Patritumab deruxtecan(第一三共,默克公司)
Patritumab deruxtecan(HER3-DXd,U3–1402)是一种ADC,由人IgG1κ单克隆抗体组成,该抗体针对HER3,通过稳定的四肽(GGFG)基础可切割连接子与拓扑异构酶I抑制剂有效载荷DXd/DX-8951结合。第一三共和默克正在合作开发patritumab deruxtecan。2023年12月,公司宣布FDA接受了并授予了patritumab deruxtecan的BLA优先审查,用于加速批准治疗成年患者,这些患者患有局部晚期或转移性EGFR突变NSCLC,之前接受过两种或更多系统治疗。该BLA基于关键的第二阶段hERTHENA-Lung01研究(NCT04619004)的结果,该研究评估了patritumab deruxtecan,通过IV作为固定剂量(5.6 mg/kg Q3W)和增量,给予之前接受过EGFR TKI治疗和铂类化疗的晚期EGFR突变NSCLC患者。2024年6月,FDA对该BLA发出了一封CRL,涉及对第三方制造设施的检查发现。CRL中未识别出提交的疗效或安全性数据的问题。公司计划尽快解决FDA的反馈。2024年9月,第一三共和默克宣布第三阶段hERTHENA-Lung02试验(NCT05338970)达到了其主要终点PFS,该试验评估了patritumab deruxtecan通过IV以5.6 mg/kg Q3W给予之前接受过EGFR TKI治疗的局部晚期或转移性EGFR突变NSCLC患者,与铂类加培美曲塞诱导化疗后培美曲塞维持化疗相比显示出统计学显著改善。公司表示hERTHENA-Lung02试验数据将与监管机构共享。
Linvoseltamab(Regeneron Pharmaceuticals, Inc.)
Linvoseltamab(REGN5458)是一种铰链稳定的双特异性IgG4κ抗体,由Regeneron开发,针对B细胞成熟抗原(BCMA)和CD3,用于治疗多发性骨髓瘤(MM)。该抗体经过Fc工程改造以减少效应功能,通过将BCMA表达的癌细胞与CD3表达的T细胞拉近,实现T细胞介导的癌细胞杀伤。FDA授予linvoseltamab快速通道认定用于MM。2024年2月,Regeneron宣布FDA接受了linvoseltamab的BLA优先审查,用于治疗成年患者,这些患者患有R/R MM,且在至少三种先前治疗后进展。EMA也接受了linvoseltamab在同一适应症中的市场申请,该申请截至2024年11月仍在评估中。2024年8月,Regeneron宣布FDA对linvoseltamab的BLA发出了一封CRL,识别出与另一家公司产品候选者在第三方灌装/包装制造商处的批准前检查发现相关的批准问题。解决此问题将是美国和欧盟监管批准的必要条件。市场申请由开放标签第一阶段/第二阶段试验(LINKER-MM1)的数据支持,该试验调查了linvoseltamab在至少接受过三种先前治疗或对三种药物均耐药的R/R MM患者中的应用。在该研究的第二部分评估了两种剂量的IV给药linvoseltamab,50 mg(n = 104)或200 mg(n = 117),均在3个周期内Q1W给药,随后Q2W给药。对于在第6周期开始时至少达到非常好的部分反应(VGPR)的200 mg组患者,剂量从第6周期开始减少到Q4W。该研究的主要终点是ORR。在中位随访7.4个月时,接受50 mg治疗的患者ORR为48%,其中21%达到≥CR。在中位随访14.3个月时,接受200 mg治疗的患者ORR为71%,其中50%达到≥CR,63%达到VGPR或更好,由IRC判定。Regeneron正在赞助一项开放标签、随机第三阶段研究(LINKER-MM3,NCT05730036),比较linvoseltamab与elotuzumab、pomalidomide和地塞米松的联合治疗在R/R MM患者中的应用。该研究于2023年9月开始,预计招募380名患者,预计主要完成日期为2032年12月。
Bifikafusp alfa,onfekafusp alfa(Philogen SpA)
Bifikafusp alfa和onfekafusp alfa是Nidlegy™的组成部分,这是一种免疫细胞因子混合物,也称为Daramun,由Philogen开发,用于治疗皮肤癌。这两种免疫细胞因子都结合了L19,这是一种单链可变片段(scFv)抗体,针对纤维连接蛋白的额外域B(EDB)。在bifikafusp alfa中,L19与IL2融合,而在onfekafusp alfa中,L19与肿瘤坏死因子(TNF)融合。Philogen和Sun Pharma达成了一项分销、许可和供应协议,以在欧洲、澳大利亚和新西兰商业化Nidlegy作为皮肤癌治疗。公司向EMA提交了Nidlegy™的市场申请,用于治疗局部晚期可完全切除的黑色素瘤的新辅助治疗,该申请于2024年6月获得验证。市场申请包括了开放标签、随机第三阶段PIVOTAL试验(NCT02938299)的数据,该试验评估了Nidlegy作为可切除、局部晚期III期黑色素瘤的新辅助局部治疗。在本研究中,总共256名患者被随机1:1分配到治疗(新辅助Nidlegy后手术)和对照组(手术)。治疗组(n = 127)的患者接受了Nidlegy(13 Mio IU的L19IL2 + 400 μg的L19TNF,Q1W最多4周)治疗,分布在所有可注射肿瘤病变中。该研究的主要终点是无复发生存(RFS),由研究者评估并经回顾性盲法ICR的PET/CT扫描确认。根据盲法ICR评估,治疗组与对照组RFS之间的HR为0.59(95% CI 0.41–0.86;log-rank p = 0.005),根据研究者评估为0.61(0.41–0.92;p = 0.018)(功效=85%;双侧α=0.05)。根据盲法ICR,治疗组和对照组的中位RFS分别为16.7和6.9个月。
曲妥珠单抗博托丁(四川科伦博泰生物医药有限公司,Sorrento Therapeutics, Inc.)
曲妥珠单抗博托丁(A166,博度曲妥珠单抗,舒泰莱®)是一种人源化IgG1κ抗HER2抗体药物偶联物(ADC),采用Levena Biopharma的专利微管抑制剂Duo-5毒素、可切割连接子和位点特异性K-Lock™偶联化学技术制造。该ADC正在开发用于治疗HER2阳性实体瘤。2023年5月,国家药品监督管理局(NMPA)接受了由四川科伦博泰生物医药有限公司赞助的曲妥珠单抗博托丁用于三线及以后HER2阳性乳腺癌的市场申请。如果获批,公司计划于2024年下半年或2025年上半年在中国推出曲妥珠单抗博托丁。
泰特利单抗(四川科伦药业有限公司)
泰特利单抗(A167,KL-A167,HBM9167,泰特利单抗,科泰莱®)是一种人源化抗PD-L1 IgG1κ单克隆抗体,其Fc段经过工程改造以降低效应功能(L234A,L235A,G237A),由四川科伦药业有限公司开发。Harbour BioMed通过与科伦博泰的许可协议,获得了除大中华区外全球开发和商业化泰特利单抗的权利。2021年11月,NMPA接受了泰特利单抗作为复发或转移性鼻咽癌三线或后续治疗的市场申请。此外,2024年5月,NMPA接受了基于一项3期注册研究的A167新药申请(NDA),用于鼻咽癌的一线治疗。如果获批,公司计划于2024年下半年或2025年上半年在中国推出泰特利单抗。
随机、双盲、安慰剂对照的3期研究(NCT05294172)评估了KL-A167联合顺铂和吉西他滨与安慰剂联合顺铂和吉西他滨在治疗复发或转移性鼻咽癌中的疗效。该研究包括295名患者,他们接受了泰特利单抗1200 mg Q3W,顺铂80 mg/m²在每个21天周期的第1天,4-6个周期,吉西他滨1000 mg/m²在每个21天周期的第1天和第8天,4-6个周期,或与顺铂和吉西他滨匹配的安慰剂治疗。截至2024年10月,研究结果尚未报告。
2022年报告了一项2期试验的结果。在该研究中,患者每2周接受一次900 mg的泰特利单抗静脉注射,直至疾病确认进展、不可耐受的毒性、或撤回知情同意。主要终点是客观反应率(ORR),由独立审查委员会(IRC)根据RECIST v1.1评估。共有153名患者接受治疗,其中132名纳入全分析集(FAS)进行疗效评估。截至2021年7月13日的数据截止日期,中位随访时间为21.7个月(95% CI:19.8–22.5)。在FAS人群中,IRC评估的ORR为26.5%(95% CI:19.2–34.9%),疾病控制率(DCR)为56.8%(95% CI:47.9–65.4%)。中位无进展生存期(PFS)为2.8个月(95% CI:1.5–4.1)。中位反应持续时间(DoR)为12.4个月(95% CI:6.8–16.5),该组的中位总生存期(OS)为16.2个月(95% CI:13.4–21.3)。
贝科妥珠单抗(上海美雅珂生物技术有限责任公司,乐普生物科技股份有限公司)
贝科妥珠单抗(MRG003)是一种人源化抗EGFR IgG1κ抗体,通过可切割的缬氨酸-瓜氨酸连接子与微管破坏剂MMAE偶联。由上海美雅珂生物技术有限责任公司和乐普生物科技股份有限公司开发,MRG003被美国食品药品监督管理局(FDA)授予突破性疗法、孤儿药和快速通道指定,用于治疗复发或转移性鼻咽癌。MRG003也获得了中国药品审评中心授予的突破性疗法指定,用于治疗复发或转移性鼻咽癌。2024年9月,乐普生物宣布NMPA接受了贝科妥珠单抗用于治疗复发或转移性鼻咽癌的新药申请,并授予该申请优先审评。
MRG003–005研究(NCT05126719,CTR20210995)是一项2部分的关键2期研究,评估贝科妥珠单抗在复发转移性鼻咽癌患者中的效果。A部分是一项开放标签、单臂、多中心研究,针对无法手术、放疗不适用的复发或转移性鼻咽癌患者,这些患者至少接受过1次先前的含铂系统化疗并失败(或不耐受)以及PD-1(L1)抑制剂。在A部分,患者每3周静脉注射一次2.0 mg/kg或2.3 mg/kg的贝科妥珠单抗,最长可达24个月。B部分是一项开放标签、随机、多中心研究,比较贝科妥珠单抗与卡培他滨/多西他赛在至少接受过2次先前系统化疗和PD-1(L1)抑制剂治疗的复发或转移性鼻咽癌患者中的疗效和安全性。在B部分,患者接受2.3 mg/kg贝科妥珠单抗每3周静脉注射一次,或卡培他滨片剂/多西他赛注射液,最长可达60个月。主要结果测量是IRC从基线到疾病进展、不可耐受的药物相关毒性、撤回同意或因任何原因停止研究(最长24个月)期间的ORR。目标入组人数为238名患者,主要完成日期为2024年10月。
贝科妥珠单抗还在一项3期试验(CTR20223356)中作为复发或转移性头颈部鳞状细胞癌(SCCHN)患者的二线或三线治疗进行评估。该试验旨在比较贝科妥珠单抗与标准治疗西妥昔单抗/甲氨蝶呤的疗效和安全性,主要完成日期为2025年8月。
艾帕洛利单抗(齐鲁制药有限公司)
艾帕洛利单抗(QL1604,艾帕洛利单抗)是一种高选择性、人源化、铰链稳定的抗PD-1 IgG4κ单克隆抗体,用于治疗实体瘤。2023年9月,NMPA接受了艾帕洛利单抗的新药申请。艾帕洛利单抗是QL1706(艾帕洛利单抗+抗CTLA-4图沃纳利单抗)的抗PD1组分;QL1706的新药申请也在NMPA审查中。
最近报告了一项2期关键临床研究(NCT04326829)的结果,该研究评估了艾帕洛利单抗用于治疗不可切除或转移性错配修复缺陷/微卫星不稳定性高的实体瘤患者。在该研究中,120名患者每3周接受一次艾帕洛利单抗静脉注射,固定剂量为200 mg(或对于体重不足40 kg的患者为3 mg/kg),治疗持续最长2年或直至疾病进展、不可耐受的毒性、开始新的抗肿瘤治疗、死亡、撤回同意或其他特定原因。研究的主要终点是客观反应率,由独立放射学审查委员会(IRRC)根据RECIST 1.1版评估。截至2024年1月20日,意向治疗(ITT)和全分析集(FAS)中的ORR分别为48.3%(58/120;95% CI:39.1–57.6%)和50.0%(30/60;36.8–63.2%)。在结直肠癌患者中,ITT和FAS中的IRRC评估的ORR分别为46.3%(37/80)和57.9%(22/38)。
菲托珠单抗(北京神州细胞生物技术集团股份公司)
菲托珠单抗(SCT-I10A)是一种人源化、铰链稳定的IgG4κ单克隆抗体,靶向免疫检查点蛋白PD-1,由北京神州细胞生物技术集团股份公司主要开发用于实体瘤。NMPA正在审查2023年11月30日接受的菲托珠单抗用于头颈部鳞状细胞癌的新药申请,以及2024年1月17日接受的菲托珠单抗用于未接受过先前系统治疗的不可切除或转移性肝细胞癌(HCC)患者的新药申请。
在一项随机、双盲的3期研究(NCT04146402)中评估了菲托珠单抗(200 mg静脉注射每3周一次)联合标准化疗(顺铂+5-氟尿嘧啶)与安慰剂联合标准化疗在一线复发/转移性头颈部鳞状细胞癌患者中的效果。主要终点是总生存期(OS),定义为从菲托珠单抗首次给药至任何原因导致的死亡日期的时间。在给予菲托珠单抗联合化疗的组(n = 247)中,OS为14.1个月(95%置信区间(CI)11.1–16.4),而安慰剂联合化疗组为10.5个月(95% CI 8.1–11.8)。
在一项3期研究(NCT04560894)中,比较了菲托珠单抗联合SCT510(一种贝伐珠单抗生物类似药抗体)与索拉非尼作为晚期HCC的一线治疗的效果。患者接受菲托珠单抗(200 mg每3周一次)联合SCT510(15 mg/kg每3周一次)或索拉非尼(400 mg口服每日两次),直至无临床益处或不可接受的毒性。在中期分析(2023年11月2日)时,共入组346名患者并至少接受了一剂(菲托珠单抗联合SCT510组,n = 230;索拉非尼组,n = 116),中位随访时间为19.7个月。菲托珠单抗联合SCT510组的中位OS显著长于索拉非尼组(分别为22.1和14.2个月;风险比0.60;95%置信区间[CI]:0.44, 0.81;p = 0.0008)。SCT-I10A联合SCT510组与索拉非尼组相比,中位无进展生存期(PFS)显著延长(分别为7.1和2.9个月;风险比0.50;95% CI:0.38, 0.65;p < 0.0001)。菲托珠单抗联合SCT510组的客观反应率(ORR)也高于索拉非尼组(分别为32.8% [75/229]和4.3% [5/116])。
苏维西塔单抗(先声再明医药有限公司,Apexigen, Inc.)
苏维西塔单抗(BD0801,ENZESHU,苏维西塔单抗)是一种人源化、兔源IgG1κ抗体,靶向VEGF,通过选择性结合VEGFA并阻断其与VEGFR1和VEGFR2的相互作用来抑制肿瘤血管生成。2024年3月15日,先声再明宣布NMPA接受了苏维西塔单抗注射液的新药申请,用于治疗复发性、铂类药物耐药的上皮性卵巢癌、输卵管癌或原发性腹膜癌患者。由先声和Apexigen, Inc.共同开发,先声再明目前持有该产品在大中华区的独家开发和商业化权利。
SCORES研究(NCT04908787)是一项3期、多中心、随机、双盲、安慰剂对照试验,评估苏维西塔单抗联合化疗在铂类药物耐药卵巢癌中的疗效和安全性,在中国55个地点入组421名患者。在初始化疗治疗后,患者被随机分配(2:1)至苏维西塔单抗(1.5 mg/kg每2周一次)或安慰剂联合化疗,直至疾病进展或不可接受的毒性。该研究的主要终点是由盲态IRC确定的PFS,OS是关键次要终点。苏维西塔单抗显著延长了PFS,实验组(n = 281)的中位PFS为5.49个月,而对照组(n = 140)为2.73个月(风险比0.46,p < 0.0001)。所有亚组(如不同年龄组、东部肿瘤协作组(ECOG)表现状态、先前治疗和铂类药物难治状态)的PFS阳性结果一致。50.1%的参与者先前接受过VEGF靶向治疗,48.9%曾接受过PARP抑制剂治疗,苏维西塔单抗联合化疗在这些患者中显示出显著的PFS改善。初步数据显示实验组有生存获益趋势,中位OS为16.07个月,而对照组为14.88个月(风险比0.79,p = 0.1244)。实验组还在其他次要疗效指标如ORR和DCR等方面表现更佳。此外,苏维西塔单抗联合化疗耐受性良好,与同类别其他药物相比没有新的安全问题。
曲妥珠单抗瑞泽替康(江苏恒瑞医药股份有限公司,苏州盛迪亚生物医药有限公司)
曲妥珠单抗瑞泽替康(SHR-A1811)是一种抗体药物偶联物(ADC),由抗HER2抗体曲妥珠单抗与作为拓扑异构酶I抑制剂的有效载荷SHR9265偶联而成。药物抗体比(DAR)平均为5.3至6.4。NMPA已授予曲妥珠单抗瑞泽替康三项突破性疗法指定:1)HER2突变、经铂类药物化疗后的晚期非小细胞肺癌(NSCLC);2)HER2阳性、复发或转移性乳腺癌;3)HER2低表达、复发或转移性乳腺癌。2024年9月,苏州盛迪亚生物医药有限公司向NMPA提交了曲妥珠单抗瑞泽替康用于治疗HER2突变NSCLC的市场申请。
曲妥珠单抗瑞泽替康在一项开放标签、剂量递增和扩展的1/2期研究(NCT04818333)中进行了评估,该研究针对HER2表达、扩增或突变的晚期NSCLC患者,这些患者先前对铂类药物化疗失败或不耐受。患者每3周静脉注射一次曲妥珠单抗瑞泽替康,剂量为3.2至8.0 mg/kg,其中4.8 mg/kg为扩展的推荐剂量。主要疗效终点是客观反应率(ORR)。根据2023年4月11日的数据,4.8 mg/kg组的ORR为41.9%(95% CI 27.0–57.9),中位反应持续时间(DoR)和无进展生存期(PFS)分别为13.7和8.4个月。
江苏恒瑞医药股份有限公司正在赞助一项随机、开放标签、多中心的3期研究(NCT06430437,CTR20241861),评估曲妥珠单抗瑞泽替康用于HER2突变晚期或转移性NSCLC患者的一线治疗,截至2024年12月初尚未招募。曲妥珠单抗瑞泽替康还在进行3期研究,作为晚期结直肠癌(NCT06199973)、复发或转移性乳腺癌(NCT05814354)以及HER2阳性晚期胃癌或胃食管结合部腺癌(NCT06123494)的治疗,截至2024年12月初正在招募患者。
瑞利珠单抗(江苏恒瑞医药股份有限公司,苏州盛迪亚生物医药有限公司)
瑞利珠单抗α(SHR-1701)是一种双功能免疫偶联物,由人抗PD-L1 IgG4抗体组成,该抗体的重链C末端通过肽连接子融合了人转化生长因子(TGF)-β受体II的N末端截短的胞外域。通过结合PD-L1和TGFβ,该分子能够同时阻断癌症细胞常用的两条免疫抑制信号通路。2024年9月19日,NMPA接受了恒瑞医药的瑞利珠单抗α市场申请,该申请寻求批准其与化疗(氟尿嘧啶和铂类药物)联合用于局部晚期不可切除、复发或转移性G/GEJ腺癌的一线治疗。
最近报告了一项随机、安慰剂对照的3期研究(NCT04950322)的结果,该研究评估了瑞利珠单抗α给予先前未经治疗、病理确诊的局部晚期不可切除或转移性G/GEJ腺癌患者的效果,这些患者HER2过表达或扩增阴性。在研究的第一部分,确定了瑞利珠单抗α的推荐剂量为30 mg/kg,与奥沙利铂和卡培他滨(CAPOX)联合使用。在研究的第二部分,731名患者被随机分配(1:1)至接受CAPOX联合瑞利珠单抗α(n = 365;30 mg/kg,静脉注射,每3周一次)或匹配的安慰剂(n = 366)。随机分配根据PD-L1 CPS(≥5 vs <5)、ECOG表现状态(0 vs 1)和腹膜转移(是vs否)进行分层。研究的主要终点是总生存期(OS),在PD-L1 CPS ≥ 5的患者群体和意向治疗(ITT)人群中进行评估。截至2024年5月20日,中位随访时间为8.5个月(四分位间距5.6–13.2)。在给予瑞利珠单抗α和CAPOX联合治疗的PD-L1 CPS ≥ 5患者中,中位OS显著延长,与安慰剂和CAPOX相比(分别为16.8和10.4个月;风险比,0.53(95% CI 0.40–0.68)。在给予瑞利珠单抗α和CAPOX联合治疗的整体人群中,也观察到了OS的统计学显著和临床意义重大的益处,无论PD-L1水平如何。
6.2025年值得关注的抗体:非癌症适应症
在这里,“值得关注的抗体”指的是到2025年底可能提交上市申请的抗体治疗药物。我们的预测基于所有证据,包括赞助公司或公司的公开披露,包括顶级临床研究数据的发布,以及正在进行的临床研究的预计主要完成日期。在我们确定的处于晚期临床研究的非癌症适应症的抗体治疗药物中,我们预计到2025年底可能会提交13个的上市申请(表3)。下面给出了这些分子的关键细节,总结按照我们估计的上市申请提交日期排序。这些分子的额外数据可以在补充表S1中找到。
6.1.Depemokimab(GSK)
Depemokimab(GSK3511294)是一种人源化单克隆IgG1κ抗体,靶向白细胞介素-5(IL-5),这是一种负责嗜酸性粒细胞的生长、激活和存活的细胞因子,但也负责2型炎症,通常通过血液嗜酸性粒细胞计数升高检测。Fc中的M252Y、S254T、T256E(YTE)突变提供了延长的半衰期,并允许每年两次给药。由GSK开发,depemokimab正在被研究用于治疗重度嗜酸性粒细胞性哮喘。Depemokimab被授予治疗高嗜酸性粒细胞性综合征的孤儿药资格。GSK计划在2024年底前在美国提交depemokimab用于重度哮喘和伴有鼻息肉的慢性鼻-鼻窦炎(CRSwNP)的监管申请,随后将在欧盟、中国和日本提交监管申请。公司预计2025年将进行双重适应症的启动。52周、随机、双盲、安慰剂对照的3期SWIFT-1(NCT04719832)和SWITF-2(NCT04718103)研究评估了depemokimab在有2型炎症的重度哮喘成人和青少年中的有效性和安全性。研究参与者(总计n = 762)被随机分配(2:1)在第0周和第26周接受100 mg SC depemokimab或安慰剂,此外还有SOC治疗。主要终点是在52周内的临床显著加重的年化率。在两项试验中,depemokimab使加重减少了54%。122
2024年10月,GSK宣布了复制的随机、双盲3期ANCHOR-1(NCT05274750)和ANCHOR-2(NCT05281523)研究的正面顶级结果,这些研究评估了100 mg SC depemokimab在CRSwNP患者中的有效性和安全性。123 ANCHOR-1包括143名接受depemokimab治疗的患者和128名接受安慰剂的患者,而在ANCHOR-2中,129名患者接受了depemokimab治疗,128名接受了安慰剂。两项试验都达到了它们的共同主要终点:1)在52周时从基线的总鼻内窥镜鼻息肉评分的变化和2)从第49周到第52周的平均鼻塞评分从基线的变化。GSK还在进行其他depemokimab的3期研究,预计2025年将有数据读出。之前参加过SWIFT试验之一的患者可以加入3期AGILE研究(NCT05243680),这是一个开放标签的12个月扩展研究,旨在描述depemokimab辅助治疗在有嗜酸性粒细胞性表型的重度未控制哮喘成人和青少年参与者中的长期安全性、有效性和免疫原性特征。该研究的预计主要完成日期是2025年5月。随机、双盲、非劣效3期NIMBLE研究(NCT04718389)正在评估大约1700名有嗜酸性粒细胞性表型的重度哮喘成人和青少年参与者接受depemokimab治疗与mepolizumab或benralizumab相比的加重率、额外的哮喘控制措施和安全性。该研究的主要完成日期是2025年5月。此外,depemokimab正在被研究用于160名接受SOC治疗的复发性或难治性嗜酸性粒细胞性肉芽肿性多血管炎(EGPA)成人患者在3期OCEAN研究(NCT05263934)中,该研究的主要完成日期是2025年10月。
6.2.Apitegromab(Scholar Rock)
Apitegromab(SRK-015)是一种铰链稳定的IgG4λ单克隆抗体,由Scholar Rock开发,用于抑制肌肉生长的负调节因子myostatin(生长分化因子8)。该药物主要用于治疗脊髓性肌萎缩症(SMA),这是一种以运动神经元丢失和肌肉逐渐萎缩为特征的疾病,也在探索用于保持肥胖患者的瘦肌肉质量。FDA已授予Apitegromab快速通道、孤儿药和罕见儿科疾病资格,EMA已授予优先药物(PRIME)和孤儿药品资格,用于治疗SMA。Scholar Rock预计将在2025年第一季度在美国和欧盟提交上市申请。最近报告了2期TOPAZ研究(NCT03921528)的结果,该研究评估了每四周一次静脉注射(Q4W)给予apitegromab在晚发性2型和3型SMA患者中的安全性和有效性。125,126 总共有58名参与者(平均年龄9.4岁)被分为三个队列。队列1(n = 23)包括接受apitegromab 20 mg/kg单独治疗或与nusinersen联合治疗的行走参与者;队列2(n = 20)包括接受与队列1相同剂量的apitegromab和nusinersen治疗的非行走患者;队列3(n = 20)评估了两种剂量的apitegromab(2 mg/kg,20 mg/kg)与nusinersen的联合治疗。主要终点,运动功能的改善,通过Hammersmith功能运动量表-扩展版(HFMSE)的变化来衡量。在第12个月,队列3观察到最显著的改善,2 mg/kg和20 mg/kg剂量的平均得分分别增加了5.3和7.1分。124 在研究的开放标签扩展期间,患者每四周一次静脉注射20 mg/kg的apitegromab,基于此,12个月观察到的益处在36个月时得以维持。TOPAZ研究的见解为随机、双盲、安慰剂对照、5臂3期SAPPHIRE研究(NCT05156320)的设计提供了信息,该研究招募了188名正在接受批准的存活运动神经元上调治疗(nusinersen或risdiplam)的晚发性SMA患者。2至12岁的2型和非行走3型SMA患者的主要疗效人群中,通过静脉注射给予10 mg/kg、20 mg/kg或安慰剂Q4W治疗52周。在筛选时年龄在13至21岁的探索性亚人群中,患者被随机分配接受20 mg/kg的apitegromab或安慰剂治疗,最多52周。正如2024年10月宣布的,该研究的主要终点,从基线的HFMSE平均变化在12个月时达到。123 在主要疗效人群中,与安慰剂(n = 50)相比,接受10 mg/kg和20 mg/kg apitegromab治疗的所有患者(n = 106)的HFMSE从基线的变化平均差异为1.8分(p = 0.0192)。接受20 mg/kg apitegromab治疗的患者(n = 53)与安慰剂相比显示出1.4分的平均差异(p = 0.1149)。126 在完成TOPAZ或SAPPHIRE的SMA患者中,通过静脉注射每四周一次给予20 mg/kg的apitegromab的长期安全性和有效性正在一个开放标签3期扩展研究(ONYX,NCT05626855)中进行评估,该研究有一个104周的治疗期。
6.3.ANX005(Annexon Biosciences, Inc.)
ANX005是由Annexon Biosciences开发的人源化抗C1q IgG4κ抗体。通过抑制C1q,ANX005旨在防止补体级联的激活,这可能导致炎症、细胞损伤和神经退行性。这种抑制旨在减轻如吉兰-巴雷综合征(GBS)等肌肉疾病中的补体介导的损伤。ANX005已从FDA获得快速通道和孤儿药资格,以及EMA的孤儿药品资格,用于治疗GBS。Annexon计划在2025年上半年向FDA提交BLA。Annexon报告了一项随机、安慰剂对照3期试验(NCT04701164)的正面顶级结果,该试验评估了30 mg/kg或75 mg/kg静脉注射剂量的ANX005与安慰剂在241名GBS患者中的效果。该研究在GBS患病率高且对SOC(静脉免疫球蛋白)获取有限的孟加拉国和菲律宾进行。结果显示,单次输注30 mg/kg的ANX005达到了研究的主要终点,在第8周GBS残疾量表(GBS-DS)改善了2.4倍。ANX005还导致神经丝轻链水平早期降低,这是一种神经损伤的生物标志物,在第2周到第4周之间相对于安慰剂降低了11.2%。
根据美国食品药品监督管理局(FDA)的反馈,Annexon启动了一项真实世界证据(RWE)协议,与国际吉兰-巴雷综合征结果研究(IGOS,NCT01582763)合作,比较第三阶段研究参与者与西方患者的结果。公司预计在2024年底获得RWE可比性协议的初步顶层数据。
6.4.Sibeprenlimab(Otsuka Pharmaceutical Co., Ltd.)
Sibeprenlimab(VIS649)是一种人源化IgG2κ抗体,靶向抗原增殖诱导配体(APRIL),后者涉及免疫球蛋白A肾病(IgAN)的发病机制。通过结合APRIL,该抗体阻断其受体BCMA和跨膜激活剂钙调蛋白及环孢素配体相互作用者的信号传导,从而干扰下游活动,如B细胞增殖、IgA产生和终末B细胞存活。美国食品药品监督管理局(FDA)授予Sibeprenlimab突破性疗法认定,用于治疗IgAN。基于第三阶段VISIONARY研究的积极结果,Otsuka计划在2025年上半年向FDA提交Sibeprenlimab治疗成人IgAN的生物制品许可申请(BLA)。
随机、双盲、安慰剂对照的第三阶段VISIONARY研究(NCT05248646)正在评估Sibeprenlimab(400 mg SC Q4W)与安慰剂相比,在接受标准治疗(SOC)的约530名IgAN患者中的效果。该研究的主要终点是治疗9个月后,24小时尿液收集中的尿蛋白与肌酐比值(uPCR)相对于基线的变化。如2024年10月宣布的,该研究在预定的中期分析中达到了其主要终点。
6.5.Denecimig(Novo Nordisk)
Denecimig(NN-7769, NNC0365–3769, Mim8)是一种由Genmab的Duobody技术衍生的人源、铰链稳定的IgG4κ双特异性抗体,正在开发用于治疗血液凝固和凝血障碍。由Novo Nordisk创建的Denecimig促进激活的凝血因子IXa(FIXa)和X(FX)在血小板膜上的组装,模仿因子VIII,使其成为治疗血友病A的潜在疗法,血友病A是由编码因子VIII的F8基因突变引起的。Denecimig获得了FDA授予的孤儿药认定,用于治疗血友病A。Novo Nordisk计划在2025年向监管机构提交Denecimig的市场申请。
Novo Nordisk的第三阶段FRONTIER临床项目正在评估Denecimig作为预防性治疗血友病A(无论是否伴有抑制剂)的疗效。该项目包括FRONTIER 2(针对12岁及以上人群,NCT05053139)、FRONTIER 3(针对儿童患者,NCT05306418)、FRONTIER 4(NCT05685238)开放标签扩展研究,旨在收集参与FRONTIER第二阶段和第三阶段研究后的长期安全数据,以及FRONTIER 5(NCT05878938)研究血友病A患者从emicizumab转换到Denecimig的效果。
2024年5月,Novo Nordisk宣布,26周开放标签、随机的FRONTIER 2第三阶段研究达到了其共同主要终点,证明每周一次和每月一次剂量的Denecimig显著减少了12岁及以上血友病A患者的治疗出血事件数量。对于那些没有先前预防性治疗的患者,每周Denecimig减少了97%的治疗出血,每月剂量减少了99%。此外,每周方案的86%患者和每月方案的95%患者经历了零治疗出血,而没有预防性治疗的组中没有患者。在已经接受凝血因子预防性治疗的患者中,每周剂量的Denecimig减少了48%的治疗出血,每月剂量减少了43%。此外,每周方案的66%患者和每月方案的65%患者报告没有治疗出血,证明Denecimig优于之前的预防方法。
6.6.Astegolimab(Hoffmann-La Roche, Amgen)
Astegolimab(RO7187807, MSTT1041A, RG6149, AMG282)是一种人源单克隆IgG2κ抗体,靶向并抑制IL-33受体,也称为ST2。IL-33是一种涉及炎症反应的细胞因子,与哮喘和慢性阻塞性肺病(COPD)等各种免疫介导疾病有关。2016年,Amgen将Astegolimab的独家全球权利授权给Genentech,Genentech是Roche的独立子公司,计划在2025年提交COPD的监管申请。
Roche正在进行两项Astegolimab的第三阶段研究用于COPD。随机、双盲、安慰剂对照的ARNASA研究(NCT05595642)正在评估1290名COPD患者的Astegolimab的疗效和安全性。在这项三臂研究中,参与者接受SC Astegolimab Q2W、SC Astegolimab Q4W或SC安慰剂Q2W。主要研究终点是在52周治疗期间中度和重度COPD加重的年化率。预计主要完成日期为2025年6月。
第三阶段开放标签扩展ALNASA研究(NCT05878769)旨在评估完成第三阶段ARNASA或第二阶段ALIENTO(NCT05037929)研究中52周安慰剂对照治疗期的COPD患者中Astegolimab的长期安全性和进一步探索其疗效。预计2000名患者将接受SC Astegolimab Q2W直至研究结束。主要结果测量是最后一次研究治疗后12周内所有不良事件的发生率。预计主要完成日期为2027年6月。
6.7.Cendakimab(Bristol Myers Squibb)
Cendakimab(CC-93538, RPC4046; ABT-308, 13C5.5, BMS-986355)是一种人源化IgG1κ抗体,阻断IL-13的结合,防止IL-13与其两个受体IL-13 Rα1和IL-13 Rα2结合。抗体的Fc部分经过工程改造,以减少Fc介导的效应功能(L234A, L235A)。Cendakimab由多家公司开发用于免疫介导疾病。2013年,AbbVie将Cendakimab授权给受体,后者在2015年被Celgene收购。Celgene在2019年被Bristol Myers Squibb(BMS)收购。一项评估Cendakimab在嗜酸性粒细胞性食管炎(EoE)患者中的疗效和安全性的第三阶段试验达到了两个共同主要终点,为2025年市场申请提供了可能。
在一项随机、双盲、安慰剂对照的诱导和长期对照第三阶段研究(NCT04753697)中评估了Cendakimab在成人和青少年EoE患者中的疗效和安全性。该研究有三个臂:1)Cendakimab 360 mg SC每周一次,持续24周,随后Cendakimab 360 mg SC每周一次,持续24周;2)Cendakimab 360 mg SC每周一次,持续24周,随后Cendakimab 360 mg SC每两周一次,持续24周,在维持阶段的交替周将给予匹配安慰剂以保持盲态;3)匹配安慰剂SC每周一次,持续24周,随后匹配安慰剂SC每周一次,持续24周。该研究达到了共同主要终点,即24周时吞咽困难日临床反应和嗜酸性粒细胞组织学反应的变化,证明与安慰剂相比,在治疗24周后症状(吞咽困难日)和食管嗜酸性粒细胞计数有统计学显著减少。
6.8.SSGJ-613(Sunshine Guojian Pharmaceutical (Shanghai) Co. Ltd., 3SBio)
SSGJ-613是一种人源化单克隆抗体,靶向IL-1β,后者是急性痛风发作的关键介质。由Sunshine Guojian Pharmaceutical (Shanghai) Co. Ltd.和3SBio开发的这种分子,目前正在进行治疗痛风和痛风性关节炎的临床研究。3SBio计划在2025年底前向国家药品监督管理局(NMPA)提交治疗急性痛风性关节炎的新药申请(NDA)。
最近报告了一项在中国急性痛风性关节炎患者中进行的活性对照第二阶段研究的积极结果。在这项研究中,共招募了90名参与者,符合条件的患者以1:1:1的比例随机接受SSGJ-613的单剂量(200或300 mg SC)或地塞米松(1 mL IM)。研究表明,SSGJ-613在任一剂量下的单次注射都能实现与类固醇相似的快速止痛效果,并有效预防发作。
2024年1月,Sunshine Guojian Pharmaceutical启动了一项活性对照第三阶段研究(CTR20233982, NCT06169891, SSGJ-613-AG-III-01),评估SSGJ-613抗体注射在中国急性痛风患者中的疗效和安全性。随机患者在第1天接受一次SSGJ-613(200 mg)的SC注射和安慰剂(0.9%氯化钠)匹配活性对照地塞米松(IM注射),或地塞米松和匹配SSGJ-613的安慰剂。预计招募500名参与者。主要结果测量包括从基线到给药后72小时目标关节疼痛强度的变化(在0-100 mm视觉模拟量表(VAS)上测量)和首次新发作的时间(在首次给药后12周内测量)。
6.9.Itepekimab(Sanofi, Regeneron)
Itepekimab(SAR440340, REGN3500)是一种使用Regeneron的专有VelocImmune技术开发的人IgG4κ单克隆抗体。该抗体结合并抑制IL-33的信号传导,IL-33是气道炎症的启动者和放大器。由Regeneron和Sanofi联合开发的Itepekimab正在研究用于治疗呼吸系统疾病。Itepekimab的主要适应症是COPD,Sanofi计划在2025年下半年在美国和欧盟提交市场申请。
Itepekimab正在两项随机、双盲、安慰剂对照的第三阶段研究AERIFY-1和2(分别为NCT04701983和NCT04751487)中进行研究。三臂AERIFY-1研究旨在评估SC Itepekimab与安慰剂在中度至重度慢性阻塞性肺病(COPD)的前吸烟者中的疗效和安全性。参与者以1:1:1的比例随机接受SC给药的Itepekimab 300 mg Q2W、Itepekimab 300 mg Q4W与在Itepekimab给药间隔的2周交替匹配安慰剂,或匹配安慰剂(Q2W)最多52周。AERIFY-2研究设计相同,但包括当前和前吸烟者患有中度至重度COPD。AERIFY-1和2的预计招募人数分别为960和1210名参与者。两项研究的主要终点是中度或重度急性COPD加重(AECOPD)的年化率,在安慰剂对照治疗期间测量。AERIFY-1和2的预计主要完成日期分别为2025年6月27日和5月30日。
Itepekimab的长期安全性和耐受性正在双盲、两臂第三阶段AERIFY-4研究(NCT06208306)中进行评估。这项扩展研究将从参与AERIFY-1和2研究的受试者中招募预计700名受试者,旨在生成额外的安全性数据,评估治疗反应的持久性,并提供Itepekimab SC Q2W或Itepekimab SC Q4W的额外药代动力学和免疫原性评估。AERIFY-4的预计主要完成日期为2026年12月。
6.10.维尔迪安治疗公司(Viridian Therapeutics, Inc.)
维尔迪安治疗公司的维尔格罗图(Veligrotug,VRDN-001,AVE-1642)是一种人源化IgG1κ单克隆抗体,靶向胰岛素样生长因子1受体(IGF-1R)的细胞外域。该药物最初由ImmunoGen与Sanofi-Aventis合作开发,Viridian从ImmunoGen, Inc.独家获得了VRDN-001的全球开发和商业化权利,用于所有不使用放射性药物的非肿瘤学适应症。Viridian预计将在2025年下半年提交用于治疗甲状腺眼病(TED)的生物制品许可申请(BLA)。2024年9月,Viridian Therapeutics宣布了安慰剂对照的III期THRIVE研究(NCT05176639)的积极顶层结果,该研究首次评估了在健康志愿者和中度至重度活动性TED参与者中多次递增剂量(MAD)的维尔格罗图的效果,然后评估了在TED参与者中的单剂量水平的维尔格罗图。在研究的MAD部分,参与者被随机分配接受30分钟静脉输注维尔格罗图,剂量范围从3 mg/kg到20 mg/kg(n = 75)或安慰剂(n = 38)。TED患者随后被随机分配接受每3周一次的10 mg/kg维尔格罗图或安慰剂静脉输注。研究的主要终点是MAD TED参与者在第6周和III期研究对象在第15周的突眼反应率。在五次输注维尔格罗图后15周,研究达到了主要和所有次要终点,显示出在所有测量的TED体征和症状上具有高度统计学意义(p < 0.0001)的改善。在接受维尔格罗图治疗的患者中,突眼反应率为70%,67%实现了总体反应,而接受安慰剂治疗的患者中,突眼反应率为5%,5%实现了总体反应。维尔格罗图的随机、双盲、安慰剂对照III期研究THRIVE-2(NCT06021054)在慢性TED患者中已超额完成入组。在这项研究中,患者将接受5次10 mg/kg维尔格罗图的输注。预计在2024年底公布顶层数据。
6.11.阿斯利康(AstraZeneca)的安塞尔米单抗(Anselamimab)
安塞尔米单抗(CAEL-101,11-1F4)是一种嵌合单克隆IgG1κ抗体,旨在靶向由骨髓中的浆细胞产生的错误折叠的轻链蛋白形成的淀粉样纤维,并介导巨噬细胞和中性粒细胞的吞噬作用。这些纤维在组织和器官中积累,导致一种称为轻链(AL)淀粉样变性的疾病。这种罕见疾病导致淀粉样物质在心脏、肾脏和肝脏等关键器官中沉积,逐渐损害其功能并随时间造成显著的器官损伤。Fortress Biotech, Inc.的子公司Caelum Biosciences从哥伦比亚大学获得了安塞尔米单抗的全球独家许可权,并随后与Alexion Pharmaceuticals, Inc.合作进行该分子的临床开发。阿斯利康在2021年收购了Alexion和Caelum Biosciences。安塞尔米单抗已获得美国食品药品监督管理局(FDA)和欧洲药品管理局(EMA)的孤儿药和孤儿药产品指定,作为一种潜在治疗AL淀粉样变性患者的疗法。FDA还授予了安塞尔米单抗针对AL淀粉样变性的快速通道指定。阿斯利康预计将在2025年获得安塞尔米单抗在AL淀粉样变性中的关键III期研究结果,这可能允许在2025年为安塞尔米单抗提交针对AL淀粉样变性的监管申请。阿斯利康的Alexion部门目前正在Cardiac Amyloid Reaching for Extended Survival(CARES)项目中评估安塞尔米单抗,该项目旨在通过两项III期研究评估其在AL淀粉样变性患者中的疗效与安慰剂相比。两项研究的主要终点是从试验药物首次给药至死亡或试验结束的时间。随机、双盲的III期NCT04512235研究评估了静脉注射安塞尔米单抗或安慰剂与SOC联合治疗281例Mayo Stage IIIa AL淀粉样变性初治患者的疗效和安全性。该研究的主要完成日期预计为2025年4月。III期NCT04504825研究设计相同,但包括125例Mayo Stage IIIb患者。该研究的主要完成日期预计为2025年5月。
6.12.默克雪兰诺(Merck Serono)、MoonLake Immunotherapeutics AG的索奈洛单抗(Sonelokimab)
索奈洛单抗(M1095,ALX-0761)是一种三特异性抗体片段,靶向IL-17A、IL-17F和白蛋白。该分子由三个纳米抗体组成,这些纳米抗体是从骆驼科动物衍生的仅重链单域抗体,通过灵活的甘氨酸-丝氨酸间隔物共价连接。一个特定于IL-17F的结构域和一个特定于IL-17A和IL-17F的结构域被一个靶向白蛋白的结构域分隔,以促进纳米抗体在炎症水肿部位的富集。2021年,MoonLake Immunotherapeutics AG从Merck KGaA获得了索奈洛单抗的许可,Merck KGaA在2013年通过与Ablynx(现为赛诺菲公司Ablynx)的全球开发和商业化协议获得了索奈洛单抗的全部独家权利。MoonLake Immunotherapeutics正在开发索奈洛单抗用于治疗汗腺炎(HS)和银屑病关节炎(PSA),以及皮肤科和风湿病学的其他适应症。在2023年宣布的全球II期MIRA试验的积极顶层结果之后,公司启动了III期VELA项目,预计将招募800名中度至重度HS患者。预计在2025年中期公布主要终点的结果;积极的研究结果可能允许在2025年底提交市场应用申请。VELA项目包括两项III期试验,VELA-1(NCT06411899)和VELA-2(NCT06411379),这些是全球、随机、双盲、安慰剂对照的研究,设计相同,评估皮下注射索奈洛单抗与安慰剂相比在成年中度至重度HS参与者中的疗效和安全性。被随机分配到索奈洛单抗组的患者将在第0至6周接受120 mg Q2W索奈洛单抗,然后从第8周开始至第48周每4周一次(Q4W)。安慰剂组的患者将在第0至6周接受Q2W安慰剂,然后从第8周开始至第16周每4周一次,之后他们将在第16至22周接受4次120 mg Q2W索奈洛单抗,然后从第24周开始至第48周每4周一次。主要终点是临床反应的更高测量值,HS临床反应(HiSCR)75,定义为从基线开始脓肿和炎性结节(AN)计数至少减少75%,且脓肿或引流窦道计数没有从基线增加,该测量在第16周进行。每项研究预计招募400名患者,主要完成日期为2025年6月。索奈洛单抗也在PSA中进行研究,II期ARGO试验达到了主要和关键次要终点,预计将在2024年第四季度启动III期试验(NCT06641076,NCT06641089)。预计将在2024年底启动掌跖脓疱病和放射学及非放射学轴向脊柱关节炎(axSpA)的II期试验。
6.13.雷斯奥单抗(Ersodetug,Rezolute, Inc.)
雷斯奥单抗(RZ358,XOMA 358)是一种人IgG2κ单克隆抗体,靶向胰岛素受体。该抗体结合到胰岛素受体上的一个变构位点,在目标组织如肝脏、脂肪和肌肉中调节胰岛素的结合、信号传导和活性,以恢复血糖水平至正常范围。雷斯奥单抗已被证明在小鼠和健康人类中诱导全身性胰岛素抵抗,并逆转胰岛素刺激的低血糖,有可能有效治疗任何形式的高胰岛素血症(HI)引起的低血糖,这是一种罕见的遗传性儿科内分泌疾病,有先天性和获得性形式。Rezolute, Inc.在2017年从XOMA Corporation获得了雷斯奥单抗的全球开发和商业化权利,正在开发该分子作为高胰岛素血症(HI)的治疗方法。雷斯奥单抗已获得美国和欧盟的孤儿药和孤儿药产品指定,以及美国的儿科罕见病指定。雷斯奥单抗在先天性HI患者中的III期sunRIZE研究的主要完成日期预计为2025年4月。预计在2025年下半年公布顶层数据。随机、双盲、安慰剂对照、平行组III期sunRIZE试验(NCT06208215)正在评估雷斯奥单抗在先天性HI患者中的疗效和安全性,作为SOC治疗的附加治疗与单独SOC治疗相比在24周内的效果,以及在随后的开放标签扩展期间雷斯奥单抗的长期安全性和疗效。该研究预计将招募48名参与者(≥1岁至≤45岁),以1:1的比例随机分配到两个剂量组(5或10 mg/kg)。每个剂量水平的参与者将进一步以2:1的比例随机分配接受雷斯奥单抗作为SOC的附加治疗或安慰剂作为SOC的附加治疗。还将平行进行一个开放标签组,针对≥3个月至<1岁的参与者,预计将招募8名参与者。在关键治疗期(24周)完成后,患者可以转入开放标签扩展期。主要终点是从基线通过即时护理自我监测血糖测量的平均每周低血糖事件的变化。
7.2025年值得关注的抗体:癌症适应症
根据截至2024年11月可用的所有证据,我们预计只有五种我们识别为处于癌症晚期临床研究中的抗体治疗药物可能会在2025年底前提交市场申请(表4)。这些分子的关键细节如下所述,总结按照我们估计的市场申请提交日期排序。这些分子的额外数据可以在补充表S1中找到。
7.1.Erfonrilimab (江苏康宁杰瑞生物制药有限公司)
Erfonrilimab (KN046) 是一种人源化双特异性抗体,具有 2 + 2 对称设计((VHH-VHH’)2-Fc),靶向免疫系统检查点蛋白 PD-L1 和 CTLA-4。江苏先声药业正在开发 Erfonrilimab 用于各种实体瘤,并与包括辉瑞、泽璟、东阳光、开拓药业、信诺维和 InxMed 在内的多家公司就 Erfonrilimab 开展了合作。Erfonrilimab 获得 FDA 授予的孤儿药资格,用于治疗胸腺上皮肿瘤和胆管癌。江苏先声药业预计将在 2024 年对鳞状(sq)非小细胞肺癌(NSCLC)的一线治疗进行最终 OS 分析,如果结果积极,可能会向 NMPA 提交 NDA。
最近报告了 Erfonrilimab 与化疗联合用于转移性 NSCLC 一线治疗的开放标签 2 期 KN046–202 试验(NCT04054531)的结果。该研究包括两个队列:1)非鳞状 NSCLC 患者接受培美曲塞与 KN046(5 mg/kg IV Q3W)和卡铂(n = 51);2)鳞状 NSCLC 患者接受紫杉醇与 KN046(5 mg/kg IV Q3W)和卡铂(n = 36)。经过四个周期后,维持治疗包括非鳞状 NSCLC 的 KN046 与培美曲塞,以及鳞状 NSCLC 的 KN046。主要终点是确认的 ORR 和中位 DoR。非鳞状 NSCLC 和鳞状 NSCLC 队列的确认 ORR 分别为 43.1% 和 50.0%。非鳞状 NSCLC 和鳞状 NSCLC 队列的中位 DOR 分别为 9.7(95% CI:4.01–20.73)和 7.3(95% CI:3.52-NR)个月。非鳞状 NSCLC 和鳞状 NSCLC 队列的中位 PFS 分别为 5.8(95% CI:4.80–7.16)和 5.7(95% CI:4.17–8.71)个月。非鳞状 NSCLC 队列的中位 OS 为 27.2(95% CI:15.18-NR)个月,鳞状 NSCLC 队列的中位 OS 为 26.6(95% CI:12.19-NR)个月。
随机、安慰剂对照的 3 期 ENREACH-LUNG-01 研究(NCT04474119,CTR20201294)旨在验证 KN046 与含铂化疗联合用于晚期鳞状 NSCLC 患者一线治疗的疗效和安全性。在这项 2 臂研究中,患者在双盲期的前 12 周接受卡铂、紫杉醇和 IV KN046 5 mg/kg Q3W,然后在交叉期接受 IV KN046 5 mg/kg Q2W,或者患者接受卡铂、紫杉醇和安慰剂。该研究于 2020 年 9 月启动,预计招募 482 名患者。主要终点是根据 RECIST 1.1 标准的 PFS,次要终点是评估期间(3 年)的 OS。
7.2.安贝尼塔单抗(上海杰迈捷生物科技有限公司、江苏康宁杰瑞生物制药有限公司)
Anbenitamab(KN026) 是一种人源化、双特异性 IgG1κ 单克隆抗体,靶向 HER2 的两个非重叠表位。该抗体设计有共同的轻链和重链,通过 knob-in-hole 和静电导向突变进行工程改造,以实现异二聚体化。通过阻断 HER2,Anbenitamab 抑制肿瘤细胞生长并促进抗体依赖性细胞介导的细胞毒性(ADCC)。
2021 年,上海 JMT-Bio 从江苏先声药业获得了 Anbenitamab 作为单一药物以及与 KN046(一种靶向免疫系统检查点蛋白 PD-L1 和 CTLA-4 的双特异性抗体)联合用于中国内地乳腺癌和胃癌适应症的独家开发和商业化许可权。Anbenitamab 与化疗联合用于治疗 HER2 阳性胃癌患者(这些患者已对一线标准治疗失败)被 NMPA 授予突破性疗法认定,FDA 也授予 Anbenitamab 与 KN046 联合用于治疗 HER2 阳性或低表达 G/GEJ 癌症的孤儿药资格。预计将在 2025 年提交 Anbenitamab 的 NDA。
上海 JMT-Bio 正在进行关键试验,评估 Anbenitamab 在胃癌和乳腺癌中的疗效。KN026–001(NCT05427383,CTR20213458)是一项两阶段随机、2/3 期临床研究,旨在评估 IV Anbenitamab 30 mg/kg Q3W 与化疗(紫杉醇/多西他赛/伊立替康)联合 vs 安慰剂和化疗在约 286 名 HER2 阳性晚期不可切除或转移性胃癌患者(包括胃食管结合部腺癌)中的疗效,这些患者已对一线治疗失败。该研究的主要终点是 PFS 和 OS,最长可达 2.5 年。预计该研究的主要完成日期为 2025 年 11 月。
上海 JMT-Bio 还正在进行一项随机、对照、开放标签的 3 期 KN026–001 试验(NCT05838066,CTR20231442),评估 Anbenitamab 与 HB1801(白蛋白结合型多西他赛)联合 vs 曲妥珠单抗 + 帕妥珠单抗 + 多西他赛在 HER2 阳性复发或转移性乳腺癌患者一线治疗中的疗效和安全性。该研究的主要终点是 PFS。预计该研究的主要完成日期为 2026 年 7 月。
7.3.诺法辛利单抗(基石药业,3SBio Inc.)
Nofazinlimab (CS1003) 是一种人源化、铰链稳定的 IgG4κ 单克隆抗体,靶向人类 PD-1,源自 CStone Pharmaceuticals 的专有杂交瘤平台。Nofazinlimab 与人类和小鼠 PD-1 均有交叉反应,便于在同种小鼠肿瘤模型中进行疗效测试。目前,该分子由 CStone 和 3SBio 开发用于各种肿瘤的免疫治疗,3SBio 拥有在中国内地开发、注册、制造和商业化 Nofazinlimab 的权利,而 CStone 保留中国内地以外的权利。Nofazinlimab 获得美国孤儿药资格,用于治疗肝细胞癌(HCC)患者。3SBio 计划在 2025 年向 NMPA 提交 Nofazinlimab 用于 HCC 的 NDA。
双盲、随机的 3 期 CS1003–305 研究(NCT04194775,CTR20192524)正在评估 IV Nofazinlimab 与仑伐替尼(一种 SOC TKI)联合 vs 安慰剂和仑伐替尼作为晚期 HCC 患者一线治疗的疗效和安全性。参与者接受 200 mg Nofazinlimab Q3W 与仑伐替尼或安慰剂和仑伐替尼,直至疾病进展、不可耐受的毒性发生或因其他原因退出研究。该研究的主要终点是 OS。招募了 534 名患者;预计最终 OS 分析将在 2025 年上半年进行。
7.4.Cobolimab (GSK) 科博利单抗
Cobolimab (GSK4069889, TSR-022) 是一种人源化、铰链稳定的 IgG4κ 单克隆抗体,靶向免疫检查点 T 细胞免疫球蛋白和黏蛋白域蛋白-3(TIM-3),与抑制抗肿瘤反应相关。通过抑制 TIM-3,Cobolimab 激活免疫系统功能,其活性在与 PD-1 药物联合时得到增强。Cobolimab 由 TESARO 发现并最初开发,TESARO 于 2019 年被 GSK 收购。GSK 计划在 2025 年上半年在美国和欧盟为二线 NSCLC 患者提交 Cobolimab 的监管申请。
随机、开放标签、三臂的 2/3 期 COSTAR Lung 试验(NCT04655976)旨在比较 1)Cobolimab 联合抗 PD-1 Dostarlimab + 多西他赛,2)Dostarlimab + 多西他赛和 3)单独多西他赛的效果。该研究已招募了 758 名先前接受过抗 PD-(L)1 治疗和化疗后进展的晚期 NSCLC 患者,分别随机分配到 3 个研究组,比例为 2:1:1。该研究的主要终点是接受联合治疗与单独多西他赛治疗的参与者的 OS,最长可达 44 个月。数据读出预计在 2025 年上半年。
7.5.Tiragolumab (Hoffmann LaRoche)
Tiragolumab (RO7092284, RG6058, MTIG7192A) 是一种人 IgG1κ 抗体,靶向免疫检查点蛋白 T 细胞免疫受体,具有免疫球蛋白和 ITIM 域(TIGIT),该蛋白存在于激活的 T 细胞、自然杀伤细胞和调节性 T 细胞上,作为免疫系统功能的抑制因子。TIGIT 和 PD-1/PD-L1 的双重阻断在一些临床前和临床研究中显示出增强的抗癌效果。罗氏正在评估 Tiragolumab 和抗 PD-L1 Atezolizumab(Tecentriq®)的联合治疗,在肺癌、食管癌和 HCC 患者的多项晚期研究中。
截至 2024 年第三季度,罗氏预计可能在 2025 年提交 Tiragolumab 和 Atezolizumab 联合治疗的市场申请,用于接受至少两个周期的同步铂类化疗放疗且未发生放射学疾病进展的 III 期不可切除 NSCLC 患者,基于 SKYSCRAPER-03 研究(NCT04513925),以及用于局部晚期不可切除或转移性 PD-L1 选择的 NSCLC 患者的一线治疗,这些患者无 EGFR 突变或间变性淋巴瘤激酶易位,基于安慰剂对照的 3 期 SKYSCRAPER-01 研究(NCT04294810)。然而,SKYSCRAPER-01 研究未达到其 PFS 或 OS 的主要终点。
2024 年 7 月,罗氏集团成员 Genentech 报告称,安慰剂对照的 2/3 期 SKYSCRAPER-06 研究(NCT04619797)未能在非鳞状 NSCLC 的一线治疗中达到 PFS 的主要终点,以及在首次中期分析中 OS 的主要终点,该研究评估了 Tiragolumab 与 Atezolizumab 和化疗的联合治疗。公司表示他们打算终止该研究。
正在进行的晚期研究还在评估 Tiragolumab 与其他疗法的联合治疗,作为食管癌(SKYSCRAPER-07(NCT04543617),SKYSCRAPER-08(NCT04540211))和 HCC 患者(SKYSCRAPER-14,NCT05904886)的一线治疗。在中国进行的安慰剂对照 3 期 SKYSCRAPER-08 研究评估了 Tiragolumab 与 Atezolizumab 和化疗的联合治疗,作为不可切除局部晚期、不可切除复发或转移性食管癌患者的一线治疗。符合条件的患者被随机分配(1:1)到两个研究组之一,接受:1)Tiragolumab 600 mg + Atezolizumab 1200 mg + 化疗,或 2)安慰剂 + 化疗。该研究达到了独立审查机构评估的 PFS 和 OS 两个主要终点,中位 PFS 分别为 6.2 个月和 5.4 个月,中位 OS 分别为 15.7 个月和 11.1 个月,对于包含 Tiragolumab 的治疗组 vs 安慰剂组。
8.未来展望
总体而言,2024年对于抗体治疗药物来说是非常好的一年,这体现在晚期临床开发中的分子数量大幅增加(此处报告的有178个)与2010-2024年间“值得关注的抗体”报告中所报告的数量(范围26-138)相比。此外,与2024年版的“值得关注的抗体”相比,我们还报告了抗体治疗药物接受监管审查以及首次获批的数量略高。然而,在这积极的消息中,我们也注意到一个令人担忧的领域,即首次周期内未获FDA批准的BLA(生物制品许可申请)的更高比例,这延迟了患者获得治疗的机会。在美国监管审查中的九种研究性抗体(即那些在其他地方未获批准的)中有四种目前正处于第二次审查周期,此前收到了FDA的CRL(表2)。FDA还在审查另外四种在其他国家首次获批的抗体治疗产品的申请,因此未包含在表2中,其中三种收到了CRL,使得FDA审查中的分子总数达到13个,其中七个(54%)处于第二次审查周期(补充表S2)。我们最近注意到FDA发出的CRL有所增加,尤其是那些因CMC(化学、制造和控制)问题而发出的(图3)。当机构对市场申请有担忧时,FDA会发出CRL。赞助公司必须在重新提交的BLA中解决这些问题,该BLA必须由FDA进一步审查,这可能会使产品的批准延迟6个月或更长时间。值得注意的是,大多数CRL是由于CMC缺陷而非与安全或有效性相关的问题发出的,这突显了赞助商及其第三方制造合作伙伴需要积极主动,确保制造场所符合FDA对现行良好生产规范的要求。
图3. 美国食品药品监督管理局发出的完整回应函的趋势。黄色部分,经过首次审查后获批或目前正在进行首次审查的抗体治疗药物。橙色部分,由FDA发出的完整回应函(CRL)。条纹橙色部分,因化学、制造和控制(CMC)问题由FDA发出的CRL。2024年的数据截至2024年12月7日。
与过去一样,我们将继续跟踪抗体治疗药物进入晚期临床研究并朝着市场批准进展的进展。我们期待在未来“值得关注的抗体”文章中进一步报告趋势并记录这些分子的成功。
识别微信二维码,添加生物制品圈小编,符合条件者即可加入
生物制品微信群!
请注明:姓名+研究方向!
版
权
声
明
本公众号所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系(cbplib@163.com),我们将立即进行删除处理。所有文章仅代表作者观点,代表本站立场。
抗体药物偶联物临床2期申请上市
2024-08-02
·药明康德
▎药明康德内容团队编辑
SFJ Pharmaceuticals和SERB Pharmaceuticals今天宣布,美国FDA已接受为在研疗法bentracimab递交的生物制品许可申请(BLA)并授予其优先审评资格,预计在2025年第一季度完成审评。
Bentracimab是一种人源化单克隆抗体片段,正在开发作为一种特定的逆转剂,用于在使用替格瑞洛(商品名Brilinta)的患者中,逆转替格瑞洛及其活性代谢物的抗血小板作用。Bentracimab在2019年获得了FDA授予的突破性治疗认定。替格瑞洛是一种靶向P2Y12的血小板抑制剂,通过抑制血小板功能防止血栓的产生,可用于预防和治疗心脑血管血栓事件和减少急性冠状动脉综合征(ACS)。然而,抑制血小板功能也让患者的出血风险增加。Bentracimab通过与替格瑞洛结合,中和其抗血小板的作用。
BLA的提交基于3期临床试验REVERSE-IT的第二次中期分析结果。REVERSE-IT试验的首次中期分析结果已于2021年发表在NEJM Evidence期刊上。结果显示,在需要接受紧急手术和大出血患者中,bentracimab可以立即和持续逆转替格瑞洛的抗血小板作用,达到主要研究终点。接受治疗5-10分钟后,血小板抑制率降低135%(p<0.01),持续24小时以上。在绝大多数病例中,该药的有效止血被评为良好或优秀,且没有发生药物相关的严重不良事件或过敏反应。
▲欲了解更多前沿技术在生物医药产业中的应用,请长按扫描上方二维码,即可访问“药明直播间”,观看相关话题的直播讨论与精彩回放
参考资料:
[1] FDA has accepted a BLA for bentracimab, the first and only ticagrelor reversal agent, for filing and priority review. Retrieved August 2, 2024, from https://www.globenewswire.com/news-release/2024/08/02/2923626/0/en/FDA-has-accepted-a-BLA-for-bentracimab-the-first-and-only-ticagrelor-reversal-agent-for-filing-and-priority-review.html
免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
版权说明:本文来自药明康德内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在「药明康德」微信公众号回复“转载”,获取转载须知。
分享,点赞,在看,聚焦全球生物医药健康创新
优先审批突破性疗法临床3期临床结果
2023-01-15
·生物谷
该研究成功制备了一种具有抗血小板药物药效逆转功能的血小板仿生纳米海绵PLT-PFC,其表面保留了大部分血小板膜表面的药物靶点,可以竞争性结合抗血小板药物,有效逆转抗血小板药物的药效。
血栓性疾病严重威胁人类的生命健康,其发病率高居各种疾病之首,主要包括心肌梗塞、缺血性脑卒中、肺栓塞等。随着人们生活水平的不断提高,血栓性疾病的发病率呈上升趋势。
抗血小板药物是多种血栓性疾病长期防治的临床指南推荐一线药物,主要包括环氧合酶-1抑制剂、磷酸二酯酶抑制剂、二磷酸腺苷受体抑制剂、糖蛋白GPIIb/IIIa抑制剂、凝血酶受体抑制剂等。与抗凝治疗相似,长期的抗血小板药物治疗势必会给病人带来严重的出血风险,如皮下出血、消化道出血、颅内出血等,引起致死或致残等严重后果。此外,长期使用抗凝药物/抗血小板药物的病人遭遇车祸或者需要进行紧急手术时,对其体内的抗凝药物/抗血小板药物进行功能逆转可以为病人争取更多的安全治疗时间。
针对抗凝药物,临床上已经具有多种逆转剂可供选择,例如鱼精蛋白、Idarucizumab、Andexanet α、Ciraparantag、重组活化凝血因子VIIa、维生素K等。而抗血小板药物目前尚无已上市逆转剂,只有针对抗血小板药物替格瑞洛的一种单克隆抗体Bentracimab处于临床三期。临床常用的血小板输注策略,在多种抗血小板药物逆转方面效果不佳,并且血小板输注的数量需要严格限制以免带来额外的血栓风险。
2023年1月10日,国家纳米科学中心聂广军研究员团队和中国科学院大学纳米学院张银龙副教授团队合作在 Circulation Research 期刊发表了题为:Platelet-mimicking nanosponges for functional reversal of antiplatelet agents 的研究论文。
该工作针对长期服用抗血小板药物带来的出血风险,以及长期服用抗血小板药物的病人需要紧急介入手术等临床实际科学问题,提出了利用血小板膜纳米海绵对抗血小板药物特异性逆转的策略。与血小板输注不同,纳米海绵惰性内核无主动的血栓块收缩能力,因此在高剂量下无明显的体内致栓风险。
为了证明血小板膜纳米海绵制备过程中,血小板膜表面受体没有丢失,研究者首先通过纳米流式证明了纳米海绵表面P2Y12和αIIb/β3受体的保留。通过SDS-PAGE实验对血小板膜纳米囊泡和纳米海绵的全蛋白进行对比,发现纳米海绵保留了血小板膜的大部分蛋白。进一步地,通过蛋白质组学和免疫印迹分析,同样证明了纳米海绵保留了大部分血小板膜蛋白及重要的受体蛋白(CD41、CD61、P2Y12)。纳米海绵中没有发现管家蛋白GAPDH的存在,证实制备过程中,成功去除血小板内容物蛋白,保证所制备的血小板膜纳米海绵不具有诱导血栓形成的风险。
为了证明纳米海绵PLT-PFC对抗血小板药物具有高的亲和力,研究者通过等温滴定量热法和微量热泳分析等技术手段,分别测定了两者的Ka值和Kd值,实验结果表明,纳米海绵与替格瑞洛(Ticagrelor)、替罗非班(Tirofiban)两种抗血小板药物具有高的亲和系数和低的解离系数,为抗血小板药物的高效逆转提供了理论基础。研究者通过体外血小板聚集实验证明了纳米海绵PLT-PFC可以有效逆转Ticagrelor的抗血小板活性。
随后,研究者在小鼠体内评价纳米海绵PLT-PFC对Ticagrelor的功能逆转效应。通过尾静脉注射的方式提前给药Ticagrelor,随后注射纳米海绵PLT-PFC。通过高效液相色谱测定给药后不同时间点血液中Ticagrelor的浓度,并通过尾尖出血实验评价小鼠的止血功能。实验结果表明,PLT-PFC可以有效降低Ticagrelor曲线下面积,并恢复小鼠的止血功能。
最后,研究者评价了纳米海绵PLT-PFC在抗血小板药物引起的卒中出血转化模型中的作用。实验性脑卒中模型小鼠在造模之前连续三天给药Ticagrelor,造模前注射纳米海绵PLT-PFC,造模完成后给予溶栓治疗,通过核磁共振成像技术和Evans blue染料渗透实验评价小鼠脑出血和坏死面积。实验结果表明,抗血小板治疗可以增加卒中溶栓治疗的出血风险和脑梗死面积,而PLT-PFC可以有效逆转抗血小板药物的药效,降低出血风险,预防抗血小板药物诱导的脑栓塞面积增加。
综上所述,该研究成功制备了一种具有抗血小板药物药效逆转功能的血小板仿生纳米海绵PLT-PFC,其表面保留了大部分血小板膜表面的药物靶点,可以竞争性结合抗血小板药物,有效逆转抗血小板药物的药效。与血小板输注相比,惰性内核的引入可以有效降低血栓风险。PLT-PFC对抗血小板药物的功能逆转在尾尖出血模型及卒中出血转化模型中都得到了验证。该研究提出了一种广谱的抗血小板药物逆转策略,为临床抗血小板药物的功能逆转提供新思路。

临床3期
分析
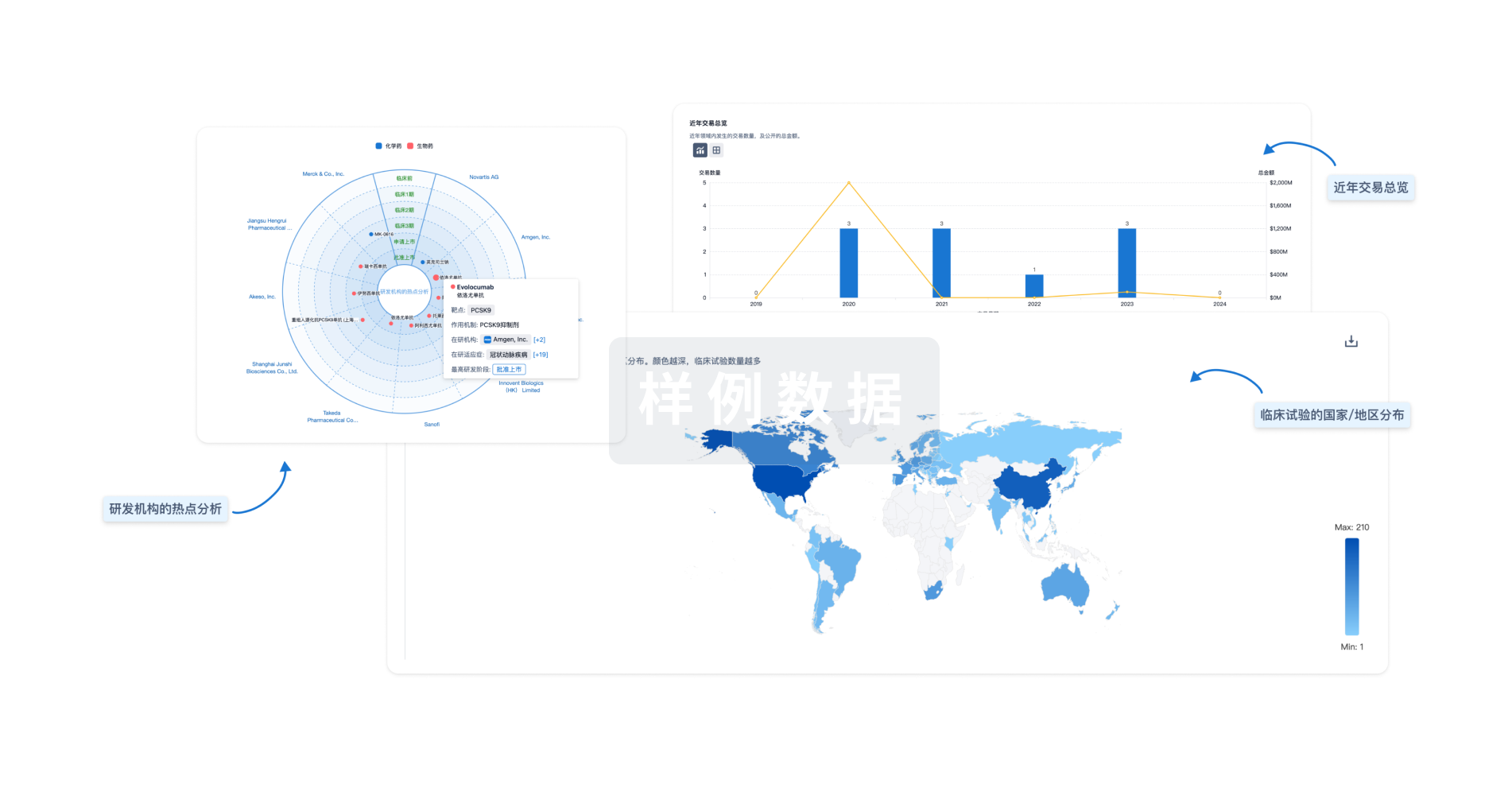
对领域进行一次全面的分析。
登录
或
生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用

