预约演示
更新于:2025-05-07
FCRL5 x Tubulin
更新于:2025-05-07
关联
3
项与 FCRL5 x Tubulin 相关的药物作用机制 FCRL5抑制剂 [+1] |
在研机构- |
原研机构 |
在研适应症- |
非在研适应症 |
最高研发阶段终止 |
首次获批国家/地区- |
首次获批日期1800-01-20 |
作用机制 FCRL5抑制剂 [+1] |
在研机构- |
原研机构 |
在研适应症- |
非在研适应症 |
最高研发阶段终止 |
首次获批国家/地区- |
首次获批日期1800-01-20 |
作用机制 FCRL5抑制剂 [+1] |
在研机构- |
原研机构 |
在研适应症- |
最高研发阶段无进展 |
首次获批国家/地区- |
首次获批日期1800-01-20 |
1
项与 FCRL5 x Tubulin 相关的临床试验NCT01432353
An Open-label, Multicenter, Phase I Trial of the Safety and Pharmacokinetics of Escalating Doses of DFRF4539A in Patients With Relapsed or Refractory Multiple Myeloma
This multicenter, open-label, dose-escalating study will assess the safety and efficacy of DFRF4539A in patients with relapsed or refractory multiple myeloma. Cohorts of patients will receive multiple ascending doses of intravenous DFRF4539A every 3 weeks or weekly. Patients exhibiting acceptable safety and evidence of clinical benefit may receive DFRF4539A for up to 17 cycles. Anticipated time on study treatment is 1 year or until disease progression or unacceptable toxicity occurs.
开始日期2011-09-01 |
申办/合作机构 |
100 项与 FCRL5 x Tubulin 相关的临床结果
登录后查看更多信息
100 项与 FCRL5 x Tubulin 相关的转化医学
登录后查看更多信息
0 项与 FCRL5 x Tubulin 相关的专利(医药)
登录后查看更多信息
1
项与 FCRL5 x Tubulin 相关的新闻(医药)2023-08-31
·研发客
// 罗氏在血液疾病领域不断推陈出新,布局了两款具有潜力的CD20/CD3双抗,glofitamab和mosunetuzumab。总的来看,罗氏的产品覆盖了CD20、CD79b、BCMA等靶点;技术上,在单抗、双抗、ADC和CAR-T均有涉猎。年初的1月,国家药监局官批准其ADC药物维泊妥珠单抗用于治疗高发弥漫性大B细胞淋巴瘤,更是突破了20年前由罗氏建立的弥漫性大B细胞淋巴瘤一线标准疗法R-CHOP(其核心药物为罗氏原研的利妥昔单抗)。日前,在“罗氏血液学术周”活动上,来自罗氏中国药品开发、转化医院和医学部门的负责人分享了罗氏在血液肿瘤与罕见血液病药物的研发战略、临床管线、靶点布局和运营实施。沈淑仪博士罗氏全球药品开发中国临床科学部负责人“罗氏中国团队努力实现全球同步研发,无论是早期项目落地中国、向中国药监部门注册申报还是开展同步国际多中心研究,中国已与世界无缝衔接。我们尝试实现在中国同步获批甚至首发。”罗氏全球药品开发中国临床科学部负责人沈淑仪博士说,罗氏中国血液部门的研发团队为总部搭建了一座桥梁,将来自中国的医疗实践和临床专家的见解融入到全球研发体系中,实现全球与中国融合。靶点丰富管线更新迭代近几年,我国肿瘤治疗取得突破性进展,在血液肿瘤领域尤为突出。以淋巴瘤为例,过往中国淋巴瘤患者5年生存率低于30%,如今,5年生存率已接近40%。不过,与欧美国家70%的5年生存率水平接近,这依然有较大差距,需要医务工作者和新药研发人员不断在诊断、治疗上,利用新技术、新疗法实现个性化治疗,实现国家在《“健康中国2030”规划纲要》中提出将我国肿瘤患者5年生存率提高15%的目标。为了提高患者的生存率,罗氏在淋巴瘤、多发性骨髓瘤及其他血液罕见病领域,正尝试以多种治疗手段,提高患者的治愈率,延长患者生命的同时提高生活质量。李滨博士罗氏制药中国医学与个体化医疗部副总裁罗氏制药中国医学与个体化医疗部副总裁李滨博士介绍了罗氏的血液疾病产品规划和具体靶点。如前所述,罗氏血液产品管线中的药物类型覆盖小分子、单抗、双抗、ADC和CAR-T等,靶点包括CD20、CD3、CD79b和FcRH5等。从时间长河来看,罗氏的产品管线也是随着疾病治疗手段的发展变迁不断迭代。例如,数十年前,淋巴瘤只有化疗作为主要治疗手段。当时,国人弥漫性大B细胞淋巴瘤的5年生存率为30%~40%,60%~70%的患者会复发。1997年,罗氏开发出全球首个靶向药物、靶向CD20的单克隆抗体——利妥昔单抗,奠定了该疾病近20年来的治疗基石。此后,以利妥昔单抗为基础的R-CHOP化疗方案(利妥昔单抗+环磷酰胺+阿霉素+长春新碱+泼尼松),成为国际上重要的一线标准治疗方案,将弥漫性大B细胞淋巴瘤患者的5年生存率从30%~40%提高到50%~60%。利妥昔单抗是通过调动人体巨噬细胞和补体系统,针对肿瘤细胞的CD20靶点进行免疫治疗。考虑到利妥昔单抗对人体免疫原性损害的局限性,不断求新求变的罗氏研发人员又开发了新型人源化、经糖基化改造的Ⅱ型CD20单抗奥妥珠单抗,并于2021年6月获得国家药监局的批准与化疗联合,用于初治II期伴有巨大肿块、III期或 IV期初治滤泡性淋巴瘤患者的治疗。“奥妥珠单抗的创新结构和机制可加强对肿瘤细胞的杀伤力,以实现患者无进展生存率的提升。“李滨补充道,罗氏选择靶点的策略是出于临床需求的考虑,并不断迭代,实现疗效上的突破。在双抗领域,李滨介绍,很值得一提的是罗氏靶向CD20和CD3的双抗mosunetuzumab和glofitamab(格菲妥单抗)。这两款双抗各分子都包含靶向T细胞表面CD3蛋白的一个蛋白域和与B细胞表面CD20蛋白结合的两个蛋白域,“这种双重靶向的策略具有更强的特异性,可有效引导T细胞靶向杀伤肿瘤细胞。”他说。这两款双抗的不同点在于靶向CD20和CD3的比例分别是1:1(mosunetuzumab)和2:1(glofitamab)。这种结构差异使得glofitamab对于进展较快的侵袭性淋巴瘤效果更好,而monsunetuzumab的安全性也得以提高。今年6月,glofitamab在美国获批用于治疗复发或难治性弥漫性大B细胞淋巴瘤。全球临床研究数据表明,患者经glofitamab治疗后,总体缓解率(ORR)为56%,中位缓解持续时间达1.5年。该药在中国正在开展注册研究,“我们期待能尽早在中国上市。”李滨说。而最新的研究表明,mosunetuzumab治疗滤泡淋巴瘤的患者ORR达到78.9%。而在目前全球很火的 ADC领域,罗氏也没有缺席。其研发的维泊妥珠单抗,是作用于CD79b抗原靶点的ADC,靶向递送破坏微管并影响有丝分裂的微管蛋白抑制剂(Monomethy lauristatin E)至B细胞,从而杀死恶性B淋巴细胞。该药是全球首个针对CD79b的 ADC,也是弥漫性大B细胞淋巴瘤针对该靶点的首个 ADC药物,实现了该领域20年的治疗突破。根据罗氏的财报,维泊妥珠单抗2023年第一季度全球销售额为3.53亿瑞士法郎,大幅增长114%。今年1月,该药在中国获批了两项适应症,分别是既往未经过治疗的弥漫性大B细胞淋巴瘤成人患者,以及用于不适合接受造血干细胞移植的复发或难治性弥漫性大B细胞淋巴瘤成人患者。在适应症选择上,除了淋巴瘤,罗氏也在骨髓瘤新药领域积极进军。例如,罗氏针对骨髓瘤独特的靶点FcRH5,开发了双抗cevostamab。这是罗氏首创的FcRH5xCD3 T细胞结合双特异性抗体。现有的临床数据表明,在多发性骨髓瘤的新药研究中,高剂量组的ORR为56.7%。“这一全新机制,为多发性骨髓瘤患者带来更多的选择和更好的临床效果。”李滨说。此外,罗氏还关注其他非恶性血液病药物研发,如针对阵发性睡眠性血红蛋白尿罕见疾病开发的C5补体抑制剂crovalimab。“罗氏希望整体产品规划能不断挑战临床金标准,为患者带来更好的临床疗效和长期获益。”沈淑仪说。试验设计以患者为中心在CDE此前出台的《以临床价值为导向的抗肿瘤药物临床研发指导原则》,对于对照药的选择提出了更高的要求。这主要基于当今药物研发飞速发展,有时试验开展到一半,标准治疗已发生改变,或同领域已有新药上市。过去,临床试验设计的开发策略往往是从末线往前线药物开发,但沈淑仪说,如今临床用药的理念已发生改变。如果从一线开始,患者的初始治愈率会更高,当然这种变化也为罗氏在中国的研发带来了更高挑战。“我们意识到中国的标准治疗与全球标准存在差异,需要跟CDE、中国的研究者、临床专家、患者组织与合作,努力满足中国患者需求。”沈淑仪说。随着CDE一系列”以患者为中心”技术指导原则出台,罗氏从试验设计到实施,也以此理念贯穿全过程。在设计时,罗氏考虑患者参加试验的便利性,开发出门诊治疗方案,患者无需每次住院,尽量不给他们增加负担,由此提高患者依从性和研究数据质量。例如,罗氏后续将开发mosunetuzumab皮下制剂,便于惰性淋巴瘤患者长期疾病管理。“患者能在社区医院进行皮下注射,而不需要到大医院住院治疗。”转化医学实现精准治疗血液肿瘤的高度异质性和治疗的复杂性,使得转化医学在血液肿瘤创新药物的研发和应用上十分重要。在罗氏,转化医学部门通过创新、严谨和“无边界”的数据、方法和工具,加速新药研发,令治疗策略更具革新性,最终让患者获益。张景宇博士罗氏制药中国转化医学部门负责人罗氏全球的转化医学科学家每天都在做什么?罗氏制药中国转化医学部门负责人张景宇博士告诉我们:首先,“血液肿瘤种类繁多,其发病机制、治疗方案、耐药机制各有千秋。” 张景宇说,转化医学有助于研发人员对疾病深入了解。因此,转化医学科学家们要通过NGS二代测序蛋白组检测,帮助医学人员对疾病分型进行深入了解。此外,罗氏关注不同分型患者人群的治疗方式、愈后及耐药机制的研究。对于耐药问题,需要转化医学科学家们与基础研究、临床研究部门紧密结合,深入研究和理解患者耐药机制的原因。第三,转化医学科学家们关注生物标志物对全病程诊疗的影响,因为生物标志物对肿瘤患者分型和预后非常重要。目前实体瘤里生物标志物运用较多,而在血液疾病领域,全病程的生物标志物研究也十分关键。“不断加深对疾病和生物学的理解,是罗氏转化医学部门的工作关键。”张景宇说,罗氏转化医学团队紧密与医生合作,掌握更多真实世界中的临床数据,患者疗效及耐药情况,让实验室的科学家利用这些数据、生物标志物和检测手段,更好重新寻找药物靶点。内外部合作创新共赢罗氏在血液领域捷报频传,陆续推出了first in class的创新产品。罗氏是如何做到不断革新?沈淑仪认为源自于以下三点:第一是内部创新与外部合作的成果。各种新型医疗技术,如细胞治疗、基因治疗、基因检测、AI不断涌现,因此,罗氏需要寻求更多对外合作,包括与本土创新公司联合。第二,努力加快药物研发速度,缩短创新药在国内外上市的时间差,甚至推出“中国首发”“中国首创”药物,争取让中国尽早参与早期全球研发。沈淑仪说,国内临床专家与医院都有很强的科研创新能力,建立了1期病房,临床专家也愿意运用庞大的患者资源开展更早期的创新产品研究。第三,坚持通过生物标志物、数字化临床试验探索新的解决方案。针对中国发病率相对高的疾病、与中国监管机构、临床专家、病患组织紧密合作。“唯有创新,方能致远。”沈淑仪如是总结罗氏在血液健康道路的未来之路。编辑 | 姚嘉yao.jia@PharmaDJ.com总第1947期访问研发客网站可浏览更多文章www.PharmaDJ.com
抗体药物偶联物免疫疗法细胞疗法
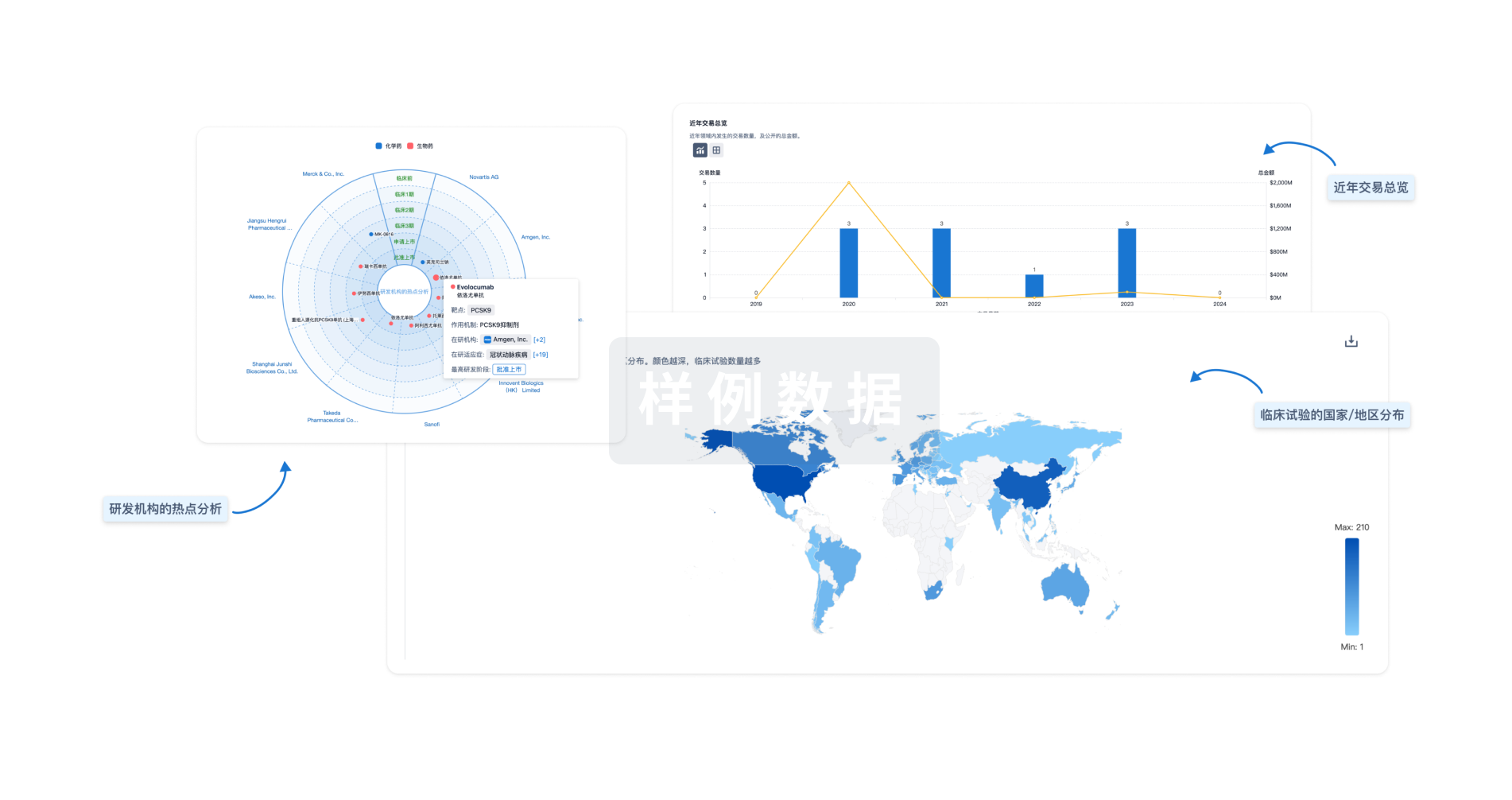
分析
对领域进行一次全面的分析。
登录
或
生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用
