预约演示
更新于:2025-05-07
FOLR1 x TRPV6 x Tubulin
更新于:2025-05-07
关联
1
项与 FOLR1 x TRPV6 x Tubulin 相关的药物作用机制 FOLR1激动剂 [+3] |
在研机构 |
原研机构 |
非在研适应症- |
最高研发阶段临床2/3期 |
首次获批国家/地区- |
首次获批日期1800-01-20 |
4
项与 FOLR1 x TRPV6 x Tubulin 相关的临床试验CTR20222941
评价注射用CBP-1008在叶酸受体α(FRα)阳性的铂耐药晚期上皮性卵巢癌、原发性腹膜癌和输卵管癌患者中的疗效和安全性的开放标签、多中心Ⅱ期单臂研究
根据实体瘤疗效评价标准1.1版(RECIST V1.1)评估的客观缓解率(ORR)评价注射用CBP-1008单药治疗FRα阳性的铂耐药晚期上皮性卵巢癌、原发性腹膜癌和输卵管癌患者的疗效。
开始日期2023-02-15 |
申办/合作机构 |
CTR20212205
多中心、开放、评价注射用 CBP-1008 周疗方案在 FOLR1 和/或 TRPV6 表达阳性的晚期恶性实体瘤患者中安全性、耐受性和药代动力学特征以及在选定适应症中扩展的 Ia、Ib 期研究
主要目的:
1. 评估DLT并确定MTD;
2. 确定RP2D;
3. 评估CBP-1008的安全性、耐受性和免疫原性。
次要目的:
1. 评估CBP-1008在晚期恶性实体瘤患者中的抗肿瘤活性;
2. 确定单次剂量下和多次剂量下CBP-1008及其主要代谢产物的PK特征。
探索性目的:
1. 识别CBP-1008疗效的潜在预测性生物标志物。
开始日期2021-09-01 |
申办/合作机构 |
NCT04740398
A Phase Ia/Ib, Open-Label, Multi-center, First in Human and Expansion Study to Assess the Safety, Tolerance, and Pharmacokinetics of the Novel Antitumor Agent CBP-1008 in Patients With Advanced Solid Tumors
The primary objective of this phase I study is to evaluate the safety and potential efficacy and to determine the recommended phase 2 dose (RP2D) of CBP-1008, a bi-specific ligand conjugated drugs in patients with advanced solid tumors.
开始日期2019-03-06 |
申办/合作机构 |
100 项与 FOLR1 x TRPV6 x Tubulin 相关的临床结果
登录后查看更多信息
100 项与 FOLR1 x TRPV6 x Tubulin 相关的转化医学
登录后查看更多信息
0 项与 FOLR1 x TRPV6 x Tubulin 相关的专利(医药)
登录后查看更多信息
4
项与 FOLR1 x TRPV6 x Tubulin 相关的新闻(医药)2025-03-01
·药时代
引言
小分子偶联药物(SMDC)是一种新型靶向治疗药物,始于对传统化疗及抗体偶联药物(ADC)的优化探索,旨在通过精准递送提高疗效并降低系统毒性,在靶向性、安全性与成本等方面具备优势。
目前全球尚无SMDC获批上市,约10款候选药物处于临床阶段,适应症集中于实体瘤,为耐药性肿瘤提供新策略,并有望拓展至其他疾病领域。
SMDC结合小分子药物的灵活性与偶联技术的增效潜力,推动肿瘤治疗向高效低毒方向演进,成为偶联药物赛道中具潜力的分支。
SMDC的作用机制
小分子偶联药物(SMDC)由三部分组成:小分子靶向配体、连接子和载荷药物。
其作用机制与ADC药物基本一致,是通过小分子配体特异性识别肿瘤细胞表面过表达的受体或转运蛋白,经内吞作用将细胞毒性药物递送至靶细胞内,实现精准杀伤[1]。
图:SMDC药物结构
来源:公开资料,药智咨询整理
小分子靶向配体
SMDC的靶向配体为小分子化合物,在SMDC中发挥的作用类似ADC抗体的作用。SMDC配体的选择需要考虑到结合亲和力、选择性和化合物大小等问题,因此主要来自天然来源配体的衍生物,如叶酸、前列腺特异性膜抗原(PSMA)抑制剂或整合素拮抗剂等,相比ADC配体选择面较小,是目前SMDC发展的主要限制。
目前靶向叶酸受体的SMDC药物研究最多,叶酸受体在多种实体瘤(如卵巢癌、肺癌)中高表达,以叶酸为配体的SMDC可通过受体介导的内吞作用高效富集于肿瘤组织。
连接子
SMDC的连接子与ADC类似,是连接小分子靶向配体与载荷药物的纽带,其设计决定SMDC的稳定性和药物释放效率。目前在研的SMDC药物主要采用酶敏感型连接子和基于二硫键的连接子两种技术路线。
载荷药物
目前在研的SMDC的载荷药物以细胞毒性化疗药物为主,如喜树碱衍生物(SN-38)、微管抑制剂(MMAE)及拓扑异构酶抑制剂等。此外,部分研究尝试将放射性核素(如锕-225)或免疫调节剂作为载荷,以扩展其治疗范围。
SMDC的临床优势
首先,SMDC的临床优势主要基于其小分子特性。
小分子靶向配体使SMDC容易渗透并能更均匀地扩散到肿瘤组织内部,使其有更高的肿瘤穿透性;并且小分子不会在肿瘤及其他正常细胞中聚集,少数脱靶的药物也会被快速排出体外,从而减少对正常细胞的毒性;同时SMDC理论上不会具有免疫原性,安全性控制更容易实现。
此外,相较于抗体药物,SMDC容易控制合成工艺和成本,工业化操作简单。
更高的肿瘤穿透性
相比ADC(分子量约150kDa)和PDC(分子量约5-10kDa),SMDC的分子量通常低于1kDa,能够通过被动扩散快速穿透实体瘤组织,克服传统大分子药物的递送瓶颈,在实体瘤中能够具有更好的细胞通透性。
肾脏代谢与低免疫原性
SMDC主要通过肾脏代谢,半衰期较短,减少了药物在肝脏和骨髓中的蓄积,少数脱靶的药物也会被快速排出体外,减少对正常细胞的毒性,具有更好的体外和体内稳定性。
例如叶酸受体SMDC 长春夫利 Vintafolide在临床试验中表现出较低的肝毒性[2]。同时,SMDC理论上不具有免疫原性,使其安全性控制更容易实现。
更低的生产成本
小分子的化学合成工艺成熟,生产成本显著低于抗体或多肽,更易于规模化生产,成本控制更容易。
精准的有效载荷
ADC药物分子的有效载荷与抗体之比通常不能确定,因此细胞内有效载荷也会出现上下浮动;SMDC的小分子靶向配体和有效载荷通常有准确比例。
SMDC全球及中国在研管线分析
相比ADC赛道的火热以及PDC、RDC在技术和市场上陆续取得的突破,SMDC的研发尚未能取得令人眼前一亮的成绩。
目前国内外尚未有SMDC获批准上市,但约十余款药物进入临床研究阶段,其中进入临床II期研究的约有7款,整体处于临床研发早期。相比其他新型偶联药物来看,RDC已有11款药物获批上市,其中Lutathera在2023年销售额达到6.05亿美元,270余款RDC新药处于临床试验及申请上市阶段;PDC已有两款药物获批,全球进入临床试验阶段的管线约有20条,多条管线进入临床后期。
目前SMDC在研管线中的靶点多样性也较低,主要集中在AKR1C3、 KRAS G12D、Tubulin等几个靶点。
表 全球在研SMDC药物(部分)
药品名称
靶点
适应症
最新状态
研发单位
长春夫利 Vintafolide
FOLR,Tubulin
三阴性乳腺癌,非小细胞肺癌,子宫内膜癌,卵巢癌,实体瘤,肺腺癌
注册申请
(2014年终止)
Endocyte Inc
长春夫利 Vintafolide
FOLR,Tubulin
三阴性乳腺癌,非小细胞肺癌,子宫内膜癌,卵巢癌,实体瘤,肺腺癌
注册申请
(2014年终止)
Endocyte Inc
NUV-1511
DDC
实体瘤
临床Ⅱ期
(2024-02-12)
Nuvation Bio
CBP-1019
Topo
实体瘤
临床Ⅱ期
(2023-03-29)
同宜医药
AST-001
KRAS
实体瘤,胰腺癌
临床Ⅱ期
(2022-04-29)
艾欣达伟
AST-3424
AKR1C3
实体瘤;急性淋巴细胞白血病;癌症;肝细胞癌
临床Ⅱ期
(2019-07-15)
艾欣达伟
ELU001
FOLR1 x Top I
肿瘤
临床Ⅱ期
(2021-07-14)
Elucida Oncology Inc
OBI-3424
AKR1C3,DNA
T细胞急性淋巴细胞白血病;
临床Ⅱ期
(2018-05-21)
Molecular Templates
PEN-866
HSP90;Topo I
实体瘤
临床Ⅱ期
(2017-07-13)
Madrigal Pharmaceuticals
Tarveda Therapeutics
VIP236
Integrin αVβ3
癌症
临床Ⅰ期
(2022-10-18)
Vincerx Pharma
拜耳制药
Legutaxel
Tubulin
实体瘤;胃癌
临床Ⅰ期
(2022-08-10)
亲合力生物
T-1201
PS;Topo I
实体瘤
临床Ⅰ期
(2021-04-23)
泰纬生命
PSMA-targeted tubulysin B conjugates
FOLH;Tubulin
前列腺癌
临床Ⅰ期
(2014-07-21)
Endocyte Inc
AST-006
-
乳腺癌;卵巢癌
临床Ⅰ期
艾欣达伟
来源:药智数据,药智咨询整理
海外布局企业中,虽布局企业相对较少,但几款领域内具有代表意义的产品也值得一讲:
Vintafolide(Endocyte):作为全球临床阶段最靠前产品,早在2014年就进入注册申请阶段,并于2014年获欧洲药品管理局的有条件批准,但最终却因未达到主要终点无进展生存期而宣告失败,Endocyte之后也彻底放弃SMDC领域,转向其他种类偶联药物的研究,大名鼎鼎的Lutathera就是转战成果,2024年全球销售额达7.24亿美元。
国内布局企业方面,布局SMDC领域的企业相对海外,则相对更多,竞争也更大,比较有代表意义的有艾欣达伟、同宜医药等。
艾欣达伟专注于SMDC创新药研发,目前已有2条SMDC药物管线进入II期临床研究,其中AST-001作为其重点管线,在一项Ⅰ期实体肿瘤的临床研究中,广泛入组的10余类不同瘤种的晚期实体瘤患者,符合靶点要求的患者中疾病控制率达到66.7%,ORR为33.3%。充分展现出AST-001广谱抗肿瘤的特性。安全性方面,大部分治疗相关的不良事件(TRAE)为1-2级,均可控可管理。AST-3424是全球首创的依赖AKR1C3酶活化的SMDC,其II期临床试验结果显示作为后线药物,AST-3424用于治疗晚期肝细胞癌具有较好的有效性,特别是用于曾经接受免疫治疗后进展的HCC受试者,仍然可以延长其生存期。
同宜医药同样也拥有多款SMDC药物在研,其中CBP-1008与CBP-1019最被寄予厚望,其中CBP-1019在一项全球多中心、开放标签的I/II期临床试验中,入组的10名晚期/转移性EC患者,研究结果显示,在3.0 mg/kg剂量水平,9名晚期/转移性EC患者中有7名有给药后至少一次肿瘤评估,客观缓解率(ORR)达42.9%,疾病控制率(DCR)为100%。
CBP-1008是一款靶向叶酸受体α(FRα)/瞬时受体电位阳离子通道6 蛋白(TRPV6)的全球双配体SMDC,其在晚期实体瘤患者开展的I期试验包括铂耐药性高级别浆液性卵巢癌 (HGSOC)、透明细胞卵巢癌 (OCCC)、转移性三阴性乳腺癌 (TNBC) 和其他实体肿瘤患者。2024年10月被FDA授予快速通道资格。
数据来源:公开数据整理(点击查看大图)
而针对上述SMDC系列管线的临床有效性数据而言,除了SMDC领域之内的数据观测外,其实针对SMDC与化疗、小分子靶向抑制剂与ADC等其他技术领域的对比反而更显重要。
目前来看,由于SMDC的临床阶段尚处于前期,很多数据还不具备统计意义,但就整体而言,部分产品目前所展示的ORR、DCR数据并不逊色于ADC或新一代PARP抑制剂,甚至因其生产成本、肿瘤穿透性等特点,想象空间反而更大。
SMDC的发展前景
SMDC药物的研发目前处于早期探索阶段,小分子配体的选择是目前SMDC开发中主要难点。
SMDC配体主要来自天然来源配体的衍生物,相比ADC配体选择面较小,合适的受体和配体难以获得,靶点和适应症都比较狭窄。因此,优化现有设计、拓展小分子配体的选择范围,并扩大靶点及适应症的覆盖领域,是SMDC突破发展瓶颈的关键策略。
小结
SMDC凭借其小分子特性,在肿瘤穿透性、生产成本和安全性方面展现显著优势,已成为偶联药物领域的重要分支。
目前SMDC临床研发面临小分子靶向配体选择面窄的限制,药物研发整体还处于早期探索阶段,相比其他种类的偶联药物研发进程滞后,国内企业已有数条SMDC管线进入II期临床研究,具有成为SMDC领域FIC的潜力。
未来可能有更多公司参与SMDC的研发,不断改善现有产品的技术瓶颈,使SMDC有望为实体瘤和难治性癌症提供更精准的治疗方案。
参考文献
1.Zhang J, Hu F, Aras O, Chai Y, An F. Small Molecule-Drug Conjugates: Opportunities for the Development of Targeted Anticancer Drugs. ChemMedChem. 2024 Jun 3;19(11):e202300720. doi: 10.1002/cmdc.202300720. Epub 2024 Mar 11. PMID: 38396351.
2.Vergote, I., & Leamon, C. P. (2015). Vintafolide: a novel targeted therapy for the treatment of folate receptor expressing tumors. Therapeutic advances in medical oncology, 7(4), 206–218.
3.评价AST-001治疗恶性肿瘤患者的安全性、耐受性、药代动力学、初步疗效以及疗效与AKR1C3表达相关性的临床研究
封面图来源:123rf
查处"政治遗产"?疫苗药企迎来“至暗时刻”!
2025-02-28
一代传奇K药:大劫降至
2025-02-27
不止有DeepSeek,中国生物制药正在崛起!
2025-02-26
版权声明/免责声明
本文为授权转载文章。
本文仅作信息交流之目的,不提供任何商用、医用、投资用建议。
文中图片、视频、字体、音乐等素材或为药时代购买的授权正版作品,或来自微信公共图片库,或取自公司官网/网络,部分素材根据CC0协议使用,版权归拥有者,药时代尽力注明来源。
如有任何问题,请与我们联系。
衷心感谢!
药时代官方网站:www.drugtimes.cn
联系方式:
电话:13651980212
微信:27674131
邮箱:contact@drugtimes.cn
点击,查看更多精彩!
抗体药物偶联物多肽偶联药物免疫疗法
2024-10-11
欢迎关注凯莱英药闻
2024年10月10日,同宜医药宣布,美国食品药品监督管理局(FDA)正式授予CBP-1008快速通道认定(FTD)资格,用于治疗铂耐药卵巢透明细胞癌(OCCC)。
CBP-1008是一款靶向叶酸受体α(FRα)/瞬时受体电位阳离子通道6 蛋白(TRPV6)的全球首款双配体偶联药物,属于小分子偶联药物;此次FTD的认定,不仅是对同宜医药研发实力和试验数据的认可,更为全球OCCC患者带来了新的希望。
关于CBP-1008
CBP-1008基于同宜医药独家Bi-XDC技术平台开发;由优化过的特异靶向FRα/ TRPV6的双配体连接子系统、可酶裂解的三功能连接子,以及作为载药的细胞毒素MMAE三部分组成,能够同时靶向两种在癌症中过表达的受体,拟开发治疗乳腺癌、卵巢癌。
2024年9月,公司在2024 ESMO大会上公布了该药物首次在晚期实体瘤患者开展的I期试验,包括铂耐药性高级别浆液性卵巢癌 (HGSOC)、透明细胞卵巢癌 (OCCC)、转移性三阴性乳腺癌 (TNBC) 和其他实体肿瘤患者。主要目的是评估药物的安全性和有效性。
研究显示,在 16 名 OCCC 患者中,ORR达31.3%,中位缓解持续时间(mDOR)为7.2个月,显著优于OCCC的历史数据(ORR<8%)。在 31 名接受过 1-2 线含紫杉烷治疗的 HGSOC 患者中,客观缓解率 (ORR) 为 48.4% (15 PR),疾病控制率为 83.9%,无论 FRα/TRPV6 表达水平如何。
关于FRα/TRPV6药物与卵巢癌
FRα由FOLR1编码,其除了运送叶酸外还参与调控肿瘤细胞的增殖和转移。叶酸是维持细胞生长和代谢所必需的重要营养物质,它在DNA和RNA的合成中起着关键作用。在某些快速增殖的癌细胞中,其对叶酸的需求更高(如乳腺癌、卵巢癌、肺癌等),叶酸受体α表达水平明显增加。据统计,FRα在实体瘤中有广泛高表达,比如间皮瘤(72-100%),三阴性乳腺癌(35-68%),卵巢癌(76-89%),非小细胞肺癌(14-74%);而在正常组织中表达率很低或仅在特定局限区域表达。
近年来,FRα相关交易频发:2023年11月,艾伯维与ImmunoGen宣布达成最终协议,以总额达约101亿美元收购ImmunoGen,获得其可治疗卵巢癌的、全球首款FRα抗体偶联药物(ADC)Elahere;Elahere曾于2022年11月获美国FDA加速批准上市,作为单药疗法治疗FRα高表达、对含铂疗法耐药的经治晚期卵巢癌患者。无独有偶,今年4月,Genmab和ProfoundBio(普方生物)共同宣布签署了一项确定性协议,Genmab将以18亿美元现金交易收购ProfoundBio;此次收购将使Genmab在全球范围内拥有三个临床开发候选药物的权利,包括rinatabart sesutecan(Rina-S)。Rina-S是一种新一代的、潜在同类最佳的FRα ADC,正在开发用于治疗卵巢癌和其他实体瘤。
TRPV6主要表达于肠道、胎盘和前列腺等组织,参与钙离子的吸收和转运。值得注意的是,TRPV6在卵巢癌、前列腺癌和胰腺癌中的表达量远高于正常组织;活检表明,乳腺癌TRPV6 mRNA表达量比正常乳腺组织高2~15 倍,且在雌激素受体阴性的乳腺癌患者中TRPV6表达量增高与预后不良相关。近年来研究也表明,TRPV6的上调与多种肿瘤的侵袭性增加有关。
据统计,卵巢癌(OC)是严重威胁女性生命的妇科恶性肿瘤,其晚期五年生存率不足30%,而OCCC约占上皮性卵巢癌的10%,其发病机制独特且预后更差。目前,OCCC患者在复发后的生存率显著低于浆液性卵巢癌患者,且缺乏针对性的获批治疗方案,这使得OCCC患者在治疗上面临巨大挑战,存在巨大未被满足的医疗需求。
根据GLOBOCAN 2020数据,2020年全球乳腺癌新发病例226万例,系全球新发病例最多的瘤种。根据国家癌症中心2022年发布的文献,2016年中国乳腺癌新发病例30.6万例,系我国第五大瘤种。陈万青等根据国家癌症中心的数据预测2022年中国乳腺癌新发病例约42.9万例。
根据弗若斯特沙利文,2021年全球乳腺癌药物市场规模345亿美元,2015-2021年复合增速为10.1%。
2021年中国乳腺癌市场规模563亿元,2017-2021年间复合增长率为13%。
关于小分子偶联药物
小分子偶联药物(SMDC)是由小分子的靶向配体与细胞毒药物偶联所得,由三部分构成:小分子靶向配体、细胞毒分子和连接子,其作用机制与ADC 类似。但与ADC相比,SMDC能更快速均匀地分散到肿瘤组织中,且成本低、无免疫原性。
在受体的选择上,SMDC可利用的受体数取决于受体的循环率和再生率,因此药物给药量要考虑到受体的循环率和再生率,避免引起毒性。目前可利用的靶标较少,比较常用的是叶酸受体、前列腺特异性膜抗原、生长抑素受体以及碳酸酐酶Ⅸ ,也有其他受体如磷脂丝氨酸。
在小分子配体的选择上,大小需合适,避免SMDC太大而影响药物在肿瘤部位的积聚速率和含量。与体积较大的ADC 相比,未与受体结合的SMDC 更能快速地从体内排泄,避免长时间血液循环导致细胞毒药物释放引起的不良反应。然而,小分子配体一直较难获得,目前,应用前景较好的是靶向叶酸受体的叶酸衍生物、靶向前列腺特异性膜抗原的谷氨酸脲衍生物、靶向生长抑素受体的生长抑素类似物、靶向碳酸酐酶Ⅸ的芳香磺酰胺类。
在细胞毒的选择上,与ADC的要求是基本一致的,所用细胞毒分子也是基本相同,如美登素、卡奇霉素等。
在连接子的选择上,与ADC也基本一致。但SMDC所用的连接基一般是可断裂的,由于SMDC 能够在几分钟至1 h 内快速地与受体结合及被肾脏清除,因此SMDC 对连接基的稳定性要求与需要在血液中循环较长时间的ADC 相比较低,一般只要求能保持几分钟至1 h 的稳定性。
据不完全统计,目前在研的SMDC约60余种;将目前处于临床以上阶段的药物统计如下:
关于同宜医药
同宜医药是一家领先的双靶向配体偶联药物Bi-XDC创新药企 ,成立于2016年,致力于双靶向XDC药物的研发及产业化。据资料显示,同宜目前共有三个平台,包括BEST™技术平台,C-PROTAC技术平台和慢性病技术平台。
双靶向XDC技术具有以细胞/组织特异性主动传递任何生物活性分子的能力,有望克服多种高生物活性分子的难治性障碍,从而实现"难以药物化"的目标。
公司不仅专注于全球高发癌症,还积极将适应症扩展到其他器官的药物传递和慢性病领域。除CBP-1008外,公司还在重点开发新一代FRα/TRPV6双配体偶联药物CBP-1019,保留、优化了双配体部分,并对链接子进行改造,使其具有更好的稳定性和更高的安全性。核心资产CBP-1008在260例从低到高不同叶酸表达水平的患者中显示出了良好的疗效和安全性。
除此以外,公司还在同步进行多个管线的早期研发,其中包括PROTAC Bi-XDC和放射性配体Bi-XDC等。
参考资料
1、Altmann K H. Tumor Targeting with Small Molecule-Drug Conjugates (SMDCs)–Can They be Better than ADCs? Medicinal Chemistry and Chemical Biology Highlights[J]. Chimia, 2018, 72(3): 154-154.
2、郭立红, 王金朋, 翟立海,等. 抗体偶联药物和小分子偶联药物的研究进展[J]. 中国医药工业杂志, 2019, 50(8):10.
3、公司官网
4、国联证券、西南证券、德邦证券
感谢关注、转发,转载授权、加行业交流群,请加管理员微信号“hxsjjf1618”。
“在看”点一下
快速通道抗体药物偶联物临床1期临床2期
2023-12-13
01 引言2023年12月12日,百利天恒子公司SystImmune和百时美施贵宝就BL-B01D1达成独家许可与合作协议。后者支付8亿美元预付款,5亿美元近期或有付款,以及71亿美元里程碑金额,总潜在价值高达84亿美元。BL-B01D1是一款潜在的同类首创双特异性EGFRxHER3 ADC,具有治疗肺癌和乳腺癌患者的潜力,并有机会扩展到其他肿瘤类型。目前正在一项全球多中心1期研究(BL-B01D1-LUNG101)中评估其在转移性或不可切除非小细胞肺癌(NSCLC)患者中的安全性和有效性。图注:BMS官方公告 图注:百利天恒官方公告来源:SystImmune官网附表:近年来全球ADC交易统计(汇总,医药笔记)02 临床阶段的双抗ADC汇总相较于单抗,双抗ADC是一个更崭新的概念。一方面,双抗可更加特异性地靶向肿瘤细胞,克服耐药性,并减少副作用。另一方面,通过交联作用促进两个靶点的协同内吞,可以提高毒素进入肿瘤细胞效率,进一步通过减少受体蛋白在细胞膜上的表达量来抑制肿瘤细胞生长信号,达到更好的治疗效果。图注:双抗ADC的作用机制但因该方向的研究尚处发展阶段,故临床的在研产品不多。原因有三:☉ 能够用于双抗构建的抗体骨架分子较少,且靶点非常集中,仅在HER2、HER3、EGFR、MUC1等几个靶点上有较好的可选抗体分子。☉ 目前的双抗大都是通过活性筛选获得的,而其内吞功能不一定满足ADC研发的需求。☉ 从生产工艺来看,双抗生产自身存在效率低下的问题,在此基础上进行偶联反应,进一步增加了生产工艺的难度和挑战。目前没有上市的双抗ADC,整体来看,进度最快的也在二期临床试验。图注:临床阶段的双抗ADC(共8款)1 Zymeworks:ZW-49公认的双抗ADC领头羊Zymeworks 公司有一款双抗Zanidatamab(ZW25)已经进入三期临床,表现优异,公司在ZW25的基础上布局了双抗ADC-Zanidatamab Zovodotin(ZW49)。ZW-49的母体单抗是两款已上市的抗体,分别为trastuzumab(曲妥珠)和pertuzumab(帕妥珠),两个母单抗分别识别HER2受体的两个非重叠表位--ECD4和ECD2,通过二硫键偶联一种新颖的微管抑制剂。图注:ZW49的结构设计在临床前PDX模型中,ZW49表现出对HER2低表达和高表达均表现出有效的杀伤效果,在非人灵长类的动物中的耐受剂量为18mg/kg。在小鼠肿瘤模型中,ZW49表现出比T-DM1和DS-8201更强的抗肿瘤活性,更长的生存期。图注:ZW49在非人灵长类的动物中的耐受剂量为18mg/kg图注:在小鼠肿瘤模型中,ZW49表现出比T-DM1和DS-8201更强的抗肿瘤活性图注:在小鼠肿瘤模型中,ZW49比 T-DM1和DS-8201具有更长的半衰期2018年,百济神州与Zymeworks就ZW49及ZW25的临床开发和商业化达成了战略合作。目前正在评估ZW49在HER2实体癌患者中的安全性和有效性(NCT03821233)。但略有失望的是,2021年1月,Zymeworks公布了ZW49的I期临床的部分数据。结果显示,ZW-49在所有治疗方案和剂量水平上均显示出一定的抗肿瘤活性。客观缓解率ORR为31%,临床获益率为38%。但与临床前实验相比,临床数据不达预期,导致股价发生暴跌。这无疑给双抗ADC药物在研企业带来压力。幸运的是,该Ⅰ期临床数据中安全性很好,所以目前Zymeworks正在积极对ZW49进行改进,希望再次上临床。图注:ZW49临床获益率效果不佳图注:ZW49安全性好,三级及三级以上不良事件10%~20%左右2 阿斯利康:MEDI4276I期临床因毒性终止开发MEDI4276为双表位四价HER2 ADC药物(母单抗与ZW49相同)。DAR为4,linker为MC-VC,毒素为微管抑制剂。图注:MEDI4276的结构设计在Ⅰ期临床中,MEDI4276确实改善了对曲妥珠单抗、帕妥珠单抗和TDM1治疗耐受的患者,展现了一定疗效。但毒性问题造成整个项目的夭折。乳腺癌患者中:0.05-0.4mg/kg队列:PFS为1.3至2.0个月; OS为19.1个月(效果差) 0.5至0.75mg / kg队列:PFS范围为4.6至15.4个月, OS数据不成熟;22例患者中有4例报告死亡(毒性大)胃癌患者中:中位PFS范围为1.3至6.0个月,没有明确的剂量反应关系。中位OS为6.5个月(效果差)图注:MEDI4276在乳腺癌和胃癌患者中的临床数据在整个ADC领域,毒性问题主要的引发点,多数来源于linker/payload,而MEDI4276却出现了一定程度的靶向毒性,引起DLT(剂量限制性毒性)。所以,双表位ADC在解决抗原低表达药物无响应问题的同时,其毒性问题,是非常值得思考的。ZW49做了一定的改进,目前,只展现了初步的临床疗效,并不惊艳,但尚未出现MEDI4276相关的严重的毒性问题,仍可以继续改进,其后续结果仍值得期待。3 康宁杰瑞:JSKN003临床前疗效和ENHERTU(DS-8201a )相当,临床结果未公布JSKN003是由康宁杰瑞开发的双抗ADC(母单抗与ZW49相同),也是基于该公司的双抗-KN026延伸的分支, JSKN003正在澳大利亚进行首次Ⅰ期试验,以评估在晚期或转移性实体恶性肿瘤患者中的安全性及耐受性。2022年8月16日,JSKN003治疗晚期实体瘤的Ⅰ期临床研究申请已获得中国国家药品监督管理局批准。图注:JSKN003的结构设计与作用机制该双抗ADC是在KN026基础上的改造和设计,其和ZW-49类似,都是靶向HER2的两个不同表位(ECD4/trastuzumab和ECD2/pertuzumab)。JSKN003利用特有的糖定点偶联平台自主研发:将抗体分子KN026重链糖基经过点击化学反应获得,DAR值约为4,无论在HER2低表达的BxPC-3动物模型中还是在HER2高表达的N87 CDX模型中,其疗效和第一三共的ENHERTU(DS-8201a )相当。另外,在稳定性方面,JSKN003在血清中展现了良好的稳定性,因此理论上可能会有更好的安全性。除了开发双抗ADC药物外,康宁杰瑞目前也在布局双抗偶联调节剂相关药物。图注:JSKN003在临床前显示出很好的抑瘤效果4 Sutro+默克:M1231“非天然氨基酸、体外蛋白合成系统” 助力M1231光明前景M1231是靶向MUCI/EGFR的双抗ADC。2021年该药已经进入临床。靶向MUCI的抗体部分为scFv,而靶向EGFR的抗体部分为Fab形式,DAR值约为4,通过可裂解的Val-Cit连接子链接微管抑制剂。默克选择MUCI/EGFR作为靶标,是因为MUCI/EGFR共表达在多种肿瘤细胞中,非小细胞肺癌(NSCLC)、食管鳞状细胞癌(ESCC)、头颈部鳞状细胞癌、三阴性乳腺癌和卵巢癌等多种癌症适应症,在正常组织中非常低,因此理论上可以降低On-target毒性,提高用药窗口。在临床前的PDX动物模型中,8mg/kg单剂量治疗小鼠可以在一定程度上抑制肿瘤的生长甚至清除肿瘤。图注:MUCI/EGFR共表达在多种肿瘤细胞中图注:8mg/kg单剂量治疗小鼠疗效目前M1231的临床数据未公布,但是我们可以解读一下其表达生产系统,该抗体的表达采用Sutro的无细胞体系XpressCF,并且在生产过程中定点插入非天然氨基酸,利于后续双特异抗体的定点偶联。图注:利用体外蛋白合成系统将非天然氨基酸引入蛋白的专利(CN102348807)5 Regenron:REGN5093-M114靶向MET两个不同表位REGN5093- M114是是由Regenron开发的靶向MET两个不同表位的双抗ADC,非对称型双特异抗体,抗体与毒素M24(美登素衍生物)连接,DAR值为3.2左右。图注:REGN5093-
M114结构设计REGN5093-M114已于2021年7月在美国启动I/II期临床试验(NCT04982224),预计完成日期为2026年12月。目前再生元也将裸双抗REGN5093和双抗ADCREGN5093- M114 两种药物都推向了临床,均处于临床Ⅰ期。与其它抗体不同,REGN5093- M114裸抗本身同样具有一定的抑制肿瘤的效果,与临床上已有的MET ADC药物相比,双特异性ADC REGN5093-M114不仅可以抑制肿瘤生长,甚至可以在相同剂量下去除肿瘤细胞,因此其疗效远优于临床上的ADC。作用机制:• 可以同时结合两个MET的不同的表位,并可以有效的阻断HGF与MET的结合(细胞生长因子HGF是唯一已知的c-Met配体),从而可以防止相关通路的激活; • 抗体和MET形成的2+2型复合物可以被内化,进入肿瘤细胞并在溶酶体中被降解,从而可以减少MET通过再循环表达在细胞表面。 • REGN5093- M114中可以被酶切的linker在溶酶体中被酶切后释放M24毒素并通过作用于微管蛋白来抑制肿瘤生长。6 百利药业:BL-B01D1公认的国内首款双抗ADCBL-B01D1是由百利药业开发的靶向EGFR/HER3的双抗ADC,2022年10月19日,百利药业双抗ADC BL-B01D1的临床试验申请获得NMPA的默示许可,用于治疗晚期或转移性上皮肿瘤,国内首款双抗ADC。2023年12月12日,百利天恒子公司SystImmune和百时美施贵宝就BL-B01D1达成独家许可与合作协议,总潜在价值高达84亿美元。将喜树碱衍生物ED04(DNA)与抗体的半胱氨酸位点连接,DAR值约为7.5从其发表的专利来看,EGFR/HER3双抗的结构可能如下图所示,为完整抗体上融合scFv的2+2对称型结构(以企业披露为准)。关于BL-B01D1的其他信息官方均未披露。图注:BL-B01D1的结构设计7/8 同宜医药:CBP-1008/CBP-1018双配体偶联药物(Bi-XDC)同宜医药进展最快的双抗ADC管线是CBP-1008,靶向叶酸α受体(FRα)和钙离子通道蛋白TRPV6,其中FRα在卵巢癌、乳腺癌、肺癌等瘤种高表达,TRPV6则在乳腺癌、卵巢癌、胰腺癌等瘤种高表达。CBP-1008目前正在进行中美临床I/II期试验、中国关键注册II期临床试验。CBP-1018的两个配体分别靶向前列腺特异性膜抗原(PSMA)和叶酸受体α(FRα),分别在前列腺癌、卵巢癌等多种实体瘤中高表达。图注:CBP-1008 /
CBP-1018的研究进度同宜医药的特色平台Bi-XDC是将抗体换成了一对分子量小得多的配体组合,降低了对单个靶点的成药要求,使得Bi-XDC药物可选择的靶点也更多。此外,Bi-XDC分子量更小(仅为ADC药物的1/50),因而进入细胞更快,半衰期更短,药效和安全性也更好。作为一类新型的偶联药物,Bi-XDC在药代动力学上更像小分子,同时又达到了生物大分子精准靶向递送的目的,因此有望攻克ADC解决不了的问题。图注:三功能连接子03 双抗ADC临床前动态(部分)百奥赛图双抗ADC平台百凯医药双抗ADC依托百凯医药自主研发的三大技术平台,公司在短期内建立了丰富的均拥有全球自主知识产权及商业化权利的产品管线,包括传统ADC、双特异性抗体ADC以及双功能ADC。其中1款双靶向双抗ADC管线BIO-201处于临床前开发阶段。总结双抗ADC前景虽好,但毒性问题需要重视,阿斯利康MEDI4276 Ⅰ期临床即出局,此外,我们需要注意到,双抗也存在作用机制,并不完全盲目地看疗效,深究原理能更加把控好安全性和效果,如靶向MET表位存在阻断HGF×MET的信号通路机制。参考资料:[1]各大公司官网与公告[2]国家药品监督管理局药品审评中心[3]临床数据中心:https://clinicaltrials.gov/[4]BMS、百利天恒、医药笔记等识别微信二维码,添加生物制品圈小编,符合条件者即可加入生物制品微信群!请注明:姓名+研究方向!版权声明本公众号所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系(cbplib@163.com),我们将立即进行删除处理。所有文章仅代表作者观点,不代表本站立场。
抗体药物偶联物引进/卖出临床2期临床1期临床3期
分析
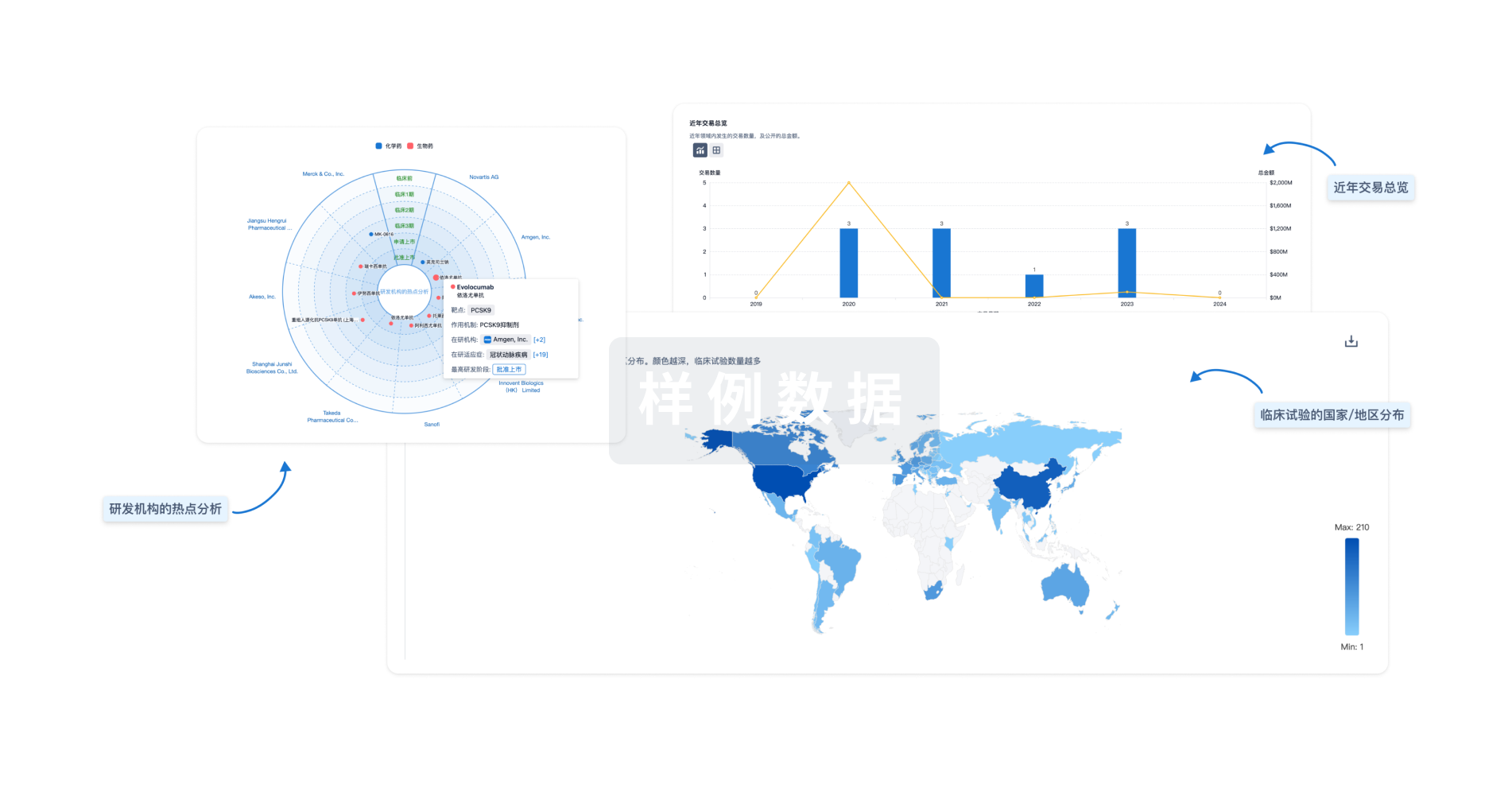
对领域进行一次全面的分析。
登录
或
生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用
