思康睿奇创新FGFR2抑制剂3HP-2827获FDA快速通道资格,针对胆管癌
2024年7月3日,思康睿奇宣布其自主研发的FGFR2抑制剂3HP-2827获得美国FDA授予快速通道资格,用于治疗含有FGFR2突变的胆管癌(CCA)患者。
3HP-2827为思康睿奇自主研发的高选择性FGFR2抑制剂,能够高特异性的抑制FGFR2磷酸化,从而抑制FGFR2信号传导通路,进而发挥抗肿瘤作用,为FGFR2异常患者特别是耐药患者带来更加高效、安全的治疗选择。成纤维细胞生长因子受体(FGFR)的基因变异存在于多种类型的人类肿瘤中,主要通过FGFR基因扩增、突变、染色体易位以及配体依赖性活化引起的FGFR信号异常。FGFR信号通过促进肿瘤细胞增殖、存活、迁移和血管生成来促进恶性肿瘤的发展。
作为国内首个针对FGFR2异常的FGFR2抑制剂,3HP-2827靶向结合并抑制FGFR2磷酸化,从而阻断FGFR2信号通路,以达到抑制肿瘤生长的目,有望为患者带来更安全的治疗。临床前研究表明,3HP-2827具有良好的抗肿瘤作用与可靠的安全性,并且对于耐药患者有不容忽视的疗效,有望成为同类药最佳。毒理学研究中,3HP-2827展现出了卓越的耐受性,未观察到高磷血症或组织矿化现象。体内试验显示,3HP-2827在不同癌种小鼠模型中表现出了强大的抗肿瘤活性。更重要的是,在ICC PDX模型中,3HP-2827使佩米替尼耐药的肿瘤消退。
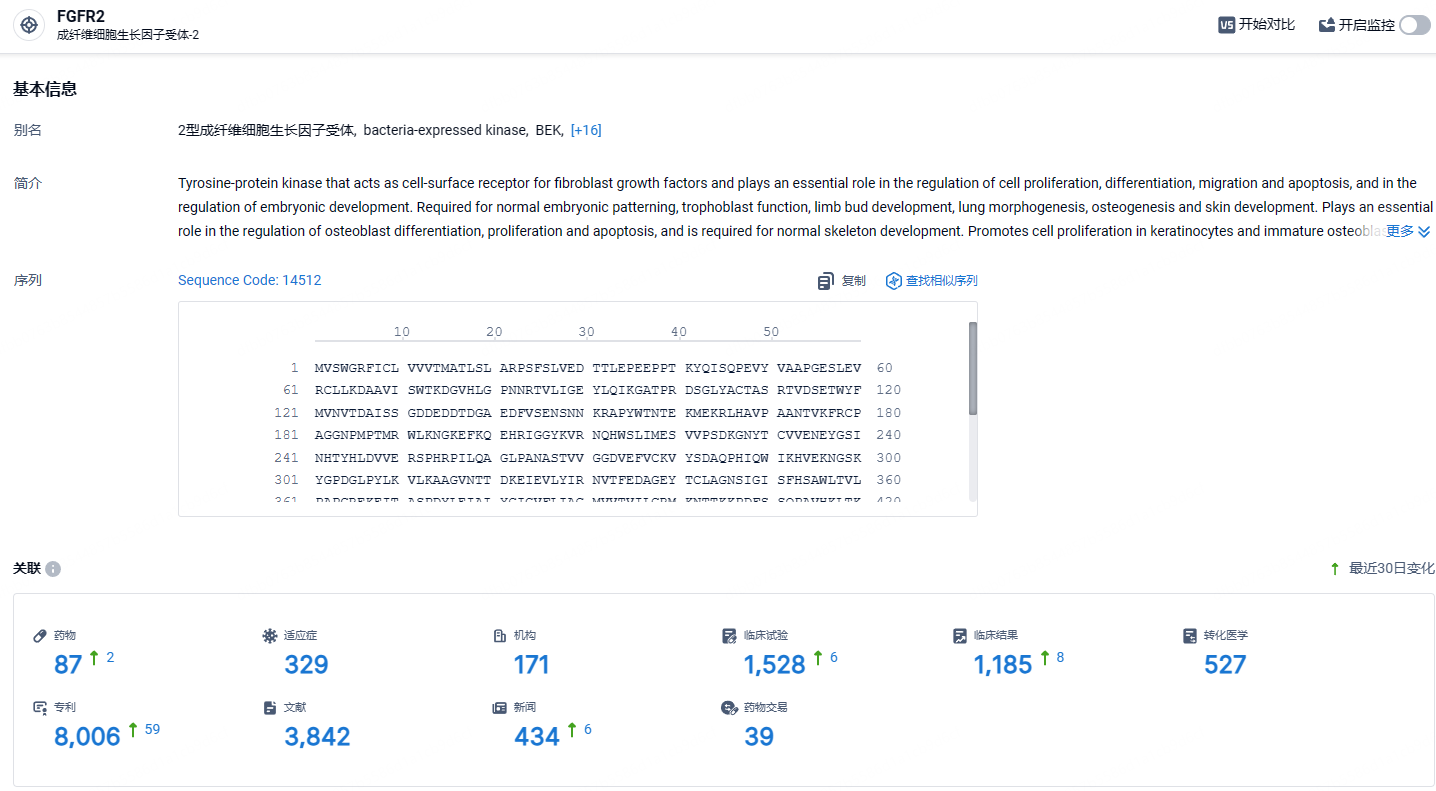
根据智慧芽新药情报库所披露的信息 (点击下方图片直达FGFR2靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2024年7月5日,FGFR2靶点共有在研药物87个,包含的适应症有329种,在研机构171家,涉及相关的临床试验1528件,专利8006件……快速通道认定(Fast Track Designation,FTD)作为一种加快药物研发与审评的通道,是FDA旨在促进治疗严重疾病、解决重大未满足医疗需求的新药研发而授予在研药物的一种资格认定。此项资格认定有助于新药研发企业在后续的药物研发和审评过程中,获得更多、更及时与FDA沟通交流的机会;新药研发企业还可在提交上市申请时向FDA滚动递交(rolling submission)新药研究资料,有助于加速药物的后续研发和批准上市。期待3HP-2827后续临床进展顺利。