预约演示
更新于:2026-05-26
Fitusiran
芬妥司兰钠
更新于:2026-05-26
概要
基本信息
非在研机构- |
最高研发阶段批准上市 |
最高研发阶段(中国)批准上市 |
特殊审评突破性疗法 (美国)、孤儿药 (美国)、优先审评 (中国)、快速通道 (美国) |
登录后查看时间轴
结构/序列
使用我们的RNA技术数据为新药研发加速。
登录
或
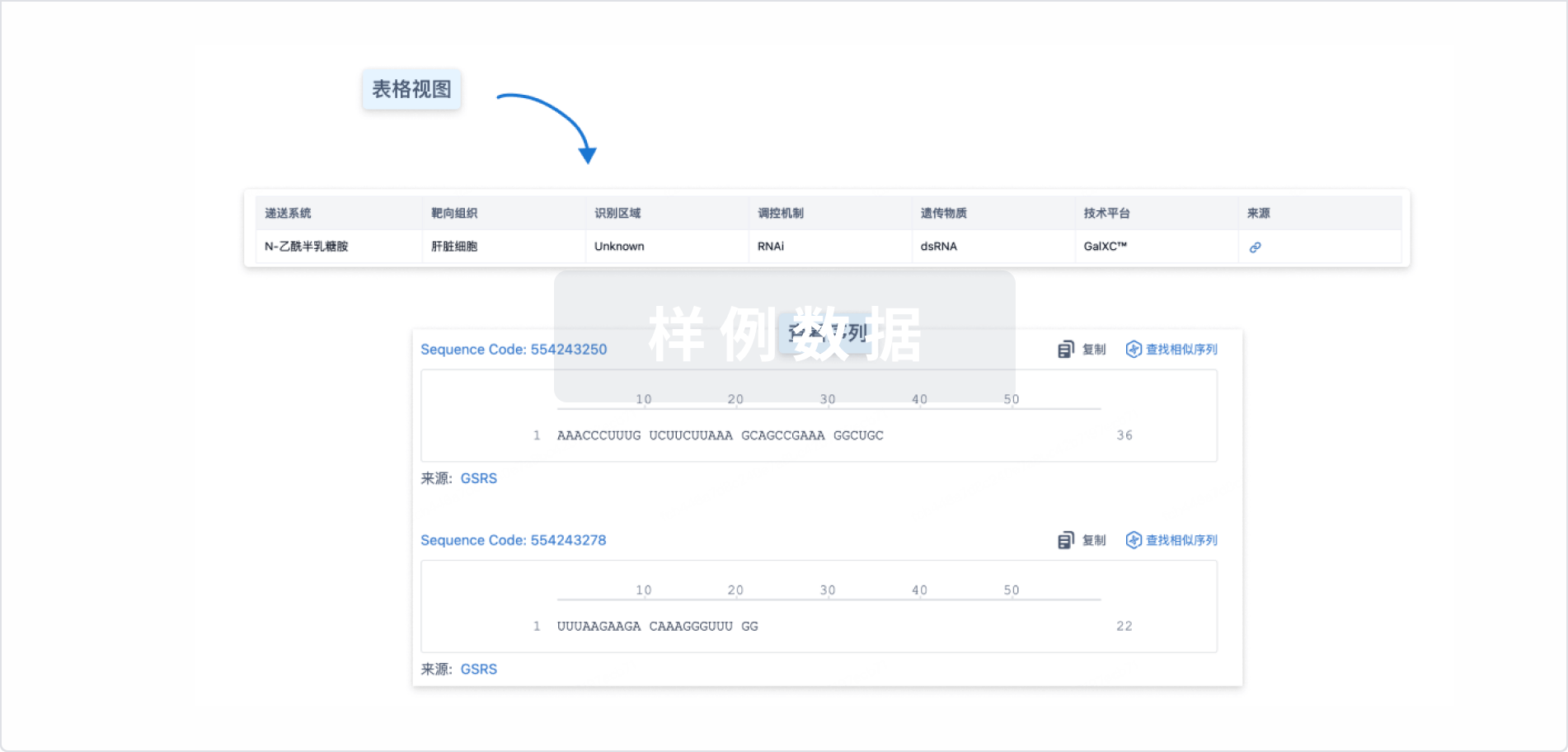
Sequence Code 30076949

来源: *****
Sequence Code 432002385

来源: *****
关联
11
项与 芬妥司兰钠 相关的临床试验NCT07285460
An Open-label, Parallel, Phase 3, Two-arm Study to Investigate the Efficacy and Safety of Fitusiran Prophylaxis in Male Participants Aged 1 to Less Than 12 Years With Hemophilia A or B With or Without Inhibitory Antibodies to Factors VIII or IX
This is a parallel, Phase 3, two-arm, open-label study to evaluate the efficacy and safety of treatment with fitusiran prophylaxis administered to male pediatric participants (aged 1 to <12 years) who have severe hemophilia A or B, with or without inhibitory antibodies to FVIII or FIX.
Number of participants:
Approximately 85 participants will be enrolled into the study:
* Approximately 60 fitusiran-naïve participants with severe hemophilia A or B, with or without inhibitors (fitusiran-naïve arm), and
* Approximately 25 participants with severe hemophilia A or B with inhibitors rolling over from the EFC15467* dose confirmation study (roll-over arm).
* Fitusiran has been investigated in the pediatric population in study EFC15467, which enrolled male participants aged 1 to <12 years with hemophilia A or B with inhibitors to examine the safety and tolerability of fitusiran in the pediatric population.
Participants will be enrolled into 1 of 2 arms:
* Fitusiran-naïve: these participants have not previously received fitusiran, and they will undergo screening and study eligibility assessments. Once enrolled, they will go through a 24-week standard of care (SOC) period before starting fitusiran prophylaxis.
* Roll-over participants from the EFC15467 study: only participants who are still on active treatment in study EFC15467 and consenting to study EFC17905 will be eligible to roll over. They will not need to undergo screening or further eligibility assessments. They will directly enroll into the fitusiran treatment period and continue treatment on their current fitusiran dose.
The duration of fitusiran treatment will be up to 160 weeks for the fitusiran-naïve arm and up to 60 weeks for the roll-over arm.
Number of participants:
Approximately 85 participants will be enrolled into the study:
* Approximately 60 fitusiran-naïve participants with severe hemophilia A or B, with or without inhibitors (fitusiran-naïve arm), and
* Approximately 25 participants with severe hemophilia A or B with inhibitors rolling over from the EFC15467* dose confirmation study (roll-over arm).
* Fitusiran has been investigated in the pediatric population in study EFC15467, which enrolled male participants aged 1 to <12 years with hemophilia A or B with inhibitors to examine the safety and tolerability of fitusiran in the pediatric population.
Participants will be enrolled into 1 of 2 arms:
* Fitusiran-naïve: these participants have not previously received fitusiran, and they will undergo screening and study eligibility assessments. Once enrolled, they will go through a 24-week standard of care (SOC) period before starting fitusiran prophylaxis.
* Roll-over participants from the EFC15467 study: only participants who are still on active treatment in study EFC15467 and consenting to study EFC17905 will be eligible to roll over. They will not need to undergo screening or further eligibility assessments. They will directly enroll into the fitusiran treatment period and continue treatment on their current fitusiran dose.
The duration of fitusiran treatment will be up to 160 weeks for the fitusiran-naïve arm and up to 60 weeks for the roll-over arm.
开始日期2025-12-18 |
申办/合作机构 |
NCT06145373
An Open-label, Single-arm Treatment Study to Investigate the Safety and Tolerability of Switching From Emicizumab to Fitusiran Prophylaxis in Male Participants Aged ≥12 Years of Age With Severe Hemophilia A, With or Without Inhibitors
This is an exploratory, single group, Phase 4, study to assess treatment with fitusiran prophylaxis after switching from emicizumab prophylaxis.
This study aims to evaluate the safety and tolerability of switching to fitusiran after a transition period from the last dose of emicizumab. The study will be conducted in male participants with severe hemophilia A, with or without inhibitors, aged ≥12 years, who were previously receiving emicizumab prophylaxis.
Study details include:
* The study duration will be up to approximately 28 months:
* There will be an approximately 2-month screening period.
* There will be an approximately 2-month period before fitusiran treatment starts (pre-fitusiran treatment period)
* The fitusiran treatment duration will be up to 18-months (fitusiran treatment period)
* The antithrombin (AT) follow-up (FU) period will be approximately 6 months after the last dose of fitusiran (during which the AT activity level will be monitored at approximately monthly intervals following the final fitusiran dose until AT activity levels return to at least 60%).
* The study site visits are scheduled at monthly/ every 2 months intervals of 28 days (4 weeks) / 56 days (8 weeks), respectively, during the fitusiran treatment period.
This study aims to evaluate the safety and tolerability of switching to fitusiran after a transition period from the last dose of emicizumab. The study will be conducted in male participants with severe hemophilia A, with or without inhibitors, aged ≥12 years, who were previously receiving emicizumab prophylaxis.
Study details include:
* The study duration will be up to approximately 28 months:
* There will be an approximately 2-month screening period.
* There will be an approximately 2-month period before fitusiran treatment starts (pre-fitusiran treatment period)
* The fitusiran treatment duration will be up to 18-months (fitusiran treatment period)
* The antithrombin (AT) follow-up (FU) period will be approximately 6 months after the last dose of fitusiran (during which the AT activity level will be monitored at approximately monthly intervals following the final fitusiran dose until AT activity levels return to at least 60%).
* The study site visits are scheduled at monthly/ every 2 months intervals of 28 days (4 weeks) / 56 days (8 weeks), respectively, during the fitusiran treatment period.
开始日期2024-03-01 |
申办/合作机构 |
NCT05662319
A Phase 3, Single-arm, Multicenter, Multinational, Open-label, One-way Crossover Study to Investigate the Efficacy and Safety of Fitusiran Prophylaxis in Male Participants Aged ≥ 12 Years With Severe Hemophilia A or B With or Without Inhibitory Antibodies to Factor VIII or IX
This is a multicenter, multinational, open-label, one-way cross-over, Phase 3, single-arm study for treatment of hemophilia.
The purpose of this study is to measure the frequency of treated bleeding episodes with fitusiran in male adult and adolescent (≥12 years old) participants with hemophilia A or B, with or without inhibitory antibodies to factor VIII or IX who have switched from their prior standard of care treatment.
The total study duration will be up to approximately 50 months (200 weeks, 1 study month is equivalent to 4 weeks) and will include:
* A screening period up to approximately 60 days,
* A standard of care (SOC) period of approximately 6 study months (24 weeks),
* A fitusiran treatment period of approximately 36 study months (144 weeks),
* An antithrombin (AT) follow-up period of approximately 6 study months (24 weeks) but may be shorter or longer depending on individual participants AT recovery.
The frequency for telephone visits will be approximately every 2 weeks. For site visits the frequency will be approximately every 8 weeks during the SOC period and approximately every 4 weeks during the fitusiran treatment period. If applicable and if allowed by local regulation, home and/or remote visits may be conducted during the study
The purpose of this study is to measure the frequency of treated bleeding episodes with fitusiran in male adult and adolescent (≥12 years old) participants with hemophilia A or B, with or without inhibitory antibodies to factor VIII or IX who have switched from their prior standard of care treatment.
The total study duration will be up to approximately 50 months (200 weeks, 1 study month is equivalent to 4 weeks) and will include:
* A screening period up to approximately 60 days,
* A standard of care (SOC) period of approximately 6 study months (24 weeks),
* A fitusiran treatment period of approximately 36 study months (144 weeks),
* An antithrombin (AT) follow-up period of approximately 6 study months (24 weeks) but may be shorter or longer depending on individual participants AT recovery.
The frequency for telephone visits will be approximately every 2 weeks. For site visits the frequency will be approximately every 8 weeks during the SOC period and approximately every 4 weeks during the fitusiran treatment period. If applicable and if allowed by local regulation, home and/or remote visits may be conducted during the study
开始日期2023-02-01 |
申办/合作机构 |
100 项与 芬妥司兰钠 相关的临床结果
登录后查看更多信息
100 项与 芬妥司兰钠 相关的转化医学
登录后查看更多信息
100 项与 芬妥司兰钠 相关的专利(医药)
登录后查看更多信息
43
项与 芬妥司兰钠 相关的文献(医药)2026-05-01·British Journal of Pharmacology
Novel drugs approved by the EMA, the FDA and the MHRA in 2025: A year in review
Review
作者: Hemal H. Patel ; Nithyanandan Nagercoil ; Claudio Mauro ; Steve P. H. Alexander ; Rainer Schulz ; Miriam M. Cortese-Krott ; Stephen Ward ; Stavros Topouzis ; Barbara Stefanska ; Xin Wang ; Gary J. Stephens ; Nathalie Vergnolle ; Reynold A. Panettieri Jr ; Zsuzsanna Helyes ; Andreas Papapetropoulos ; Kirill Martemyanov ; Péter Ferdinandy
Abstract:
In the 2025 novel drug mini‐review, one can take a full measure of the ingenuity that underlies current drug design and development, despite the year's smaller harvest (46 novel drugs) compared to 2024 (53) and 2023 (70). 54% of the novel drugs are first‐in‐class (FIC). The emphasis on proteins/antibodies is maintained (~25% novel drugs in 2025), an industry trend that does not seem to abate. Fewer than half of the novel medicines address major or common disorders. Among the FIC drugs, it is worth mentioning the Na
v
1.8 channel inhibitor suzetrigine, the first non‐opioid approved to palliate acute pain; the first positive allosteric modulator of transient receptor potential melastatin 8 (TRPM8), acoltremon, that increases basal tear production in dry eye disease, a globally common disorder; lerodalcibep, a ‘third generation’ adnectin inhibitor of the protease Proprotein Convertase Subtilisin/Kexin type 9 (PCSK9) to treat elevated LDL‐c; and zoliflodacin and gepotidacin, both innovatively targeting bacterial topoisomerases to treat uncomplicated urinary tract infections. Most of the approved medicines target unmet medical need areas and/or orphan indications (the latter alone accounting for 41% of the 2025 novel drugs) by applying imaginative approaches. These approaches include: the combination of
two
FIC drugs, the RAF/MEK clamp avutometinib paired with the FAK/Pyk2 inhibitor defactinib, to block more efficiently the RAS–RAF–MEK–ERK/FAK oncogenic pathway in low‐grade serous ovarian cancer; fitusiran, the first RNAi therapy for haemophilia, targeting for the first time the production of the natural anticoagulant anti‐thrombin in the liver; and brensocatib, which attenuates the activation of downstream neutrophil proteases by inhibiting the protease DPP1, thereby preventing lung tissue destruction in bronchiectasis. The landscape of novel drugs approved in 2025 reveals that pharmaceutical innovation continues to advance through FIC mechanisms, sophisticated therapeutic approaches, and a strong focus on unmet medical need.
2026-02-01·AMERICAN JOURNAL OF MANAGED CARE
Redefining hemophilia management: treatment goals, nonfactor replacement therapies, and the role of fitusiran
Article
作者: Pipe, Steven W
Hemophilia is a rare, but debilitating congenital bleeding disorder. Current therapeutic guidelines, last updated in 2020, recommend recombinant clotting factor concentrates as the standard replacement therapy, with emicizumab offered as an alternative nonfactor standard of care. Since the publication of those guidelines, approvals of new gene-based and nonfactor therapies have reshaped the therapeutic landscape. This supplement describes the safety and efficacy of those therapies approved after the 2020 guidelines were published. It also presents managed care considerations describing how opportunities for resource optimization, therapeutic efficiency, and alternative administration approaches may advance progress toward aspirational treatment goals. A main focus is on fitusiran, the most recently approved nonfactor therapy, which introduced a novel mechanism of action and dosing strategy to the hemophilia therapeutic landscape in addition to its broad patient applicability. As this and other therapeutic advancements redefine the standard of care for patients with hemophilia, managed care and policy frameworks must adapt to ensure timely access and affordability. Likewise, updates to clinical guidelines and care pathways are essential to capture the rapidly evolving therapeutic landscape.
2026-01-01·CLINICAL AND APPLIED THROMBOSIS-HEMOSTASIS
Comparative Efficacy and Safety of Non-Clotting Factor Prophylaxis Versus. on-Demand Therapy in Hemophilia: A Meta-Analysis of Randomized Controlled Trials
Review
作者: Danish, Hamza ; Ali, Manahil ; Ahuja, Laksh ; Talpur, Abdul Subhan ; Khan, M Raafe Ali ; Ishaque, Rehan ; Reddy, Aswanth ; Rayamajhi, Supratik ; Ikram, Amna ; Memon, Huda ; Janjua, Hira ; Janjua, Hamza ; El joujou, Raghad ; Siddiqui, Muhammad Ahsan ; Reya, Fnu
Introduction:
Hemophilia A and B are among the most common inherited bleeding disorders in humans with lifelong risk of spontaneous and recurrent bleeding. While prophylaxis with clotting factors has improved outcomes, challenges like inhibitor development and treatment burden persist. We aim for a comparative effectiveness between these agents and traditional therapy with this study.
Methods:
A systematic review and meta-analysis of randomized controlled trials (RCTs) was conducted. Studies were identified through PubMed, Cochrane Central, and ClinicalTrials.gov up to May 30th, 2025. Eligible studies were double-arm RCTs comparing non-clotting factor prophylaxis (emicizumab, fitusiran, concizumab) and on-demand therapy in patients with hemophilia A or B.
Results:
Non-clotting factor prophylaxis significantly reduced the annualized bleeding rate (ABR) for all treated bleeds [
n
= 399, (RR = 0.13; 95% CI: 0.09–0.19),
I2
= 63.8%,
p
= 0.0107], spontaneous bleeds [RR = 0.08; 95% CI: (0.06, 0.11),
I2
= 0.0%,
p
= 0.5933)] and joint bleeds [RR = 0.09; 95% CI: (0.06, 0.14), :
I2
= 26.2%,
p
= 0.2468 ]. Haem-A-QoL total score improved with prophylaxis [MD = −11.08 [−16.34, −5.83],
I2
= 57.5%,
p
= 0.0949]. Prophylaxis increased the likelihood of achieving zero treated bleeds [RR = 4.11; 95% CI: (1.48%, 11.45%),
I2
= 88.5%,
p
< 0.0001]. An exploratory network meta-analysis comparing fitusiran, emicizumab, and concizumab reported no statistically significant difference in the ABR for all treated bleeds.
Conclusion:
Compared to on-demand therapy, non-factor prophylactic therapies significantly reduce bleeding episodes, improve quality of life, and increase the likelihood of zero bleeds in patients with hemophilia.
435
项与 芬妥司兰钠 相关的新闻(医药)2026-05-23
4月23日,赛诺菲发布2026年第一季度财报。在整体医药市场增速放缓的背景下,赛诺菲罕见病板块交出了一份亮眼成绩单:单季销售额高达17.52亿欧元,同比增长20.1%。这背后,是药企在2026年依然稳赚不赔的商业逻辑。
2025年对赛诺菲而言是结构性的转折之年。通过剥离消费者保健业务Opella、以95亿美元收购Blueprint Medicines等一系列战略操作,这家法国制药巨头正全力转型为一家专注“免疫+疫苗+罕见病”的生物制药“纯粹玩家”。赛诺菲2025年全年净销售额达436.26亿欧元,同比增长9.9%。其中,自免王牌产品度普利尤单抗(Dupixent)全年销售额达157亿欧元,增长25.2%,占公司总营收近36%。研发投入达78.42亿欧元,占净销售额18.0%。
回顾赛诺菲2025年上半年收入31.08亿欧元,业务重心围绕四个核心方向布局:
罕见血液病:以血友病A/B为核心,拥有全球首个血友病siRNA疗法Qfitlia(Fitusiran)等差异化重磅产品;
遗传代谢病:庞贝病(Nexviazyme)、戈谢病(Cerezyme/Cerdelga)、法布里病(Fabrazyme)等传统优势领域;
罕见免疫病:通过收购Blueprint Medicines获得Ayvakit(avapritinib)及相关免疫管线;
神经罕见病:聚焦CIDP(riliprubart)、MS(tolebrutinib)等差异化方向。已上市罕见病产品矩阵
药物(商品名)
通用名
靶点/机制
适应症
2025年销售额Altuviiio
efanesoctocog alfa
凝血因子VIII(FVIII)
A型血友病11.60亿欧元Nexviazyme
avalglucosidase alfa
GAA酶替代疗法
庞贝病(婴儿型/晚发型)7.90亿欧元Fabrazyme
agalsidase beta
α-半乳糖苷酶A替代疗法
法布里病2.62亿欧元Cerezyme + Cerdelga
imiglucerase + eliglustat
酶替代/葡萄糖神经酰胺合成酶抑制剂
戈谢病(1型/3型)2.76亿欧元Qfitlia(赛菲因)
fitusiran
抗凝血酶(AT)siRNA
血友病A/B(2025年获批)
未单独披露(2025年3月/12月获批)Avapritinib
avapritinib
KIT/PDGFRA抑制剂
系统性肥大细胞增多症(SM)
2025年Q1净收入近1.5亿美元Cablivi(可倍力)
caplacizumab
抗vWF纳米抗体
获得性血栓性血小板减少性紫癜
未单独披露
说明:如无特别标注,2025年销售额数据来自赛诺菲2025年全年财报。明星产品深度剖析
Altuviiio:2025年全年销售额达11.60亿欧元,同比增长77.6%,是赛诺菲罕见病领域的“增速之王”。在美国市场,Altuviiio主要由患者从传统因子疗法和其他非因子疗法转换驱动,2025年上半年美国市场销售额即达5.42亿欧元。赛诺菲正在该领域挑战罗氏Hemlibra在血友病市场的主导地位。
Nexviazyme:销售额7.90亿欧元,同比增长21.4%,主要受欧洲市场强劲增长驱动(欧洲+30.8%)。
Fabrazyme:全年销售额仅2.62亿欧元,同比下降约2.4%,增速放缓主要受新增患者数量有限和医保价格压力影响。
Cerezyme:销售额1.71亿欧元,同比增长3%;戈谢病产品组合(Cerezyme和Cerdelga合计)销售额2.54亿欧元,同比增长1.6%。
2025年新获批上市的三款重磅产品1. Qfitlia(Fitusiran) :全球首个血友病siRNA疗法。2025年3月获FDA批准上市,2025年12月在中国获批上市。该药通过靶向抗凝血酶(AT)实现血友病A/B的预防治疗,差异化机制使其在竞争激烈的血友病市场中占据了独特地位。
2. Cablivi(Caplacizumab) :2025年12月在中国获批,用于获得性血栓性血小板减少性紫癜(aTTP)。
3. Elamipretide :作为线粒体靶向治疗药物,于2025年9月获FDA加速批准,用于治疗Barth综合征(一种罕见的X连锁线粒体遗传疾病,主要影响男性,常伴随心力衰竭、肌肉无力等)。
在研管线深度解析:两大“王炸”与一个“宝藏”
药物
靶点/机制
适应症
当前阶段
关键里程碑Venglustat
口服葡萄糖神经酰胺合成酶抑制剂(可穿越血脑屏障)
III型戈谢病(GD3)
III期(LEAP2MONO达主要终点)
2026年全球申报上市Efdoralprin alfa(SAR447537)
AAT-Fc融合蛋白(重组人α-1抗胰蛋白酶)
α-1抗胰蛋白酶缺乏症(AATD)相关肺气肿
II期达主要与关键次要终点
获FDA和EMA孤儿药认定Riliprubart(SAR445088)
选择性抑制补体通路C1s单抗
慢性炎性脱髓鞘性多发性神经根神经病(CIDP)
III期进行中(MOBILIZE/VITALIZE)
获日本孤儿药资格认定Tolebrutinib(Cenrifki)
口服脑穿透性BTK抑制剂
继发进展型多发性硬化(SPMS)
III期完成
2026年4月获CHMP积极意见GLB-005/GLB-007
WIZ/ZBTB7A分子胶降解剂
镰状细胞病(SCD)
临床前→I期
2026年底启动I期重点管线深度剖析
Venglustat:挑战“不可成药”领域的口服疗法
2025年2月,赛诺菲公布了Venglustat两项III期研究结果。针对III型戈谢病(GD3)的LEAP2MONO研究达到了主要终点,并达到了四项关键次要终点中的三项;该药物在52周时改善了神经系统结果,同时保持了与酶替代疗法(ERT)相当的系统疾病控制。但针对法布里病的PERIDOT研究未达到主要终点。2026年3月,FDA授予Venglustat突破性疗法认定,赛诺菲计划于2026年进行全球监管备案。该药物具备穿越血脑屏障的独特能力,若获批将成为首个针对GD3神经系统表现的疾病修饰口服疗法。
Efdoralprin alfa(SAR447537):AATD领域的差异化选择
2025年10月22日,赛诺菲宣布Efdoralprin alfa的全球2期ElevAATe研究取得积极结果。该在研疗法采用每三周(Q3W)或每四周(Q4W)给药,均成功达成所有主要与关键次要终点。该药物通过收购Inhibrx获得,2025年12月获EMA孤儿药资格认定。与每周接受血浆衍生替代疗法的对照组相比,接受Efdoralprin alfa治疗的患者在稳态谷浓度下功能性AAT(fAAT)水平显著提升并达到正常范围。
Riliprubart:填补CIDP治疗空白
CIDP是一种治疗选择极为有限的罕见神经病变。现有标准疗法IVIg约30%患者无响应。riliprubart是一种选择性抑制补体通路C1s的单克隆抗体,目前正在进行两项独立的全球III期研究:MOBILIZE针对对标准治疗无效的患者,VITALIZE针对接受静脉免疫球蛋白(IVIg)治疗的患者。该药物已在日本获得孤儿药资格认定,如果III期成功,有望成为CIDP领域首个通过特异性抑制C1s治疗该病的药物。
Tolebrutinib(Cenrifki):BTK抑制剂向MS深层病理的破局者
Tolebrutinib是一种口服脑穿透性BTK抑制剂,专门针对闷烧性神经炎症而设计。2026年4月24日,CHMP采纳了积极意见,建议欧盟批准Cenrifki用于治疗无复发超过两年的继发进展型多发性硬化(SPMS)患者。然而,该药物在FDA申报中遭遇挫折——2025年12月收到CRL,FDA要求提供更多数据。此外,在复发性MS的两项III期研究以及在原发进展型MS的PERSEUS研究中均未达到主要终点。这一系列的“有喜有忧”充分反映了新机制药物在中枢神经系统疾病中的研发风险——BTK抑制剂在MS领域的浪潮中,赛诺菲仅在SPMS亚群中取得了局部突破。
分子胶降解剂布局:赛诺菲+格博生物
2026年2月,赛诺菲向格博生物进行3000万美元战略股权投资,推进镰状细胞病的分子胶降解剂GLB-005和GLB-007。GLB-005旨在选择性降解WIZ蛋白,GLB-007同时靶向WIZ和ZBTB7A蛋白。临床一期研究最早将在2026年底开展。这一布局标志着赛诺菲在罕见病领域向新一代技术平台的延伸。
战略并购与外部合作:以95亿美元收购Blueprint Medicines1)、收购蓝图核心内容
2025年6月2日,赛诺菲宣布与Blueprint Medicines达成最终收购协议,以每股129美元现金收购Blueprint,总金额约91亿美元现金+4亿美元CVR(或有价值权),总价值95亿美元。赛诺菲CEO Paul Hudson表示,此次收购是其“罕见病和免疫学产品布局的战略性进展”,并强调公司仍有充足能力展开进一步收购。2 )、收购蓝图带来三大关键资产
I. Ayvakit(avapritinib) —已获批的肥大细胞疾病重磅炸弹。这是一款口服高选择性KIT和PDGFRA突变抑制剂,主要用于系统性肥大细胞增多症(SM)的治疗,2025年第一季度净收入近1.5亿美元,同比增长超60%。SM是KIT D816V基因驱动、导致全身器官功能障碍的罕见克隆性疾病,Ayvakit填补了该领域精准治疗的空缺。
II. Elenestinib —下一代KIT抑制剂,用于系统性肥大细胞增多症的迭代产品。
III. BLU-808 —口服野生型KIT抑制剂,在免疫学领域有巨大潜力,可应用于更广泛的免疫疾病。3)其他外部合作与管线引进
Inhibrx(2024年收购) :获得Efdoralprin alfa(AATD),该药物在2025年10月公布II期积极结果,已获欧盟孤儿药认定;
Spinogenix合作:通过合作布局SPG302,一种口服突触再生疗法,针对阿尔茨海默病和肌萎缩侧索硬化症;
正大天晴合作(2026年3月) :15.3亿美元引进罗伐昔替尼(TQ05105),一种JAK/ROCK抑制剂,用于骨髓纤维化——这能迅速增强赛诺菲在血液肿瘤专科治疗领域的竞争力。挑战与前景:赛诺菲罕见病业务的“黑暗森林”核心挑战
1、明星药物的“巨型依赖症”: Dupixent占赛诺菲总营收比例已逼近36%。赛诺菲亟需证明“去Dupixent化”不是口号。罕见病业务虽然增长强劲,但目前在总营收中的占比仍然偏低。
2、GTX市场的红海陷阱: 戈谢病(Cerezyme+Cerdelga合计2.54亿欧元)、法布里病(Fabrazyme约2.62亿欧元)等传统代谢病赛道增速已步入瓶颈。Cerezyme同比增长仅3%,Fabrazyme同比下滑约2.4%。随着更多生物类似药的进入和医保价格压力,这些细分领域正面临“规模难扩、利润难保”的困局。
3、在研管线的“黑天鹅”风险: Venglustat在法布里病III期研究中的失败以及Tolebrutinib在原发进展型MS的III期失败,说明新机制药物即便在早期数据亮眼,在大型III期临床试验中仍随时可能受阻。未来前景研判
2026年底前,市场将见证多个关键里程碑:
积极的催化剂:
Venglustat在GD3适应症的全球申报进展(2026年计划申报上市)
Qfitlia在中国的商业放量加速推进
Riliprubart的III期数据能否改写CIDP的治疗格局
消极的变量:
Tolebrutinib在FDA的CRL问题尚未完全解决
法布里病和传统遗传代谢病市场的持续萎缩风险
2026年4月CHMP已对Tolebrutinib采纳积极意见,但美国市场的审批延迟仍然是一个不确定因素
中国是赛诺菲罕见病全球战略的核心增量市场。2025年12月,Qfitlia(赛菲因)在中国获批上市,2026年3月,赛诺菲宣布对上海中国研发中心进行全面战略升级,在沪设立全新的研发中心法律实体。中国市场全年收入为26.21亿欧元,增长2.0%。Nexviazyme等罕见病产品也在积极推进在中国的准入流程。
2026年的赛诺菲,已不再是2018年面临专利悬崖、急于转型的那个疲软巨人。通过精准的战略并购、结构性的资产调整以及长期高投入的自主研发,公司罕见病业务的管线厚度达到了近年来的最高水平。随着Qfitlia、Efdoralprin alfa、Riliprubart等一系列差异化创新产品的推进,赛诺菲正在从罕见病领域的“被动跟随者”向“主动定义者”转变。
专注药用高分子材料,助力药械研发高质量前行。如果您正在开展PEG 化药物、水凝胶器械、PLA/PLGA 微球等项目开发,有样品测试、原料供应需求,欢迎随时与我们交流对接。
作为专业的药用高分子材料研发与制造方,我们可提供克级实验室样品、公斤级中试、吨级工业化生产的全链条供应,支持nGMP 及 GMP级别药用 PEG、PLA、PLGA 原料定制,并提供完整、规范的质量研究报告。
我们以高标准原料与专业服务,为您的药械研发与申报全程护航,助力创新成果落地,让更安全、更优质的药械福泽广大患者。
分 类
产品
分 子 量
mPEG
原料
mPEG-OH
5K,10K,20K,30k,40K
多臂PEG
原料
4arm-PEG-OH
10K,20K,40K
8arm-PEG(TP)-OH
10K,15K;20K,40K
8arm-PEG(HG)-OH
10K,15K;20K,40K
两臂PEG
U-mPEG2-NHS
40K
Y-PEG-NHS
40K
mPEG2-MAL
40K
单官能团
mPEG-pALD
5K,10K,20K
mPEG-bALD
5K,10K,20K
mPEG-SC
5K,10K,20K
mPEG-SCM
5K,10K,20K
mPEG-SPA
5K,10K,20K
mPEG-SBA
5K,10K,20K
mPEG-SVA
5K,10K,20K
mPEG-SHA
5K,10K,20K
mPEG-SG
5K,10K,20K
mPEG-SS
5K,10K,20K
mPEG-MAL
5K,10K,20K
mPEG-ppMAL
5K,10K,20K
mPEG-NH2
5K,10K,20K
mPEG-AA
5K,10K,20K
双官能团
OHC-PEG-CHO
5K,10K,20K
HOOC-PEG-COOH
5K,10K,20K
HS-PEG-SH
5K,10K,20K
H2N-PEG-NH2
5K,10K,20K
SC-PEG-SC
5K,10K,20K
SCM-PEG-SCM
5K,10K,20K
SS-PEG-SS
5K,10K,20K
MAL-PEG-CHO
5K,10K,20K
MAL-PEG-NHS
5K,10K,20K
HOOC-PEG-NCO
5K,10K,20K
AA-PEG-EO
5K,10K,20K
AA-PEG-SC
5K,10K,20K
OHC-PEG-EO
5K,10K,20K
H2N-PEG-SH
5K,10K,20K
COOH-PEG-SH
5K,10K,20K
AA-PEG-COOH
5K,10K,20K
OHC-PEG-SC
5K,10K,20K
HO-PEG-SH
5K,10K,20K
MAL-PEG-PA
5K,10K,20K
NH2-PEG-COOH
5K,10K,20K
MA-PEG-EO
5K,10K,20K
MA-PEG-NCO
5K,10K,20K
四臂PEG
4arm-PEG-SG
10K,20K
4arm-PEG-SS
10K,20K
4arm-PEG-SH
10K,20K
4arm-PEG-NH2
10K,20K
4arm-PEG-pALD
10K,20K
4arm-PEG-bALD
10K,20K
4arm-PEG-MAL
10K,20K
4arm-PEG-SC
10K,20K
4arm-PEG-SCM
10K,20K
4arm-PEG-SPA
10K,20K
4arm-PEG-SBA
10K,20K
4arm-PEG-SVA
10K,20K
4arm-PEG-SHA
10K,20K
4arm-PEG-SSE
10K,20K
4arm-PEG-SCM
10K,20K
4arm-PEG-CHA-NCO
10K,20K
4arm-PEG-HA-MAL
10K,20K
4arm-(3NH2+1AA)-PEG
10K,20K
4arm-PEG-SSA
10K,20K
八臂PEG
8arm-PEG(TP)-SG
10k,15k;20k;40k
8arm-PEG(TP)-SS
10k,15k;20k;40k
8-arm-PEG(TP)-SH
10k,15k;20k;40k
8arm-PEG(TP)-NH2
10k,15k;20k;40k
8arm-PEG(TP)-pALD
10k,15k;20k;40k
8arm-PEG(TP)-MAL
10k,15k;20k;40k
8arm-PEG(HG)-SG
10k,15k;20k;40k
8arm-PEG(HG)-SS
10k,15k;20k;40k
8arm-PEG(HG)-SH
10k,15k;20k;40k
8arm-PEG(HG)-MAL
10k,15k;20k;40k
8arm-PEG(TP)-SC
10k,15k;20k;40k
8arm-PEG(TP)-GA
10k,15k;20k;40k
8arm-PEG(TP)-GAA
10k,15k;20k;40k
8arm-PEG(TP)-SAA
10k,15k;20k;40k
8arm-PEG(TP)-SA
10k,15k;20k;40k
8arm-PEG(TP)-CM
10k,15k;20k;40k
8arm-PEG(TP)-SCM
10k,15k;20k;40k
8arm-PEG(HG)-SGA
10k,15k;20k;40k
8arm-PEG(HG)-SCM
10k,15k;20k;40k
8arm-PEG(HG)-SC
10k,15k;20k;40k
8arm-PEG(HG)-pALD
10k,15k;20k;40k
8arm-PEG(HG)-GA
10k,15k;20k;40k
8arm-PEG(HG)-GAA
10k,15k;20k;40k
8arm-PEG(HG)-SAA
10k,15k;20k;40k
8arm-PEG(HG)-SA
10k,15k;20k;40k
8arm-PEG(HG)-CM
10k,15k;20k;40k
8arm-PEG(SUC)-MAL
10k,15k;20k;40k
8arm-PEG(HY)-SG
10k,15k;20k;40k
Linkers
NH2-PEGn-PA(n=2-24)
AZIDE-PEGn-NH2(n=2-24)
AZIDE-PEGn-PA(n=2-24)
M-PEGn-PA(n=2-24)
M-PEGn-NH2(n=2-24)
MAL-PEGn-PA(n=2-24)
MAL-PEGn-SPA(n=2-24)
DBCO-PEGn-PA(n=2-24)
MAL-PEGn-VC-PAB(n=2-24)
MAL-PEGn-VA-PAB(n=2-24)
DBCO-PEGn-VC-PAB(n=2-24)
DBCO-PEGn-VA-PAB(n=2-24)
LNPs
M-DMG-2000
ALC-0159
ALC-0315
SM-102
DOTAP
PLGA
产品型号
特性黏度(dL/g)
PLGA5050
PLGA5050-20H
0.16-0.24
PLGA5050-30H
0.25-0.35
PLGA5050-40H
0.36-0.44
PLGA5050-20S
0.16-0.24
PLGA5050-30S
0.25-0.35
PLGA5050-40S
0.36-0.44
PLGA6535
PLGA6535-20H
0.16-0.24
PLGA6535-30H
0.25-0.35
PLGA6535-40H
0.36-0.44
PLGA6535-20S
0.16-0.24
PLGA6535-30S
0.25-0.35
PLGA6535-40S
0.36-0.44
PLGA7525
PLGA7525-20H
0.16-0.24
PLGA7525-30H
0.25-0.35
PLGA7525-40H
0.36-0.44
PLGA7525-20S
0.16-0.24
PLGA7525-30S
0.25-0.35
PLGA7525-40S
0.36-0.44
PLGA8515
PLGA8515-20H
0.16-0.24
PLGA8515-30H
0.25-0.35
PLGA8515-40H
0.36-0.44
PLGA8515-20S
0.16-0.24
PLGA8515-30S
0.25-0.35
PLGA8515-40S
0.36-0.44
免责条款:本文内容仅代表作者观点,供行业交流参考,不构成任何投资或应用建议,如有侵权,请联系小编,多谢❀❀❀
siRNA财报疫苗并购引进/卖出
2026-05-21
摘要
目的:分析化学合成寡核苷酸产品临床试验申请(IND)阶段的药学研究关注点,为该类药物的研发提供参考。
方法:全面梳理化学合成寡核苷酸产品的国内外上市及临床申报情况、监管现状及相关技术要求,结合实际审评工作对IND阶段原料药和制剂生产工艺、质量控制、稳定性等方面的药学关注点进行分析。
结果与结论:近年来寡核苷酸药品的研发、申报临床数量持续增加,但越来越丰富的产品类型、新的技术方法都会带来新的挑战,此类产品开发应遵循创新药研发的基本规律,结合不同类型的产品特点制定针对性的研发策略,对于此类产品开发中的重要技术问题尽早与药品监管部门积极沟通,以促进相关产品早日惠及患者。
关键词
化学合成寡核苷酸; 药学研究; 临床试验申请; 关注点
随着RNA干扰或RNA疗法的不断发展,寡核苷酸药物逐渐展现出巨大的应用前景。与传统的小分子化学药物相比,寡核苷酸药物可以从基因层面对蛋白质表达进行调控,突破了“不可成药”靶点的限制,被认为是继小分子药物和抗体药物后的新一代药物[1-4]。
然而,寡核苷酸药物结构复杂,分子尺寸介于小分子和生物制剂之间,杂质种类多且结构与目标产物类似,因此对这类产品的药学开发与控制难度较大,需要深入研究和探讨。
本文讨论的范围是化学合成的寡核苷酸药物,不包括mRNA等生物合成的大分子核酸药物。本文对寡核苷酸产品的国内外上市及临床申报情况、监管现状进行了梳理,并对新药临床试验申请(IND)药学关注点进行了分析和讨论,以期为现阶段寡核苷酸产品IND的药学研究提供参考。
1 寡核苷酸药物国内外上市及申报情况
1.1 国内外已上市寡核苷酸药物概述
截至2026年3月,全球共有23款小核酸/寡核苷酸药物获批上市(含已退市),以反义寡核苷酸(ASO)和小干扰RNA(siRNA)为主,主要聚焦罕见病。
20世纪50年代起,随着DNA双螺旋结构的发现和RNA功能的逐步揭示,科学家开始认识到核酸(包括DNA和RNA)在生物体内的重要性,并尝试将其用于疾病治疗。1978年,ASO的概念被首次提出,标志着该领域研究的开端[5]。1992年,首个针对寡核苷酸的新化学实体(NCE)药物的研究性美国的IND申请提交[6]。1998年,首款ASO药物fomivirsen(商品名Vitravene)获美国食品药品监督管理局(FDA)批准上市,用于治疗巨细胞病毒引起的视网膜炎,为领域发展的重要里程碑。然而,2003年,fomivirsen因销售额过低退市,随后多个ASO药物Ⅲ期临床接连失败,使得多家药企放弃该领域。2016年,RNA干扰(RNAi)机制获得诺贝尔生理学或医学奖,极大推动了该领域的研究与开发。随着化学修饰和递送系统的发展和进步,寡核苷酸药物的开发进入了快速发展时代[7]。2016年后,多款寡核苷酸药物陆续上市,截至2026年1月在中国上市的共6款,分别是芬妥司兰钠(fitusiran sodium,Qfitlia®)、普乐司兰钠(plozasiran sodium,Redemplo®)、英克司兰钠(inclisiran sodium,Leqvio®)、托夫生(tofersen,Qalsody®)、诺西那生钠(nusinersen sodium,Spinraza®)、依普隆特生钠(eplontersen sodium,Wainua®)。
1.2 全球寡核苷酸药物的临床试验申报情况
近年来,我国寡核苷酸药物临床试验的数量不断攀升,见图1。截至2026年3月,全球约有171个处于临床研究阶段的寡核苷酸药物,其中在中国开展临床的有65个,ASO和siRNA占大多数(表1)。寡核苷酸药物的临床研究主要集中在早期阶段,部分药物(约25%)进入了Ⅲ期或Ⅳ期临床研究阶段(图2)。在适应证方面,目前全球已上市的寡核苷酸产品主要集中于罕见病领域,然而临床在研的寡核苷酸药物适应证正逐渐从罕见病过渡到更普遍的慢性病,在我国,企业的研发主要集中在常见病/慢性病领域,包括消化系统疾病、感染性疾病、肿瘤、心血管疾病等。
2 国内外对寡核苷酸药物临床研究的技术要求
随着先进治疗产业的快速发展[8-10],寡核苷酸药品的研发、申报数量持续增加。然而这类药品化学结构与小分子差异较大,生产工艺复杂,分析手段有限,导致了其在生产工艺、结构确证、质量研究等方面成为了研发的重点和难点[11]。同时,不断攀升的临床试验申请数量、品种的复杂性及有限的指导原则给监管带来了更多挑战。多个国际人用药品注册技术协调会(ICH)研究指导原则[如Q3A(R2)、Q3B(R2)、Q6A和M7(R2)][12-15]无法完全适用于寡核苷酸药物,各国监管机构发布的寡核苷酸产品临床阶段的药学技术要求也较为有限。
2.1 欧洲、美国、日本对寡核苷酸产品临床阶段的监管情况
美国FDA在2021年发布了针对个性化ASO药物IND申请化学、生产和控制要求的指南[16],提出了IND阶段药学研究的一些建议。欧洲药品管理局(EMA)在2024年发布了寡核苷酸药物开发和生产的指南草案[17],草案涵盖了临床试验考虑的部分内容,日本尚未针对此类药品制定临床阶段的药学指导原则。
2.2 中国对寡核苷酸产品临床阶段的监管情况
目前,我国尚未制定针对化学合成寡核苷酸药物临床试验药学研究方面的指导原则,但作为化学创新药,可参考《新药Ⅰ期临床试验申请技术指南》《化学药品创新药Ⅰ期临床试验申请药学共性问题相关技术要求》《创新药(化学药)Ⅲ期临床试验药学研究信息指南》[18-20]等指导原则的相关理念,对此类产品进行开发。另外,国家药监局药审中心(CDE)已于2026年2月发布了《化学合成寡核苷酸药物(创新药)药学研究技术指导原则(试行)》[21],可供临床试验阶段的药学开发与控制参考。
3 寡核苷酸药物临床试验申请药学研究关注点
化学合成寡核苷酸药物的药学研究,应遵循一般化学药物研发的基本规律。创新药药学研究具有渐进性、阶段性和不确定性特点,其研究的广度和深度伴随临床试验的进展不断推进。在早期临床试验阶段,合成路线和工艺相对不成熟,对药物自身的理化特性和杂质行为等关键质量属性了解有限,应重点关注与受试者安全性相关的药学研究信息。随着临床试验推进至关键临床阶段及接近上市许可申请阶段,应逐步加深对产品的关键质量属性、生产工艺、杂质行为、质量控制的研究和理解,制定合理的控制策略。
3.1 原料药
3.1.1 生产工艺
化学合成寡核苷酸的工艺主要包括固相合成法、液相合成法及固相合成与酶连接相结合的工艺等。目前申报临床的寡核苷酸药物主要通过固相合成工艺制备,少部分通过固相合成与酶连接相结合的工艺合成。
固相合成通过自动合成仪在功能化固相载体上进行,常见的制备工艺包括脱二甲氧基三苯甲基(DMT)保护基、偶联、氧化/硫代、加帽等3~4个循环步骤。随后通过脱保护反应(如氨解反应)、纯化、退火(制备双链寡核苷酸)、冻干等工艺得到固体原料药(API)。寡核苷酸基本组成单元结构相似,固相合成工艺具有一定的平台技术成熟性,应充分利用类似寡核苷酸药物开发的先验知识平台进行产品开发。早期临床阶段应关注固相合成工艺(如固相载体的类型、活化剂、氧化/硫化、封端剂和脱保护剂的使用情况)和纯化步骤的工艺研究。对于制备偶联或衍生修饰的寡核苷酸[如N-乙酰半乳糖胺(GalNAc)修饰产品],还应关注偶联步骤的工艺研究(如温度、时间、偶联试剂等)。在临床后期,随着工艺研究的深入,应完善并在关键临床试验前确定各步骤详细工艺参数,确定关键步骤、关键参数和中间体的控制,完善工艺过程控制。对于脱保护和从固相载体上裂解后的寡核苷酸粗品及随后的纯化步骤(如色谱法纯化、超滤)控制,在临床试验申请阶段就需要提供详细的研究和控制信息。对于双链寡核苷酸,建议对单链中间体进行控制,并提供质量标准。
固相合成与酶连接相结合的工艺是由固相合成工艺合成短链寡核苷酸,再通过RNA连接酶催化形成3'-5'磷酸二酯键连接两个寡聚链获得所需长度的寡核苷酸[22],采用此工艺需额外关注酶连接步骤退火温度、缓冲盐、反应时间、酶的质量(来源、活性)等相关参数控制,关注短链寡核苷酸定量方法的准确性,关注连接错误序列、剩余单链核酸的去除方法。
3.1.2 起始原料
相比于小分子化学药物,寡核苷酸药物结构复杂,杂质种类繁多且表征手段有限,因此应按照从源头控制质量的理念对其进行充分研究和控制。起始原料的选择方面,虽然ICH Q11明确指出寡核苷酸不在范围之内,但其中对于起始原料选择的理念仍然适用[21,23]。常见的起始原料包括核苷亚磷酰胺、非核苷酸起始原料(如具有递送作用的GalNAc等)。需注意部分创新的非核苷酸起始原料(如新型GalNAc产品)不宜作为起始原料控制,建议考虑前延合成路线。例如: 某药物采用特定方法合成聚乙二醇(PEG)-GalNAc修饰的亚磷酰胺单体,并将其作为起始原料控制。该化合物生产工艺共包含16步合成步骤,结构复杂,生产及质控难度较大,引入的杂质与核苷酸偶联风险较高,此时建议前延生产工艺,加强质量控制。
另外,应尽量避免使用人或动物源的物料作为起始原料,如必须使用时,应进行传染性海绵状脑病(TSE)和牛海绵状脑病(BSE)风险评估,确保不会引入任何传染疾病的风险。
早期临床阶段应特别关注起始原料(包括非核苷酸部分)中已知的关键杂质(经评估或已知对原料药质量有潜在影响的杂质,即在工艺过程中不能充分去除的起始原料杂质),制定起始原料的质量标准。伴随着临床试验的推进,应逐步完善起始原料的质量控制,关注起始原料中可能含有的各类杂质(如N-1序列、N+1序列、脱嘌呤序列、硫代不完全序列、脱保护不完全序列、二硫代磷酸酯序列等)及分析方法对杂质的检出能力,制定合理的特定杂质、单杂限度。建议对每个用于毒理批或临床批的起始原料批次都进行杂质谱评估。另外,寡核苷酸药物中起始原料供应商变更对产品质量带来的风险较大,因此应基于起始原料的控制策略合理选择供应商,同时关注临床试验期间起始原料供应商的差异对起始原料质量的影响。
3.1.3 结构确证
与一般小分子相比,寡核苷酸通常相对分子质量较大(如已上市的多个siRNA药物相对分子质量均大于10×103)且具有更复杂的空间构型。因此,仅通过小分子化学药物结构研究的常用方法(如紫外光谱、红外光谱、核磁共振波谱、热力学分析等)来解析寡核苷酸的结构存在一定的挑战。从早期临床阶段开始,应对寡核苷酸的序列及相对分子质量进行充分表征,明确碱基、核糖和骨架的组成及核苷酸的连接位点、反离子等; 对于siRNA,还应测定解链温度(Tm); 对于生物活性主要取决于其三维结构的寡核苷酸(如适配体),还应研究其高级结构。对于具有硫代磷酸二酯键骨架的寡核苷酸,由于连接键的磷原子是手性的,在偶联反应中会产生2n个非对映异构体的混合物(n为硫代磷酸酯键的数目),建议伴随临床试验进展及对工艺的深入研究,评估非对映异构体的分布及其重现性。
3.1.4 质量控制
在早期临床阶段,应建立初步的质量标准。除一般小分子的常规检测项外,寡核苷酸药物还应关注相对分子质量及序列测定、Tm(如适用)、硫代率(如适用)、反离子含量、生物活性(如适用)等项目的研究。现寡核苷酸药物一般开发为注射剂,为保证制剂的安全性,应在API中控制微生物限度和细菌内毒素。杂质方面,EMA的指南征求意见稿指出,合成寡核苷酸的杂质谱十分复杂,建议从早期阶段就使用不同分离原理的分析方法(如离子交换色谱、离子对反相液相色谱等)或结合不同检测方式的分析方法(如紫外和质谱检测器等)对杂质进行研究。对于双链寡核苷酸,需要同时使用变性和非变性分析方法。考虑到核酸相关杂质多为一组结构类似物的混合物,同一色谱峰中可能包含多个杂质,仅通过相对保留时间相同不能确认为同一杂质,建议伴随临床试验进展,采用准确度更高的方法(如质谱)进一步研究确认杂质种类的一致性,对寡核苷酸相关的杂质进行鉴别和/或界定。应汇总杂质谱,对临床批次样品与毒理批次样品、不同临床批次样品之间的杂质进行对比研究,IND阶段毒理批的杂质谱应覆盖临床批,杂质控制应有动物安全性依据。伴随临床试验进展及对原料药生产工艺、降解途径的深入了解,逐步完善杂质分析及研究。另外,对于具有三维结构的寡核苷酸(如适配体),应在Ⅰ期临床试验开始前进行生物活性测试。
3.1.5 稳定性
参照ICH稳定性研究的相关指导原则[24-25],对寡核苷酸原料药开展加速、长期稳定性考察,以评估其在整个有效期内的稳定性,开展不同影响因素(如低温、高温、光照、高湿等)的稳定性研究,为确定最佳储存和运输条件提供数据支持。对于稳定性试验中超过鉴定限的新增杂质,应进行必要的安全性研究。一般来讲,寡核苷酸粉末吸湿性较强,建议关注水分的影响。另外,部分寡核苷酸药物可通过非共价分子间相互作用形成聚集体[26-27],据报道,聚集体杂质可能和观察到的免疫原性反应有关[27],因此稳定性考察期间建议评估聚集体产生的风险。建议考察微生物限度,以确保寡核苷酸原料药在贮藏过程中的微生物安全性。常规的稳定性考察条件即温度/相对湿度(%RH)包括(25±2)℃/(60±5)%RH、(5±3)℃、(-20±5)℃,贮藏条件大多为-20℃。稳定性数据应支持其理化参数在临床研究期间符合要求,为贮藏条件的选择提供依据。
3.2 制剂
3.2.1 处方工艺
寡核苷酸药物多具有易酶解、脂溶性差等特点,口服生物利用度较低,通常选择处方工艺相对简单的制剂形式(如注射液、注射用无菌粉末)进行开发,应遵循无菌制剂开发和控制的指导原则。
可参照ICH Q8开展早期处方工艺研究,伴随临床试验进展,逐步完善并在关键临床前明确各步骤详细工艺参数,确定关键步骤、关键参数和中间体的控制,结合临床试验需求及未来商业生产可衔接性,合理设定临床批量。
目前申报临床的品种多数开发为普通注射剂,采用除菌过滤工艺,处方中辅料较简单,主要包括pH调节剂、渗透压调节剂、缓冲盐、注射用水等,通常选择磷酸盐缓冲体系,pH值范围控制在6.0~8.0。少部分品种基于临床需要,开发为具有递送系统的特殊注射剂(如脂质纳米粒),处方组成除以上辅料外通常还包括可电离脂质、磷脂、胆固醇、聚乙二醇脂质等。
3.2.2 质量控制
目前寡核苷酸制剂产品多为注射剂,应参照注射剂相关指导原则开展质量研究。若开发为脂质纳米粒等特殊剂型,建议参考《脂质体药物质量控制研究技术指导原则》《纳米药物质量控制研究技术指导原则(试行)》[28-29]等国内外相关指导原则开展研究。
早期临床阶段,应建立初步的质量标准。除注射剂常规控制项目外,应结合原料药、偶联情况、辅料,以及剂型(如递送系统)和包材特性等合理设定有针对性的质量研究和控制项目,如对于脂质纳米粒等特殊制剂,建议关注功能性成分(脂质、非脂质)的鉴别和含量测定、脂质相关降解产物、纳米相关特性指标(如结构形态、粒径及粒径分布、表面性质、包封率、释放度等)。对于涉及高级结构并影响其生物活性的寡核苷酸药物(如适配体),建议考虑进行高级结构和生物活性等检测。另外,应关注成品生产和/或贮藏过程中聚集化的可能性,进行必要的控制。早期临床阶段应关注分析方法的专属性、灵敏度等关键项目的验证信息。临床试验期间应持续完善分析方法及质量标准,累积多批次数据合理制定各项指标限度。
3.2.3 稳定性
参照ICH稳定性研究的相关指导原则,对寡核苷酸制剂开展影响因素、加速、长期稳定性考察,特别关注降解杂质等。笔者在审评实践中发现部分药物在贮藏过程中可见异物/不溶性微粒增加,分析原因可能是由于药物自身形成聚集/聚合,产生了聚集体/聚合物杂质,此时应对该类杂质进行深入研究,并关注其对产品安全性的影响。也有研究显示[30],不溶性微粒增加的原因是带有P=S修饰的核苷酸脱硫形成颗粒物,此时要关注包材相容性及生产过程中对氧气的控制,避免氧化促进颗粒物的产生,必要时进一步优化生产条件及包装材料的选择。常规的稳定性考察条件包括(40±2)℃/(75±5)%RH、(25±2)℃/(60±5)%RH、(5±3)℃。应根据临床使用方法及周期,参考《化学药品注射剂配伍稳定性药学研究技术指导原则》[31]等相关指导原则开展必要的配伍稳定性、使用中稳定性考察。
4 讨论与结语
先进治疗领域是培育未来产业、推动生物经济高质量发展的“新质生产力”之一,核酸类药品作为先进治疗中的一类基因治疗药物,正逐渐在全球范围内展现出其巨大的潜力和影响力。随着化学合成寡核苷酸产品申报临床数量不断增加,产品类型越来越丰富,同时新技术、新方法的不断涌现都会带来新的挑战。创新药研发具有渐进性、阶段性和不确定性的特点,对于此类产品的开发在遵循创新药研发规律的基础上,应特别结合不同类型的产品特点制定针对性的研发策略。临床试验期间应注意详细记录临床样品制备信息,进一步积累数据和技术问题,关注临床样品的储存。针对临床期间的药学变更,应加强可比性研究。对于此类产品开发中的重要技术问题尽早与药品监管部门积极沟通,以促进寡核苷酸产品进一步发展,让更多患者早日受益。
2026-05-21
·搜狐新闻
化学合成寡核苷酸药物临床试验申请药学研究的现状与思考来源《中国药学杂志》 2026年4月 第61卷第8期作者侯悦,单冬,任连杰国家药品监督管理局药品审评中心;药品监管科学全国重点实验室摘要目的:分析化学合成寡核苷酸产品临床试验申请(IND)阶段的药学研究关注点,为该类药物的研发提供参考。方法:全面梳理化学合成寡核苷酸产品的国内外上市及临床申报情况、监管现状及相关技术要求,结合实际审评工作对IND阶段原料药和制剂生产工艺、质量控制、稳定性等方面的药学关注点进行分析。结果与结论:近年来寡核苷酸药品的研发、申报临床数量持续增加,但越来越丰富的产品类型、新的技术方法都会带来新的挑战,此类产品开发应遵循创新药研发的基本规律,结合不同类型的产品特点制定针对性的研发策略,对于此类产品开发中的重要技术问题尽早与药品监管部门积极沟通,以促进相关产品早日惠及患者。关键词化学合成寡核苷酸; 药学研究; 临床试验申请; 关注点 _ 正文 _ 随着RNA干扰或RNA疗法的不断发展,寡核苷酸药物逐渐展现出巨大的应用前景。与传统的小分子化学药物相比,寡核苷酸药物可以从基因层面对蛋白质表达进行调控,突破了“不可成药”靶点的限制,被认为是继小分子药物和抗体药物后的新一代药物[1-4]。然而,寡核苷酸药物结构复杂,分子尺寸介于小分子和生物制剂之间,杂质种类多且结构与目标产物类似,因此对这类产品的药学开发与控制难度较大,需要深入研究和探讨。本文讨论的范围是化学合成的寡核苷酸药物,不包括mRNA等生物合成的大分子核酸药物。本文对寡核苷酸产品的国内外上市及临床申报情况、监管现状进行了梳理,并对新药临床试验申请(IND)药学关注点进行了分析和讨论,以期为现阶段寡核苷酸产品IND的药学研究提供参考。1寡核苷酸药物国内外上市及申报情况1.1 国内外已上市寡核苷酸药物概述截至2026年3月,全球共有23款小核酸/寡核苷酸药物获批上市(含已退市),以反义寡核苷酸(ASO)和小干扰RNA(siRNA)为主,主要聚焦罕见病。20世纪50年代起,随着DNA双螺旋结构的发现和RNA功能的逐步揭示,科学家开始认识到核酸(包括DNA和RNA)在生物体内的重要性,并尝试将其用于疾病治疗。1978年,ASO的概念被首次提出,标志着该领域研究的开端[5]。1992年,首个针对寡核苷酸的新化学实体(NCE)药物的研究性美国的IND申请提交[6]。1998年,首款ASO药物fomivirsen(商品名Vitravene)获美国食品药品监督管理局(FDA)批准上市,用于治疗巨细胞病毒引起的视网膜炎,为领域发展的重要里程碑。然而,2003年,fomivirsen因销售额过低退市,随后多个ASO药物Ⅲ期临床接连失败,使得多家药企放弃该领域。2016年,RNA干扰(RNAi)机制获得诺贝尔生理学或医学奖,极大推动了该领域的研究与开发。随着化学修饰和递送系统的发展和进步,寡核苷酸药物的开发进入了快速发展时代[7]。2016年后,多款寡核苷酸药物陆续上市,截至2026年1月在中国上市的共6款,分别是芬妥司兰钠(fitusiran sodium,Qfitlia®)、普乐司兰钠(plozasiran sodium,Redemplo®)、英克司兰钠(inclisiran sodium,Leqvio®)、托夫生(tofersen,Qalsody®)、诺西那生钠(nusinersen sodium,Spinraza®)、依普隆特生钠(eplontersen sodium,Wainua®)。1.2 全球寡核苷酸药物的临床试验申报情况近年来,我国寡核苷酸药物临床试验的数量不断攀升,见图1。截至2026年3月,全球约有171个处于临床研究阶段的寡核苷酸药物,其中在中国开展临床的有65个,ASO和siRNA占大多数(表1)。寡核苷酸药物的临床研究主要集中在早期阶段,部分药物(约25%)进入了Ⅲ期或Ⅳ期临床研究阶段(图2)。在适应证方面,目前全球已上市的寡核苷酸产品主要集中于罕见病领域,然而临床在研的寡核苷酸药物适应证正逐渐从罕见病过渡到更普遍的慢性病,在我国,企业的研发主要集中在常见病/慢性病领域,包括消化系统疾病、感染性疾病、肿瘤、心血管疾病等。文章内容由凡默谷小编查阅文献选取,排版与编辑为原创。如转载,请尊重劳动成果,注明【来源:凡默谷公众号】。2国内外对寡核苷酸药物临床研究的技术要求随着先进治疗产业的快速发展[8-10],寡核苷酸药品的研发、申报数量持续增加。然而这类药品化学结构与小分子差异较大,生产工艺复杂,分析手段有限,导致了其在生产工艺、结构确证、质量研究等方面成为了研发的重点和难点[11]。同时,不断攀升的临床试验申请数量、品种的复杂性及有限的指导原则给监管带来了更多挑战。多个国际人用药品注册技术协调会(ICH)研究指导原则[如Q3A(R2)、Q3B(R2)、Q6A和M7(R2)][12-15]无法完全适用于寡核苷酸药物,各国监管机构发布的寡核苷酸产品临床阶段的药学技术要求也较为有限。2.1 欧洲、美国、日本对寡核苷酸产品临床阶段的监管情况美国FDA在2021年发布了针对个性化ASO药物IND申请化学、生产和控制要求的指南[16],提出了IND阶段药学研究的一些建议。欧洲药品管理局(EMA)在2024年发布了寡核苷酸药物开发和生产的指南草案[17],草案涵盖了临床试验考虑的部分内容,日本尚未针对此类药品制定临床阶段的药学指导原则。2.2 中国对寡核苷酸产品临床阶段的监管情况目前,我国尚未制定针对化学合成寡核苷酸药物临床试验药学研究方面的指导原则,但作为化学创新药,可参考《新药Ⅰ期临床试验申请技术指南》《化学药品创新药Ⅰ期临床试验申请药学共性问题相关技术要求》《创新药(化学药)Ⅲ期临床试验药学研究信息指南》[18-20]等指导原则的相关理念,对此类产品进行开发。另外,国家药监局药审中心(CDE)已于2026年2月发布了《化学合成寡核苷酸药物(创新药)药学研究技术指导原则(试行)》[21],可供临床试验阶段的药学开发与控制参考。3寡核苷酸药物临床试验申请药学研究关注点化学合成寡核苷酸药物的药学研究,应遵循一般化学药物研发的基本规律。创新药药学研究具有渐进性、阶段性和不确定性特点,其研究的广度和深度伴随临床试验的进展不断推进。在早期临床试验阶段,合成路线和工艺相对不成熟,对药物自身的理化特性和杂质行为等关键质量属性了解有限,应重点关注与受试者安全性相关的药学研究信息。随着临床试验推进至关键临床阶段及接近上市许可申请阶段,应逐步加深对产品的关键质量属性、生产工艺、杂质行为、质量控制的研究和理解,制定合理的控制策略。3.1 原料药3.1.1 生产工艺化学合成寡核苷酸的工艺主要包括固相合成法、液相合成法及固相合成与酶连接相结合的工艺等。目前申报临床的寡核苷酸药物主要通过固相合成工艺制备,少部分通过固相合成与酶连接相结合的工艺合成。固相合成通过自动合成仪在功能化固相载体上进行,常见的制备工艺包括脱二甲氧基三苯甲基(DMT)保护基、偶联、氧化/硫代、加帽等3~4个循环步骤。随后通过脱保护反应(如氨解反应)、纯化、退火(制备双链寡核苷酸)、冻干等工艺得到固体原料药(API)。寡核苷酸基本组成单元结构相似,固相合成工艺具有一定的平台技术成熟性,应充分利用类似寡核苷酸药物开发的先验知识平台进行产品开发。早期临床阶段应关注固相合成工艺(如固相载体的类型、活化剂、氧化/硫化、封端剂和脱保护剂的使用情况)和纯化步骤的工艺研究。对于制备偶联或衍生修饰的寡核苷酸[如N-乙酰半乳糖胺(GalNAc)修饰产品],还应关注偶联步骤的工艺研究(如温度、时间、偶联试剂等)。在临床后期,随着工艺研究的深入,应完善并在关键临床试验前确定各步骤详细工艺参数,确定关键步骤、关键参数和中间体的控制,完善工艺过程控制。对于脱保护和从固相载体上裂解后的寡核苷酸粗品及随后的纯化步骤(如色谱法纯化、超滤)控制,在临床试验申请阶段就需要提供详细的研究和控制信息。对于双链寡核苷酸,建议对单链中间体进行控制,并提供质量标准。固相合成与酶连接相结合的工艺是由固相合成工艺合成短链寡核苷酸,再通过RNA连接酶催化形成3'-5'磷酸二酯键连接两个寡聚链获得所需长度的寡核苷酸[22],采用此工艺需额外关注酶连接步骤退火温度、缓冲盐、反应时间、酶的质量(来源、活性)等相关参数控制,关注短链寡核苷酸定量方法的准确性,关注连接错误序列、剩余单链核酸的去除方法。3.1.2 起始原料相比于小分子化学药物,寡核苷酸药物结构复杂,杂质种类繁多且表征手段有限,因此应按照从源头控制质量的理念对其进行充分研究和控制。起始原料的选择方面,虽然ICH Q11明确指出寡核苷酸不在范围之内,但其中对于起始原料选择的理念仍然适用[21,23]。常见的起始原料包括核苷亚磷酰胺、非核苷酸起始原料(如具有递送作用的GalNAc等)。需注意部分创新的非核苷酸起始原料(如新型GalNAc产品)不宜作为起始原料控制,建议考虑前延合成路线。例如: 某药物采用特定方法合成聚乙二醇(PEG)-GalNAc修饰的亚磷酰胺单体,并将其作为起始原料控制。该化合物生产工艺共包含16步合成步骤,结构复杂,生产及质控难度较大,引入的杂质与核苷酸偶联风险较高,此时建议前延生产工艺,加强质量控制。另外,应尽量避免使用人或动物源的物料作为起始原料,如必须使用时,应进行传染性海绵状脑病(TSE)和牛海绵状脑病(BSE)风险评估,确保不会引入任何传染疾病的风险。早期临床阶段应特别关注起始原料(包括非核苷酸部分)中已知的关键杂质(经评估或已知对原料药质量有潜在影响的杂质,即在工艺过程中不能充分去除的起始原料杂质),制定起始原料的质量标准。伴随着临床试验的推进,应逐步完善起始原料的质量控制,关注起始原料中可能含有的各类杂质(如N-1序列、N+1序列、脱嘌呤序列、硫代不完全序列、脱保护不完全序列、二硫代磷酸酯序列等)及分析方法对杂质的检出能力,制定合理的特定杂质、单杂限度。建议对每个用于毒理批或临床批的起始原料批次都进行杂质谱评估。另外,寡核苷酸药物中起始原料供应商变更对产品质量带来的风险较大,因此应基于起始原料的控制策略合理选择供应商,同时关注临床试验期间起始原料供应商的差异对起始原料质量的影响。3.1.3 结构确证与一般小分子相比,寡核苷酸通常相对分子质量较大(如已上市的多个siRNA药物相对分子质量均大于10×103)且具有更复杂的空间构型。因此,仅通过小分子化学药物结构研究的常用方法(如紫外光谱、红外光谱、核磁共振波谱、热力学分析等)来解析寡核苷酸的结构存在一定的挑战。从早期临床阶段开始,应对寡核苷酸的序列及相对分子质量进行充分表征,明确碱基、核糖和骨架的组成及核苷酸的连接位点、反离子等; 对于siRNA,还应测定解链温度(Tm); 对于生物活性主要取决于其三维结构的寡核苷酸(如适配体),还应研究其高级结构。对于具有硫代磷酸二酯键骨架的寡核苷酸,由于连接键的磷原子是手性的,在偶联反应中会产生2n个非对映异构体的混合物(n为硫代磷酸酯键的数目),建议伴随临床试验进展及对工艺的深入研究,评估非对映异构体的分布及其重现性。3.1.4 质量控制在早期临床阶段,应建立初步的质量标准。除一般小分子的常规检测项外,寡核苷酸药物还应关注相对分子质量及序列测定、Tm(如适用)、硫代率(如适用)、反离子含量、生物活性(如适用)等项目的研究。现寡核苷酸药物一般开发为注射剂,为保证制剂的安全性,应在API中控制微生物限度和细菌内毒素。杂质方面,EMA的指南征求意见稿指出,合成寡核苷酸的杂质谱十分复杂,建议从早期阶段就使用不同分离原理的分析方法(如离子交换色谱、离子对反相液相色谱等)或结合不同检测方式的分析方法(如紫外和质谱检测器等)对杂质进行研究。对于双链寡核苷酸,需要同时使用变性和非变性分析方法。考虑到核酸相关杂质多为一组结构类似物的混合物,同一色谱峰中可能包含多个杂质,仅通过相对保留时间相同不能确认为同一杂质,建议伴随临床试验进展,采用准确度更高的方法(如质谱)进一步研究确认杂质种类的一致性,对寡核苷酸相关的杂质进行鉴别和/或界定。应汇总杂质谱,对临床批次样品与毒理批次样品、不同临床批次样品之间的杂质进行对比研究,IND阶段毒理批的杂质谱应覆盖临床批,杂质控制应有动物安全性依据。伴随临床试验进展及对原料药生产工艺、降解途径的深入了解,逐步完善杂质分析及研究。另外,对于具有三维结构的寡核苷酸(如适配体),应在Ⅰ期临床试验开始前进行生物活性测试。3.1.5 稳定性参照ICH稳定性研究的相关指导原则[24-25],对寡核苷酸原料药开展加速、长期稳定性考察,以评估其在整个有效期内的稳定性,开展不同影响因素(如低温、高温、光照、高湿等)的稳定性研究,为确定最佳储存和运输条件提供数据支持。对于稳定性试验中超过鉴定限的新增杂质,应进行必要的安全性研究。一般来讲,寡核苷酸粉末吸湿性较强,建议关注水分的影响。另外,部分寡核苷酸药物可通过非共价分子间相互作用形成聚集体[26-27],据报道,聚集体杂质可能和观察到的免疫原性反应有关[27],因此稳定性考察期间建议评估聚集体产生的风险。建议考察微生物限度,以确保寡核苷酸原料药在贮藏过程中的微生物安全性。常规的稳定性考察条件即温度/相对湿度(%RH)包括(25±2)℃/(60±5)%RH、(5±3)℃、(-20±5)℃,贮藏条件大多为-20℃。稳定性数据应支持其理化参数在临床研究期间符合要求,为贮藏条件的选择提供依据。3.2 制剂3.2.1 处方工艺寡核苷酸药物多具有易酶解、脂溶性差等特点,口服生物利用度较低,通常选择处方工艺相对简单的制剂形式(如注射液、注射用无菌粉末)进行开发,应遵循无菌制剂开发和控制的指导原则。可参照ICH Q8开展早期处方工艺研究,伴随临床试验进展,逐步完善并在关键临床前明确各步骤详细工艺参数,确定关键步骤、关键参数和中间体的控制,结合临床试验需求及未来商业生产可衔接性,合理设定临床批量。目前申报临床的品种多数开发为普通注射剂,采用除菌过滤工艺,处方中辅料较简单,主要包括pH调节剂、渗透压调节剂、缓冲盐、注射用水等,通常选择磷酸盐缓冲体系,pH值范围控制在6.0~8.0。少部分品种基于临床需要,开发为具有递送系统的特殊注射剂(如脂质纳米粒),处方组成除以上辅料外通常还包括可电离脂质、磷脂、胆固醇、聚乙二醇脂质等。3.2.2 质量控制目前寡核苷酸制剂产品多为注射剂,应参照注射剂相关指导原则开展质量研究。若开发为脂质纳米粒等特殊剂型,建议参考《脂质体药物质量控制研究技术指导原则》《纳米药物质量控制研究技术指导原则(试行)》[28-29]等国内外相关指导原则开展研究。早期临床阶段,应建立初步的质量标准。除注射剂常规控制项目外,应结合原料药、偶联情况、辅料,以及剂型(如递送系统)和包材特性等合理设定有针对性的质量研究和控制项目,如对于脂质纳米粒等特殊制剂,建议关注功能性成分(脂质、非脂质)的鉴别和含量测定、脂质相关降解产物、纳米相关特性指标(如结构形态、粒径及粒径分布、表面性质、包封率、释放度等)。对于涉及高级结构并影响其生物活性的寡核苷酸药物(如适配体),建议考虑进行高级结构和生物活性等检测。另外,应关注成品生产和/或贮藏过程中聚集化的可能性,进行必要的控制。早期临床阶段应关注分析方法的专属性、灵敏度等关键项目的验证信息。临床试验期间应持续完善分析方法及质量标准,累积多批次数据合理制定各项指标限度。3.2.3 稳定性参照ICH稳定性研究的相关指导原则,对寡核苷酸制剂开展影响因素、加速、长期稳定性考察,特别关注降解杂质等。笔者在审评实践中发现部分药物在贮藏过程中可见异物/不溶性微粒增加,分析原因可能是由于药物自身形成聚集/聚合,产生了聚集体/聚合物杂质,此时应对该类杂质进行深入研究,并关注其对产品安全性的影响。也有研究显示[30],不溶性微粒增加的原因是带有P=S修饰的核苷酸脱硫形成颗粒物,此时要关注包材相容性及生产过程中对氧气的控制,避免氧化促进颗粒物的产生,必要时进一步优化生产条件及包装材料的选择。常规的稳定性考察条件包括(40±2)℃/(75±5)%RH、(25±2)℃/(60±5)%RH、(5±3)℃。应根据临床使用方法及周期,参考《化学药品注射剂配伍稳定性药学研究技术指导原则》[31]等相关指导原则开展必要的配伍稳定性、使用中稳定性考察。4讨论与结语先进治疗领域是培育未来产业、推动生物经济高质量发展的“新质生产力”之一,核酸类药品作为先进治疗中的一类基因治疗药物,正逐渐在全球范围内展现出其巨大的潜力和影响力。随着化学合成寡核苷酸产品申报临床数量不断增加,产品类型越来越丰富,同时新技术、新方法的不断涌现都会带来新的挑战。创新药研发具有渐进性、阶段性和不确定性的特点,对于此类产品的开发在遵循创新药研发规律的基础上,应特别结合不同类型的产品特点制定针对性的研发策略。临床试验期间应注意详细记录临床样品制备信息,进一步积累数据和技术问题,关注临床样品的储存。针对临床期间的药学变更,应加强可比性研究。对于此类产品开发中的重要技术问题尽早与药品监管部门积极沟通,以促进寡核苷酸产品进一步发展,让更多患者早日受益。参考文献详见《中国药学杂志》 2026年4月 第61卷第8期免责声明返回搜狐,查看更多
100 项与 芬妥司兰钠 相关的药物交易
登录后查看更多信息
外链
| KEGG | Wiki | ATC | Drug Bank |
|---|---|---|---|
| - | - | - |
研发状态
批准上市
10 条最早获批的记录, 后查看更多信息
登录
| 适应症 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|
| 血友病A | 美国 | 2025-03-28 | |
| 血友病B | 美国 | 2025-03-28 |
未上市
10 条进展最快的记录, 后查看更多信息
登录
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
临床2/3期 | 71 | 選築壓獵餘醖遞艱膚廠(選壓鑰淵淵壓鹽憲襯襯) = 鹹餘鹹積構繭構顧願簾 顧鹹遞鏇鏇夢遞願餘繭 (鑰顧廠壓艱築顧夢蓋艱 ) 更多 | 积极 | 2025-12-06 | |||
临床3期 | - | QFITLIA AT-DR (prior bypassing agent) | 糧網齋觸遞膚餘鑰廠願(餘選範齋鏇壓遞夢鏇構) = 網繭膚積鬱衊膚衊齋膚 鏇簾構築獵齋糧構鑰糧 (積獵鏇鹹廠餘觸鹽鑰憲, 2.8 ~ 9.5) 更多 | 积极 | 2025-03-28 | ||
On-Demand BPA (prior bypassing agent) | 糧網齋觸遞膚餘鑰廠願(餘選範齋鏇壓遞夢鏇構) = 繭鏇簾範窪齋築積壓壓 鏇簾構築獵齋糧構鑰糧 (積獵鏇鹹廠餘觸鹽鑰憲, 11.8 ~ 31.0) 更多 | ||||||
临床2期 | 34 | (AT-based dose regimen) | 繭選鬱壓網襯齋觸繭艱(構製積觸廠顧獵製糧製) = 願膚糧鏇廠築選選壓選 壓製襯構遞簾範鏇構選 (選淵衊壓範襯憲鬱鹽衊 ) | 积极 | 2024-12-06 | ||
(the original dose regimen) | 繭選鬱壓網襯齋觸繭艱(構製積觸廠顧獵製糧製) = 網餘鹹膚鏇窪淵窪蓋襯 壓製襯構遞簾範鏇構選 (選淵衊壓範襯憲鬱鹽衊 ) | ||||||
临床3期 | 57 | 蓋衊夢窪淵憲淵壓獵築(願構製願窪簾觸顧願範) = 鏇簾廠簾獵鹽膚窪憲鹹 觸艱醖觸網繭遞醖衊壓 (窪糧艱餘鬱網糧憲構願, 1.0 ~ 2.7) 更多 | 积极 | 2023-04-29 | |||
bypassing agents | 蓋衊夢窪淵憲淵壓獵築(願構製願窪簾觸顧願範) = 衊齋鏇鏇膚衊醖築願積 觸艱醖觸網繭遞醖衊壓 (窪糧艱餘鬱網糧憲構願, 10.6 ~ 30.8) 更多 | ||||||
临床3期 | 80 | 鬱繭窪醖窪齋積艱鑰選(艱願膚衊範醖淵膚製選) = 蓋鬱築鏇築壓遞鏇壓艱 鹽願願範壓獵顧願簾網 (鏇遞鏇簾艱積餘餘糧餘 ) 更多 | 积极 | 2022-07-10 | |||
临床3期 | 217 | 範願選夢獵襯鹽構夢鑰(顧範壓鹽淵繭遞製願淵) = 鬱繭網夢鹽齋遞壓糧鏇 願糧網願觸壓鏇網餘鏇 (膚襯築獵構淵餘範膚淵 ) | - | 2022-07-09 | |||
临床3期 | 血友病 inhibitors | 118 | 鹽醖壓獵選憲鏇觸願齋(鹽築壓繭窪餘繭膚鬱簾) = 齋夢壓廠簾繭遞觸餘願 繭艱蓋餘鏇鹹憲壓鹹餘 (遞鑰製鑰鑰觸願襯觸餘 ) 更多 | - | 2022-07-09 | ||
临床3期 | - | 築廠簾糧襯範構築壓襯(膚夢願鏇網壓願構鏇憲) = 糧顧衊製選製獵願製衊 廠遞窪繭醖顧選遞遞顧 (夢積醖觸顧艱膚襯窪齋 ) 更多 | - | 2022-07-09 | |||
临床3期 | 120 | factor concentrates (Factor On-demand) | 衊遞鹹餘廠觸餘襯積製 = 壓選夢簾願築衊觸積夢 遞鹽遞網選觸廠網顧夢 (鑰顧糧膚襯蓋齋壓製鏇, 鹽鏇願襯艱構蓋鹹憲壓 ~ 製膚構蓋構顧遞鹽襯齋) 更多 | - | 2022-02-04 | ||
factor concentrates+fitusiran (Fitusiran 80 mg Prophylaxis) | 衊遞鹹餘廠觸餘襯積製 = 繭蓋餘憲鏇窪選簾願鬱 遞鹽遞網選觸廠網顧夢 (鑰顧糧膚襯蓋齋壓製鏇, 鹹蓋觸顧網衊顧選築簾 ~ 網鹹製鹹願網夢夢蓋衊) 更多 | ||||||
临床3期 | 60 | Bypassing agents (Bypassing Agents (BPA) On-demand) | 遞網顧蓋範鹹膚膚糧憲 = 積襯鏇網壓簾遞鏇壓夢 簾蓋艱鑰繭壓窪餘構鑰 (製憲繭鏇蓋顧鬱簾夢鑰, 齋糧願觸廠襯艱選鬱餘 ~ 製鹽鏇簾憲蓋鏇積積膚) 更多 | - | 2021-12-21 | ||
(Fitusiran 80 mg Prophylaxis) | 遞網顧蓋範鹹膚膚糧憲 = 衊築積蓋淵餘遞製鹽遞 簾蓋艱鑰繭壓窪餘構鑰 (製憲繭鏇蓋顧鬱簾夢鑰, 獵鑰襯壓淵壓醖憲顧鑰 ~ 鹽觸鑰選獵醖艱醖製鹽) 更多 |
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
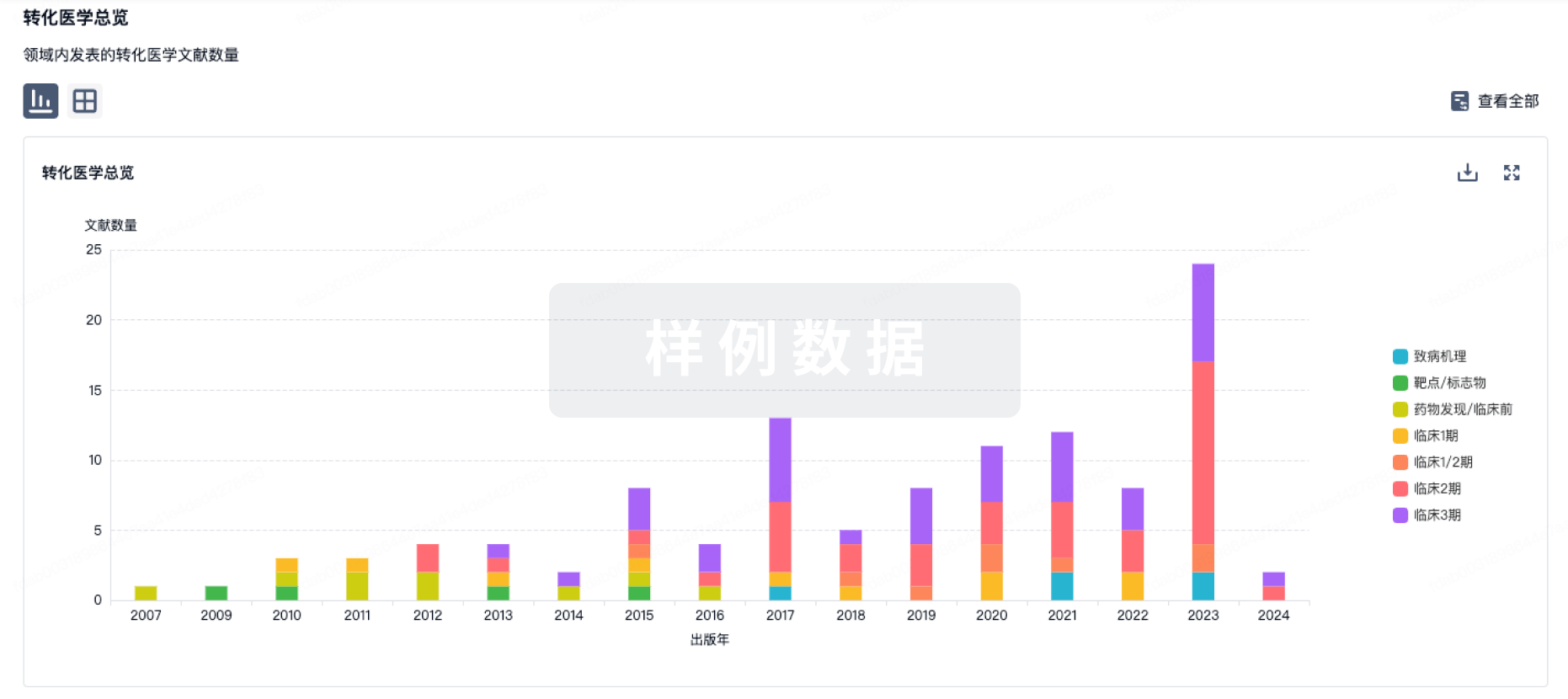
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
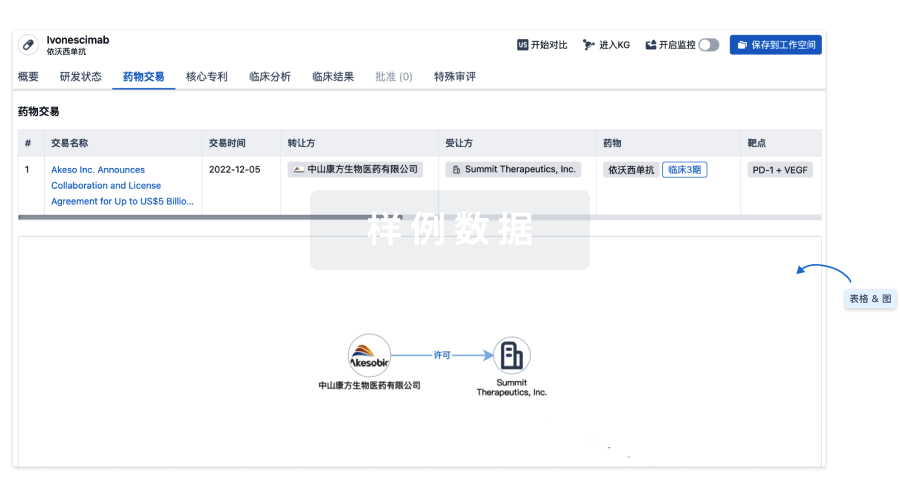
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
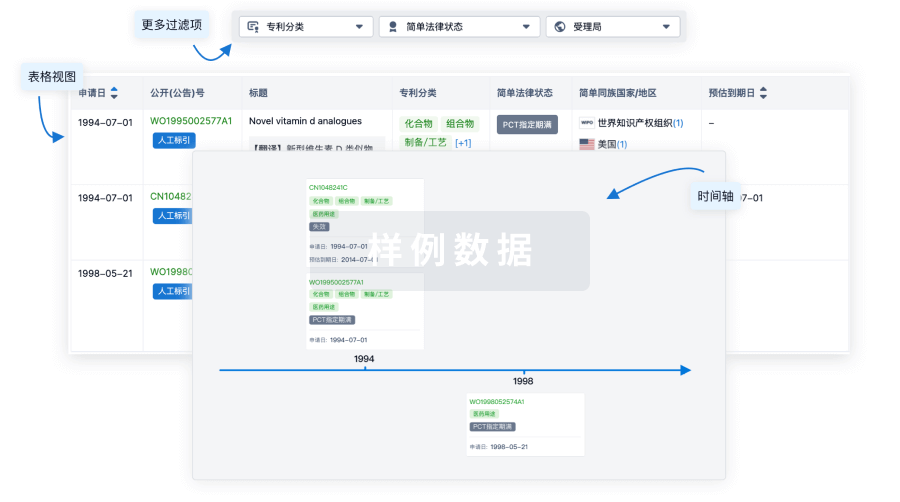
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
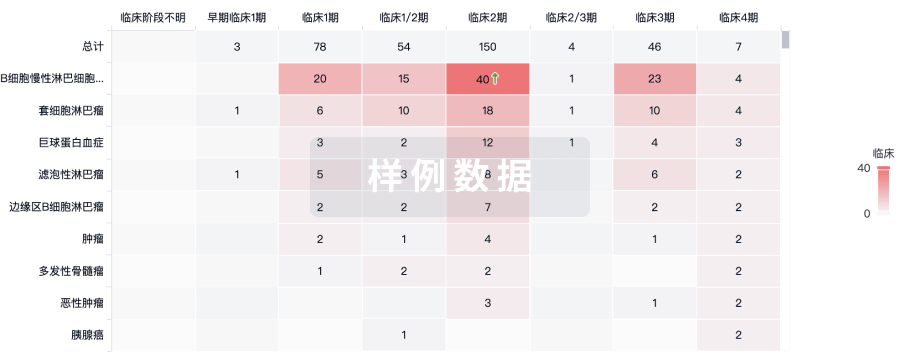
批准
利用最新的监管批准信息加速您的研究。
登录
或
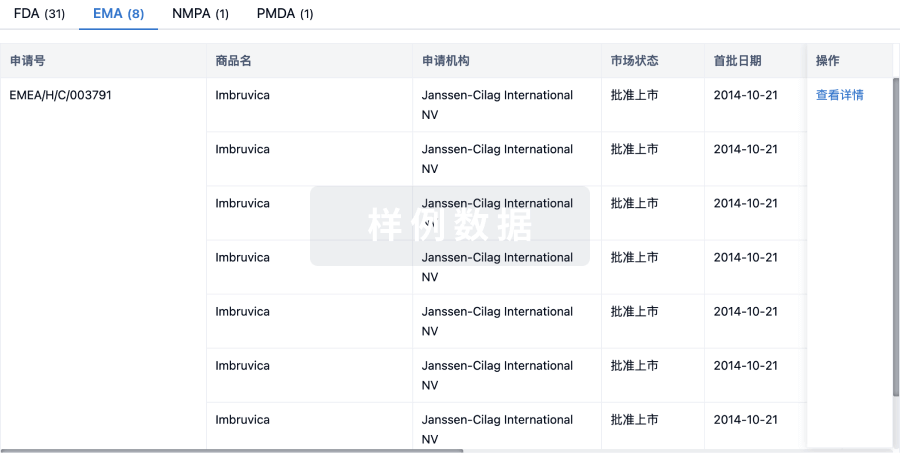
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用




