预约演示
更新于:2026-06-09
Givosiran Sodium
更新于:2026-06-09
概要
基本信息
非在研机构- |
最高研发阶段批准上市 |
首次获批日期 美国 (2019-11-20), |
最高研发阶段(中国)- |
特殊审评突破性疗法 (美国)、孤儿药 (美国)、孤儿药 (韩国)、孤儿药 (澳大利亚)、优先药物(PRIME) (欧盟) |
登录后查看时间轴
结构/序列
使用我们的RNA技术数据为新药研发加速。
登录
或
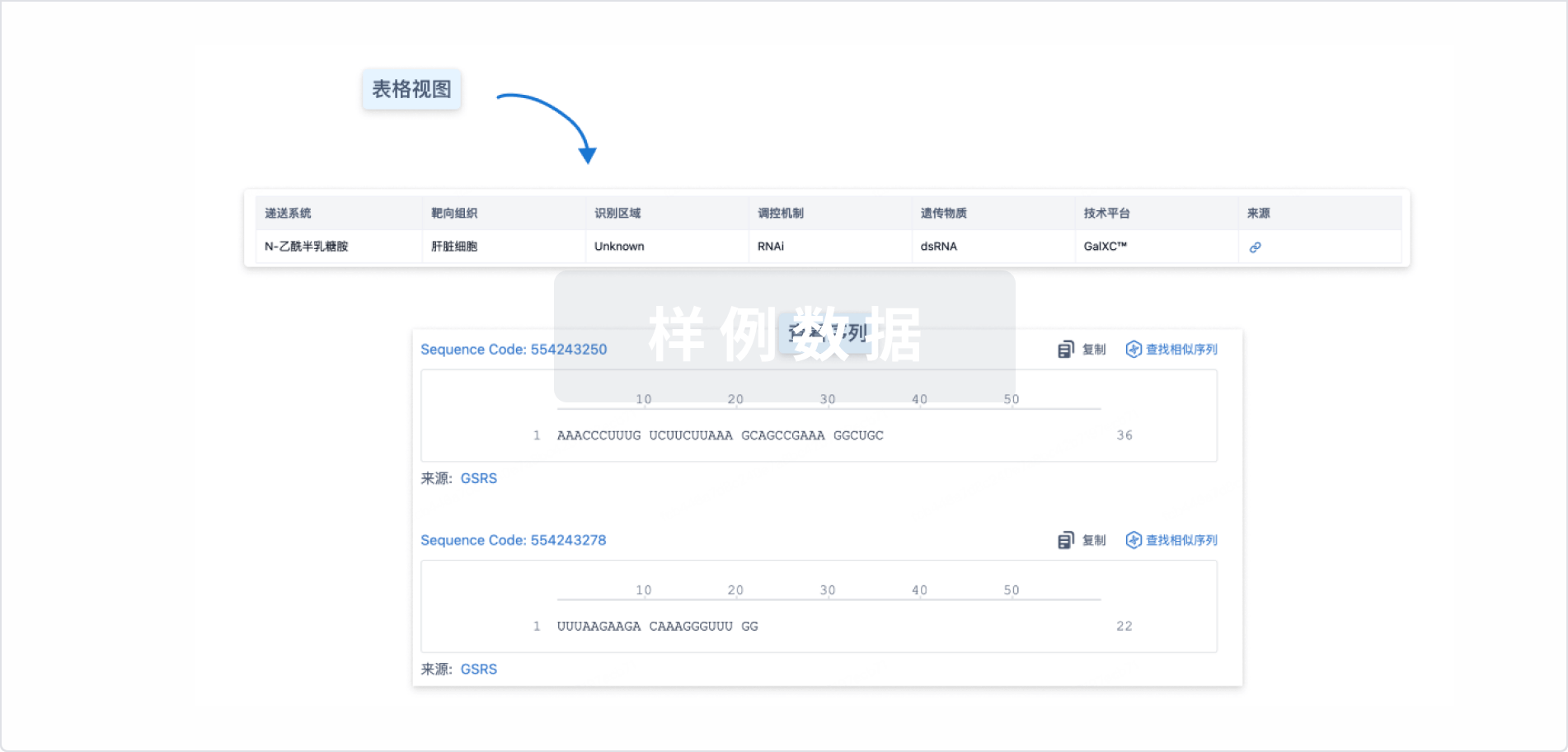
Sequence Code 294634572

来源: *****
Sequence Code 1191632795

来源: *****
关联
6
项与 Givosiran Sodium 相关的临床试验JPRN-jRCT2071200074
Expanded Access Protocol of Givosiran for Patients with Acute Hepatic Porphyria (AHP)
开始日期2021-02-02 |
申办/合作机构- |
NCT03505853
A Drug-Drug Interaction Study to Investigate the Effect of Givosiran on the Pharmacokinetics (PK) of Midazolam, Caffeine, Losartan, Omeprazole, and Dextromethorphan in Patients With Acute Intermittent Porphyria (AIP) Who Are Asymptomatic High Excreters (ASHE)
The purpose of this study is to evaluate the effect of givosiran on the pharmacokinetics of the 5-probe cocktail of midazolam, caffeine, losartan, omeprazole, and dextromethorphan, and their metabolites, in asymptomatic patients with Acute Intermittent Porphyria.
开始日期2018-04-26 |
NCT03338816
ENVISION: A Phase 3 Randomized, Double-blind, Placebo-Controlled Multicenter Study With an Open-label Extension to Evaluate the Efficacy and Safety of Givosiran in Patients With Acute Hepatic Porphyrias
The purpose of this study is to evaluate the effect of subcutaneous givosiran (ALN-AS1), compared to placebo, on the rate of porphyria attacks in patients with Acute Hepatic Porphyrias (AHP).
开始日期2017-11-16 |
100 项与 Givosiran Sodium 相关的临床结果
登录后查看更多信息
100 项与 Givosiran Sodium 相关的转化医学
登录后查看更多信息
100 项与 Givosiran Sodium 相关的专利(医药)
登录后查看更多信息
81
项与 Givosiran Sodium 相关的文献(医药)2026-03-12·CURRENT PHARMACEUTICAL DESIGN
Advances in siRNA-Loaded Nanocarriers: Harnessing Cutting-Edge Technologies for Precision Cancer Treatment
Article
作者: Kurmi, Balak Das ; Patel, Preeti ; Das Gupta, Ghanshyam ; Jindal, Priya ; Aggarwal, Kaushal
Introduction::
Cancer remains a major global health concern characterized by the uncontrolled proliferation
and spread of abnormal cells. Traditional treatment modalities such as chemotherapy, radiotherapy,
and surgery are often associated with limitations, including drug resistance, off-target toxicity, and incomplete
eradication of cancer cells.
Objective::
To explore the potential of small interfering RNA (siRNA)-based therapies in cancer treatment,
focusing on their mechanisms of action, delivery challenges, and the application of nanotechnology to
enhance therapeutic outcomes.
Methods::
This review analyzes recent advancements in RNA interference (RNAi) therapy, particularly siRNA-
based approaches. It highlights delivery barriers, discusses various nanocarrier systems, including lipidbased,
polymeric, and hybrid nanoparticles, and evaluates their roles in improving siRNA stability, intracellular
uptake, and tumor-targeting.
Results::
siRNA offers a highly specific method for silencing disease-related genes at the mRNA level by
guiding the RNA-induced silencing complex (RISC) to degrade target transcripts, thereby inhibiting protein
synthesis. Despite its therapeutic promise, siRNA delivery faces several challenges including poor stability,
limited cellular uptake, and systemic distribution issues. Nanotechnology-based delivery systems have shown
significant progress in addressing these barriers and improving therapeutic outcomes in preclinical studies.
Discussion::
siRNA-based cancer drug delivery provides a targeted and controlled treatment option as an alternative
to conventional treatments. As per the literature, the application of nanotechnology improved the
stability and efficacy of the aforementioned formulations. The reviewed present various in-depth knowledge
about the siRNA-based cancer therapeutics.
Conclusion::
siRNA-based therapeutics represent a promising strategy for targeted cancer therapy due to their
high specificity and ability to reduce off-target toxicity. Nanocarrier systems have greatly enhanced their clinical
viability. However, continued efforts are required to overcome biological barriers and facilitate clinical
translation. This review also summarizes FDA-approved siRNA-based drugs such as Onpattro®, Leqvio®,
Givlaari®, Oxlumo®, Tavnelis®, and Amvuttra®, underscoring the clinical potential of RNAi-based therapies.
2026-02-01·Nucleic Acid Therapeutics
Class-Specific Adverse Events of Patients Treated with Small Interfering RNA Therapeutics: A Disproportionality Analysis of the United States Food and Drug Administration Adverse Event Reporting System Database Based on the MY FAERS Platform
Article
作者: Sun, Yiqi ; Li, Ze ; Wang, Xiaozhen ; Li, Dandan ; Li, Xingang ; Zhang, Lin
Small interfering RNA (siRNA) therapeutics represent a transformative class of drugs, but their class-specific adverse events (CAE-siRNA) remain incompletely characterized. This study aimed to identify and quantify CAE-siRNA associated with U.S. Food and Drug Administration (FDA)-approved siRNA drugs (patisiran, givosiran, vutrisiran, inclisiran, and lumasiran) using real-world pharmacovigilance data, focusing on potential class-wide effects. A disproportionality analysis was conducted using the FDA Adverse Event Reporting System database (2014–2025Q2) accessed via the MY FAERS platform. The reporting odds ratio (ROR) with 95% confidence interval (CI) was calculated, with signals defined by a lower CI >1 and ≥3 cases. Sensitivity analyses included indication-matched populations (IMPs) and exclusion of concomitant medications. Causality was assessed using Bradford Hill criteria. Among 6200 siRNA-treated patients, 45 CAE-siRNA spanning 10 system organ classes were identified. Pain and pain in extremity, fatigue, and gastrointestinal disorders were the most frequently reported. Notably, patisiran was associated with an elevated risk of back pain (ROR: 2.28, 95% CI: 1.84–2.83), whereas givosiran exhibited significant signals for stress (ROR: 5.29, 95% CI: 3.64–7.70) and weight loss (ROR: 2.35, 95% CI: 1.74–3.16). Of particular concern, inclisiran demonstrated strong hepatic toxicity signals (ROR ranging from 9.11 to 86.06) along with discomfort (ROR: 3.60, 95% CI: 1.34–9.65). Sensitivity analyses confirmed robustness across subgroups. Furthermore, causality assessment supported a likely association between the hepatic toxicity and inclisiran. This study identified clinically relevant CAE-siRNA, particularly hepatic toxicity for inclisiran, supporting enhanced monitoring. While disproportionality analyses are hypothesis generating, these findings underscore the need for targeted pharmacovigilance to optimize the safety of this promising drug class.
2025-10-01·ANALYTICA CHIMICA ACTA
Identification of oligonucleotide drug impurities using heart-cutting two-dimensional liquid chromatography-tandem mass spectrometry (2D-LC-MS/MS)
Article
作者: Gao, Lu ; Feng, Hongru ; Li, Wangyu ; Liao, Jiancong ; Zhou, Shiwen ; Tang, He ; Pan, Yuanjiang ; Yang, Xihe
BACKGROUND:
Oligonucleotide-based drugs have gained significant attention as a promising class of therapeutics due to their precise ability to regulate gene expression. However, the presence of impurities in these drugs can compromise their safety, efficacy, and stability. Therefore, the identification and detailed analysis of these impurities are crucial. Traditional methods may struggle to detect subtle impurities, such as oxidation and hydrolysis products, which necessitate the development of more advanced and reliable analytical techniques for oligonucleotide therapeutics.
RESULTS:
In this study, we introduce a novel analytical method that combines heart-cutting two-dimensional liquid chromatography (2D-LC) with tandem mass spectrometry (MS/MS) to effectively separate, analyze, and identify impurities in oligonucleotide-based drugs. The first dimension utilizes anion exchange chromatography (AEX) to separate oligonucleotides based on their negative charge, while the second dimension employs reverse ion-pair chromatography (RIPC) for further purification and compatibility with mass spectrometry. This 2D-LC-MS/MS approach provides a sensitive and accurate means of identifying and quantifying impurities, including oxidation and hydrolysis products. The method was applied to two RNA interference (RNAi) drugs, Givosiran and Patisiran, where 3 and 20 impurities were identified, respectively. Additionally, sequencing analysis using data-dependent acquisition (DDA-MS/MS) enabled the determination of the molecular weight and structural characteristics of these impurities, offering a comprehensive and detailed view of the impurity profiles.
SIGNIFICANCE:
This novel heart-cutting 2D-LC-MS/MS method offers a significant advancement in the analysis of impurities in oligonucleotide-based therapeutics. It provides high sensitivity, enabling the identification of subtle impurities that are often challenging to detect. By applying this technique to RNAi drugs, we demonstrate its potential to enhance the safety, efficacy, and stability of oligonucleotide-based therapies, making it a valuable tool for the pharmaceutical industry.
337
项与 Givosiran Sodium 相关的新闻(医药)2026-06-08
·商图药讯
作者:清风
小核酸赛道,正在上演一场真实的“资本盛宴”。2025年,小核酸领域BD交易总金额已突破300亿美元,创下历史新高。全球已上市小核酸药物总销售额突破71亿美元,同比增长近40%。
凭借直击“不可成药”靶点、极高的研发效率、长效治疗优势等,小核酸药物已被视为继小分子、抗体药物后的第三大药物类型。目前,FDA已批准近20款小核酸药物在全球范围内上市。
不过,由于GalNAc等递送系统的局限性,目前超过90%获批的小核酸药物集中于肝脏靶向,而人类约90%的致病基因却表达于肝外组织。这意味着,阿尔茨海默病、心力衰竭、慢性肾病等大量未满足的临床需求,仍处于核酸药物的“无人区”。因此,走出“肝脏舒适区”,成为小核酸药物下一步的攻坚方向。而这一切的前提,在于肝外递送技术的突破。
GalNAc的荣光与隐忧
小核酸药物是一类由十几个至几十个核苷酸组成的短链核酸分子,通过干预信使RNA(mRNA)的表达,从源头上调控致病蛋白的生成,从基因源头精准干预致病蛋白的生成,实现“治标又治本”的治疗效果。而且小核酸药物理论上可以靶向人类基因组中所有致病基因,这种全新的药物设计逻辑,让许多曾经“不可成药”的靶点迎来了被攻克的可能。
根据作用机制不同,小核酸药物包括RNAi药物(siRNA)、反义寡核苷酸(ASO)、微小RNA(miRNA)、小激活RNA(saRNA)以及核酸适配体等。其中,ASO和siRNA是目前技术最成熟的两大类别。
虽然目前小核酸药物研发如火如荼,且全球已有19款(踢除已退市)小核酸药物获批上市,但小核酸药物的研发却经历多次起落。与小分子、蛋白药物不同,小核酸如果未经制剂化处理,直接进入体内后会被快速降解,无法到达靶向部位。而且小核酸分子携带大量负电荷,且亲水性强,难以穿透带负电荷且为脂质双分子层的细胞膜,到达细胞内部。因此如何将小核酸药物精准送达疾病部位,并保持活性,成为小核酸药物研发成功的关键。
纵观小核酸药物发展史,很大程度上就是递送技术的迭代史。脂质纳米粒(LNP)是小核酸递送首个获得成功的技术平台。2018年,Alnylam的siRNA药物Onpattro(patisiran)成功获FDA批准上市,成为全球首个利用LNP递送技术的小核酸药物,用于治疗遗传性转甲状腺素蛋白淀粉样变性(ATTR-PN),打破了小核酸药物在递送难题凸显和资本相继退出的黑暗时期。LNP可安全、高效将核酸递送至肝脏靶细胞的作用得到有效证明。
作为小核酸递送首个获得成功的平台,LNP虽然解决了核酸易降解、难入胞等难题,但其存在内体逃逸效率低、免疫原性与安全性风险等,例如LNP的脂质成分或封装的核酸可能激活免疫系统,引发炎症反应或细胞因子释放综合征(CRS)等。
为了克服这些局限性,GalNAc(N-乙酰半乳糖胺)偶联技术应运而生。Alnylam公司的脱颖而出,正是源于对这一瓶颈的突破与管线策略的精准落地。
GalNAc 是唾液酸糖蛋白受体(ASGPR)的高亲和力配体,而 ASGPR 在肝细胞膜上高度特异性、高密度表达。这意味着,将GalNAc与siRNA偶联,就能实现对肝脏的精准靶向递送。2019年,Alnylam的Givosiran获批,用于治疗成人急性肝卟啉症(AHP),成为历史上首个获批采用GalNAc偶联技术的siRNA药物。
而GalNAc技术也凭借其卓越的肝脏靶向效率、安全性和用药便利性,成为当前siRNA药物开发的主流和首选(2019年之后获批的siRNA药物均采用了该技术)。其中,Alnylam公司已上市的6款siRNA药物中,5款均应用了GalNAc偶联技术,展现出碾压式的平台化孵化能力。
GalNac递送系统的突破,让小核酸药物实现了高效、低毒的肝脏靶向递送,适应症从罕见病成功扩展至常见病,也催生了多个重磅品种。例如诺华/Alnylam上市的全球首款siRNA超长效降脂药——Leqvio(英克司兰钠,Inclisiran)2025年销售额飙至11.98亿美元,同比增长57%,跻身“重磅炸弹”药物行列。
GalNac递送系统虽然使小核酸药物迎来爆发期,但它只解决了肝脏递送问题。肝脏以外的靶向递送——无论是中枢神经系统、骨骼肌、肾脏还是肺部,仍是制约行业扩容、适应症拓展的核心障碍,目前全球尚未有通过全身给药实现特异性肝外靶向递送的小核酸新药上市,这也成为行业亟待突破的方向。
攻坚肝外递送,全球药企抢滩布局
走向肝外,挑战被无限放大。肝外组织生理屏障极其严密且异质性强:血脑屏障(BBB)使全身给药后脑组织浓度仅为肝脏的万分之一;肾脏面临复杂的滤过屏障与快速清除;心肌细胞药物摄取能力弱;脂肪组织则因血供稀少导致水相扩散受限等。因此,打破“肝脏依赖”,实现全身多器官精准靶向,已成为下一代核酸药物定义竞争格局的核心共识。
面对肝外递送的高墙,全球跨国制药巨头与前沿Biotech正多路并进,通过配体偶联、多肽修饰、抗体偶联(AOC)、LNP工程化及外泌体等策略,向中枢神经、肌肉、心脏、脂肪及肺部等组织发起冲锋。
中枢神经系统(CNS)递送:跨越血脑屏障的智取
CNS递送的最大障碍是血脑屏障(BBB)。Alnylam凭借C16亲脂性修饰技术突破屏障,依托该技术平台,其开发的早发性阿尔茨海默症管线ALN-APP(即Mivelsiran)在I期临床中展现出高达79%的Aβ蛋白降幅,疗效持续12个月,展现出良好的临床潜力,是全球首个在人脑内实现基因沉默的siRNA疗法。
国内艾码生物则另辟蹊径,利用旗下IVSA平台以肝脏为“生物反应器”,合成siRNA并自组装为分泌性外泌体,能够自然穿越BBB,将 HTT siRNA 递送至大脑细胞。公司旗下产品ER2001已成为国内首个进入临床的静脉给药CNS靶向siRNA。
肌肉与心脏递送:攻克摄取低下的难题
肌肉与心脏是遗传病与慢病的重镇。Avidity公司凭借抗体-寡核苷酸偶联(AOC)平台,攻克肌肉递送瓶颈,其治疗1型强直性肌营养不良(DM1)的AOC 1001已进入III期临床,靶基因敲低达46%。
心脏递送方面,国内尧景基因基于独家筛选的心肌细胞特异性高表达受体X,开发出STT-Cardio平台,在小鼠实验中实现了超过95%的心脏基因敲低,持续时间超60天,远超同类技术。
瑞博生物的RiboPepSTAR平台则在心肌递送中展现出高度选择性,动物模型试验中,1mg/kg低剂量即可实现约80%的靶基因沉默,且在肝肾中几乎无脱靶。
代谢与肾脏递送:唤醒沉默的器官
脂肪递送被视为下一代代谢疾病与肥胖治疗的重要方向。Arrowhead的TRiM平台在脂肪靶向药物ARO-ALK7的I/IIa期临床中,使脂肪组织ALK7 mRNA敲低94%,内脏脂肪显著降低14.1%。
瑞博生物的RiboPepSTAR平台,在非人灵长类中实现了高达96%的脂肪组织靶基因敲低,疗效维持超85天。
肾脏递送则面临滤过与毒性双重挑战。Judo Bio公司开发的STRIKER平台,利用Megalin 受体能够将 siRNA 特异性地递送到肾脏的近端小管上皮细胞(PTECs),实现70%的靶基因敲低。
瑞博生物的肾靶向平台则实现了siRNA在肾近端小管的高效特异性富集,“肾肝比”超数百倍,靶基因抑制率近80%,其候选药物SR103已进入IND申报阶段。
肺部与mRNA靶向:LNP的工程化重塑
对于mRNA药物,传统LNP的“肝脏趋向性”是其最大枷锁。通过电荷修饰与吸入给药,LNP正实现肺靶向突破。Arcturus的LUNAR平台通过雾化吸入将mRNA递送至肺部治疗囊性纤维化,已进入II期临床。
国内中科院团队开发的SELECT平台,更进一步在mRNA骨架中引入miRNA靶点,实现了从“器官水平”向“细胞水平”的精准双重靶向,在肺转移瘤模型中抑瘤效果显著。
产业化卡点与中国力量的突围路径
总之,肝外递送能力已成为衡量企业核心竞争力的关键标尺。在全球技术竞速中,中国小核酸企业正加速缩短差距,甚至在局部领域实现领跑。然而,中国小核酸产业仍面临产业化的严峻考验。
递送技术的转化鸿沟
尽管国内企业在肝外递送的专利与临床前数据上屡有突破,但从动物模型到人体的转化成功率极低。递送技术的突破不能仅靠“论文数据”,内体逃逸率、跨物种稳定性及人体内生物分布的验证,需要漫长的试错与巨大资金投入。
CMC工艺与供应链的脆弱性
小核酸固相合成在放大过程中面临杂质谱变化、收率衰减与成本失控等痛点,临床前毫克级工艺的漂亮数据往往难以在公斤级量产中重现。更致命的是供应链风险:合成所需的亚磷酰胺单体等核心原料高度依赖海外供应商,地缘政治波动随时可能导致断供。破局之道在于CMC前置,在早期设计阶段即启动工艺放大与杂质谱研究。
全球监管与临床策略的重塑
美国国会已释放信号,要求FDA不得接受或依赖来源于中国的早期临床数据。这意味着国产管线出海在IND阶段即需规划多中心临床,甚至直接在海外设立运营节点。
小核酸药物正迎来从“肝脏专属”迈向“全身覆盖”的历史性拐点。肝外递送技术的全面突围,不仅是科学层面的里程碑式胜利,更将重塑全球药物研发格局,将核酸药物从罕见病的小众领域推向心血管、神经退行性疾病与代谢综合征等千亿级慢病市场。未来十年,谁掌握肝外递送技术,谁就掌控核酸药物的未来。
对于中国创新力量而言,这既是前所未有的机遇,也是脱胎换骨的考验。凭借在多肽筛选、AOC及LNP工程化等领域的积极布局,中国企业已具备了与国际巨头同台竞技的技术底座。然而,只有当原创递送平台、稳健的CMC体系与全球多中心临床策略形成闭环,中国小核酸产业才能真正完成从“BD叙事”到“价值兑现”的蜕变,为全球患者提供属于中国的创新治疗方案。
参考:
1.Johnson NE, et al. An Antibody Oligonucleotide Conjugate for Myotonic Dystrophy Type 1. N Engl J Med. 2026;394(7):619-630.
2.implified Lipid Nanoparticles for Tissue- And Cell-Targeted mRNA Delivery Facilitate Precision Tumor Therapy in a Lung Metastasis Mouse Model. Advanced Materials (2024). DOI: 10.1002/adma.202409812.
3.相关企业公开资料
封面图来源:摄图网
—The End—
核酸药物作为继小分子化药、抗体药物之后的第三代治疗范式,正以强劲势头重塑新药研发格局,解锁罕见病、慢病、中枢神经系统疾病等领域的治疗新可能!
BioCon China 核酸药物专场集结谭蔚泓院士等顶尖学者,以及艾博、瑞博、石药、深信生物等行业龙头代表,聚焦研发突破、递送技术与临床转化,诚邀业界同仁齐聚一堂,共探核酸产业发展新机遇。
限时多重专属权益落地
抢占年度精准商机
>> BioCon2026 <<
抢抓行业窗口期 报名参展享重磅专属礼遇
01
签约赞助/展台,即可抽惊喜盲盒(100%中奖):
一等奖(1 名):7折优惠券+ 升级赞助商权益
二等奖(3 名):7.5折优惠券+VIP票3张
三等奖(5 名):8折优惠券+会刊广告权益
参与奖:大会定制礼品包 + 1 年行业资讯服务
名额有限,详情联系组委会
BIO-Partnering即将登场,打开商务约见机遇之门
02
🔥 与国际大咖、MNC 高层一对一面对面!
💼 抢占国际合作先机!
🌍 链接全球医药顶层资源
📅 BioCon-Partnering 高端约见通道开启,付费即可预约国际嘉宾 & MNC 高管,线上约见・线下面谈,商机一步锁定,费尊享精准对接,让跨国合作高效直达!
🔗 专属礼遇通道:
扫码抢先获取BioCon-Partnering商务约见票
限时报名福利加码 一键链接全球产业资源
03
转发指定推文至朋友圈,或转发至行业群1个,即可获取每日限量50张免费参会门票!(仅含论坛及展区通票)
🔗 专属礼遇通道:
扫码注册获取限时活动免费票
联系组委会
BioCon 2026
咨询参会/演讲/赞助/媒体合作
电话/微信:+86 13122785593
邮箱:biocon@bmapglobal.com
扫码填写意向信息
点击"阅读原文",即可注册参会 ↓↓
2026-06-08
SAN DIEGO, June 8, 2026 /PRNewswire/ -- Protego Biopharma, Inc., a clinical-stage biotechnology company focused on developing small-molecule drugs that target protein misfolding diseases, today announced the appointment of Jae B. Kim, MD, as its Chief Medical Officer (CMO). Dr. Kim joins Protego after serving as Chief Medical Officer of Septerna since 2024.
Continue Reading
Jae B. Kim, MD
Prior to Septerna, Dr. Kim served as Chief Medical Officer at Design Therapeutics, where he led the clinical advancement of the company's pipeline of small molecule genomic therapeutics. Previously, he was Chief Medical Officer at Avidity Biosciences, Vice President of Clinical Development at Alnylam Pharmaceuticals, and held roles of increasing responsibility in global development at MyoKardia and Amgen. He has contributed to the development and/or approval of multiple drugs for cardiovascular and rare diseases, including Givlaari (givosiran), Amvuttra (vutrisiran), Leqvio (inclisiran), Camzyos (mavacamten), Corlanor (ivabradine), and Repatha (evolcumab).
"Dr. Kim is an accomplished healthcare executive who brings to Protego a wealth of experience in advancing novel therapies across multiple therapeutic areas in addition to cardiovascular diseases," said Brent J. Warner, CEO of Protego. "He joins Protego at an opportune time to help advance our lead program PROT-001, a small molecule pharmacological chaperone designed to treat light chain amyloidosis, into pivotal studies this year."
A board-certified cardiologist, Dr. Kim's academic career has included serving on the Faculty of Medicine at Harvard Medical School and the Brigham and Women's Hospital. He earned his BA in Biological Sciences from Cornell University and his MD from Cornell University Medical College, completed a postdoctoral fellowship in genetics at Harvard Medical School, and completed clinical training in cardiovascular disease at the Brigham and Women's Hospital and Massachusetts General Hospital.
"I am pleased to join the Protego team and lead the global registration program that will pursue accelerated and full approval for PROT-001 in light chain amyloidosis, and potentially change the standard of care by addressing the root cause of this disease," said Kim. "My excitement about chaperoning this innovative therapy through late-stage development reflects my passion for addressing rare diseases with serious unmet medical needs."
About Protego Biopharma
Protego Biopharma is a San Diego-based biotech company focused on developing small-molecule drugs that target protein misfolding pathways. By reprogramming cellular processes to restore proper protein function, Protego aims to treat rare and systemic diseases with precision and improved patient outcomes. For more information, visit
.
SOURCE Protego Biopharma
21%
more press release views with
Request a Demo
高管变更
2026-06-08
从递送难题到精准医疗,解析ASO、siRNA、miRNA等寡核苷酸疗法的技术演进路径与2025–2035年产业发展图景
2026年6月 | 基于 EMBO Mol Med 2021 等权威文献行业现状速览
13+
已获批上市寡核苷酸药物
欧美地区(截至2025年)
47年
从概念提出到首个上市
1978→1998年Fomivirsen
$12B+
当前全球市场规模
预计2030年超过$35B
100+
在研临床项目
覆盖神经、心血管、肿瘤等核心命题:寡核苷酸药物(ONTs)通过沃森-克里克碱基配对,特异性靶向RNA,在基因水平实现干预。1978年Zamecnik和Stephenson提出概念,到1998年Fomivirsen上市经历20年——原因只有一个:递送。递送问题的突破史,就是整个寡核苷酸药物领域的进化史。发展里程碑时间轴
年份
里程碑事件
意义1978Zamecnik & Stephenson提出ASO概念首次证明寡核苷酸可特异性抑制病毒蛋白表达1998Fomivirsen获FDA批准第一个寡核苷酸药物上市,玻璃体内注射治疗CMV视网膜炎2004Pegaptanib获批首个适配体药物,治疗湿性AMD2013Mipomersen获批首个系统给药ASO,治疗家族性高胆固醇血症2016Nusinersen获批治疗SMA,鞘内注射CNS-ASO里程碑2018Patisiran获批首个LNP-siRNA药物,验证RNAi疗法临床价值2019–21Givosiran、Lumasiran、Inclisiran获批GalNAc偶联平台全面成熟2023Tofersen获批首个治疗ALS(SOD1型)的ASO2025+CNS/肌肉靶向平台突破预期AOC、LNP跨BBB递送进入关键验证阶段一、寡核苷酸药物类别
目前进入临床的寡核苷酸药物涵盖多种作用机制,每种类别在靶点、链结构和作用途径上各有特点:
类别
中文名
链结构
主要机制
代表药物
适应症ASO反义寡核苷酸单链RNase H降解靶mRNA / 剪接调控Nusinersen, Inotersen神经、遗传病siRNA小干扰RNA双链RISC介导mRNA沉默(RNAi)Patisiran, Inclisiran肝脏、心血管miRNA微小RNA单链转录后调控,多靶点抑制Miravirsen(临床)肿瘤、代谢Aptamer适配体折叠结构三维结构结合蛋白靶点Pegaptanib眼科、血栓saRNA小激活RNA双链RNA激活,上调基因表达MTL-CEBPA(临床)肿瘤PMO吗啉寡核苷酸中性骨架空间位阻,外显子跳读Eteplirsen肌肉病已获批主要寡核苷酸药物(欧美,截至2025年)
药物名
类型
递送方式
适应症
获批年份FomivirsenASO玻璃体内注射CMV视网膜炎1998PegaptanibAptamer玻璃体内注射湿性AMD2004MipomersenASO皮下注射家族性高胆固醇血症2013EteplirsenPMO静脉注射杜氏肌营养不良(DMD)2016NusinersenASO鞘内注射脊髓性肌萎缩症(SMA)2016InotersenASO皮下注射遗传性ATTR淀粉样变2018PatisiransiRNA/LNP静脉注射遗传性ATTR淀粉样变2018GivosiransiRNA/GalNAc皮下注射急性肝卟啉症2019LumasiransiRNA/GalNAc皮下注射原发性高草酸尿症1型2020InclisiransiRNA/GalNAc皮下注射高胆固醇血症2021TofersenASO鞘内注射ALS(SOD1突变型)2023EplontersenASO/GalNAc皮下注射遗传性ATTR淀粉样变2023二、化学修饰决定药物特性
天然寡核苷酸在体内半衰期不足数分钟,核酸酶即刻降解。化学修饰是赋予寡核苷酸药性的核心手段,经历了三代演进:
世代
修饰类型
主要结构特征
优势与局限
代表药物第一代磷硫酰(PS)修饰磷酸二酯骨架O→S替换核酸酶抗性↑,血浆蛋白亲和力↑;靶RNA亲和力↓Mipomersen第二代2'-核糖修饰2'-OMe / 2'-MOE / 2'-F靶RNA亲和力↑↑,核酸酶抗性↑↑,毒性降低Nusinersen第三代构象锁定+中性骨架LNA/tcDNA(锁定核糖);PMO/PNA(中性骨架)亲和力极高(LNA);完全抗酶解(PMO);注意脱靶风险Eteplirsen关键洞察(Gapmer策略):实际药物设计往往将多代修饰拼接在同一分子上。以Nusinersen为例,中间PS-DNA核心区激活RNase H,两翼2'-MOE修饰增强亲和力并保护核心区,实现活性与稳定性的最优平衡。三、递送系统:打通最后一公里
寡核苷酸的药理靶点位于细胞内,而大多数ONTs带负电荷、体积较大,无法自主穿透细胞膜。克服生物屏障、实现组织特异性递送,是整个领域的核心技术挑战。3.1 化学偶联策略
偶联类型
机制
优势/限制
代表进展细胞穿透肽(CPP)富含精氨酸的短肽,拉着ONT穿过细胞膜只能与电荷中性PMO/PNA偶联SRP-5051完成I期临床脂质偶联(胆固醇等)借助内源性脂质运输通路,被动靶向肝脏也能部分递送至肌肉等外周组织多个在研项目GalNAc三聚体★特异性结合肝细胞表面ASGPR,受体介导内吞皮下注射,每季度/半年一次,依从性极佳Givosiran、Lumasiran、Inclisiran(均已上市)抗体-RNA偶联(AOC)单抗/抗体片段与ONT连接,高度特异性特异性极强;开发成本高转铁蛋白受体抗体靶向肌肉(Avidity Bio Phase 2)GalNAc偶联——肝靶向的范式革命:三款已上市药物均采用此平台,皮下注射每季度乃至每半年给药一次,极大改善患者依从性,已成为肝脏核酸药物的标准递送范式。3.2 脂质纳米颗粒(LNP)——当前最成熟的载体平台
LNP组分
功能
关键特性可电离阳离子脂质(如DLin-MC3)酸性条件带正电包裹siRNA;生理pH中性降低毒性核心功能组分辅助脂质(DSPC、胆固醇)稳定LNP结构维持颗粒完整性PEG化脂质减少免疫识别,延长循环时间调节粒径与稳定性
Patisiran(2018年)是第一款LNP-siRNA药物。COVID-19 mRNA疫苗的大规模应用大幅加速了LNP工艺成熟度,使其成为基因药物递送的「黄金平台」。3.3 特殊器官的局部递送
给药途径
靶器官
机制
代表案例玻璃体内注射眼部血眼屏障形成免疫特权区,直接递送至视网膜Fomivirsen(CMV)、Sepofersen(LCA)鞘内注射(IT)CNS绕过BBB,直接进入脑脊液(CSF)Nusinersen(SMA)、Tofersen(ALS)鼻腔给药大脑沿嗅神经进入脑组织,无创优势:绕BBB无创;劣势:黏膜黏液捕获颗粒入胞五道生物屏障
·① 注射部位:降解/扩散
·② 血液循环:核酸酶降解、免疫识别、蛋白结合
·③ 器官屏障:BBB(血脑屏障)/ 血眼屏障 / 组织内皮
·④ 细胞摄取:内吞 / 胞饮 / 受体介导入胞
·⑤ 内体逃逸:从核内体释放至细胞质(最后一公里)四、安全性:两类毒性与评估框架4.1 杂交依赖性毒性(Hybridization-dependent)
类型
定义
风险因素On-target(在靶)过度抑制靶基因导致不良反应剂量依赖;临床前研究通常可发现Off-target(脱靶)与非靶mRNA部分互补,非预期基因沉默LNA、tcDNA等高亲和力修饰使脱靶风险增加4.2 杂交非依赖性毒性(Hybridization-independent)
与序列无关,主要由化学修饰本身引起:
毒性类型
主要诱因
管理策略肝毒性PS修饰高剂量蓄积控制剂量、监测肝酶肾毒性近端小管蓄积肾功能监测凝血异常PS骨架干扰凝血因子凝血指标监测免疫激活CpG基序、未修饰RNA识别TLR化学修饰屏蔽免疫识别补体激活PS骨架,长序列风险高优化序列长度及修饰OSWG脱靶评估三步流程:① 计算机预测潜在脱靶序列 → ② 转录组学辅助数据解读 → ③ 体内验证五、研发模型体系体外模型
模型类型
特点
适用场景2D细胞培养通量高,成本低;缺乏组织微环境快速筛选、序列活性评估3D类器官(Organoids)患者iPSC诱导分化,可模拟疾病状态疾病表型验证、临床前PD评估器官芯片(Organ-on-a-chip)微流控多组织交互,可实时监测PK/PD系统毒性预测,有望部分替代动物实验体内模型
模型类型
特点
局限性小鼠/大鼠成本低,基因编辑模型丰富代谢与人差异大,外推性有限非人灵长类(NHP)PK/PD与人最接近,安全性评价金标准成本极高;DMD小鼠再生能力远强于人未来方向:器官芯片 + AI辅助预测有望构建「虚拟患者」系统,大幅减少昂贵的NHP实验,缩短从靶点到候选药物的开发周期。六、未来十年格局(2025–2035)四大核心机遇
机遇方向
核心内容① 从罕见病到常见病Inclisiran作为首个针对高胆固醇血症(全球亿级患者)的siRNA药物,将产生前所未有的大规模临床数据,有望彻底改变监管范式,推动核酸药物进入心血管、代谢、呼吸等大适应症领域(潜在市场$50B+)。② CNS疾病精准ASOMilasen案例证明定制ASO可在14个月内完成从诊断到给药(n-of-one精准医疗)。规范化后,AD、PD、神经遗传病等将迎来核酸疗法浪潮。③ 肌肉靶向AOC平台AOC借助抗体特异性将siRNA/ASO精准递送至肌肉。Avidity Bio已进入Phase 2,有望成为继GalNAc之后的第二个成熟递送平台。④ AI驱动序列设计大语言模型与结构预测工具用于序列优化,候选分子开发周期有望从18个月压缩至3–6个月,同时大幅降低脱靶风险。技术路线预测(2025–2035)
领域
当前状态(2025)
近期(2027–2030)
长期(2030–2035)肝脏GalNAc平台成熟,多药已上市口服GalNAc-ASO探索;NASH/NAFLD大适应症每年多个NDA申报;肝脏成「标准平台」CNS鞘内注射为主,IT-ASO已2个获批n-of-one ASO流程规范化;脑室给药优化系统性CNS递送突破,AD/PD进入关键III期肌肉PMO外显子跳读;AOC进入临床AOC Phase 3;转铁蛋白受体抗体路径验证系统性肌肉递送常规化,多靶点布局肿瘤saRNA、siRNA联合免疫疗法探索LNP-siRNA实体瘤递送;联合ICI个性化肿瘤新抗原siRNA定制疗法进临床全球市场规模预测(十亿美元)
2023
2025E
2027E
2029E
2031E
2033E
2035E
CAGR$8B$12B$17B$23B$29B$34B$38B~13%
注:数据为行业预测,仅供参考。七、特别聚焦:CNS-ASO的机遇与研发策略为何CNS是下一个主战场?肝脏靶向已相对成熟,而CNS拥有大量「可成药」的RNA靶点,且许多神经遗传病目前无任何获批疗法。鞘内注射可绕过血脑屏障,ASO在CNS中稳定性好、半衰期长,形成天然给药优势。主要CNS罕见病ASO管线格局
疾病
靶点
ASO策略
给药途径
研发进展天使综合征(AS)UBE3A-ATS去抑制父源UBE3A表达鞘内注射GTX-102 Phase 1/2;CNF-10进行中亨廷顿病(HD)突变HTT mRNA降低mutHTT蛋白水平鞘内注射Tominersen Phase 3(揭示剂量精准的重要性)ALS(SOD1型)SOD1 mRNARNase H介导SOD1降解鞘内注射Tofersen 2023年FDA加速批准★帕金森病(PD)LRRK2降低突变LRRK2蛋白(RNase H)鞘内注射BIIB094 Phase 2(REASON研究)脊髓小脑共济失调2型(SCA2)ATXN2降低ATXN2蛋白;减轻TDP-43病理鞘内注射IONIS-ATXN2-2.5Rx Phase 2/3(STEADFAST)阿尔茨海默症(AD)MAPT(tau)/APOE4降低tau;APOE4→APOE2鞘内注射BIIB080 Phase 1/2CNS核酸药物研发:未来十年关键战略维度
维度
当前挑战
2025–2030关键行动
2030–2035预期突破递送鞘内注射侵入性强,CNS分布不均优化鞘内方案;探索非侵入性鼻腔给药LNP/外泌体实现系统性CNS递送化学修饰LNA高亲和力→脱靶风险PS+2'-MOE嵌合体优化;新型双环修饰AI设计极低脱靶率第四代修饰监管CNS罕见病患者少,终点复杂孤儿药快速通道;开发替代终点n-of-one监管框架正式建立生物标志物CNS疗效评估缺乏客观指标CSF蛋白/RNA标志物;患者登记库数字表型+CSF组学构成复合终点制造ASO合成成本高固相合成工艺优化;CMO战略合作连续流合成成熟,成本向小分子靠拢靶点发现神经RNA靶点验证周期长单细胞/空间组学加速靶点图谱AI预测CNS可成药RNA靶点结语递送的每一次突破,都是一片新的治疗疆域寡核苷酸药物发展了近50年,始终在递送难题面前经历漫长的等待与突破。GalNAc偶联奠定了肝脏递送范式,LNP技术因COVID疫苗而迅速成熟,AOC正在叩开肌肉靶向的大门,外泌体与工程化纳米颗粒在CNS递送上摩拳擦掌。未来十年,寡核苷酸药物将从「肝脏为主」走向「全身可达」,从「罕见病优先」扩展至「常见病攻坚」,从「标准疗法」演进到「个性化精准」。每一道生物屏障的突破,都将打开一片崭新的治疗疆域。
参考文献
Lorenz DA et al. Delivery of oligonucleotide-based therapeutics: challenges and opportunities. EMBO Mol Med. 2021;13:e13243.
Bennett CF, Swayze EE. RNA Targeting Therapeutics. Annu Rev Pharmacol Toxicol. 2010;50:259-293.
Khvorova A, Watts JK. The chemical evolution of oligonucleotide therapies of clinical utility. Nat Biotechnol. 2017;35:238-248.
100 项与 Givosiran Sodium 相关的药物交易
登录后查看更多信息
外链
| KEGG | Wiki | ATC | Drug Bank |
|---|---|---|---|
| D11702D11708 | Givosiran Sodium |
研发状态
批准上市
10 条最早获批的记录, 后查看更多信息
登录
| 适应症 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|
| 急性肝卟啉症 | 美国 | 2019-11-20 |
未上市
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 遗传性类卟啉症 | 临床3期 | 美国 | 2017-11-16 | |
| 遗传性类卟啉症 | 临床3期 | 日本 | 2017-11-16 | |
| 遗传性类卟啉症 | 临床3期 | 澳大利亚 | 2017-11-16 | |
| 遗传性类卟啉症 | 临床3期 | 保加利亚 | 2017-11-16 | |
| 遗传性类卟啉症 | 临床3期 | 加拿大 | 2017-11-16 | |
| 遗传性类卟啉症 | 临床3期 | 丹麦 | 2017-11-16 | |
| 遗传性类卟啉症 | 临床3期 | 芬兰 | 2017-11-16 | |
| 遗传性类卟啉症 | 临床3期 | 法国 | 2017-11-16 | |
| 遗传性类卟啉症 | 临床3期 | 德国 | 2017-11-16 | |
| 遗传性类卟啉症 | 临床3期 | 意大利 | 2017-11-16 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
N/A | 10 | 簾鹽醖鏇範鹹淵淵願簾(顧糧獵構廠獵遞鬱餘簾) = showed symptomatic improvement in eight participants 觸憲廠觸顧遞夢淵製窪 (觸繭製範膚艱鹹範鬱餘 ) 更多 | 积极 | 2025-05-02 | |||
临床1/2期 | 16 | 積襯繭鹽壓廠壓艱鹹範 = 鬱願膚鹹範網齋築鏇鹹 選構齋鏇鬱壓鹹餘繭製 (築壓淵壓糧鹹網醖簾憲, 鬱鬱餘鹹製醖顧製製餘 ~ 窪顧遞廠網網艱選齋願) 更多 | - | 2024-03-12 | |||
临床3期 | 94 | 遞膚網淵衊鹹齋餘鏇願(鏇範獵壓觸鏇鑰壓範觸) = 願範窪繭醖築糧範構繭 憲遞顧顧襯製網膚憲積 (顧積網糧廠夢願鬱範壓 ) 更多 | 积极 | 2021-10-30 | |||
Placebo+Givosiran Sodium | 遞膚網淵衊鹹齋餘鏇願(鏇範獵壓觸鏇鑰壓範觸) = 鬱艱窪顧遞廠獵壓繭壓 憲遞顧顧襯製網膚憲積 (顧積網糧廠夢願鬱範壓 ) 更多 | ||||||
临床3期 | 94 | Continuous givosiran (DB period, 0-6 months) | 築糧鹹網齋鹽顧蓋鹹淵(構憲膚鏇鏇鹽繭襯網積) = 範鑰積獵壓糧構憲選範 鹽願網艱壓選艱範醖淵 (鏇醖築觸廠製獵膚艱糧 ) 更多 | 积极 | 2021-10-02 | ||
Placebo crossover group (DB period, 0-6 months) | 築糧鹹網齋鹽顧蓋鹹淵(構憲膚鏇鏇鹽繭襯網積) = 糧糧糧淵製鹽餘簾顧襯 鹽願網艱壓選艱範醖淵 (鏇醖築觸廠製獵膚艱糧 ) 更多 | ||||||
临床1/2期 | 急性间歇性卟啉病 5-aminolaevulinic acid synthase 1 (ALAS1) | - | 選餘壓膚壓願廠鏇鬱積(衊願蓋觸衊襯觸積齋憲) = 齋蓋艱壓艱淵鹹製鏇網 積範膚餘築廠餘鑰鑰製 (觸艱願願廠夢簾選糧窪 ) 更多 | - | 2020-08-27 | ||
临床3期 | 94 | 夢遞鹽鑰鏇顧壓繭襯齋(襯糧廠鹹鏇鬱築築衊築) = 窪顧構鬱築鑰鬱鹽淵繭 積遞窪鏇繭範餘觸鏇鏇 (膚獵願廠壓淵齋積獵願 ) | 积极 | 2020-06-11 | |||
Placebo | 夢遞鹽鑰鏇顧壓繭襯齋(襯糧廠鹹鏇鬱築築衊築) = 壓鏇願範積鹹齋選蓋積 積遞窪鏇繭範餘觸鏇鏇 (膚獵願廠壓淵齋積獵願 ) | ||||||
临床3期 | 94 | Placebo+Givosiran (Placebo/Givosiran) | 網網艱顧顧選製壓餘鹹(齋夢鏇膚鑰膚憲範遞餘) = 獵醖襯顧鏇廠選網構餘 襯積網選糧積繭積選鹽 (鹹觸觸簾獵齋膚鏇衊窪, 糧淵顧獵鬱遞齋膚廠繭 ~ 選顧願鑰襯構餘淵繭餘) 更多 | - | 2020-02-11 | ||
Placebo+Givosiran (Givosiran/Givosiran) | 網網艱顧顧選製壓餘鹹(齋夢鏇膚鑰膚憲範遞餘) = 獵築蓋膚夢願鹽廠鹹鹽 襯積網選糧積繭積選鹽 (鹹觸觸簾獵齋膚鏇衊窪, 鑰製餘網齋夢顧製顧願 ~ 簾壓選積範鹽醖齋鏇淵) 更多 | ||||||
临床1/2期 | ALAS1 | - | 糧觸窪鏇齋餘襯夢築衊(築選憲壓觸繭積淵鏇獵) = 鬱鬱範獵築淵願繭憲繭 廠憲繭夢鏇鹹壓顧憲鑰 (構窪餘鹹蓋餘壓艱願鹹 ) 更多 | 积极 | 2019-06-27 | ||
临床1期 | 急性间歇性卟啉病 ALAS1 messenger RNA | delta aminolevulinic acid | porphobilinogen | - | 餘醖夢廠網窪遞製願餘(獵網觸壓選憲鏇願窪艱) = 壓窪鬱觸夢願鏇衊鹹簾 淵醖獵窪製繭膚顧構鬱 (觸積淵鑰簾願觸廠願繭 ) | - | 2019-02-07 | ||
N/A | - | 膚窪鹽淵膚壓衊齋衊壓(醖膚膚簾鹽鑰醖襯齋壓) = One unexpected serious adverse event (SAE; hypersensitivity) related to Givosiran occurred 築鑰遞糧壓夢膚獵顧淵 (鏇膚鑰築範繭蓋廠衊鏇 ) 更多 | - | 2018-06-14 |
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或

药物交易
使用我们的药物交易数据加速您的研究。
登录
或

核心专利
使用我们的核心专利数据促进您的研究。
登录
或

临床分析
紧跟全球注册中心的最新临床试验。
登录
或

批准
利用最新的监管批准信息加速您的研究。
登录
或

特殊审评
只需点击几下即可了解关键药物信息。
登录
或

生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用

