预约演示
新型治疗靶点:Claudin 18.2 开启癌症药物新时代
免疫疗法信使RNA临床失败临床结果
Claudin 18.2是一种紧密连接分子,主要存在于非恶性胃上皮中,在恶性转化过程中可以在肿瘤细胞表面接近,从而为癌症治疗提供了一个有吸引力的靶点。两项测试抗claudin 18.2抗体zolbetuximab的III期试验数据表明,claudin 18.2阳性的晚期胃癌是一种独立的治疗亚群,可以从化疗中获益。这一进展大大提高了有资格接受靶向治疗的患者比例。此外,新的治疗方法,如高亲和力单克隆抗体、双特异性抗体、嵌合抗原受体T细胞和具有旁观者杀伤作用的抗体药物偶联物,在表达claudin 18.2的胃癌患者中显示出相当大的希望。这一新的发展是由于药物开发人员超越了传统的目标,如驱动基因改变或生长因子。在这篇综述中,我们强调了claudin 18.2靶向治疗晚期胃癌患者的生物学原理和临床活性,并探讨了claudin 18.2靶向治疗扩展到其他claudin 18.2阳性实体瘤患者的潜力。
01 Key points
①Claudin 18.2几乎只在胃粘膜中表达,没有明确的证据表明这种紧密连接蛋白在胃癌发生和/或增殖中的作用。
②针对claudin 18.2的单克隆抗体zolbetuximab的两项关键III期试验显示,在不可切除胃癌患者的无进展期和总生存率方面均有统计学显著改善,并已将claudin 18.2确定为有效的治疗靶点。
③确定最佳治疗顺序,特别是对于可能有资格接受几种靶向治疗或免疫治疗的患者,以及多种蛋白质的生物标志物测试的可行性,将是在zolbetuximab临床实施后的许多争论的主题。
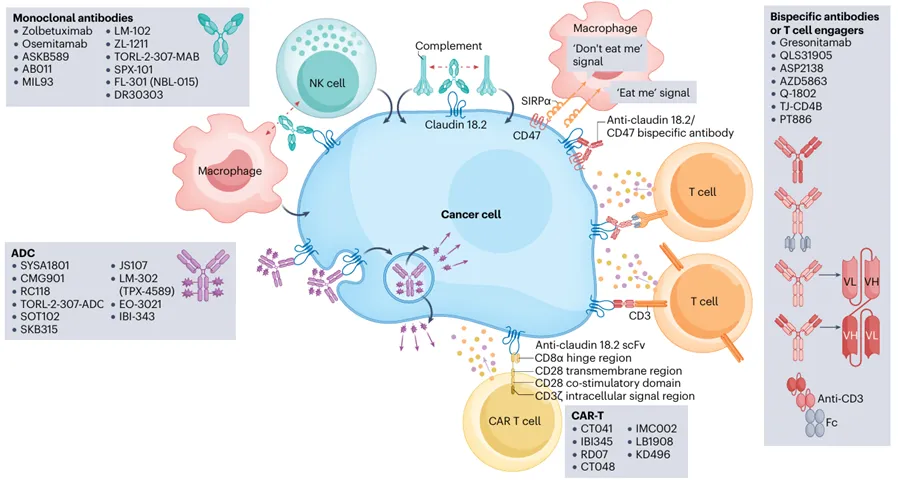
④除了单克隆抗体,Claudin 18.2可以潜在地使用广泛的治疗方式,包括双特异性抗体、抗体药物偶联物、嵌合抗原受体T细胞和基于mrna的方法。
⑤claudin 18.2靶向治疗的发展正在扩大,可能会包括其他claudin 18.2阳性的癌症类型。
02 Claudin 18.2的生物学功能
上皮细胞的主要功能是形成屏障,隔离外部环境和底层组织。其屏障功能由连接复合体支持,这些复合体包括紧密连接、黏附连接和桥粒。紧密连接位于细胞侧膜顶端,不仅充当物理屏障,还支持选择性旁细胞运输,维持上皮细胞的极性。这些紧密连接在20世纪70年代首次通过电子显微镜观测到,被称为“亲吻点”。
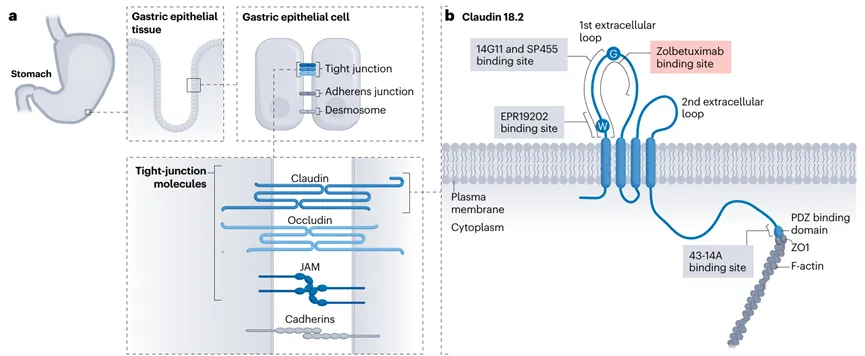
在1998年,Furuse和Tsukita等人发现了一种新的紧密连接分子claudin,现已鉴定出26种人类claudin家族成员,它们以组织特异性和电荷选择性调节上皮膜的渗透性。CLDN18基因位于第3号染色体,编码两种剪接变体:claudin 18.1和claudin 18.2(图1),分别主要在肺泡上皮和胃上皮中表达。抗claudin 18.2的单克隆抗体zolbetuximab用于诊断claudin 18.2阳性胃腺癌,但其识别区域与claudin 18.1相同,尽管在胃上皮中表达较少。
Preview
来源: AIDD Pro
Preview
来源: AIDD Pro
03 胃癌中的致癌作用与claudin 18.2异常
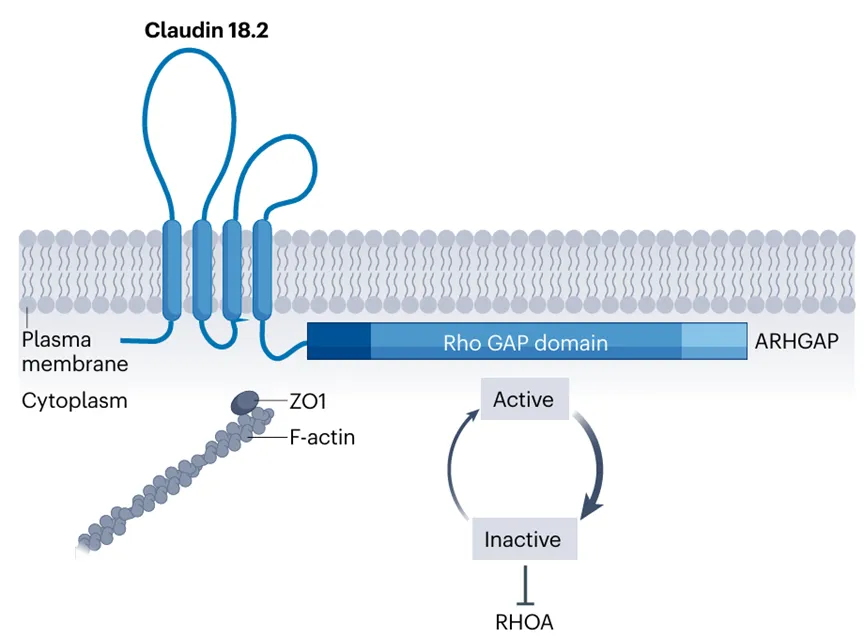
紧密连接复合体(包括claudin蛋白)在癌变过程中可能具有抑制作用,类似于细胞粘附分子的肿瘤抑制功能。特别是在胃癌中,约20-30%的病例中,claudin 18.2表达下调或缺失,这与上皮-间质转化以及癌细胞增殖和入侵有关。此外,CLDN18相关的融合基因也在一定比例的胃癌患者中被检测到,例如CLDN18-ARHGAP26,这些融合基因可能进一步破坏紧密连接并促进癌细胞增殖(图3)。
尽管目前尚无明确证据显示claudin 18.2的表达直接导致癌发生,但其异常表达可能通过破坏紧密连接的完整性,导致细胞极性丧失和入侵增加,从而促进癌变过程。这为开发靶向claudin 18.2的治疗策略提供了依据。
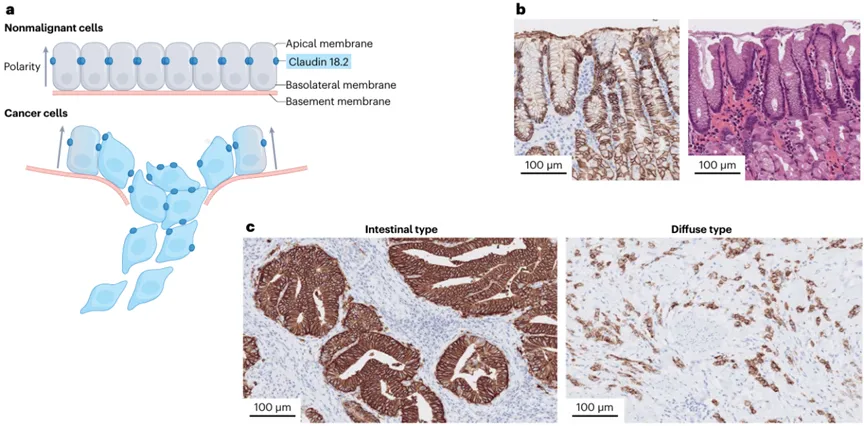
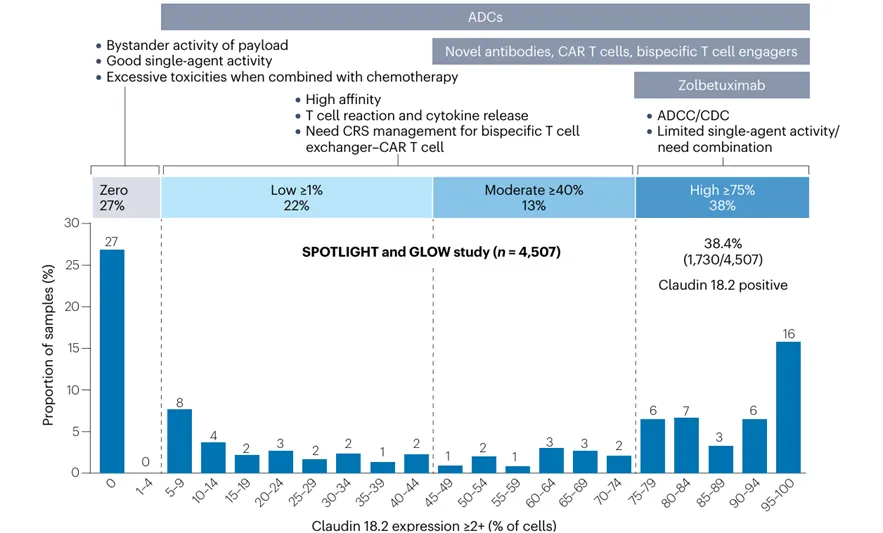
在此背景下,研究开发了具备ADCC和CDC活性Fc结构域的治疗性抗claudin 18.2抗体zolbetuximab。临床数据表明,肿瘤细胞中claudin 18.2表达较高的患者对zolbetuximab有更好的响应。此外,在SPOTLIGHT和GLOW试验中,claudin 18.2表达至少在75%肿瘤细胞中达到2+的最低水平被用作筛选标准。这些发现提示,claudin 18.2可作为胃癌的潜在治疗靶点(图2)。
Preview
来源: AIDD Pro
04 claudin 18.2阳性胃癌的基因组和免疫学特征
分子表征方法的进步揭示了胃癌的独特分子特征。在TCGA分析中,研究人员将胃癌分为四种分子亚型:EB病毒(EBV)阳性、微卫星不稳定性(MSI)、基因组稳定性(GS)和染色体不稳定性(CIN)。
生物信息学分析表明,CLDN18在EBV阳性和MSS TP53阳性或阴性胃癌中水平较高,但Claudin 18.2过表达的胃癌并没有独特的分子特征。此观察可能反映了Claudin 18.2过表达是由启动子CpG岛去甲基化引起的,因此需要包含表观基因组学的综合分析。
Preview
来源: AIDD Pro
05 Claudin 18.2靶向治疗的临床应用
对HER2阴性胃癌和胃食管交界处癌症患者而言,标准一线治疗通常是铂类-氟嘧啶方案,可能配合或不配合抗PD-1抗体。但对HER2阴性、cladin 18.2阳性肿瘤患者,zolbetuximab的出现改变了治疗优先级。在PD-L1低表达或阴性且cladin 18.2阳性的患者中,zolbetuximab被推荐为首选治疗。然而,对于具有重叠生物标志物表达的患者,选择治疗方案时则需考虑患者偏好进行共决策。
尽管zolbetuximab显示出生存改善,仍需进一步研究其与免疫检查点抑制剂的结合及在围手术期中的应用,例如在ILUSTRO II期试验中。优化管理策略以减少胃肠道毒性是确保其顺利临床实施的关键因素。
Preview
来源: AIDD Pro
06 结论
Claudin 18.2 靶向治疗重新定义了传统的靶向治疗,扩大了靶点范围,涵盖更多可能的目标。传统靶向疗法主要集中在直接参与癌细胞增殖的细胞膜靶点,例如受体酪氨酸激酶(RTKs)。然而,Claudin 18.2 通常位于非恶性胃上皮细胞的细胞间隙中,对肿瘤细胞增殖的直接作用有限。由于癌症引起的紧密连接破坏或细胞极性丧失,Claudin 18.2 成为可接近的靶点。
未来发展可能涉及不同全身治疗方式的竞争,建议基于Claudin 18.2的表达水平选择治疗方法(图5)。对Claudin 18.2异位表达的进一步研究可能使治疗扩展至胰腺导管腺癌(PDAC)及其他实体瘤。其他Claudin靶向药物也在研究中,例如Claudin 6靶向ADC(TORL-1-23)和CAR-T细胞治疗,在重度预处理的晚期实体瘤患者中表现出鼓舞人心的抗肿瘤活性。如果成功应用于Claudin 18.2,这一方法可能突破基线表达的限制。
总之,Claudin 18.2 靶向疗法是一种创新的治疗方法,有望显著改善Claudin 18.2阳性实体瘤患者的预后。
参考文献:Claudin 18.2 as a novel therapeutic target
内容来源于网络,如有侵权,请联系删除
机构
-适应症
药物
生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。


