预约演示
6.1亿美元!艾伯维、安进投资的神经退行性疾病公司--Caraway,被默沙东收购
并购
2023年11月21日,默沙东(“MSD”)与Caraway Therapeutics(简称“Caraway”)共同宣布,两家公司已达成最终协议。根据协议条款:默沙东将通过子公司收购Caraway,总金额约6.1亿美元,包括未披露的预付款以及或有里程碑付款。
关于Caraway
Caraway利用遗传数据和独特的生物学理解,来开发专有的小分子,激活细胞清除和回收过程-加速清除累积的有毒物质和有缺陷的细胞成分。
遗传学的新见解强调了溶酶体功能与多器官系统病理之间的联系,包括中枢神经系统(CNS)、心脏、肾脏和肌肉。以这些机制为靶点,Caraway为患有神经退行性疾病和罕见疾病(包括帕金森病(PD)、肌萎缩性侧索硬化症(ALS)和溶酶体沉积病(lsd)的患者提供潜在的疾病修饰化合物。
Part.1 公司管线
公司正在推进一系列强大的新型小分子疗法,用于治疗神经退行性疾病和罕见疾病,目前均处于临床前的阶段。
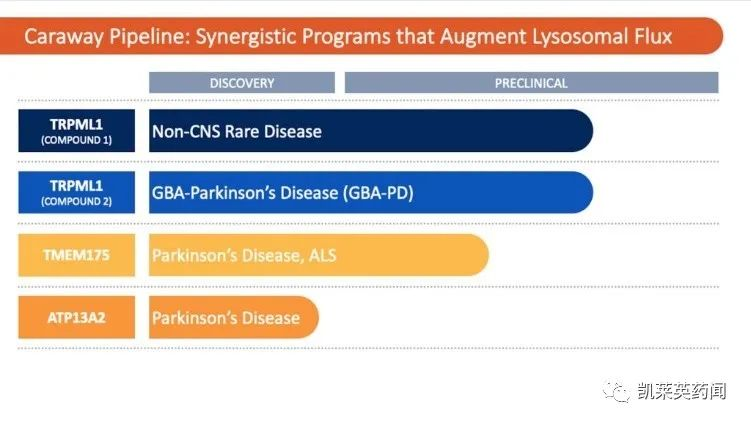
Preview
来源: 药时代
TRPML1:TRPML1是通道粘磷脂亚家族的成员,像其他TRP通道一样,TRPML1 具有六个跨膜螺旋 (S1~S6),以及一个由 S5、S6和 2 个孔螺旋 (PH1和PH2) 组成的孔区域。它是一种释放 Ca2+的阳离子通道,可以介导溶酶体的钙信号传导和稳态,也是转运和自噬相关事件的重要调节因子。
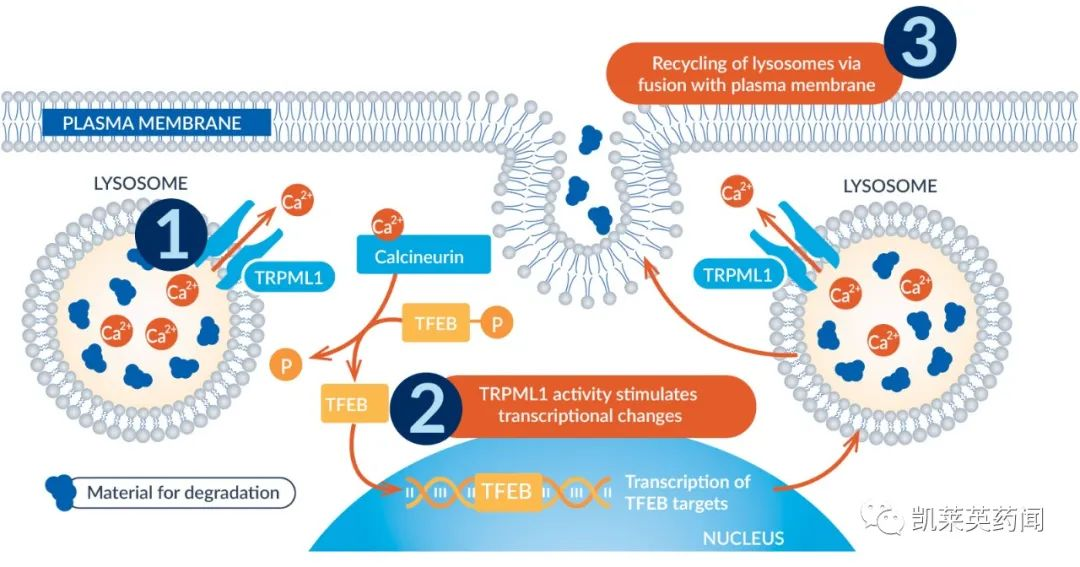
Preview
来源: 药时代
TRPML1的突变能够导致溶酶体贮积病黏液脂病 IV (MLIV) 的发生,会造成认知、语言和运动缺陷和视网膜变性等各种症状的发生,因此TRPML1作为治疗溶酶体贮积症的靶点,在临床上表现出巨大的潜能。
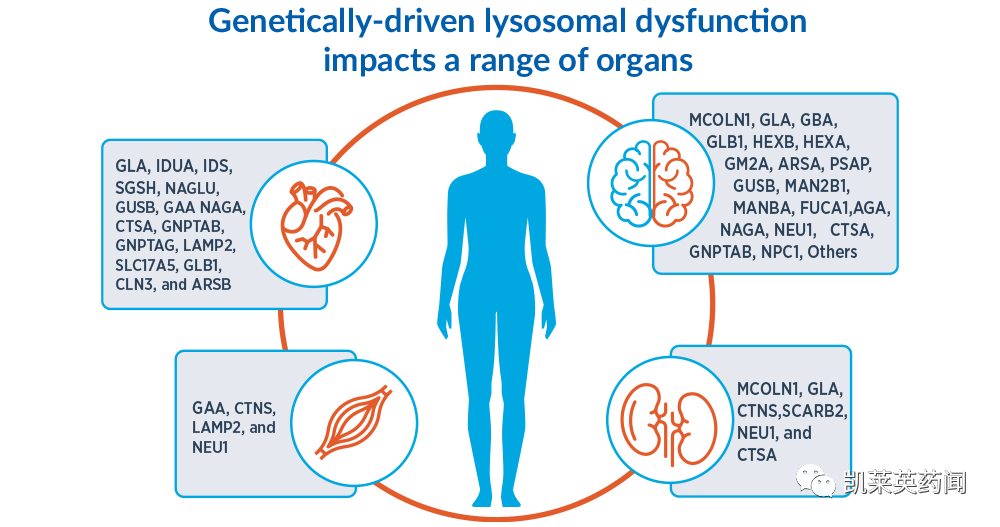
Preview
来源: 药时代
TMEM175:TMEM175是一种新型的氢离子激活的氢离子通道(LyPAP),介导氢离子快速流出。TMEM175缺乏可导致溶酶体过度酸化,破坏蛋白水解活性,促进体内帕金森致病相关的α-突触核蛋白聚集。2022年6月,Cell杂志在线发表了美国密西根大学徐浩新(Haoxing Xu)团队的相关研究,证实在溶酶体生理条件下,TMEM175作为氢离子激活的氢离子通道介导溶酶体氢离子外流,平衡V-ATP酶介导的氢离子内流,以维持稳定的溶酶体pH值。此外,作为维持溶酶体最佳pH值的氢离子激活的氢离子通道TMEM175在细胞水平上调节溶酶体蛋白水解酶Cathepsin B和Cathepsin D活性,以及体内α-突触核蛋白的清除,为PD、AD等神经退行性疾病和LSDs的病理过程和治疗方法研究提供新思路。
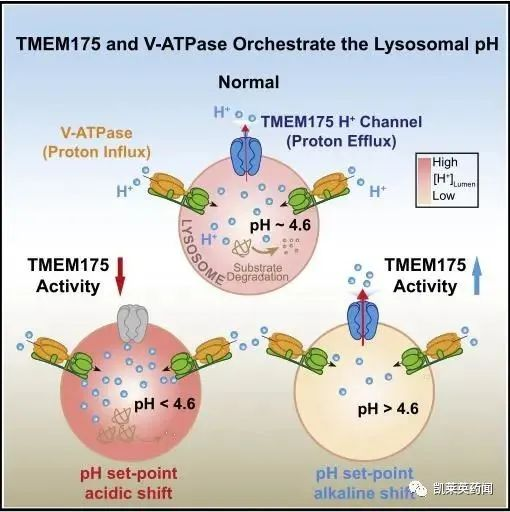
Preview
来源: 药时代
Part.2 融资情况
2018年11月,Caraway前身Rheostat Therapeutics宣布完成2300万美元A轮融资,该轮融资由MRLV和AbbVie Ventures领投,包括Amgen Ventures,
Alexandria Venture Investments和Mayo Clinic。现有投资者SV Health investors和Dementia Discovery Fund跟投。
Part.3 合作交易
2021年6月,该公司曾与艾伯维达成一项合作,开发和商业化靶向TMEM175的小分子疗法,首付款1700万美元。
参考资料
1、公司官网
2、公众号:晶蛋生物、医药魔方
3、Hu M, Li P, Wang C, et al. Parkinson’s disease-risk protein TMEM175 is a proton-activated proton channel in lysosomes[J]. Cell, 2022, 185(13): 2292-2308. e20.
内容来源于网络,如有侵权,请联系删除。
药物
-生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。




