预约演示
疗效持续维持达50周!口服小分子3期试验积极,显著改善亨廷顿病症状
基因疗法临床结果
Neurocrine Biosciences日前公布KINECT-HD2临床3期研究的中期结果,该研究评估Ingrezza(valbenazine)胶囊作为亨廷顿病(HD)相关舞蹈病成人患者长期治疗选择的作用。初步数据表明,早在第2周时每日一次Ingrezza胶囊给药即改善患者的舞蹈病症状,该获益持续至第50周。

Preview
来源: 药明康德
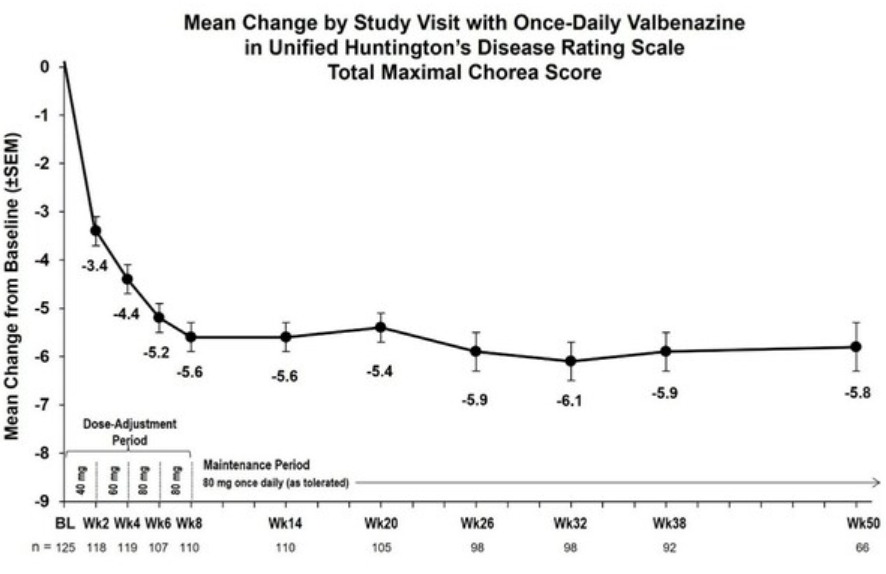
KINECT-HD2的中期分析显示,在初始剂量40 mg下,Ingrezza在第2周起表现出疗效,并在高达80 mg的剂量下维持其疗效至第50周(参见下图)。
Preview
来源: 药明康德
相当大比例的受试者(60.9%)及其临床医生(58.9%)报告,到第6周时症状状态“改善”或“极大改善”。到第50周,这些数值进一步增加,约四分之三的受试者(74.2%)和研究人员(76.9%)报告症状显著改善。
本试验中显示的安全性特征与既往结果一致。最常见治疗相关不良事件包括跌倒(30.4%)、疲乏(24.0%)和嗜睡(24.0%)。

Preview
来源: 药明康德
Ingrezza是一款选择性囊泡单胺转运体2(VMAT2)抑制剂,对VMAT1、多巴胺能、5-羟色胺能、肾上腺素能、组胺能或毒蕈碱受体无明显亲和力。Ingrezza通过选择性靶向VMAT2,被认为可减少额外的多巴胺信号,这可能导致不可控运动的减少。Ingrezza已获FDA批准用于治疗成人亨廷顿病患者的迟发性运动障碍,并可与大多数精神科药物(如抗精神病药或抗抑郁药)联合使用。今年8月,Ingrezza获FDA批准用于治疗亨廷顿病相关舞蹈病成人患者。
参考资料:[1] Neurocrine Biosciences® Presents INGREZZA® (valbenazine) Capsules Interim Data Demonstrating Sustained Improvements in Chorea Associated With Huntington's Disease Through Week 50 at Huntington Study Group 2023.
Retrieved November 3, 2023 from https://neurocrine.gcs-web.com/news-releases/news-release-details/neurocrine-biosciencesr-presents-ingrezzar-valbenazine-capsules
内容来源于网络,如有侵权,请联系删除。
药物
生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。



