预约演示
【JMC】 靶向KRAS多样性——G12X及其它在癌症治疗中的共价调控
AACR会议
侃言
就这个话题,侃侃来解读一篇本周一JMC刚发表的文章“Targeting KRAS Diversity: Covalent Modulation of G12X and Beyond in Cancer Therapy"。主要解读以下几点:
※ KRASG12X突变与癌症
※ 不同突变亚型的共价抑制剂设计
※ G12X以外突变的展望

Preview
来源: 精准药物
01 KRAS G12X突变与癌症
Preview
来源: 精准药物
Preview
来源: 精准药物
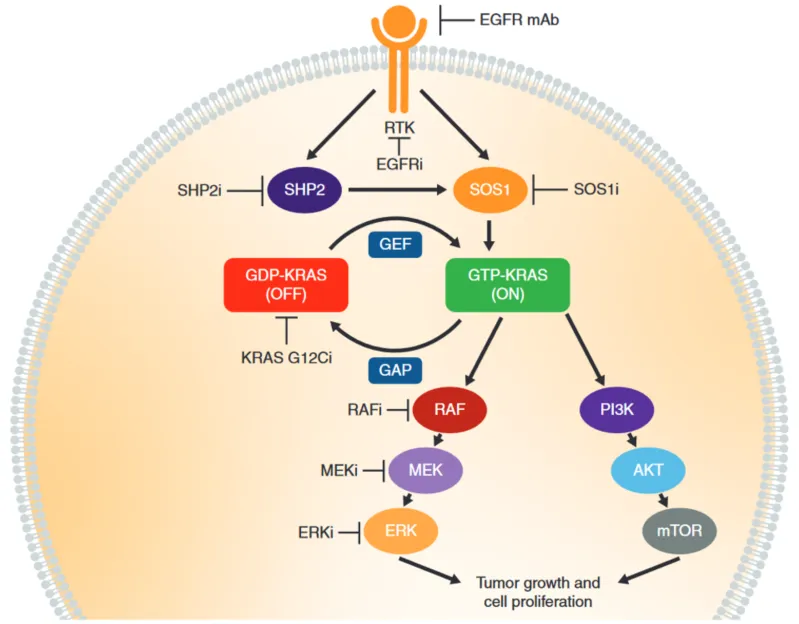
在细胞内,KRAS蛋白好比一个“开关”,在失活和激活状态之间转变:当KRAS与鸟苷二磷酸(GDP)结合时,失活没有酶活性;当其与鸟苷三磷酸(GTP)结合时,激活具有活性,激活下游信号通路。
野生型KRAS在失活与激活状态之间的转换受上游两类因子的调节。一类是鸟嘌呤核苷酸交换因子(GEF),这类蛋白催化KRAS与GTP的结合,从而促进KRAS的激活,其中包括SOS蛋白;另一类是GTP酶激活蛋白(GAP),这类蛋白能够促进与KRAS结合的GTP水解成为GDP,从而抑制KRAS的活性。
当KRAS发生基因突变后,会破坏GAP活性,使KRAS一直保持与GTP结合,将KRAS锁定在活跃状态,并持续激活下游信号通路,导致细胞增殖、迁移,最终促成癌症发生!
Preview
来源: 精准药物
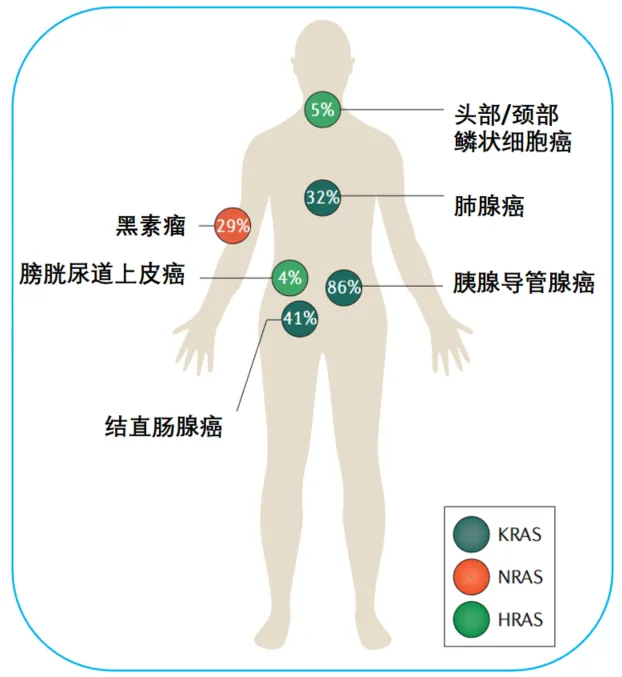
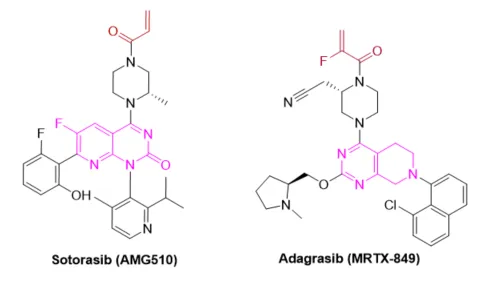
在KRAS的基因突变中,主要发生在第12号、第13号、第61号、第146号等Hotspots上密码子对应的氨基酸残基上:G12(80%)、G13(~15%)、Q61(<5%)、和A146(4%-5%)。其中,最普遍的突变发生在G12上单个氨基酸的取代,主要包括G12D、G12V、G12C、G12A、G12S、G12R,将野生的甘氨酸取代分别获得突变后天门冬氨酸(D)、缬氨酸(V)、半胱氨酸(C)、丙氨酸(A)、丝氨酸(S)、精氨酸(R),其中具有亲核性反应活性,可以用来设计共价抑制剂有半胱氨酸、天门冬氨酸、丝氨酸、精氨酸。
靶向KRAS的药物发现非常具有挑战性,因为①其表面缺少明显的药物可结合口袋,而且②KRAS与底物GDP或GTP结合力非常强,结合亲和系数在PicoMolar级(pM皮摩尔浓度级别),对竞争性抑制剂的亲和力要求很高!
Preview
来源: 精准药物
Preview
来源: 精准药物
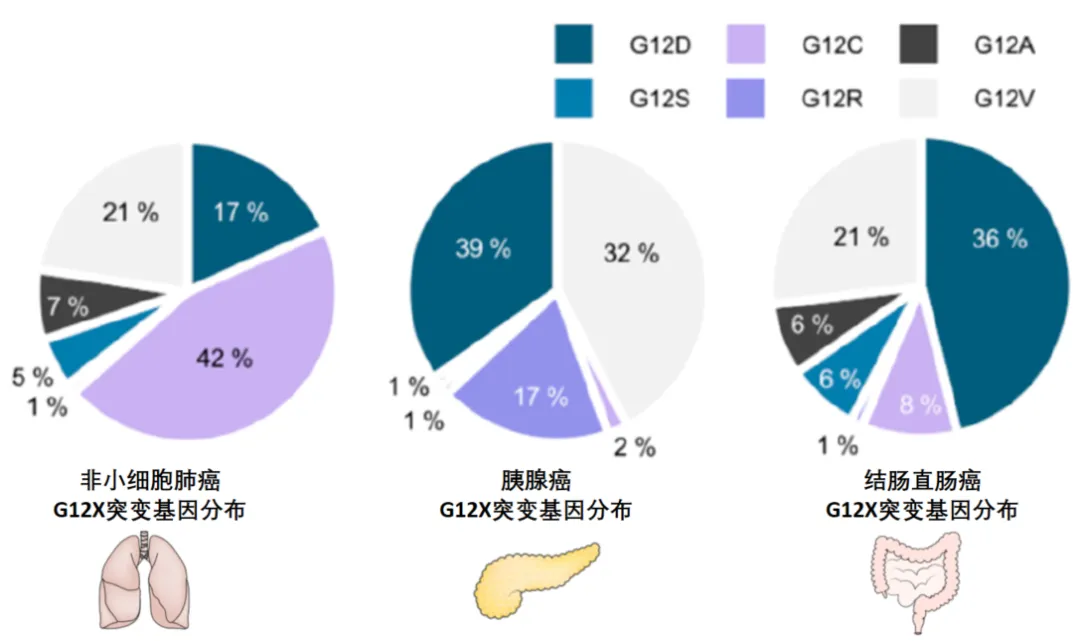
对KRAS突变抑制剂的开发,长时间以来比较依赖于Cys12的共价识别,但其只是在非小细胞肺癌的基因突变比例较高(约42%),而在胰腺癌(2%)、直肠癌(8%)等癌症中并不是主要的突变形式,而对G12C以外的靶向突变体的研究更加具有挑战,直到最近才得以实现。
02 非G12C突变的KRAS靶向共价抑制剂设计
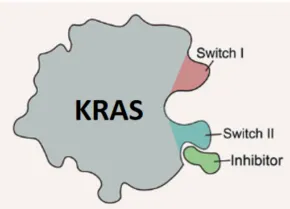
最近研究表明,SWIIP具有KRAS抑制剂结合的优先“特权”,并且提供了直接进入并作用Hotspot位置12突变残基的机会。KRASG12C共价抑制剂开发成功的经验,可以用于参考,设计靶向其他突变的共价抑制剂。
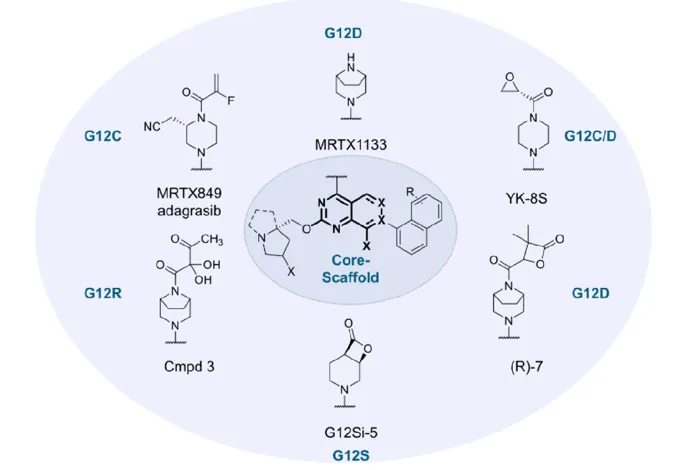
Preview
来源: 精准药物
KRAS抑制剂需要有较高的亲和力参与竞争,KRASG12C抑制剂的成功开发提供了SWIIP强结合力的骨架结构。因此,以SWIIP作为设计的起点,进一步修饰和改造可以于不同的G12X突变获得的氨基酸残基直接作用(主要指共价作用)的片段;同时,通过形成这些特异性的相互作用,而不影响正常野性KRAS蛋白的功能。如上图,是近些时间发现的针对G12X不同亚型突变的获得氨基酸残基特异性共价弹头。
KRASG12D
KRASG12D是最频繁的KRAS突变亚型,在人类各种癌症中,约39%胰腺导管腺癌、36%结直肠癌、17%非小细胞肺癌病例来自KRASG12D型基因突变。但是,G12D型突变缺少G12C突变的共价作用锚点(Cys12),要想将G12C突变体共价抑制剂转化成G12D型突变体的可逆抑制剂,具有一定的挑战性。

Preview
来源: 精准药物
要获得KRASG12D型突变体可逆性抑制元件,需要克服两大障碍:①一种完全可逆的抑制剂需要更高的亲和力和选择性来替代缺失的共价键;这里选择Adagrasib作为起始模板,因为它相比于其他KRASG12C抑制剂,具有更高的可逆亲和力和额外的相互作用,即其氰基中N与Gly10中的羰基形成相互作用,增强了亲和力。②2位的N-甲基吡咯烷元件与Glu62侧链形成相互作用。
结合以上共晶结构发现的问题,研究人员通过替换骨架、修饰骨架2、4、7位取代基,发现了针对野生KRAS具有更高亲和力的可逆抑制分子MTYX1133。其与KRASG12D突变体的共晶结构提供了有价值的信息,降低解离常数低至皮摩尔级别(~0.2 pM)。
从结构上看,2位取代基的修饰与Glu62形成潜在的离子相互作用;7位萘环取代占据了由Val9、Met72、Phe78、 Ile100、和Val103形成的疏水口袋;萘环上的炔烃元件进一步和与Gly10、Val8、Thr58配位的水分子相互作用;此外,设计的刚性双环胺与突变获得的Asp12形成了盐桥作用。这些设计,提高了分子相对于野性KRAS的选择性(500倍)。目前MRTX1133在临床1/2期研究中。
鉴于共价抑制剂相对于非共价抑制剂的优势,以及靶向KRASG12C不可逆共价抑制剂的成功,开发共价靶向KRASG12D的抑制剂非常具有吸引力。然而,G12D突变获得的天门冬氨酸侧链相比于G12C突变获得的半胱氨酸,是一个比较弱的亲核侧链,用来开发共价弹头,相当具有挑战性!
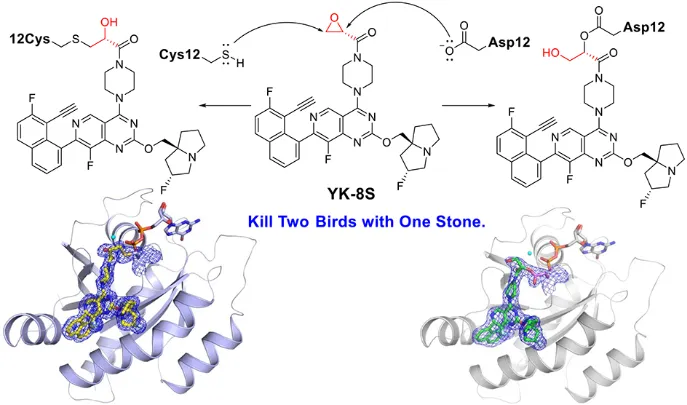
Preview
来源: 精准药物
鉴于MRTX1133对KRASG12D强有力的亲和力,广州暨南大学以其位模板,在和与G12D突变而获得的Asp12形成盐桥的元件上安装上环氧乙烷和氮杂环丙烷作为共价弹头,通过优化,最终获得可“一石二鸟”的共价抑制分子YK-8S,更能够同时共价作用于KRASG12C、和KRASG12D。注意,作用位点不同,而且对应其他亚型如G12R、G13D、Q61R、Q61K以及野生型KRAS并不起作用(或很弱)。
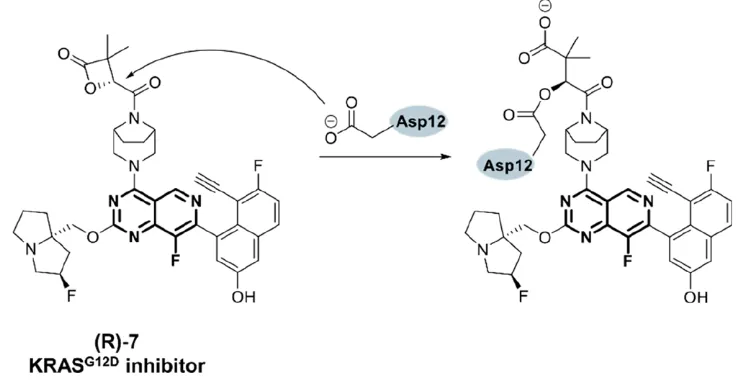
Preview
来源: 精准药物
加利福尼亚大学以同样的策略,利用β-环丙酯作为共价弹头,同样发现了KRASG12D的共价抑制剂,如上图(R)-7。
KRASG12R型突变主要在胰腺癌患者中观察到,约占17%;在其他人类癌症如结直肠癌、非小细胞肺癌等也有少数发现,约占1%。假设共价结合G12R突变获得的精氨酸残基可能有利于与该突变体的结合效力和选择性,参考KRASG12D共价抑制剂的开发,需要探索靶向精氨酸残基的共价弹头。然而,精氨酸残基也是一种比较弱的亲核性官能团。
Preview
来源: 精准药物
Preview
来源: 精准药物
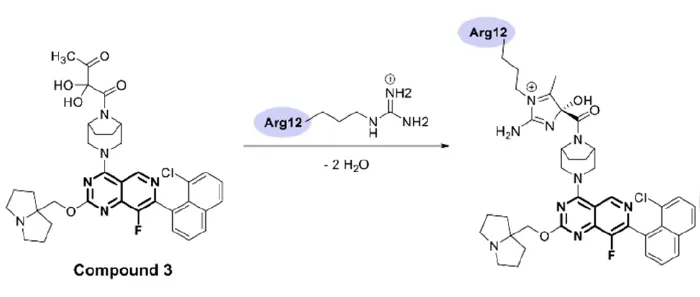
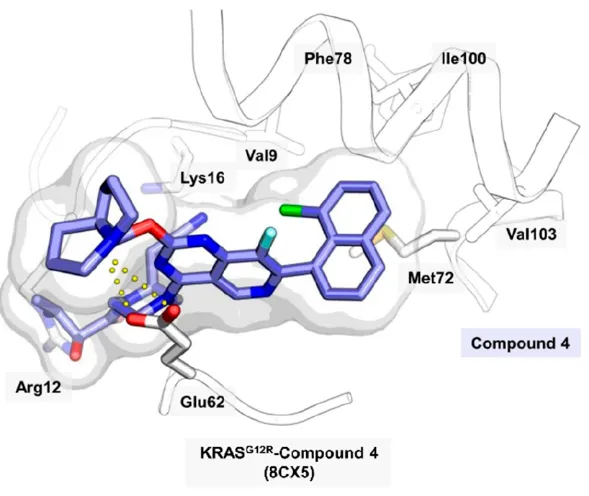
同样是加利福尼亚大学,2022年,利用α,β-二羰基酰胺类元件作为靶向精氨酸残基的共价弹头,获得了化合物3,能把选择性靶向KRASG12R,而对其他亚型和野生型KRAS不起作用。
KRASG12S
KRASG12S型突变在6%的结直肠癌、和5%的非小细胞肺癌患者中被观察到,这是另一个值得关注的Hotspot。
Preview
来源: 精准药物
Preview
来源: 精准药物
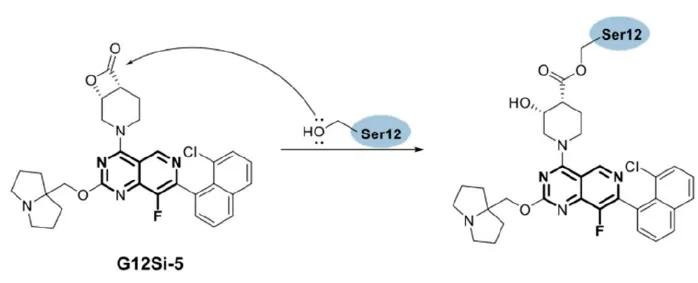
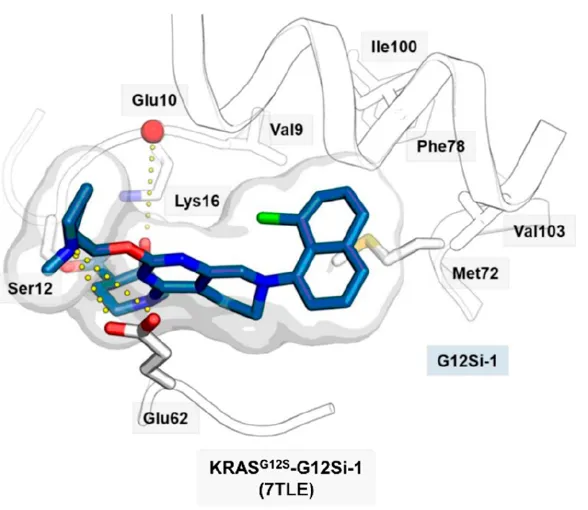
还是加利福尼亚大学团队,2022年,利用β-环丙酯元件作为亲电弹头,设计合成并优化获得了选择性靶向KRASG12S的共价抑制剂G12Si-5。
03 G12X及其以外的展望
在KRAS的致癌突变中,靶向半胱氨酸以外突变体是主要的,但是靶向非半胱氨酸残基的方法确面临着更大的限制。
这些限制除了非共价弹头的反应性以外,还有来自其他弹头药物代谢稳定性和药代动力学性质的问题。
而且,目前针对其他突变亚型,如KRASG12V、KRASG13X、以及KRASQ61X等还没有相应配体确认报道。这些亟待解决的问题,还需要从更多的策略发展出发来解决。
比如泛RAS抑制剂的方法,开发小分子、多肽、分子胶等。
比如靶向嵌合体的蛋白质分解的方法(PRATACs),开发linker连接E3连接酶识别元件和KRAS不同亚型突变体抑制剂,尤其是开发连接可逆共价抑制剂。
内容来源于网络,如有侵权,请联系删除。
机构
-生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。


