预约演示
更新于:2026-05-28

Vor Biopharma, Inc.
更新于:2026-05-28
概览
标签
肿瘤
其他疾病
免疫系统疾病
Fc融合蛋白
CAR-T
ADC
疾病领域得分
一眼洞穿机构专注的疾病领域
暂无数据
技术平台
公司药物应用最多的技术
暂无数据
靶点
公司最常开发的靶点
暂无数据
| 排名前五的药物类型 | 数量 |
|---|---|
| CAR-T | 3 |
| ADC | 2 |
| Fc融合蛋白 | 1 |
| T细胞疗法 | 1 |
关联
7
项与 Vor Biopharma, Inc. 相关的药物作用机制 APRIL抑制剂 [+2] |
在研机构 |
原研机构 |
非在研适应症 |
最高研发阶段批准上市 |
首次获批国家/地区 中国 |
首次获批日期2021-03-09 |
靶点 |
作用机制 IL-3 modulators |
在研适应症 |
非在研适应症- |
最高研发阶段临床前 |
首次获批国家/地区- |
首次获批日期- |
靶点 |
作用机制 CD123抑制剂 |
在研适应症 |
非在研适应症- |
最高研发阶段临床前 |
首次获批国家/地区- |
首次获批日期- |
7
项与 Vor Biopharma, Inc. 相关的临床试验NCT07404865
A Multicenter, Randomized, Double-Blind, Placebo-Controlled, Phase 3 Study to Evaluate the Efficacy and Safety of Telitacicept in Adult Participants With Active Primary Sjögren's Disease
Phase 3 Study of Telitacicept in Active Primary Sjögren's Disease (UPSTREAM SjD)
开始日期2026-02-26 |
申办/合作机构 |
NCT06456567
A Multicenter, Randomized, Double-Blind, Placebo-Controlled, Phase 3 Study to Evaluate the Efficacy and Safety of Telitacicept Compared to Placebo in Patients With Moderately to Severely Active Systemic Lupus Erythematosus (REMESLE-2)
The purpose of this study is to evaluate the efficacy and safety of telitacicept in the treatment of moderately to severely active SLE.
开始日期2024-09-01 |
申办/合作机构 |
NCT06456580
A Phase 3, Randomized, Double-Blind, Placebo-Controlled Study With an Open-label Extension Period to Evaluate the Efficacy and Safety of Telitacicept in Patients With Generalized Myasthenia Gravis
The purpose of this study is to evaluate the efficacy and safety of telitacicept in the treatment of generalized myasthenia gravis.
开始日期2024-07-17 |
申办/合作机构 |
100 项与 Vor Biopharma, Inc. 相关的临床结果
登录后查看更多信息
0 项与 Vor Biopharma, Inc. 相关的专利(医药)
登录后查看更多信息
243
项与 Vor Biopharma, Inc. 相关的新闻(医药)2026-05-27
·药事纵横
5月19日,宜明昂科宣布全球首款CD47xCD20双靶点特异性分子阿沐瑞芙普α(IMM0306),在治疗活动性系统性红斑狼疮(SLE)的II期随机对照临床试验中成功完成首例患者入组给药。
系统性红斑狼疮(systemic lupus erythematosus,SLE)患者群体庞大,且目前缺少有效的治疗手段。SLE又被称为“美女病”,原因是SLE与雌激素关系密切,女性发病率明显高于男性,男女比率约1:9。荣昌生物的泰它西普SLE适应症已在国内上市,并成功授权出海;多款SLE创新药正在加速研发。(一)系统性红斑狼疮患者多,目前治疗手段疗效有限、安全性不足
系统性红斑狼疮是一种系统性自身免疫病,以全身多系统多脏器受累、反复的复发与缓解、体内存在大量自身抗体为主要临床特点,如不及时治疗,会造成受累脏器的不可逆损害,最终导致患者死亡。系统性红斑狼疮又被称为“美女病”,究其原因,在于该疾病好发于18-45岁女性,且女性患者人数远远大于男性患者人数,女性患者和男性患者比例约9:1。根据中华医学会风湿病学分会制定的《2020中国系统性红斑狼疮诊疗指南》,我国约有100万名SLE患者,发病率位居全球第二。
目前,SLE临床常用的治疗药物包括激素、非甾体类抗炎药、免疫抑制剂、抗疟药和生物制剂。尽管激素是SLE治疗的基础用药,但长期使用激素易导致高血压、糖尿病、骨质疏松等副作用,免疫抑制剂存在感染、骨质疏松、骨髓抑制等风险。此外,很多SLE患者使用激素及多种免疫抑制剂后仍不能控制病情,因此,这部分患者存在迫切的临床治疗需求。
SLE的发病与遗传和基因关系密切。遗传学认为,SLE是具有分子遗传和表观遗传背景的自身免疫性疾病,其发病常需要多个基因的共同作用,如补体因子C1、C2和C4、参与核酸内源性代谢的酶、直接参与Ⅰ型IFN(干扰素)途径的蛋白和参与调节T、B淋巴细胞自我耐受的基因等。鉴于SLE与遗传和基因的密切关系,企业相继开展针对关键细胞/通路的靶向药物,目前在临床上已取得了诸多进展。
SLE临床表现复杂多样。多数呈隐匿起病,开始仅累及1—2个系统,部分患者长期稳定在亚临床状态或轻型狼疮,部分患者可由轻型突然变为重症狼疮,更多的则由轻型逐渐出现多系统损害。SLE的自然病程多表现为病情的加重与缓解交替。 SLE常见的症状包括全身表现,如发热、疲乏;在鼻梁和双颧颊部呈蝶形分布的红斑;皮肤损害包括光敏感、脱发、结节性红斑等;肾脏损害如蛋白尿、血尿、管型尿。(二)三款生物制剂上市,SLE领域的新革命
近年来,随着分子生物学、免疫学等学科的发展,许多针对SLE发病机制中不同环节的特异性生物制剂不断出现,目前,临床上常用于SLE的生物制剂包括贝利尤单抗、利妥昔单抗、泰它西普和阿尼鲁单抗等,奥妥珠单抗于2026年申报SLE适应症的上市申请,有望于2026年12月上市。
(1)贝利尤单抗(Benlysta)是首个B淋巴细胞刺激因子(B lymphocyte stimulator,BLyS)特异性抑制剂,由GSK研发。Benlysta与B细胞不直接结合,但通过与BLyS结合,Benlysta可抑制B细胞(包括自身反应性B细胞)的生存、减少B细胞向制造免疫球蛋白的浆细胞的分化。贝利尤单抗于2017年在美国上市后,销售额持续攀升,2025年全球销售额达23.4亿美元(+22%)。
贝利尤单抗的上市基于两项三期研究,分别是BEL110751 和 BEL110752,研究纳入1684 例SLE 患者。在这两项研究中,贝利尤单抗 10mg/kg 组中52周SLE 应答者指数(SRI-4)比例显著高于安慰剂组,52周SRI-4为50.6%和38.8%(p<0.0001),研究达到主要终点。
(2)泰它西普是全球首个靶向B淋巴细胞刺激因子(BLyS)和增殖诱导配体(APRIL) 双靶点机制药物,由荣昌生物研发。2021年3月,泰它西普获NMPA批准上市,用于治疗系统性红斑狼疮。泰它西普的上市基于一项多中心、随机、双盲、安慰剂对照的Ⅲ期确证性临床研究。试验共入组335例SLE患者,患者被随机分配到泰它西普(160毫克)组或安慰剂组,每周皮下注射一次,与标准治疗相结合,为期52周。研究达到了预设的临床终点,泰它西普组的SRI-4反应率均明显高于安慰剂组。第52周SRI-4应答率在泰它西普组为82.6%,安慰剂组为38.1%。
图:泰它西普治疗SLE的Ⅲ期52周SRI-4结果
数据来源:2022ACR
泰它西普牵手Vor Bio,顺利出海。2025年6月,荣昌生物宣布,将泰它西普有偿许可给美国公司Vor Biopharma,Vor Bio获得泰它西普在除大中华区以外的全球范围内开发、生产和商业化的独家权利;荣昌生物将取得Vor Bio价值1.25亿美元现金及认股权证、最高可达41.05亿美元的里程碑付款,总金额达42.3亿美元。牵手Vor Bio有望加速泰它西普在美国的临床研发,未来为荣昌生物贡献海外收入。
图:荣昌生物与VOR BIO签订授权协议
数据来源:荣昌生物宣传材料
(3)Anifrolumab(阿尼鲁单抗)可与I型干扰素受体的亚基1相结合,进而拮抗所有I型干扰素(IFN-α、IFN-β和IFN-ω)的相关活性。60%~80%的系统性红斑狼疮患者存在I型干扰素高表达特征,而且I型干扰素浓度与系统性红斑狼疮患者疾病活动指数(SLEDAI)评分呈正相关。
Anifrolumab于2021年7月获FDA批准上市。Anifrolumab的上市基于两项名为TULIP的3期临床试验以及名为MUSE的2期临床试验的疗效和安全性数据。Anifrolumab治疗系统性红斑狼疮的第一个III期试验TULIP-1未达到主要临床终点SRI4,TULIP-2试验改用BICLA作为主要临床终点,证明anifrolumab优于安慰剂。2024年,Anifrolumab销售额达4.74亿美金,2025年销售额达6.86亿美元。
(4)奥妥珠单抗是罗氏旗下一款CD20单抗。2026年4月,FDA受理了奥妥珠单抗用于治疗系统性红斑狼疮的上市申请,PDUFA为2026年12月。奥妥珠单抗目前已获批滤泡性淋巴瘤、慢性淋巴白血病/小细胞淋巴瘤等多项适应症,2025年全球销售额达11.9亿美元。
奥妥珠单抗申报上市基于一项名为ALLEGORY的Ⅲ期研究,研究纳入303名SLE患者。在治疗52周时,达到系统性红斑狼疮应答指数4(SRI-4)缓解标准的患者比例,奥妥珠单抗组为76.7%,安慰剂组为53.5%(p<0.001)。若奥托珠单抗获批SLE适应症,将成为全球首个用于SLE治疗的抗CD20疗法。
图:奥妥珠单抗ALLEGORY三期研究结果
数据来源:罗氏官网
(三)国内SLE竞争格局:蓝海竞争,机会庞大
鉴于SLE存量患者庞大,且缺少良好的治疗手段,国内多家企业布局这一适应症,除了荣昌生物外,在研企业还包括诺诚健华、药明巨诺、宜明昂科、恒瑞医药、康诺亚等。
(1)诺诚健华:奥布替尼是诺诚健华旗下一款BTK抑制剂,目前系统性红斑狼疮适应症处于临床Ⅲ期。Ⅱb期研究结果显示,第48周时,每天一次(QD)75毫克奥布替尼剂量组的SLE反应指数-4(SRI-4 )应答率显著高于安慰剂组(57.1% vs. 34.4%),具有高度统计学意义(p<0.05),达到主要终点。2026年4月,奥布替尼治疗系统性红斑狼疮III期注册临床完成首例患者入组。
(2)药明巨诺:CAR-T通过深度清除自身免疫性疾病致病性B 细胞,触发免疫系统“重置”,有望实现SLE的根治,有望成为SLE治疗的潜力手段。2023年,药明巨诺宣布CAR-T免疫细胞疗法瑞基奥仑赛注射液(倍诺达®)获得临床试验默示许可,用于治疗中重度难治性系统性红斑狼疮(SLE)。2025年10月,药明巨诺向CDE递交瑞基奥仑赛治疗系统性红斑狼疮患者中的I期研究数据,12例受试者SRI-4达标12例(100%),LLDAS达标6例(50%),Drug-Free达标12例(100%)。疾病活动度量表SLEDAI-2K、SELENA-SLEDAI、SLE-DAS和PGA量表评分等均呈下降趋势,初步显现出显著的疗效。
(3)宜明昂科:阿沐瑞芙普α(IMM0306)是宜明昂科自主研发的CD47×CD20双特异性抗体,目前处于临床Ⅱ期。IMM0306治疗系统性红斑狼疮的Ib期临床研究结果显示,IMM03060.8mg/kg组24周SRI-4应答率达71.4%(5/7),1.2mg/kg组24周SRI-4应答率达80%(4/5)。患者关节炎、血管炎、脱发均痊愈,抗dsDNA抗体、24小时尿蛋白、补体C3/C4等关键生物标志物显著改善。安全性方面,未发生DLT、CRS或重要感染事件,整体安全耐受性良好。
(4)恒瑞医药:恒瑞医药布局了多款SLE创新药,SHR0302(艾玛昔替尼)是恒瑞医药开发的一种高选择性JAK1抑制剂,可通过抑制JAK1信号传导发挥抗炎和抑制免疫的生物学效应。2023年12月20日,恒瑞医药宣布SHR0302缓释片获批开展系统性红斑狼疮临床试验。SHR-2001是恒瑞医药自主研发的抗体-细胞因子融合蛋白,临床皮下注射给药,2023年5月获得药物临床试验批准通知书。
(5)康诺亚:CM313是康诺亚旗下一款靶向CD38的人源化单克隆抗体。鉴于CM313对浆细胞优异的清除效果,公司正在推进一项评价CM313注射液在系统性红斑狼疮受试者中的安全性、耐受性、药代动力学、药效动力学、免疫原性及初步疗效的随机、双盲、安慰剂对照、剂量递增、多次给药的Ib/IIa期临床研究。2025年1月,康诺亚与Timberlyne达成独家授权许可协议,授予Timberlyne在全球(不包括中国内地、香港、澳门及台湾地区)开发、生产及商业化CM313的独家权益。(四)小结
SLE又称为“美女病”,但美女对其避之不及,毕竟在鼻梁和双颧颊部呈蝶形分布的红斑严重影响美观。目前,临床上常用于SLE的生物制剂包括贝利尤单抗、利妥昔单抗、泰它西普和Anifrolumab等,荣昌生物的泰它西普已成功授权出海。多家国产创新药企业正在针对SLE加速研发,其中诺诚健华的奥布替尼处于临床Ⅲ期,宜明昂科的阿沐瑞芙普α和药明巨诺的瑞基奥仑赛处于临床Ⅱ期,期待国产创新药在SLE适应症开花结果。
立即扫码加入药事纵横交流群
2026-05-27
PLANO, Texas--(BUSINESS WIRE)--Secretome Therapeutics, a clinical-stage biotechnology company developing novel therapies derived from neonatal cardiac progenitor cells (nCPC), today announced the closing of a $30 million Series A financing from RA Capital Management, LP (“RA Capital”), a multi-stage investment manager dedicated to evidence-based investing in public and private healthcare, life sciences, and planetary health companies. RA Capital was the sole investor in the financing.
The Series A financing will support company operations and the continued development of Secretome’s innovative pipeline, including STM-01, an nCPC-derived therapy in development for Duchenne muscular dystrophy-associated cardiomyopathy and other rare forms of cardiomyopathy secondary to neuromuscular disease. Secretome expects to use the proceeds to advance STM-01 toward pivotal Phase 2 and Phase 3 development in Duchenne muscular dystrophy, an indication with few disease-modifying therapeutic options.
In connection with the financing, Mr. David Lubner has joined the company’s Board of Directors, and Dr. Charles Edwards will be resigning from the Board. Mr. Lubner is a seasoned biotechnology leader with more than 25 years of experience as a senior executive and Board member in the life sciences industry. He previously served as Executive Vice President and Chief Financial Officer of Ra Pharmaceuticals until its acquisition by UCB in 2020. Prior to Ra Pharmaceuticals, Mr. Lubner served as Chief Financial Officer of Tetraphase Pharmaceuticals, PharMetrics, and ProScript. He currently serves on the Boards of Crescent Bio and Dyne Therapeutics, as well as several private companies. He previously served on the boards of Arcellx, Inc. until its acquisition by Gilead in April 2026, Nightstar Therapeutics and POINT Biopharma through their acquisitions by Biogen and Eli Lilly, respectively. He also served on the boards of Cargo Therapeutics and Vor Biopharma until August 2025.
Additionally, Matthew Hammond, Ph.D., MBA, a Partner at RA Capital Management, will serve in the role of Board Observer. Secretome also announced that Dr. Charles Edwards has resigned from the Board of Directors. The company thanks Dr. Edwards for his meaningful contributions, guidance, and service during an important period of Secretome’s growth.
“RA Capital’s investment represents an inflection point for Secretome, and a validation of our science, team, and clinical development strategy,” said Vinny Jindal, President, Chief Executive Officer and Co-founder of Secretome Therapeutics. “Moreover, with this financing, Secretome can develop STM-01 expeditiously as a potential gold standard therapy for patients and families affected by Duchenne muscular dystrophy. We are grateful for the deep financial, operational, and strategic expertise that David Lubner brings to our Board as Secretome enters its next major stage of growth. On behalf of the company, I also want to thank Dr. Charles Edwards for his long-standing support of our mission and team, and the many contributions he has made to Secretome.”
“Secretome is emerging as a leading immunology and inflammation (I&I) company in the area of cardiac disease, and a leader in the development of progenitor cell-based therapeutics,” said Matthew Hammond, PhD, MBA, Partner at RA Capital Management, “We believe in STM-01 will be a disease-modifying and best-in-class cellular therapy for patients with DMD, and the first of a broader pipeline of nCPC-based therapies from Secretome.”
About Secretome Therapeutics
Secretome Therapeutics is a clinical-stage biotechnology company based in Plano, Texas, developing novel therapies derived from neonatal cardiac progenitor cells. The company’s lead product candidate, STM-01, is a cellular therapy designed to modulate inflammatory and fibrotic pathways and support myocardial function in Duchenne muscular dystrophy-associated cardiomyopathy, dilated cardiomyopathy, and heart failure with preserved ejection fraction. Secretome is also advancing STM-21, a secretome-based therapeutic currently in preclinical development, and other novel nCPC-based products.
About RA Capital Management
Founded in 2004, RA Capital Management is a multi-stage investment manager dedicated to evidence-based investing in public and private healthcare, life sciences, and planetary health companies. RA Capital creates and funds innovative companies, from private seed rounds to public follow-on financings, allowing management teams to drive value creation from inception through commercialization and beyond. RA Capital’s knowledge engine is guided by its dedicated internal research division, and Raven, RA Capital’s healthcare incubator, offers entrepreneurs and innovators a collaborative and comprehensive platform to explore the novel and the re-imagined. RA Capital has more than 170 employees and over $10 billion in assets under management.
高管变更并购细胞疗法
2026-05-23
·今日头条
> **三个月600亿美元**——这是2026年第一季度中国创新药对外授权交易额。这个数字,已接近2025年全年1356.55亿美元总额的一半。一场从“价格内卷”到“全球授权”的战略转型,正以前所未有的速度与规模,重塑中国制药业的全球坐标。

跨国巨头扫货、百亿交易频现,中国药企从昔日的“跟随者”变为全球创新管线的重要供给方,一张清晰的竞争格局地图正在展开。
## 头部企业引领:从“产品出海”到“全球共创”的范式升级
头部企业凭借深厚的管线储备和全球化布局,成为这轮浪潮的绝对主力。他们不再满足于简单的产品授权,而是通过深度合作,在全球价值链中争取更大话语权。

- **恒瑞医药:管线厚度与平台化优势**。2025年7月,恒瑞与**GSK达成潜在总额120亿美元的合作**,不仅涉及核心产品,更包含**11个早期项目**。这标志着跨国药企对中国早期研发能力的信任。
恒瑞的策略是构建多元化平台,2026年一季度其非肿瘤产品收入同比增长92.13%,创新药收入占比首次突破60%。
- **百济神州:自主出海的标杆**。作为首个在美国获批上市中国本土自研抗癌药(泽布替尼)的企业,百济构建了“自主出海+授权合作”的双轮驱动模式。2026年一季度,其核心产品泽布替尼全球销售额达75.98亿元,占总营收72%。
同时,它也在积极引入外部管线,如以“独家选择权”模式锁定华辉安健的三特异性化合物。
- **信达生物:速度与模式创新**。信达与武田制药2025年10月达成的**114亿美元合作**,开创了“利润共享”新模式——双方按**40%:60%的比例共享美国市场利润**。这超越了传统的里程碑付费,转向风险共担、价值共享的“共同体”合作,标志着中国药企商业谈判能力的质变。
## 明星Biotech破局:以差异化创新切入全球赛道
一批聚焦前沿技术的生物科技公司,凭借“全球新”或“同类最优”的潜力,在激烈竞争中脱颖而出,成为跨国药企争相合作的对象。

- **康方生物:“头对头”击败标准疗法**。从早期将CTLA-4授权给默沙东,到以“50亿美元+提成+股权”将依沃西授权给Summit,康方的策略是聚焦能解决全球未满足临床需求、或能在临床试验中“头对头”击败现有标准疗法的产品。
- **荣昌生物:核心管线的价值释放**。2025年6月,荣昌将自身免疫药物泰它西普的海外权益授予Vor Biopharma,交易包含**8000万美元认股权证**。这种“股权+权益”的复合模式,在实现现金流回笼的同时,保留了长期的股权增值空间。
- **前沿生物:押注下一代技术平台**。2026年2月,前沿生物将两款小核酸药物全球独家权益授予**葛兰素史克**,交易总额**10.03亿美元**。这体现了中国Biotech在ADC、双抗等热门领域外,于新兴技术平台上的突破能力。
## 传统药企转型与新兴势力崛起
除了头部企业和明星Biotech,赛道中还有两类重要玩家:积极转型的传统大型药企,以及凭借技术特色崭露头角的新兴力量。
- **石药集团、中国生物制药:在细分领域实现突破**。2026年1月,石药与阿斯利康就肥胖症和糖尿病管线达成**潜在185亿美元的合作**。同年3月,中国生物制药将双靶点抑制剂罗伐昔替尼全球独家授权给赛诺菲,交易额**15.3亿美元**,创造了中国药企在移植领域的授权纪录。
它们证明了在代谢、移植等特定领域,中国药企也能产出具有全球竞争力的资产。
- **新兴技术平台公司**。如百奥赛图、药明生物等,凭借独特的抗体发现或CRDMO平台技术,在全球研发链条中扮演关键角色。在2026年AACR会议上,这类企业展示了大量新技术,如双载荷ADC、掩蔽型TCE等。
## 格局分层与终局推断:从“扫货”到“建厂”的产业出海
当前,中国创新药全球授权的玩家格局已清晰分层:

- **全球化巨头(恒瑞、百济)**:具备从研发、注册到商业化的全链条能力,模式上自主出海与合作授权并举。
- **创新驱动型Biotech(信达、康方、荣昌)**:以差异化的尖端管线和灵活的合作模式(Co-Co、股权绑定)为核心筹码,成为最活跃的交易方。
- **聚焦赛道的传统药企(石药、中国生物制药)**:在自身优势治疗领域产出“全球新”资产,实现单点突破。
- **技术平台型公司**:为整个生态提供研发、生产等基础设施支持。
这场转型的终局,远不止于交易额的飙升。更深层的变化在于合作模式的演进:从一次性买断的License-out,到风险共担的Co-Co(共同开发),再到更彻底的**NewCo(海外新设公司)模式**。2025年,中国药企完成**16笔NewCo出海交易**,涉及15家企业。
这种模式将管线海外权益注入独立海外主体,实现“股权绑定、全球运营”,标志着中国创新药正从“产品出海”迈向“产业出海”。
尽管挑战犹存——如欧美自主注册能力薄弱、国际化运营经验欠缺——但趋势已然不可逆转。中国创新药凭借其高效的研发体系、丰富的早期管线集群和不断提升的原始创新能力,正从全球医药创新的“成本洼地”,稳步迈向举足轻重的“价值高地”。
引进/卖出财报上市批准
100 项与 Vor Biopharma, Inc. 相关的药物交易
登录后查看更多信息
100 项与 Vor Biopharma, Inc. 相关的转化医学
登录后查看更多信息
组织架构
使用我们的机构树数据加速您的研究。
登录
或

管线布局
2026年06月09日管线快照
管线布局中药物为当前组织机构及其子机构作为药物机构进行统计,早期临床1期并入临床1期,临床1/2期并入临床2期,临床2/3期并入临床3期
药物发现
1
5
临床前
临床3期
1
5
其他
登录后查看更多信息
当前项目
登录后查看更多信息
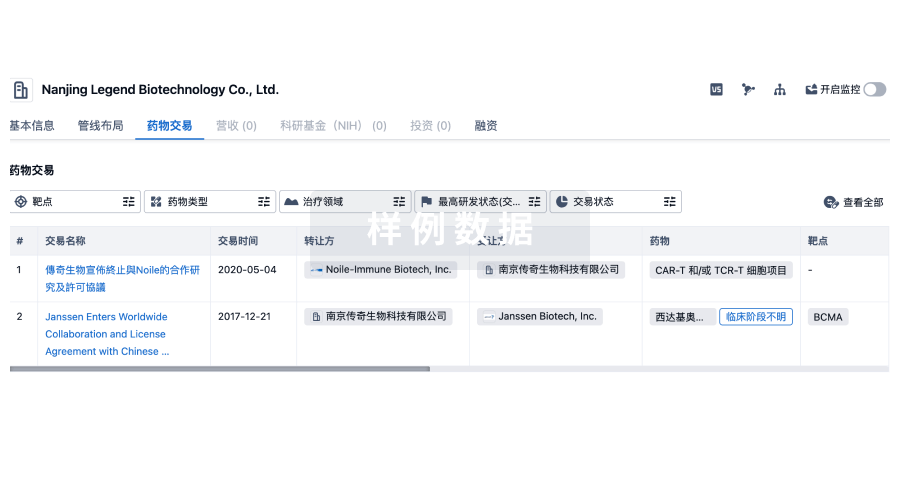
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
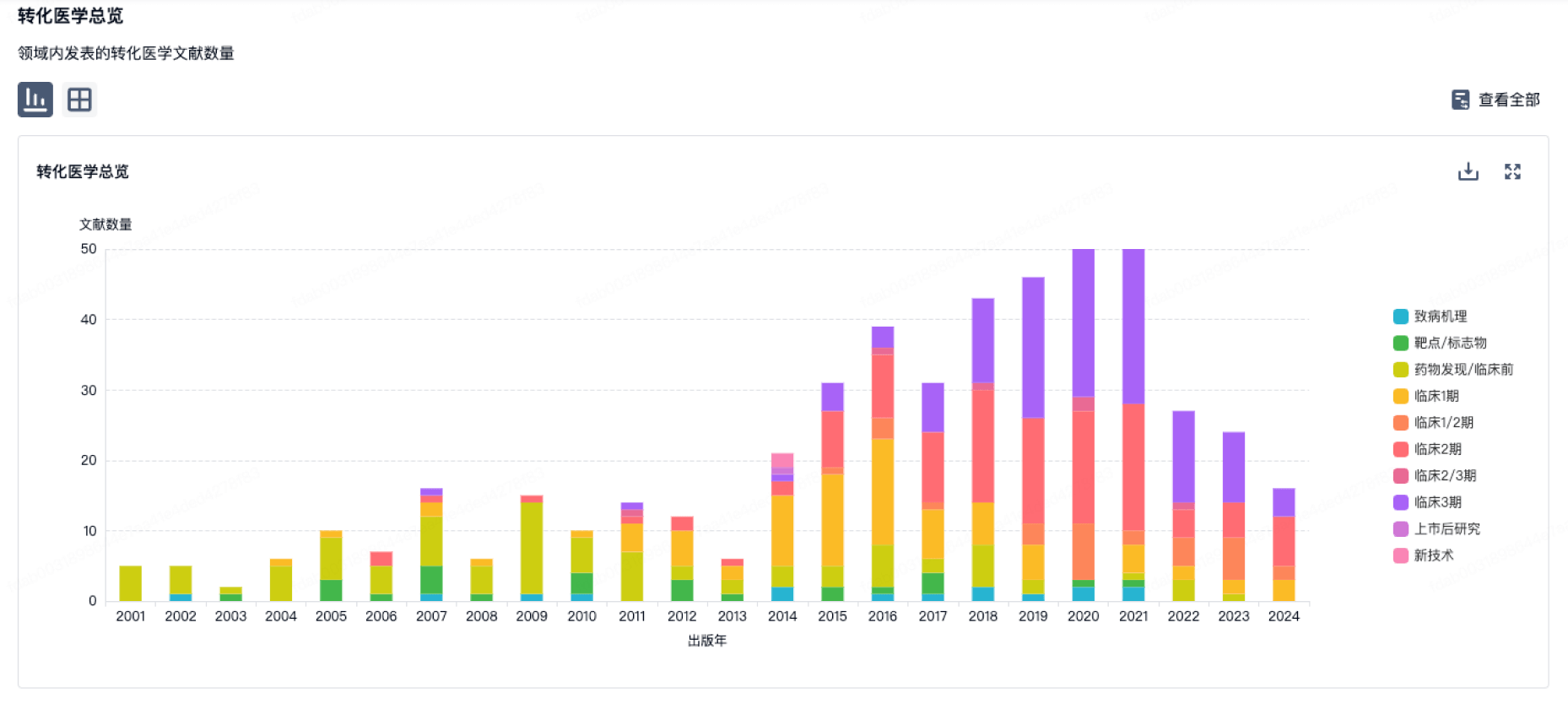
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
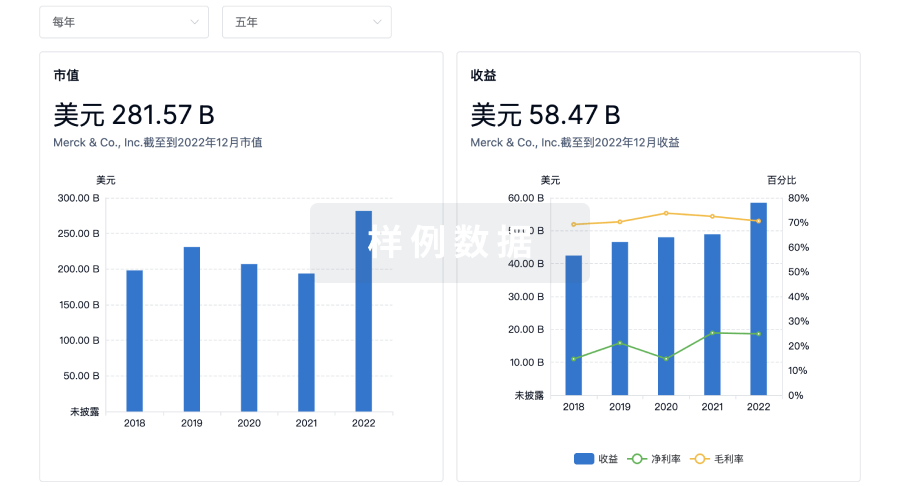
营收
使用 Synapse 探索超过 36 万个组织的财务状况。
登录
或
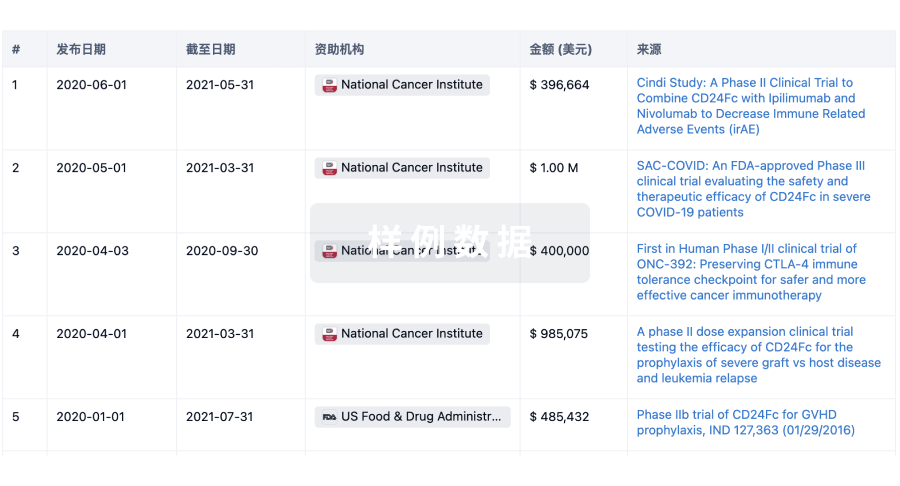
科研基金(NIH)
访问超过 200 万项资助和基金信息,以提升您的研究之旅。
登录
或
投资
深入了解从初创企业到成熟企业的最新公司投资动态。
登录
或
融资
发掘融资趋势以验证和推进您的投资机会。
登录
或
生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用
