预约演示
更新于:2025-10-29
Shanghai Junpaiyingshi Pharmaceutical Co., Ltd.
上海英派药业有限公司|合资公司 | 子公司|2020|中国上海市
上海英派药业有限公司|合资公司 | 子公司|2020|中国上海市
更新于:2025-10-29
概览
标签
肿瘤
呼吸系统疾病
泌尿生殖系统疾病
小分子化药
关联
1
项与 上海英派药业有限公司 相关的药物作用机制 PARP1抑制剂 [+1] |
在研机构 |
原研机构 |
最高研发阶段批准上市 |
首次获批国家/地区 中国 |
首次获批日期2025-01-14 |
3
项与 上海英派药业有限公司 相关的临床试验CTR20241823
一项开放、随机、单剂量、双交叉、比较中国健康受试者在空腹状态下单次口服IMP4297胶囊两种规格(10 mg和20 mg)的生物等效性研究。
主要目的: 中国健康男性受试者在空腹状态下,单次口服60 mg(3*20 mg规格)IMP4297胶囊和60 mg(6*10 mg规格)IMP4297胶囊,确定两者是否具有生物等效性。
开始日期2024-06-21 |
申办/合作机构 |
NCT05824455
An Open, Multicenter, Phase Ib/II Clinical Study of IMP4297 Capsule (JS109) Combined With Irinotecan in the Treatment of Advanced Malignant Solid Tumors
The Phase Ib study was designed to evaluate the safety of JS109 in combination with irinotecan in the treatment of advanced solid tumors and to determine the Phase II recommended dose (RP2D). The Phase II study was designed to evaluate the efficacy and safety of the combination regimen in patients with extensive small-cell lung cancer (SCLC) that failed first-line platinum-containing regimen.
开始日期2023-03-23 |
申办/合作机构 |
CTR20221169
一项在晚期实体瘤和小细胞肺癌患者中评估IMP4297与替莫唑胺联用的安全性、耐受性、药代动力学及抗肿瘤活性的Ⅰb/Ⅱ期、开放性、多中心、剂量递增和扩展研究
在晚期实体瘤和在接受1L含铂方案治疗后出现疾病进展的ES-SCLC患者中评估PARP抑制剂IMP4297与替莫唑胺联用的安全性、耐受性、PK特性及抗肿瘤活性。
开始日期2022-06-06 |
申办/合作机构 |
100 项与 上海英派药业有限公司 相关的临床结果
登录后查看更多信息
0 项与 上海英派药业有限公司 相关的专利(医药)
登录后查看更多信息
15
项与 上海英派药业有限公司 相关的新闻(医药)2025-10-27
·登高观识
2025年9月,国家药品监督管理局一次性批准12个新药上市,创下近年来单月审批数量新高。这一标志性事件背后,是2025年1-9月累计1168个品种的药品注册申请,其中161个为1类创新药的强劲申报态势。国产CDK4/6抑制剂"复妥宁"新适应症获批,全球首款PDE4B抑制剂"莫米司特"上市等案例,都彰显着中国创新药研发正在进入"快车道"。
然而,创新药的爆发式增长也带来了支付难题。当基本医保坚守"保基本"的定位时,这些承载着患者希望的创新疗法,其支付重任将不可避免地滑向商业健康险。商保,是迎来了梦寐以求的增量市场,还是背上了不可承受之重?
一、创新药获批全景:数量与质量的双重飞跃
1.1 审批效率显著提升
2025年前三季度,国家药监局共批准创新药56款,其中包括18款生物制品。已超过去年全年的总和(48款)。这一数据背后反映的是审评审批效率的大幅提升。创新药临床试验和上市申请的审评用时已从2017年的175个和420个工作日,分别缩短至2024年的50个和235个工作日。
审批加速不仅体现在时间上,还表现在批量审批的创新模式上。5月29日单日集中批准11款创新药,1-5月批准20余款1类创新药,均刷新近五年同期纪录。这种高效审批为创新药更快惠及患者提供了制度保障。
2025年第一季度(1月至3月)在国内获批上市的创新药清单
药品名称
研发公司
关键作用机理
获批适应症
核心特点
费用
塞纳帕利胶囊
上海英派药业有限公司
PARP1/2抑制剂
晚期上皮性卵巢癌、输卵管癌或原发性腹膜癌成人患者在一线含铂化疗缓解后的维持治疗
新型高效PARP抑制剂,具有高靶向选择性和广泛的安全窗口
20mg 规格的单价约为 60 元
利厄替尼片
江苏奥赛康药业有限公司
第三代EGFR酪氨酸激酶抑制剂(TKI)
用于治疗携带EGFR T790M突变阳性的局部晚期或转移性非小细胞肺癌(NSCLC)
具有自主知识产权的第三代EGFR-TKI,其二线适应症也于同期获批
零售价为 6800 元 / 盒
芪防鼻通片
北京以岭药业有限公司
中药(益气通窍)
改善肺脾两虚型持续性变应性鼻炎症状(如喷嚏、流涕等)
2025年获批的中药1.1类创新药,为变应性鼻炎患者提供新的治疗选择
268.00 元 / 盒
普卢格列汀片
石药集团欧意药业有限公司
DPP-4抑制剂(化药1类新药)
改善成人2型糖尿病患者的血糖控制
临床试验显示其降糖效果持久,安全性方面表现出色,不易诱发低血糖和导致体重增加
100mg 125 元
注射用瑞卡西单抗
广东恒瑞医药有限公司
PCSK9单抗
用于降低原发性高胆固醇血症和混合型血脂异常成人患者的低密度脂蛋白胆固醇等指标
注射间隔可长达8周,优于当时已获批的其他PCSK9单抗(通常需每2-4周注射一次)
1660 元 / 支,规格为 150mg
小儿黄金止咳颗粒
北京东方运嘉药业有限公司
中药(清肺化痰,肃肺止咳)
用于儿童轻度急性支气管炎痰热阻肺证引起的咳嗽
源自国医大师临床经验方,为儿童急性支气管炎咳嗽提供新的中药选择
169元/盒
艾米迈托赛注射液
铂生卓越生物科技(北京)有限公司
干细胞疗法(人脐带间充质干细胞)
治疗14岁以上、激素治疗失败的消化道受累为主的急性移植物抗宿主病
国内首款获批上市的干细胞治疗药物,标志着细胞治疗领域的重大进展
一次标准疗程15.84万元人民币
达伯乐® (己二酸他雷替尼胶囊)
信达生物制药
ROS1酪氨酸激酶抑制剂(TKI)
用于治疗ROS1阳性的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者
临床数据显示,对于初治患者客观缓解率(ORR)高达88.8%,中位无进展生存期长达45.6个月
约 14,520元 - 16,800元/盒
捷帕力® (匹妥布替尼片)
信达生物制药
BTK抑制剂(非共价可逆结合)
治疗复发或难治性 B 细胞恶性肿瘤
以其独特的非共价可逆结合方式,有望解决前代BTK抑制剂的耐药性问题
每盒售价约为 4 万元人民币
信必敏® (替妥尤单抗注射液)
信达生物制药
胰岛素样生长因子 1 受体(IGF—1R)抗体药物
治疗甲状腺眼病
信达生物在综合产品线领域获批的新药
病程费用约为 15-20 万人民币
利生奇珠单抗
艾伯维
IL-23抑制剂
中重度活动性克罗恩病
全球首个获批用于该适应症的IL-23抑制剂,提供随身给药器,患者可在家用药
尚未公布
2025年第二季度,国内创新药审批显著加速,在国内获批上市的部分创新药清单。
药品名称 (商品名)
研发公司
关键作用机理
获批适应症
核心特点
费用
苹果酸法米替尼胶囊 (艾比特)
恒瑞医药
小分子多靶点酪氨酸激酶抑制剂(TKI)
联合卡瑞利珠单抗用于既往治疗失败的复发或转移性宫颈癌
对c-Kit、VEGFR、PDGFR等多种激酶有明显抑制作用
尚未公布
氘恩扎鲁胺软胶囊 (海纳安)
海创药业
新型雄激素受体抑制剂
接受过阿比特龙及化疗后进展的转移性去势抵抗性前列腺癌(mCRPC)
为经治mCRPC患者提供了新的治疗选择
预测价格可能在 1.9万元/盒
枸橼酸伏维西利胶囊 (复妥宁)
锦州奥鸿药业
CDK4/6抑制剂
联合氟维司群用于HR阳性、HER2阴性复发或转移性乳腺癌
适用于既往内分泌治疗后疾病进展的患者
尚未公布
芦沃美替尼片 (复迈宁)
复星医药
MEK1/2选择性抑制剂
朗格汉斯细胞组织细胞增生症(LCH)等组织细胞肿瘤;2岁及以上NF1相关丛状神经纤维瘤(PN)
通过优先审评审批程序批准,覆盖成人罕见肿瘤及儿童患者
12,600元/盒(1mg)
注射用瑞康曲妥珠单抗 (艾维达)
恒瑞医药(子公司盛迪亚生物)
HER2抗体偶联药物(ADC)
存在HER2激活突变且经治的局部晚期或转移性非小细胞肺癌(NSCLC)
国内NSCLC领域首个获批的国产HER2 ADC,通过优先审评附条件批准
7800元/瓶 ,年度费用约43万元
注射用磷罗拉匹坦/帕洛诺司琼 (瑞坦宁)
恒瑞医药(子公司盛迪医药)
NK-1受体拮抗剂与5-HT3受体拮抗剂的复方制剂
预防高度致吐性化疗(HEC)引起的急性和迟发性恶心、呕吐
为化疗引起的恶心呕吐提供了新的预防方案
约 878.14 元/支
沙库巴曲阿利沙坦钙片 (S086)
信立泰
血管紧张素受体脑啡肽酶抑制剂(ARNi)类小分子药物
用于轻、中度高血压治疗
全球第二个ARNi类小分子药物,安全性优于现有ARNi药物
尚未公布
安瑞克芬注射液
海思科
- (镇痛新药)
用于腹部手术后轻、中度疼痛治疗
填补国内空白
昂拉地韦片
众生睿创
-
用于治疗甲型流感
-
枸橼酸戈来雷塞片
艾力斯
KRAS G12C抑制剂
用于KRAS G12C突变肺癌
成为国内首款同类药物
约 3.8万元/月
瑞格列汀二甲双胍片
恒瑞医药
-
用于治疗糖尿病
-
从这份清单可以看出2025年第二季度创新药审批的一些特点:肿瘤领域持续领跑
:获批的创新药中,抗肿瘤药物占据了绝对主力,覆盖了宫颈癌、前列腺癌、乳腺癌、肺癌等多个高发癌种,并且技术路径多样,包括靶向药(TKI、CDK4/6抑制剂)、ADC、免疫联合疗法等。罕见病与儿童用药受关注
:例如复星医药的芦沃美替尼片,其适应症涵盖了朗格汉斯细胞组织细胞增生症和儿童神经纤维瘤病,体现了对罕见病和儿童患者群体的关注。非肿瘤领域亦有突破
:在糖尿病、高血压、术后镇痛、流感治疗等领域也有新药获批,满足了不同的临床需求。
2025年第三季度国内获批重点创新药一览
药品名称 (商品名)
研发公司
关键作用机理
获批适应症
核心特点
泽美妥司他片 (艾瑞璟)
恒瑞医药
EZH2抑制剂 (组蛋白甲基转移酶抑制剂)
既往接受过至少1线系统性治疗的复发或难治外周T细胞淋巴瘤(PTCL)成人患者
是首款国产EZH2抑制剂,通过优先审评审批程序附条件批准上市,为PTCL患者提供了新的治疗选择
昂拉地韦片
众生睿创 (众生药业控股子公司)
- (抗病毒药物)
用于治疗甲型流感
一类创新药物,为流感治疗提供了新的用药选择
罗泽利昔珠单抗注射液 (优迪革®)
优时比 (UCB)
- (生物制剂)
用于治疗重症肌无力
全球创新生物制剂,于2025年5月底在国内正式上市,为国内重症肌无力治疗领域带来新进展
莱博雷生片
卫材 (Eisai)
- (失眠治疗药)
治疗成人失眠,尤其适用于入睡困难及/或睡眠维持困难人群
此前已在包括美国、日本在内的多个国家和地区上市,此次正式进入中国市场
从2025年第三季度的获批情况来看,创新药的研发继续聚焦于填补临床空白和满足未竟的医疗需求,特别是在肿瘤、神经系统疾病、传染性疾病等领域。
对于刚获批的创新药,其价格制定和进入医保目录通常需要一个过程,咨询主治医生或医院药房是获取准确信息最直接的途径。
1.2 技术平台多元化突破
2025年获批的创新药展现出强大的源头创新能力。ADC(抗体药物偶联物)、双特异性抗体、基因和细胞治疗等前沿技术领域的成果集中涌现。我国首个干细胞治疗产品和首个血友病基因治疗产品的获批,实现了"全球首发"。
在治疗领域方面,虽然抗肿瘤药物依然是主力(上半年获批18款,占比约40%),但在代谢性疾病、自身免疫病以及罕见病等领域也取得了重要突破。全球首个GCG/GLP-1双受体激动减重药物信达玛仕度肽、恒瑞医药的硫酸艾玛昔替尼片等产品,满足了多样化的临床需求。
1.3 国产创新与国际认可
2025年上半年,中国创新药达成的对外授权交易总金额接近660亿美元,已超过2024年全年的519亿美元。三生制药与辉瑞达成总金额高达60.5亿美元的授权协议,刷新了纪录。这些数据充分证明了国际医药巨头对中国原创研发实力的认可。
二、支付压力
2.1 基本医保的"天花板"效应
2024年中国创新药械市场规模约1620亿元,其中个人现金支付占比高达49%,而商业健康险支付仅占7.7%。这一结构性失衡凸显了在医保"保基本"和个人自付之间存在的巨大支付空白。
随着DRG/DIP支付方式改革的全面推进,医院使用高价创新药的动力不足。即使创新药被纳入医保范围,患者也常常面临"有药无方"的困境。在集采和DRG支付方式改革背景下,医疗机构配备创新药的积极性受到影响。
2.2 惠民保的衔接与局限
普惠型商业健康保险在各地迅猛发展,成为商保参与创新药支付的重要突破口。例如"龙江惠民保"累计参保人数达936.67万人,参保保费13.84亿元,已为12.90万人赔付11.43亿元。
然而,惠民保百亿级保费池难以支撑千亿级创新药市场的精算逻辑。2024年惠民保对创新药总支付约18亿元,仅占创新药市场的1%,无法单独承担支付重任。
三、商保衔接
3.1 市场机遇与产品创新
创新药支付领域为商保公司提供了高达千亿级的潜在市场。各险企积极创新产品设计,开发与商保创新药目录动态挂钩的保险产品、探索带病体保险扩大保障人群、尝试"疗效保证+保险"模式与药企共担风险。
3.2 风控挑战与数据壁垒
创新药支付对保险公司的专业能力提出了极高要求。缺乏历史赔付数据使得高值创新药的精准定价和风险管理构成巨大挑战。医疗机构、药企和保险公司之间的数据互通仍存在诸多壁垒,导致险企难以获取准确的用药效果和费用数据。
道德风险与逆向选择也是重要挑战。高危人群投保倾向更高,可能导致风险池失衡。如果保险公司无法有效评估和管理风险,可能导致赔付率大幅上升,甚至影响盈利能力。
2025年7月国家医保局发布的《支持创新药高质量发展的若干措施》首次提出设立"商业健康保险创新药品目录"。该政策配套了三大关键支持:目录内药品不计入基本医保自费率考核、不列入集采可替代药品监测范围、以及单独定价与结算机制。
当患者、药企、保险和医疗系统真正实现共赢,一个更具韧性和创新活力的健康中国生态也将随之加速到来。商业健康险在创新药支付领域的深度参与,不仅关乎行业自身发展,更关乎国家多层次医疗保障体系的完善和医药创新产业的可持续发展。
注:由于新药上市时间短,本文提到的药品价格部分是估算数据,具体以官方公布数据为准。
上市批准加速审批
2025-04-02
·药事纵横
2025年第一季度,国家药品监督管理局(NMPA)在创新药物审批方面取得了显著进展,共批准了16款新药上市,涵盖了抗病毒感染、肿瘤治疗、自身免疫性疾病、代谢性疾病等多个领域。这些新药的获批不仅丰富了临床治疗选择,也为患者带来了新的希望。以下是获批新药的具体情况:一、抗病毒感染领域突破1.艾考磷布韦片(东英贺)·获批时间:2025年3月27日·企业:宜昌东阳光长江药业股份有限公司·适应症:与磷酸萘坦司韦胶囊联用,治疗初治或干扰素经治的基因1、2、3、6型成人慢性丙型肝炎病毒(HCV)感染,可合并或不合并代偿性肝硬化。2.玛舒拉沙韦片(伊速达)·获批时间:2025年3月27日·企业:江西科睿药业有限公司·适应症:适用于既往健康的12岁及以上青少年和成人单纯性甲型和乙型流感患者的治疗,不包括存在流感相关并发症高风险的患者。3.磷酸萘坦司韦胶囊(东卫卓)·获批时间:2025年2月8日·企业:广东东阳光药业股份有限公司·适应症:与艾考磷布韦片联用,治疗初治或干扰素经治的基因1、2、3、6型成人慢性丙型肝炎病毒(HCV)感染,可合并或不合并代偿性肝硬化。4.复方比那甫西颗粒·获批时间:2025年2月27日·企业:新疆银朵兰药业股份有限公司·适应症:用于热性感冒(发热、鼻塞、流涕、咽痛、头痛、口干等),基于维吾尔医药理论组方,具有清除异常体液质的功效。二、肿瘤治疗领域创新1.伊那利塞片(伊赫莱)·获批时间:2025年3月14日·企业:Roche Pharma(Schweiz)AG·适应症:联合哌柏西利和氟维司群,适用于内分泌治疗耐药(包括在辅助内分泌治疗期间或之后出现复发)、PIK3CA 突变、激素受体(HR)阳性、人表皮生长因子受体 2(HER2)阴性的局部晚期或转移性乳腺癌成人患者。2.塞纳帕利胶囊(派舒宁)·获批时间:2025年1月16日·企业:上海英派药业有限公司·适应症:适用于晚期上皮性卵巢癌、输卵管癌或原发性腹膜癌成人患者在一线含铂化疗达到完全缓解或部分缓解后的维持治疗。3.利厄替尼片(奥壹新)·获批时间:2025年1月16日·企业:江苏奥赛康药业有限公司·适应症:适用于既往经表皮生长因子受体(EGFR)酪氨酸激酶抑制剂(TKI)治疗时或治疗后出现疾病进展,并且经检测确认存在EGFR T790M 突变阳性的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者的治疗。4.菲诺利单抗注射液(安佑平)·获批时间:2025年2月8日·企业:神州细胞工程有限公司·适应症:本品与含铂化疗联合用于复发性和/或转移性头颈部鳞状细胞癌的一线治疗。菲诺利单抗注射液是一种重组人源化抗程序性死亡受体-1(PD-1)单克隆抗体,可通过阻断PD-1与其配体的结合,从而抑制肿瘤的生长。三、自身免疫性疾病管理1.硫酸艾玛昔替尼片(艾速达)·获批时间:2025年3月21日·企业:江苏恒瑞医药股份有限公司·适应症:适用于对一种或多种TNF抑制剂疗效不佳或不耐受的活动性强直性脊柱炎成人患者。2.艾米迈托赛注射液(睿铂生)·获批时间:2025年1月2日·企业:铂生卓越生物科技(北京)有限公司·适应症:用于治疗14岁以上消化道受累为主的激素治疗失败的急性移植物抗宿主病。移植物抗宿主病是异基因造血干细胞移植后,来源于供者的淋巴细胞攻击受者组织发生的一类多器官综合征,表现为主要累及皮肤、胃肠道、肝、肺和黏膜表面的组织炎症、纤维化等。3.斯泰度塔单抗注射液(新替妥)·获批时间:2025年2月14日·企业:珠海泰诺麦博制药股份有限公司·适应症:用于成人破伤风紧急预防。本品为重组抗破伤风毒素单克隆抗体,主要通过结合破伤风毒素的AB片段,起到被动免疫作用。四、代谢性疾病调控1.普卢格列汀片(善泽平)·获批时间:2025年1月10日·企业:石药集团欧意药业有限公司·适应症:改善成人2型糖尿病患者的血糖控制。2.注射用瑞卡西单抗(艾心安)·获批时间:2025年1月10日·企业:广东恒瑞医药有限公司·适应症:在控制饮食的基础上,与他汀类药物、或者与他汀类药物及其它降脂疗法联合用药,用于接受中等或以上剂量他汀类药物治疗仍无法达到低密度脂蛋白胆固醇(LDL-C)目标的原发性高胆固醇血症(包括杂合子型家族性和非家族性高胆固醇血症)和混合型血脂异常的成人患者;或单药用于非家族性高胆固醇血症和混合型血脂异常的成人患者,以降低低密度脂蛋白胆固醇(LDL-C)、总胆固醇(TC)、载脂蛋白B(ApoB)水平。五、特殊人群用药1. 小儿黄金止咳颗粒·获批时间:2025年1月3日·企业:北京东方运嘉药业有限公司·适应症:用于儿童轻度急性支气管炎痰热阻肺证引起的咳嗽,舌红苔薄黄或黄腻。2025年第一季度NMPA批准的16款新药,展现了我国在创新药物研发领域的快速进步。这些药物覆盖了从常见病到罕见病的广泛适应症,尤其在抗病毒、肿瘤免疫治疗和代谢性疾病领域实现了重要突破。随着更多创新药物的上市,患者将获得更精准、更安全的治疗选择,推动我国医疗健康事业持续发展。药事纵横投稿须知:稿费已上调,欢迎投稿
上市批准申请上市
2025-02-25
·英派药业
2025年2月20日下午,上海市药监局由局党组成员、二级巡视员张清带队,在药品注册处、药品监管处、上海药品审评核查中心相关负责人陪同下,联合国家药监局药品审评检查长三角分中心范乙主任及医学审评部、药学审评部相关负责人莅临上海英派药业有限公司视察指导。
公司两位创始人蔡遂雄博士、田野博士及企业负责人马宁总全程陪同,重点围绕公司发展历史、创新管线布局、全球化战略规划及上市后管理计划等做了专题汇报。各位领导对英派管线内的创新药产品早期临床开发、上市后管理及出海等工作给予了高度的重视和指导,就行业政策、上市后研究、上市后检查等议题展开了深入的交流。
塞纳帕利胶囊(商品名:派舒宁)是2025年上海市获批上市的第一款创新药。在上海药监局的帮助和指导下,实现了获得药品注册证书后72小时内首方上市。上海药监局领导充分肯定了英派药业在临床研究、药学研究中的合规性,并围绕塞纳帕利胶囊上市后的全生命周期管理计划提出了指导性意见,在符合《个人信息保护法》及相关法规要求下持续开展收集真实世界数据,积极开发新的适应症及联合用药,鼓励企业把握政策红利,依据ICH指导原则推进国际多中心临床试验,努力加快国产创新药的出海,提升国产创新药的全球竞争力。对于具有重大临床价值的创新产品,将结合上海药监局“一清单、两优化、三联动”的服务机制,在申报准备、启动实施、现场核查等关键环节,主动跨前,加强服务。
药品长三角分中心领导也表示,对于具有重大临床价值的重点品种,分中心将在一般性技术问题解答、面对面咨询、沟通交流会等方面给予企业更多的指导服务,为重点品种稳步推进保驾护航,加快新药好药上市进程。
此次视察工作标志着监管机构对英派药业创新能力的认可,也为公司未来管线药品的研究与发展指明了方向。英派药业团队将全面落实各位药监部门领导的指导意见,加快推动在研管线的临床开发和上市进程,持续深化与监管机构的沟通交流,紧跟政策,打造开放型创新生态,力争为广大癌症患者带来更多的创新好药。
100 项与 上海英派药业有限公司 相关的药物交易
登录后查看更多信息
100 项与 上海英派药业有限公司 相关的转化医学
登录后查看更多信息
组织架构
使用我们的机构树数据加速您的研究。
登录
或

管线布局
2026年06月09日管线快照
管线布局中药物为当前组织机构及其子机构作为药物机构进行统计,早期临床1期并入临床1期,临床1/2期并入临床2期,临床2/3期并入临床3期
批准上市
1
登录后查看更多信息
当前项目
| 药物(靶点) | 适应症 | 全球最高研发状态 |
|---|---|---|
塞纳帕利 ( PARP1 x PARP2 ) | 晚期恶性实体瘤 更多 | 临床2期 |
登录后查看更多信息
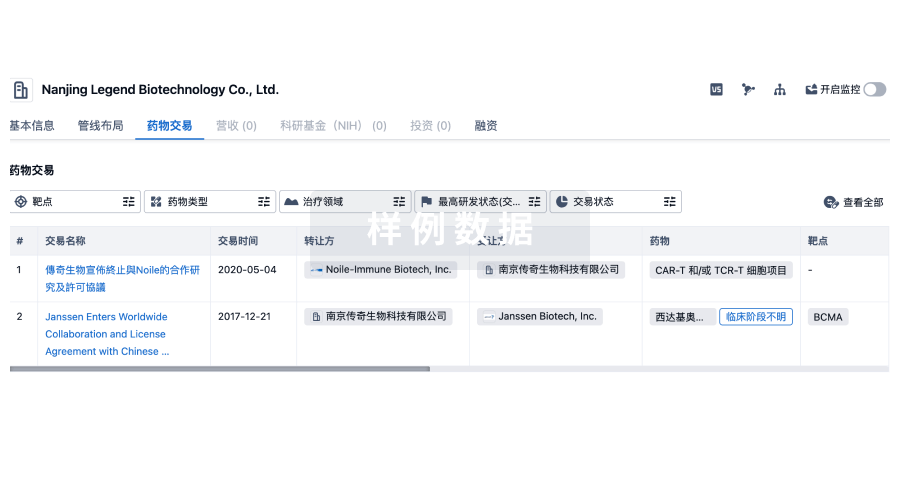
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
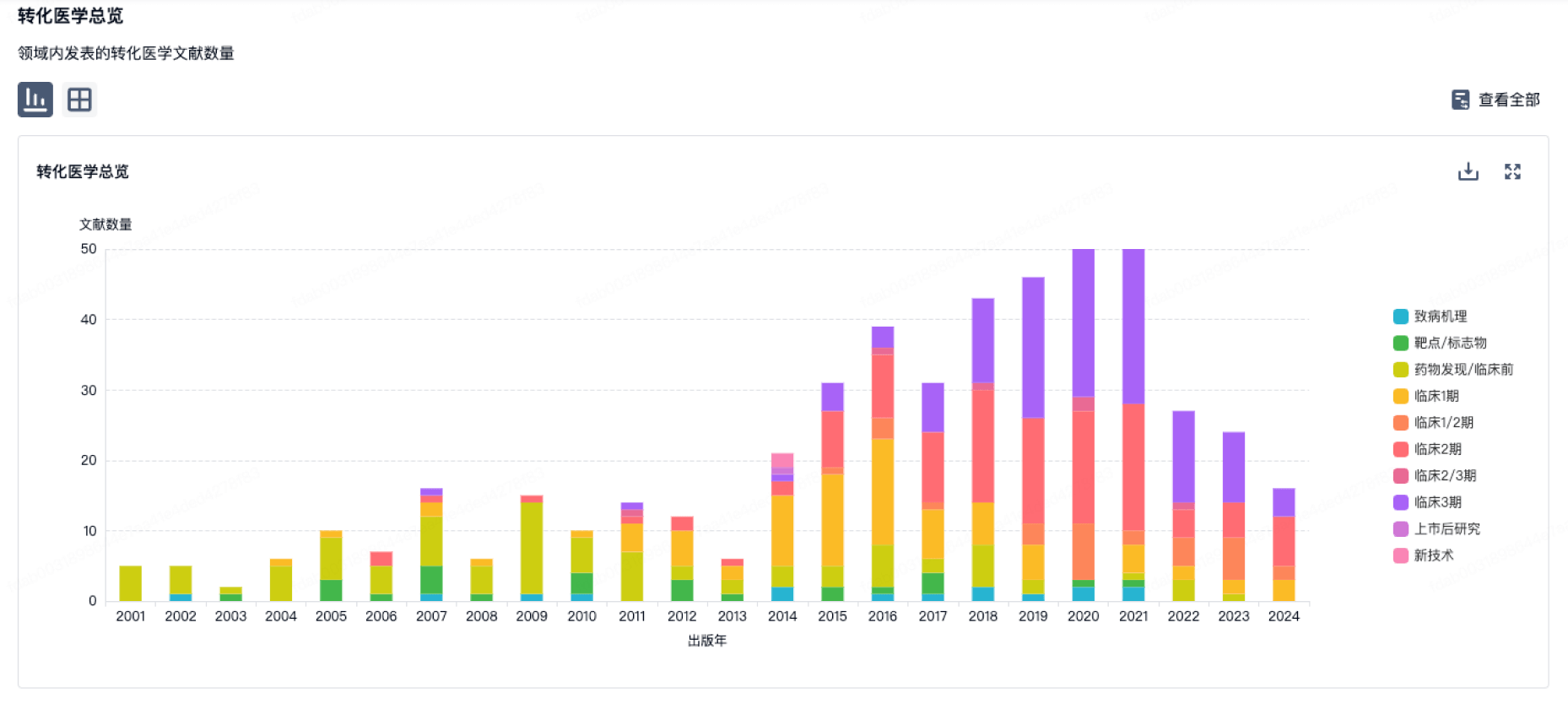
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
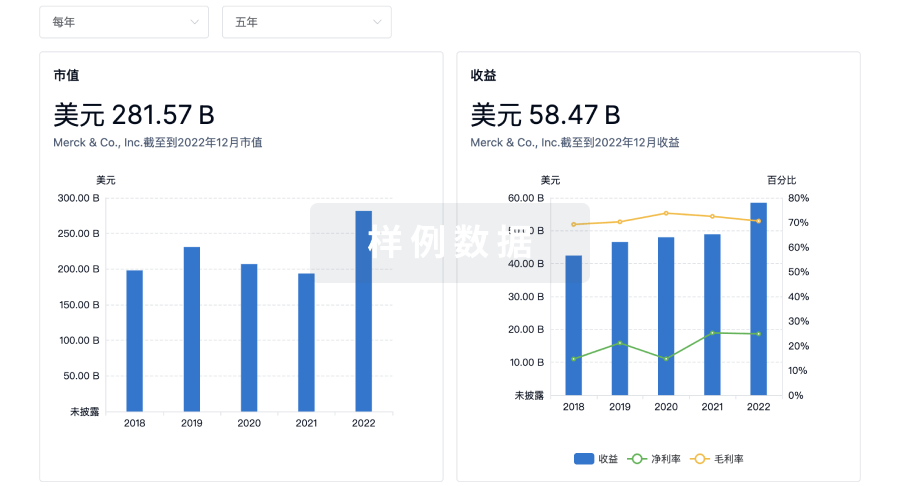
营收
使用 Synapse 探索超过 36 万个组织的财务状况。
登录
或
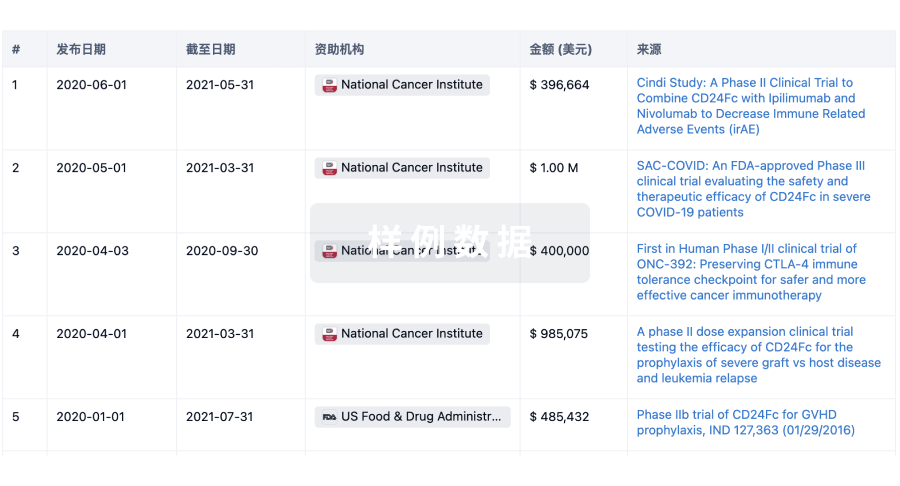
科研基金(NIH)
访问超过 200 万项资助和基金信息,以提升您的研究之旅。
登录
或
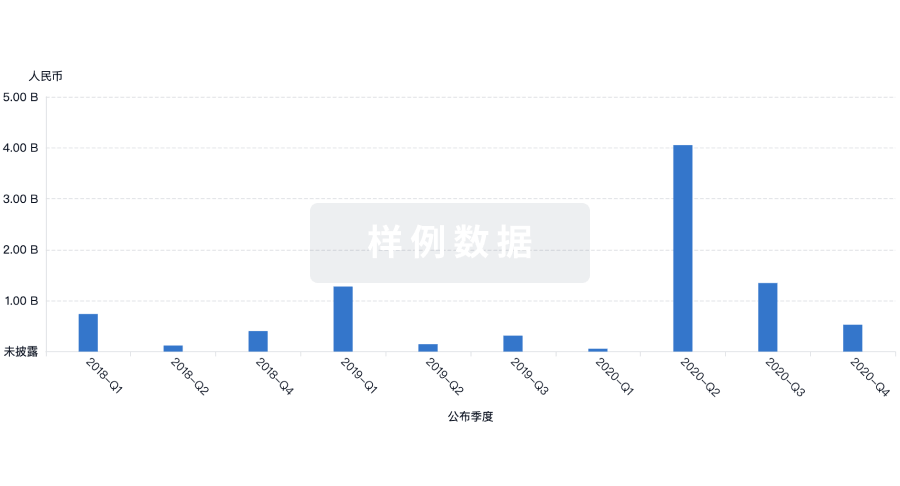
投资
深入了解从初创企业到成熟企业的最新公司投资动态。
登录
或
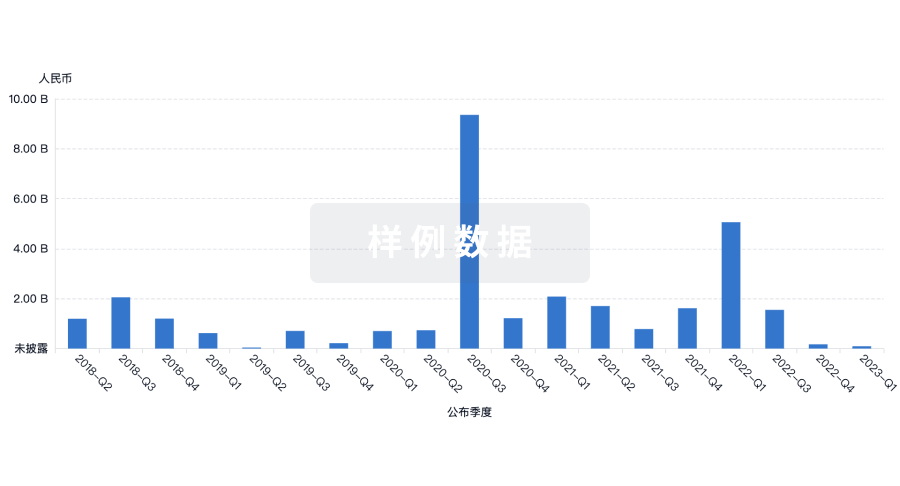
融资
发掘融资趋势以验证和推进您的投资机会。
登录
或
生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用
