甘李药业开发GLP-1R激动剂GZR18 IIb期肥胖研究积极,减重效果显著!
7月22日,甘李药业宣布,GZR18用于成人肥胖/超重的IIb期临床试验取得了积极结果,每2周1次12mg、18mg、24mg、48mg以及每周1次24mg剂量组患者在治疗30周后,平均体重较基线分别降低了11.15%、13.22%、14.25%、17.29%和17.78%。
GZR18注射液是甘李药业开发的一种每一周/每两周给药一次的GLP-1R激动剂,旨在治疗成人2型糖尿病及肥胖/超重个体的体重管理。早期临床数据表明GZR18能够有效降低血糖水平和体重。目前,GZR18的全球开发已进入II期临床研究阶段。
该IIb期临床试验(CTR20231695)是一项多中心、随机、双盲、安慰剂对照研究,在中国25家临床试验中心共计招募340名受试者,均为经饮食运动控制不佳的成年超重(BMI≥24 kg/m2)且伴有至少一种体重相关合并症或肥胖(BMI≥28 kg/m2)的受试者。受试者随机接受每两周一次12 mg、18 mg、24 mg、48 mg以及每周一次24 mg GZR18注射液或安慰剂治疗30周(含剂量递增期),研究的主要疗效终点为治疗30周后体重相对基线变化的百分比。本研究评估了受试者平均体重、腰围、腰臀比(腰围/臀围)、体重指数(BMI)、糖代谢指标等相对基线的变化,以及药物的安全性与耐受性。治疗30周后,与安慰剂对照组相比,不同剂量和给药频次的GZR18注射液(每两周一次12 mg,18 mg、24 mg和48 mg;每周一次24 mg)受试者体重自基线变化百分比显著降低。GZR18注射液组受试者平均体重自基线分别降低11.15%(12 mg组,每两周一次)、13.22%(18 mg组,每两周一次)、14.25%(24 mg组,每两周一次)、17.29%(48 mg组,每两周一次)和17.78%(24 mg组,每周一次),均优效于安慰剂组(降低0.99%)。每两周一次48 mg剂量组与每周一次24 mg剂量组的减重比例之间未见显著差异(单侧检验,P>0.025)。本研究中,每两周一次的GZR18注射液总体安全性和耐受性良好,与GLP-1受体激动剂的已知安全性特征一致。最常见的不良事件为胃肠道反应,大多数事件的严重程度为轻中度,与同类药物相当。该IIb期研究更为全面的结果计划于今年晚些时候公布,并将在同行评审期刊上发表。
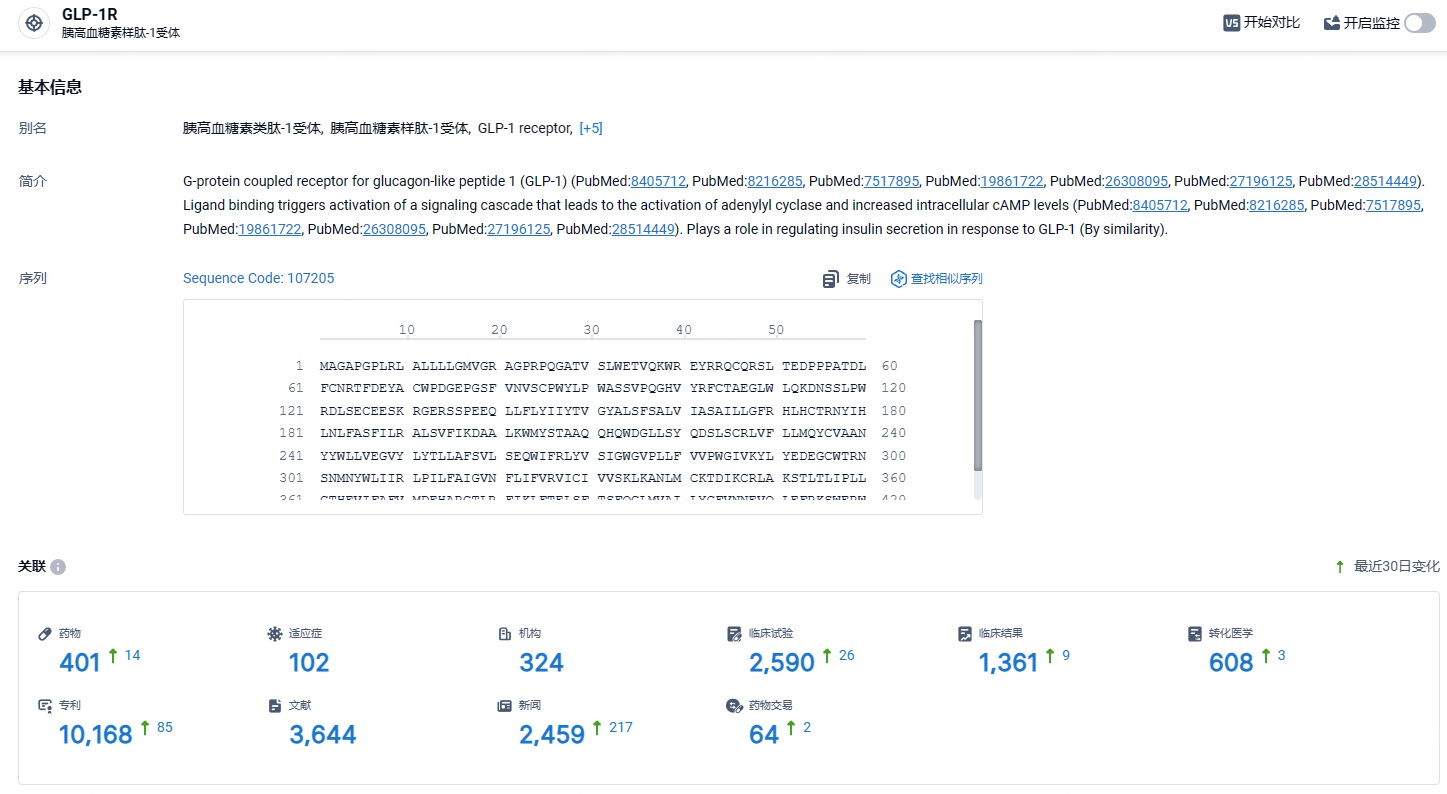
根据智慧芽新药情报库所披露的信息 (点击下方卡片直达GLP-1R靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2024年7月24日,GLP-1R靶点共有在研药物401个,包含的适应症有102种,在研机构324家,涉及相关的临床试验2590件,专利多达10168件……目前,甘李药业拥有六款核心胰岛素产品,包括五个胰岛素类似物品种:长效甘精胰岛素注射液(长秀霖®)、速效赖脯胰岛素注射液(速秀霖®)、门冬胰岛素注射液(锐秀霖®)、预混精蛋白锌重组赖脯胰岛素混合注射液(25R)(速秀霖® 25)、门冬胰岛素30注射液(锐秀霖® 30);以及人胰岛素品种:预混精蛋白人胰岛素混合注射液(30R)(普秀霖®30),产品覆盖长效、速效、预混三个胰岛素功能细分市场。同时,公司产品覆盖相关医疗器械,包括可重复使用的胰岛素注射笔(秀霖笔®)和一次性注射笔用针头(秀霖针®)。GLP-1R药物的开发有助于甘李药业在降糖减重领域的占据稳固地位。