免疫方舟CD40/4-1BB双功能分子IMB071703获FDA批准临床,针对实体瘤
2024年2月22日,免疫方舟宣布,其自主研发的针对肿瘤微环境的免疫激活剂IMB071703注射液正式获得美国FDA批准开展临床试验。
IMB071703作为免疫方舟利用自有XFab平台开发的双功能性融合蛋白,可同时靶向4-1BB x CD40信号通路,其被开发用来激活先天免疫和适应性免疫的有效反应,以及削弱肿瘤防御。IMB071703可以实现APC与T细胞在时间和空间上的连接,还可使DC成熟,促进抗原提呈,然后促进T细胞的活化和增殖。IMB071703具有独特的DC-T细胞衔接功能,其活化特异性细胞毒性T细胞显著优于传统的非特异性免疫刺激剂。
根据免疫方舟在2022年第18届基本蛋白质工程与细胞疗法波士顿年会(PEGS-BOSTON)上公布的IMB071703临床前研究结果:体外功能实验结果表明,IMB071703可以与细胞表面的4-1BB和/或CD40结合,触发NF-κB信号通路;体内药效试验结果表明,肿瘤内单独给药IMB071703可以显著抑制MC38小鼠肿瘤的生长,此外,静脉注射IMB071703联合化疗药物吉西他滨可以抑制Panc02小鼠肿瘤的生长;药物的毒理研究表明IMB071703在食蟹猴中具有良好的耐受性,其毒性参数显著高于对照水平。
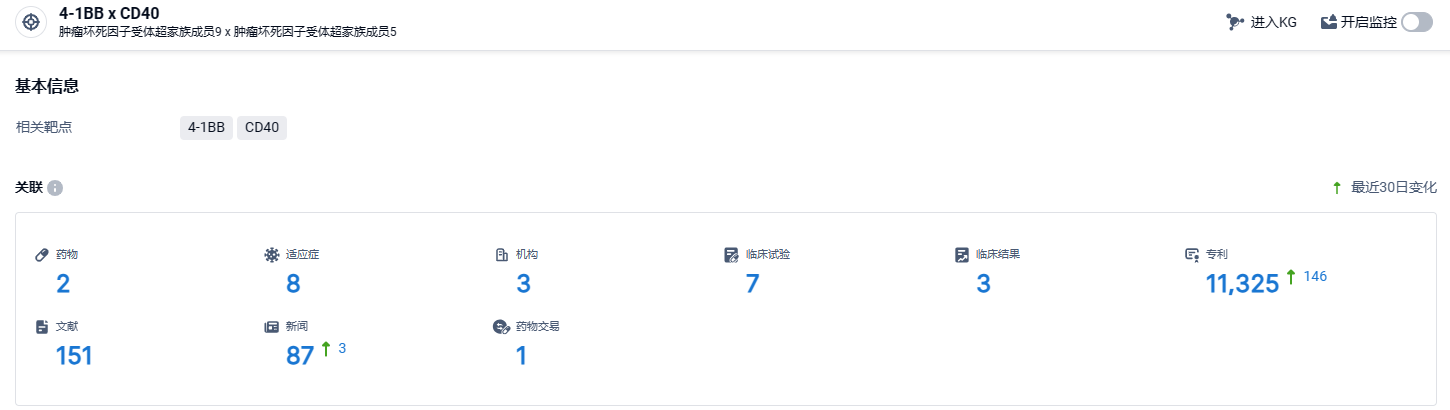
根据智慧芽新药情报库所披露的信息 (点击下方卡片直达4-1BB x CD40靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2024年2月24日,4-1BB x CD40靶点共有在研药物2个,包含的适应症有8种,在研机构3家,涉及相关的临床试验7件,专利多达11325件……中国药物临床试验登记与信息公示平台显示,目前IMB071703正在上海市东方医院开展1期临床研究,以评估治疗复发或转移的晚期恶性实体瘤患者的安全性、耐受性、药代动力学特征和初步疗效。期待IMB071703后续研发顺利。




