罗氏/Poseida非病毒CAR-T疗法临床结果积极,多发性骨髓瘤ORR达82%!
2023年12月12日,Poseida Therapeutics宣布其与罗氏(Roche)共同开发的在研同种异体CAR-T疗法P-BCMA-ALLO1临床1期试验的早期疗效和安全性积极结果,该疗法用于治疗复发/难治性多发性骨髓瘤(RRMM)患者。
P-BCMA-ALLO1是一款BCMA靶向的同种异体、富含干细胞记忆型T细胞(TSCM)的在研“现货型”CAR-T疗法,是通过非病毒载体piggyBac的DNA修饰系统所开发,能将表达CAR的转基因运送到T细胞内,且载体能装载更多的遗传物质。这有望带来成本更低、生产时间更短的CAR-T疗法,且避免潜在安全性风险。2022年8月,Poseida与罗氏达成策略性合作与许可协议,将合作开发包含P-BCMA-ALLO1在内的现货型同种异体CAR-T疗法。根据此项协议,Poseida将获得1.1亿美元的预付款,有资格获得研究、开发、发布、净销售里程碑以及其他付款,总额可能高达60亿美元。与此同时,罗氏将从Poseida获得独家授权,对P-BCMA-ALLO1等同种异体CAR-T项目进行开发和商业化。
在该试验中,可评估患者(n=33)的随访时间至少4周,且皆接受了大量预治疗,中位既往治疗线数为7线。分析显示,在接受充分淋巴细胞耗竭的强化预治疗患者中,接受CAR-T疗法P-BCMA-ALLO1治疗患者的客观缓解率(ORR)为82%(n=9/11),并具有深度临床缓解。而在既往未接受过B细胞成熟抗原(BCMA)靶向双特异性T细胞衔接抗体治疗患者的ORR则为100%。该疗法展现良好的安全性和可靠性特征,所有意向治疗(ITT)患者均未观察到移植物抗宿主病(GvHD)或剂量限制性毒性,且观察到的细胞因子释放综合征(CRS)和神经毒性发生率较低(均≤2级)。
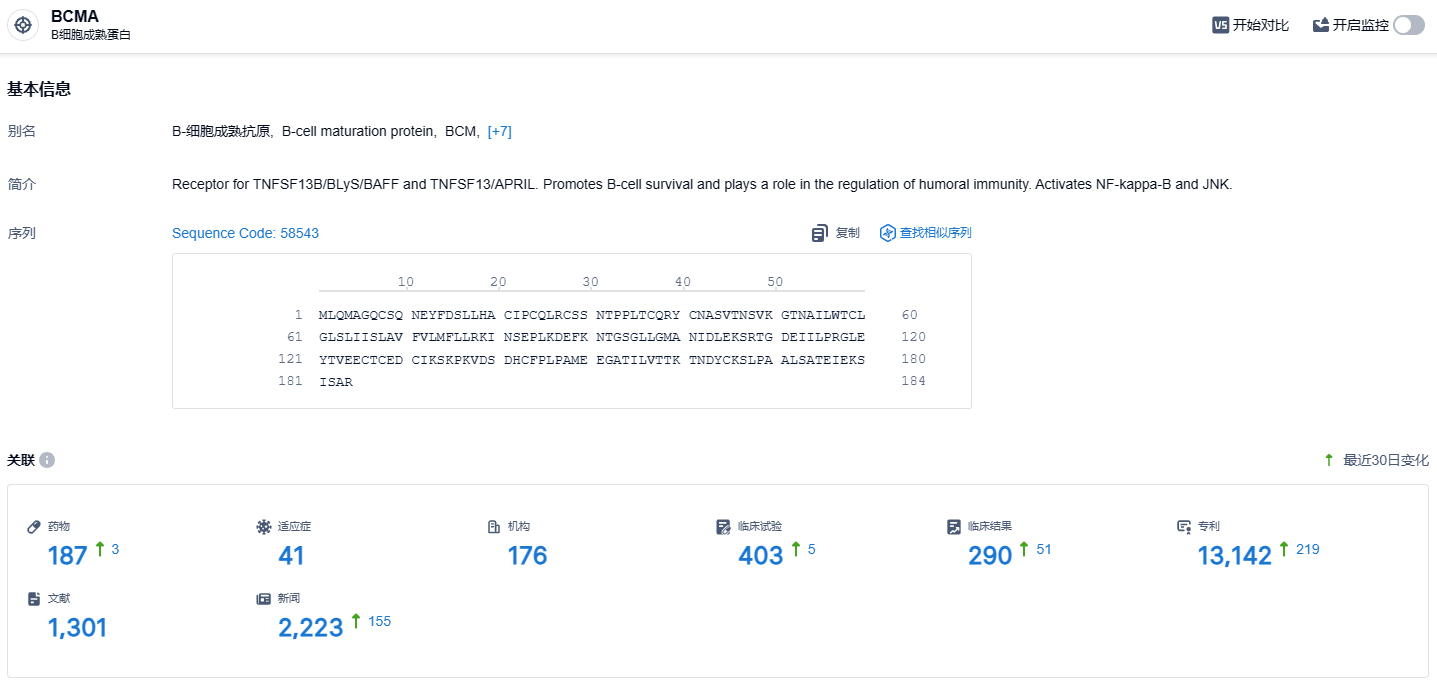
根据智慧芽新药情报库所披露的信息 (点击下方卡片直达BCMA靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2023 年12月13日,BCMA靶点共有在研药物187个,包含的适应症有41种,在研机构176家,涉及相关的临床试验403件,专利多达13142件……从目前的技术来看,生产CAR-T疗法的主要方法基于病毒,而病毒能运送的遗传物质有限,且有安全性上的潜在风险。而piggyBac DNA系统不使用病毒,就能将CAR分子运送到T细胞内,且运送的遗传物质要更多。这有望带来成本更低、生产时间更短的CAR-T疗法,解决当下的瓶颈。