预约演示
JCI | 科学家识别出癌症免疫逃逸的新型调节子
免疫疗法基因疗法
调节肿瘤PD-L1的表达对于提高研究人员对肿瘤免疫逃逸的理解和改进当前抗肿瘤免疫疗法至关重要。近日,一篇发表在国际杂志Journal of Clinical Investigation上题为“CRISPR screening identifies the deubiquitylase ATXN3 as a PD-L1–positive regulator for tumor immune evasion”的研究报告中,来自美国西北大学等机构的科学家们识别出了一种此前未知的肿瘤免疫逃逸调节子,这或许有望帮助改善当前以及未来的抗肿瘤免疫疗法的疗效。
研究者Deyu Fang博士说道,本文研究有助于我们理解为何不能利用免疫检查点阻断疗法去治疗一些癌症患者。
抗肿瘤免疫疗法是一种能帮助机体免疫系统抵御癌症的特殊癌症疗法,其包括一系列疗法类型,比如免疫检查点抑制剂等,免疫检查点能帮助预防免疫系统过于强大从而消除包括癌细胞在内的其它细胞。通过利用检查点抑制剂药物来靶向作用这些检查点,免疫系统就能更好地产生反应并抵御癌细胞,然而,并非所有患者都会对免疫疗法产生反应,其背后的原因目前研究人员并不清楚。
目前最大的问题在于是否研究人员能找到一种更好的方法来让疗法对所有患者都有效;抗肿瘤免疫疗法药物所靶向作用的一种常见的免疫检查点蛋白是PD-L1,其能在免疫细胞表面表达,而且在某些癌细胞表面的表达量会增加,这或许就能帮其逃避免疫系统的攻击。因此,识别出肿瘤中PD-L1表达的新型调节子或能帮助改善抗肿瘤免疫疗法的疗效。
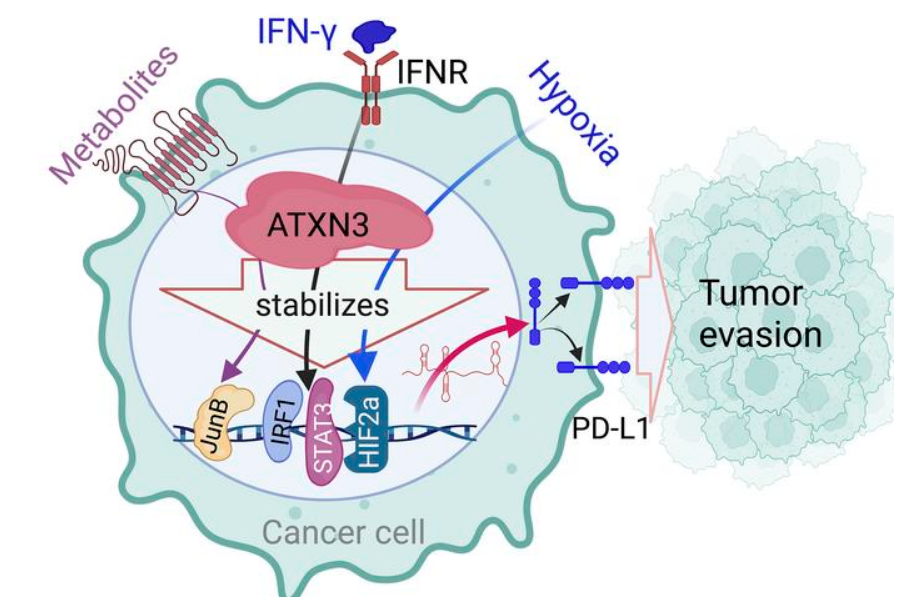
Preview
来源: 生物谷
如果研究人员能将ATNX3抑制剂与当前的抗肿瘤免疫疗法相结合,他们或许就能改善疗法的疗效并减少所需抗体的数量,也就意味着患者的治疗副作用会明显降低。综上,本文研究中,研究人员确定了此前未知的去泛素化酶ATXN3或能作为PD-L1转录的正向调节子,并为靶向作用ATXN3,从而使免疫检查点阻断疗法更敏感提供了一定的理论依据。
参考文献:Shengnan Wang,Radhika Iyer,Xiaohua Han, et al. CRISPR screening identifies the deubiquitylase ATXN3 as a PD-L1–positive regulator for tumor immune evasion, Journal of Clinical Investigation (2023). DOI:10.1172/JCI167728
内容来源于网络,如有侵权,请联系删除。
机构
-药物
-生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。


