预约演示
《细胞·代谢》:脂肪肝促进肠癌肝转移的机制,找到了!
2023-07-09
临床研究临床终止
研究发表在《细胞·代谢》上,华中科技大学同济医学院的汪志军及涂炜也是本文的共同第一作者[1]。

Preview
来源: 生物谷
论文首页截图
Preview
来源: 生物谷
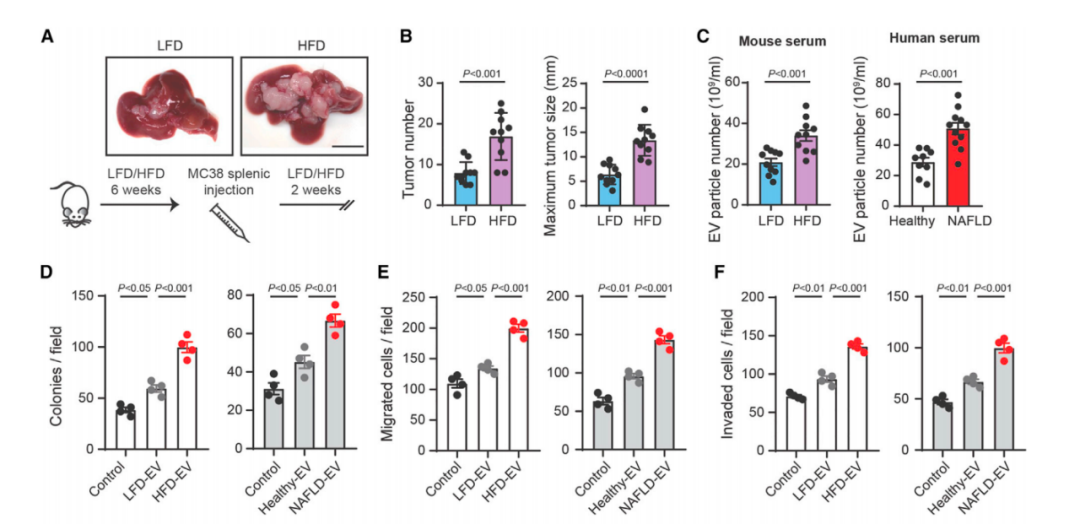
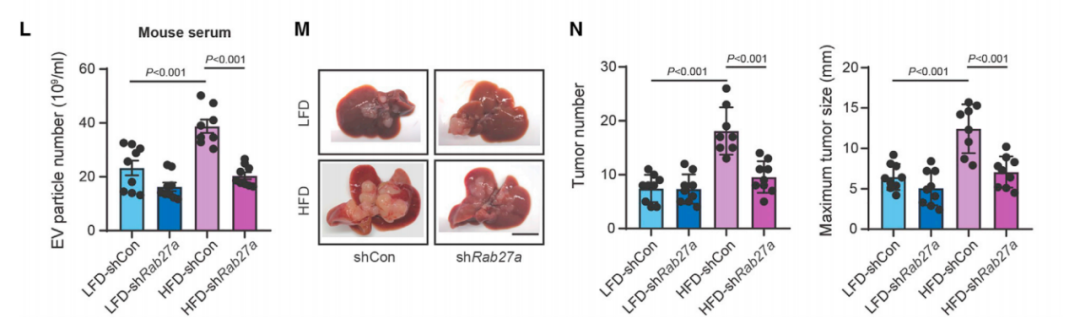
EVs促进结直肠癌肝转移
Preview
来源: 生物谷
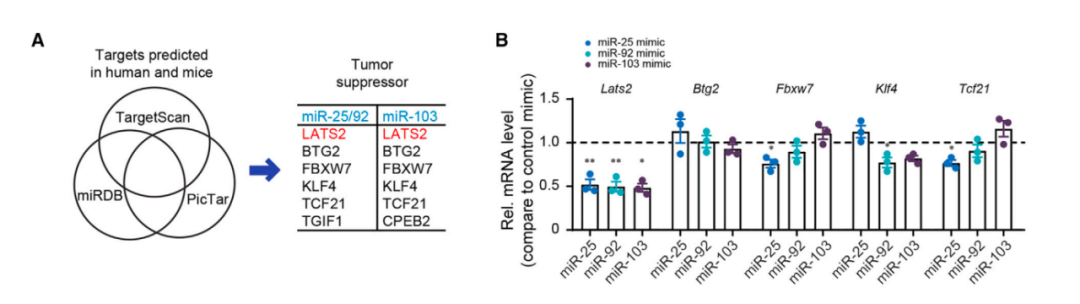
接下来,研究人员分析了EVs的组成,通过miRNA PCR定量分析发现,miR-103、miR-25和miR-92a这三种miRNA在肝脏来源的EVs中表达特别丰富。当研究人员用这三个miRNA处理MC38和HCT116细胞后,这些癌细胞的增殖、迁移和侵袭能力都会增加。
Preview
来源: 生物谷
LATS2表达下调
Preview
来源: 生物谷
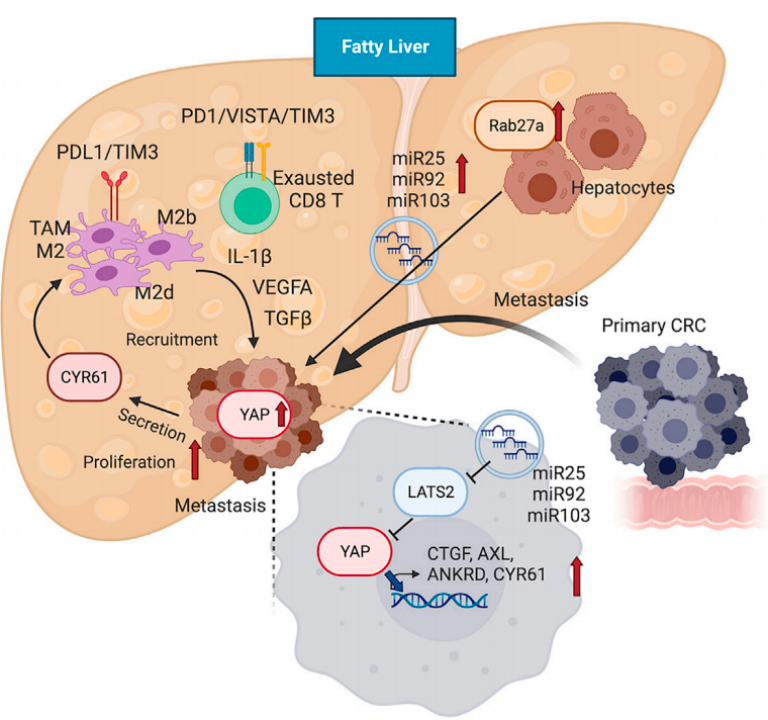
研究机制图
参考文献:
[1]Wang Z, Kim SY, Tu W, Kim J, Xu A, Yang YM, Matsuda M, Reolizo L, Tsuchiya T, Billet S, Gangi A, Noureddin M, Falk BA, Kim S, Fan W, Tighiouart M, You S, Lewis MS, Pandol SJ, Di Vizio D, Merchant A, Posadas EM, Bhowmick NA, Lu SC, Seki E. Extracellular vesicles in fatty liver promote a metastatic tumor microenvironment. Cell Metab. 2023 May 9:S1550-4131(23)00140-7. doi: 10.1016/j.cmet.2023.04.013.
更多内容,请访问原始网站
文中所述内容并不反映新药情报库及其所属公司任何意见及观点,如有版权侵扰或错误之处,请及时联系我们,我们会在24小时内配合处理。
药物
-生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。


