预约演示
更新于:2025-05-07

Hunan Mingrui Pharmaceutical Co. Ltd.
更新于:2025-05-07
概览
标签
泌尿生殖系统疾病
感染
免疫系统疾病
小分子化药
疾病领域得分
一眼洞穿机构专注的疾病领域
暂无数据
技术平台
公司药物应用最多的技术
暂无数据
靶点
公司最常开发的靶点
暂无数据
| 排名前五的药物类型 | 数量 |
|---|---|
| 小分子化药 | 2 |
| 排名前五的靶点 | 数量 |
|---|---|
| HMGB1(高迁移率族蛋白B1) | 1 |
关联
3
项与 湖南明瑞医药有限责任公司 相关的药物作用机制 质子泵抑制剂 |
原研机构 |
最高研发阶段批准上市 |
首次获批国家/地区 日本 |
首次获批日期1997-10-14 |
靶点 |
作用机制 HMGB1抑制剂 |
在研机构 |
非在研适应症 |
最高研发阶段批准上市 |
首次获批国家/地区 日本 |
首次获批日期1979-12-21 |
靶点- |
作用机制- |
在研机构 |
原研机构 |
非在研适应症- |
最高研发阶段批准上市 |
首次获批国家/地区 美国 |
首次获批日期1967-07-05 |
25
项与 湖南明瑞医药有限责任公司 相关的临床试验CTR20221736
马来酸阿伐曲泊帕片人体生物等效性研究(餐后试验)
本试验旨在研究单次餐后口服湖南明瑞制药有限公司研制、生产的马来酸阿伐曲泊帕片(20 mg)的药代动力学特征;以AkaRx Inc.持证、Kawashima Plant, Eisai Co.,Ltd.生产的马来酸阿伐曲泊帕片(苏可欣®,20 mg)为参比制剂,比较两制剂中药动学参数Cmax、AUC0-t、AUC0-∞,评价两制剂的人体生物等效性,并观察两制剂在健康受试者中的安全性。
开始日期2022-09-20 |
申办/合作机构 |
CTR20221737
马来酸阿伐曲泊帕片人体生物等效性研究(空腹试验)
本试验旨在研究单次空腹口服湖南明瑞制药有限公司研制、生产的马来酸阿伐曲泊帕片(20 mg)的药代动力学特征;以AkaRx Inc.持证、Kawashima Plant, Eisai Co.,Ltd.生产的马来酸阿伐曲泊帕片(苏可欣®,20 mg)为参比制剂,比较两制剂中药动学参数Cmax、AUC0-t、AUC0-∞,评价两制剂的人体生物等效性,并观察两制剂在健康受试者中的安全性。
开始日期2022-09-13 |
申办/合作机构 |
CTR20210698
草木犀流浸液片人体药代动力学研究
本试验旨在研究单次空腹口服湖南明瑞制药有限公司研制、生产的草木犀流浸液片〔400 mg(含草木犀流浸液25 mg)〕的药代动力学特征;以生晃荣养药品株式会社生产的草木犀流浸液片〔消脱止-M®,400 mg(含草木犀流浸液25 mg)〕为参比制剂,比较两制剂中药动学参数Cmax、AUC0-t、AUC0-∞。
开始日期2021-04-02 |
申办/合作机构 |
100 项与 湖南明瑞医药有限责任公司 相关的临床结果
登录后查看更多信息
0 项与 湖南明瑞医药有限责任公司 相关的专利(医药)
登录后查看更多信息
3
项与 湖南明瑞医药有限责任公司 相关的新闻(医药)2022-07-25
·信狐药迅
每周药品注册受理数据,分门别类呈现,一目了然。新药上市申请药品名称企业名称分类受理号奥雷巴替尼片广州顺健生物医药科技有限公司2.4CXHS2200039注射用艾普拉唑钠丽珠集团丽珠制药厂2.4CXHS2200040新药临床申请药品名称企业名称分类受理号HTMC0435片上海壹典医药科技开发有限公司1CXHL22005091CXHL22005101CXHL22005111CXHL22005121CXHL22005131CXHL2200514HZ-A-018胶囊杭州和正医药有限公司1CXHL22005061CXHL2200507LF0001片杭州瓴方生物医药科技有限公司1CXHL2200504LJ01005颗粒长春澜江医药科技有限公司2.2CXHL2200503LV232胶囊苏州旺山旺水生物医药有限公司1CXHL22005191CXHL2200520LW402片上海长森药业有限公司1CXHL22005151CXHL22005161CXHL2200492RX04胶囊上海日馨医药科技股份有限公司1CXHL22005231CXHL2200524WXSH0176片辰欣药业股份有限公司1CXHL22005211CXHL2200522XH-5102片上海勋和医药科技有限公司1CXHL22005171CXHL2200518XYP-001健康元药业集团股份有限公司2.2;2.4CXHL2200508苯乙基异硫氰酸酯液体硬胶囊无锡杰西医药股份有限公司1CXHL22005251CXHL2200526盐酸纳布啡注射液宜昌人福药业有限责任公司2.4CXHL2200505仿制药申请药品名称企业名称分类受理号阿立哌唑口服溶液浙江百代医药科技有限公司3CYHS22011163CYHS22011173CYHS22011183CYHS2201119奥硝唑片福安药业集团烟台只楚药业有限公司3CYHS2201100胞磷胆碱钠注射液海南全星制药有限公司3CYHS22011033CYHS2201104贝前列素钠片北京诚济制药股份有限公司3CYHS2201090吡仑帕奈片西安远大科创医药科技有限公司4CYHS22010914CYHS2201092醋酸阿比特龙片江苏联环药业股份有限公司4CYHS2201111蛋白琥珀酸铁口服溶液湖南明瑞制药有限公司4CYHS2201128度骨化醇注射液南京海融医药科技股份有限公司3CYHL22000593CYHL2200060富马酸比索洛尔片宁波科尔康美诺华药业有限公司4CYHS2201095腹膜透析液(乳酸盐-G1.5%)青岛瑞奈医疗科技有限公司4CYHS2201083腹膜透析液(乳酸盐-G2.5%)4CYHS2201085腹膜透析液(乳酸盐-G4.25%)4CYHS2201086肝素钠注射液烟台东诚北方制药有限公司3CYHS2201115枸橼酸托瑞米芬片江苏奥赛康药业有限公司4CYHS2201062酒石酸布托啡诺注射液成都苑东生物制药股份有限公司3CYHS22011013CYHS2201102糠酸莫米松鼻喷雾剂四川大冢制药有限公司4CYHS2201122立他司特滴眼液鲁南贝特制药有限公司3CYHL2200058利伐沙班片悦康药业集团股份有限公司4CYHS2201123武汉同济中维医药有限责任公司4CYHS2201050硫酸镁注射液广州瑞尔医药科技有限公司3CYHS2201096硫酸羟氯喹片福建海西新药创制有限公司4CYHS2201108硫酸沙丁胺醇注射液石家庄四药有限公司3CYHS2201078罗库溴铵注射液山东新时代药业有限公司4CYHS22011204CYHS2201121帕立骨化醇注射液南京海融医药科技股份有限公司4CYHS2201089普瑞巴林胶囊浙江诺得药业有限公司4CYHS22011094CYHS2201110乳酸环丙沙星氯化钠注射液浙江国镜药业有限公司4CYHS22011064CYHS2201107头孢丙烯干混悬剂苏州第三制药厂有限责任公司3CYHS22010983CYHS2201099头孢地尼颗粒广州白云山天心制药股份有限公司4CYHS2201105头孢克肟片温岭市创新生物医药科技股份有限公司3CYHS2201124硝苯地平控释片燃点(南京)生物医药科技有限公司4CYHS2201094盐酸阿考替胺片北京亚宝生物药业有限公司3CYHS2201087盐酸氮卓斯汀滴眼液南京恒道医药科技股份有限公司4CYHS2201080盐酸多巴酚丁胺注射液成都苑东生物制药股份有限公司3CYHS2201088盐酸二甲双胍缓释片成都京汇诚生物科技有限公司4CYHS2201097盐酸莫西沙星滴眼液杭州民生药业股份有限公司4CYHS22011294CYHS2201130盐酸帕洛诺司琼注射液贵州阜康仁制药有限公司4CYHS22011254CYHS2201126注射用尼可地尔江苏博新医药科技有限公司3CYHS22011133CYHS2201114注射用替加环素海南普利制药股份有限公司4CYHS2201112进口申请药品名称企业名称分类受理号Amlitelimab注射液赛诺菲(中国)投资有限公司1JXSL2200128AZD5718片阿斯利康全球研发(中国)有限公司1JXHL2200204BI685509片勃林格殷格翰(中国)投资有限公司1JXHL22002051JXHL22002061JXHL2200207Cendakimab注射液百时美施贵宝(中国)投资有限公司1JXSL2200127Efgartigimod注射液再鼎医药(上海)有限公司2.2JXSL2200125Linzagolix片上海葆正医药科技有限公司2.4JXHL22002022.4JXHL2200203MK-4280A注射液默沙东研发(中国)有限公司1JXSL2200126Nolasiban分散片杭州育源生命科技有限公司1JXHL22002001JXHL2200201RO7082859罗氏(中国)投资有限公司1JXSL2200124安纳白介素注射液(预充式)苏庇医药(上海)有限公司3.1JXSS2200024奥马珠单抗注射液北京诺华制药有限公司3.1JXSS2200025达格列净片上海上药信谊药厂有限公司5.2JYHS22000725.2JYHS2200073熊去氧胆酸口服混悬液深圳市康哲生物科技有限公司5.1JXHS2200062依库珠单抗注射液阿斯利康投资(中国)有限公司3.1JXSS2200023中药相关申请药品名称企业名称分类受理号复方野菊花黄酮颗粒浙江中医药大学1.1CXZL2200034抗敏镇咳颗粒天津乐敦中药有限公司1.1CXZL2200033
2022-06-20
·药通社
导读:2022年06月20日药品批准证明文件待领取信息发布,共78个受理号获批。其中,共有6个一致性受理号获批,包括2品规注射剂/注射用药品。过评药品分别为:马尿酸乌洛托品片(湖南明瑞制药有限公司)、奥美沙坦酯片(上海信谊百路达药业有限公司)、注射用头孢呋辛钠(国药集团致君(深圳)制药有限公司)、吲达帕胺片(遂成药业股份有限公司)、卡前列素氨丁三醇注射液(常州四药制药有限公司)、注射用头孢噻肟钠(瑞阳制药股份有限公司)。此外,另有40个上市注册申请受理号获批,包括4品规进口药品和36品规国产药品。其中值得关注的是信达生物PD-1产品信迪利单抗新适应症的获批,这是该产品获批的第五项适应症,具体为联合化疗(顺铂+紫杉醇/顺铂+5-氟尿嘧啶)一线治疗食管鳞癌。且第三家舒更葡糖钠注射液获批,来自成都苑东生物制药股份有限公司。获批第一家为扬子江药业,第二家为湖南科伦制药。首家:扬子江药业 早在2022年4月12日,CDE官网数据显示扬子江药业集团江苏海慈生物药业有限公司的舒更葡糖钠原料药状态转A,其规格为:1kg/桶,3kg/桶,5kg/桶,10kg/桶或根据客户需求提供。且扬子江的舒更葡糖钠原料药也为国内首个转A。原料药转A后不久,扬子江药业子公司江苏海岸药业有限公司的舒更葡糖钠注射液就获批,成为国产首家获批。共获批2品规【按舒更葡糖钠活性实体与单-羟基舒更葡糖钠活性实体的总量计 5ml:500mg;按舒更葡糖钠活性实体与单-羟基舒更葡糖钠活性实体的总量计 2ml:200mg】第二家:科伦药业 2022年4月24日,科伦药业的舒更葡糖钠原料药状态转A,同时受理号为CYHS1800436国的上市注册申请状态变为在审批。原料药转A后不久,在近日发布的2022年05月07日药品批准证明文件待领取信息中,湖南科伦制药的舒更葡糖钠注射液成功获批。此外,就在湖南科伦获批后不久,2022年5月10日四川青木制药有限公司的舒更葡糖钠原料药状态转A,其规格为:1kg/瓶、2kg/瓶、4kg/瓶、8kg/瓶、12kg/瓶。四川青木制药成为国内第三家舒更葡糖钠原料药状态转A企业。批件信息:
抗体免疫疗法
2021-01-06
·药筛
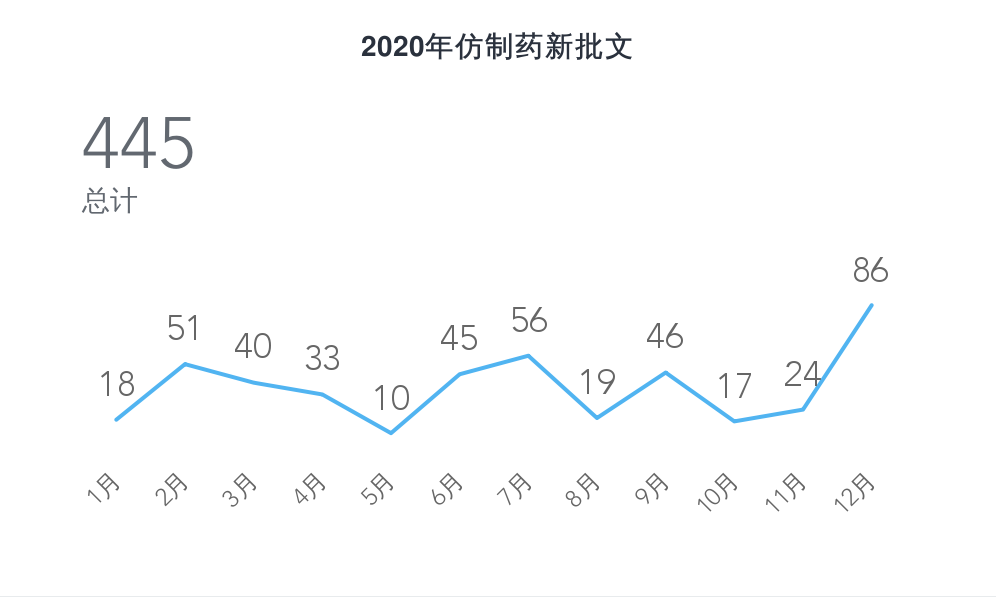
一、仿制药新批文
点评:
最后一月,批文数量创新高;
齐鲁哌柏西利胶囊首仿;
氯吡格雷、阿格列汀又有新成员;
深圳太太吸入用布地奈德混悬液国产第2家;
云南龙海的吸入用盐酸氨溴索溶液首家国产;
科兴生物23价肺炎球菌多糖疫苗获批
仿制药新批文目录:
产品名称生产厂家规格23价肺炎球菌多糖疫苗北京科兴生物制品有限公司0.5mlω-3鱼油中/长链脂肪乳注射液丽珠集团利民制药厂100mlω-3鱼油中/长链脂肪乳注射液丽珠集团利民制药厂250ml阿达木单抗注射液上海复宏汉霖生物制药有限公司40mg奥美沙坦酯氨氯地平片南京正大天晴制药有限公司20mg/5mg奥美沙坦酯片成都倍特药业股份有限公司20mg苯磺顺阿曲库铵注射液北京泰德制药股份有限公司5ml:10mg苯磺顺阿曲库铵注射液南京健友生化制药股份有限公司5ml:10mg苯甲酸阿格列汀片广东东阳光药业有限公司12.5mg苯甲酸阿格列汀片广东东阳光药业有限公司6.25mg苯甲酸阿格列汀片湖南千金湘江药业股份有限公司12.5mg苯甲酸阿格列汀片湖南千金湘江药业股份有限公司25mg苯甲酸阿格列汀片湖南千金湘江药业股份有限公司6.25mg单硝酸异山梨酯缓释胶囊合肥合源药业有限公司50mg碘克沙醇注射液正大天晴药业集团股份有限公司100ml:32g(I)碘克沙醇注射液正大天晴药业集团股份有限公司50ml:16g(I)厄贝沙坦氢氯噻嗪片珠海润都制药股份有限公司150mg/12.5mg恩替卡韦片湖南千金湘江药业股份有限公司0.5mg恩替卡韦片湖南千金湘江药业股份有限公司1mg恩替卡韦片浙江爱诺生物药业股份有限公司0.5mg恩替卡韦片浙江爱诺生物药业股份有限公司1.0mg复合磷酸氢钾注射液湖南华纳大药厂股份有限公司2ml枸橼酸氢钾钠颗粒浙江施强制药有限公司2.5g:2.4275g枸橼酸舒芬太尼注射液江苏恩华药业股份有限公司10ml:50ug枸橼酸舒芬太尼注射液江苏恩华药业股份有限公司1ml:50ug枸橼酸舒芬太尼注射液江苏恩华药业股份有限公司2ml:100ug枸橼酸舒芬太尼注射液江苏恩华药业股份有限公司5ml:250ug琥珀酸索利那新片武汉人福利康药业有限公司5mg磺达肝癸钠注射液辽宁海思科制药有限公司0.5ml:2.5mg酒石酸美托洛尔片陕西步长高新制药有限公司25mg酒石酸美托洛尔片陕西步长高新制药有限公司50mg卡贝缩宫素注射液杭州澳亚生物技术有限公司1ml:100ug拉米夫定片天地恒一制药股份有限公司0.1g利伐沙班片南京柯菲平盛辉制药有限公司10mg利培酮口服溶液安徽新世纪药业有限公司0.1%(30ml:30mg)磷酸依米他韦胶囊宜昌东阳光长江药业股份有限公司0.1g硫酸氢氯吡格雷片吉林省博大伟业制药有限公司75mg硫酸氢氯吡格雷片深圳信立泰药业股份有限公司25mg硫酸氢氯吡格雷片深圳信立泰药业股份有限公司75mg罗库溴铵注射液海南斯达制药有限公司2.5ml:25mg门冬胰岛素30注射液甘李药业股份有限公司3ml:300单位哌柏西利胶囊齐鲁制药有限公司100mg哌柏西利胶囊齐鲁制药有限公司125mg哌柏西利胶囊齐鲁制药有限公司75mg普瑞巴林胶囊宁波美诺华天康药业有限公司150mg普瑞巴林胶囊宁波美诺华天康药业有限公司75mg人凝血酶原复合物博雅生物制药集团股份有限公司复方瑞舒伐他汀钙片广东东阳光药业有限公司10mg瑞舒伐他汀钙片广东东阳光药业有限公司5mg他达拉非片广东东阳光药业有限公司10mg他达拉非片广东东阳光药业有限公司2.5mg他达拉非片广东东阳光药业有限公司20mg他达拉非片广东东阳光药业有限公司5mg吸入用布地奈德混悬液深圳太太药业有限公司2ml:1mg吸入用盐酸氨溴索溶液云南龙海天然植物药业有限公司2ml:15mg辛伐他汀片厦门力卓药业有限公司10mg辛伐他汀片厦门力卓药业有限公司20mg盐酸氨溴索注射液河北凯威制药有限责任公司2ml:15mg盐酸氨溴索注射液山东华鲁制药有限公司2ml:15mg盐酸奥洛他定片河北创健药业有限公司2.5mg盐酸奥洛他定片河北创健药业有限公司5mg盐酸度洛西汀肠溶胶囊青岛百洋制药有限公司20mg盐酸度洛西汀肠溶胶囊青岛百洋制药有限公司30mg盐酸度洛西汀肠溶胶囊青岛百洋制药有限公司60mg盐酸二甲双胍片广东东阳光药业有限公司0.5g盐酸二甲双胍片广东东阳光药业有限公司0.85g盐酸二甲双胍片广东东阳光药业有限公司1.0g盐酸羟考酮注射液东北制药集团沈阳第一制药有限公司1ml:10mg盐酸羟考酮注射液东北制药集团沈阳第一制药有限公司2ml:20mg盐酸左西替利嗪片北京韩美药品有限公司5mg依替巴肽注射液成都圣诺生物制药有限公司10ml:20mg注射用艾司奥美拉唑钠重庆莱美药业股份有限公司40mg注射用多种维生素(13)国药集团广东环球制药有限公司5ml注射用培美曲塞二钠连云港杰瑞药业有限公司0.1g注射用培美曲塞二钠连云港杰瑞药业有限公司0.2g注射用培美曲塞二钠齐鲁制药(海南)有限公司0.1g注射用培美曲塞二钠齐鲁制药(海南)有限公司0.5g注射用培美曲塞二钠苏州特瑞药业有限公司100mg注射用盐酸吉西他滨海南全星制药有限公司0.1g注射用盐酸兰地洛尔南京海辰药业股份有限公司50mg注射用盐酸头孢替安深圳立健药业有限公司0.5g紫杉醇注射液四川汇宇制药股份有限公司16.7ml:100mg紫杉醇注射液四川汇宇制药股份有限公司5ml:30mg左乙拉西坦注射用浓溶液北京四环制药有限公司5ml:0.5g左乙拉西坦注射用浓溶液成都倍特药业股份有限公司5ml:500mg左乙拉西坦注射用浓溶液扬子江药业集团南京海陵药业有限公司5ml:500mg
二、仿制药申报
点评:
高难度品种增多,如奥贝胆酸、达比加群、泊沙康唑
推荐关注品种:
药品名称企业名称分类受理号艾司奥美拉唑镁肠溶胶囊辰欣药业股份有限公司3CYHS2000880氨氯地平阿托伐他汀钙片福建海西新药创制有限公司;宁波美诺华天康药业有限公司4CYHS2000874奥贝胆酸片江苏恒瑞医药股份有限公司3CYHS2000853泊沙康唑肠溶片四川科伦药业股份有限公司4CYHS2000954达比加群酯胶囊齐鲁制药(海南)有限公司4CYHS2000831地夸磷索钠滴眼液齐鲁制药有限公司4CYHS2000857富马酸丙酚替诺福韦片宜昌人福药业有限责任公司4CYHS2000915富马酸伏诺拉生片四川海汇药业有限公司4CYHS2000937酒石酸阿福特罗吸入溶液江苏长泰药业有限公司3CYHS2000890哌柏西利胶囊江苏豪森药业集团有限公司4CYHS2000894普瑞巴林缓释片上海宣泰海门药业有限公司3CYHS2000932去氧肾上腺素酮咯酸溶液江苏恒瑞医药股份有限公司3CYHS2000851吸入用异丙托溴铵溶液济南景笙科技有限公司;潍坊中狮制药有限公司4CYHS2000877盐酸奥普力农注射液山东齐都药业有限公司3CYHS2000939盐酸左沙丁胺醇雾化吸入溶液江苏长泰药业有限公司3CYHS2000947注射用阿扎胞苷健进制药有限公司4CYHS2000897
三、一致性评价获批
点评:
注射剂越来越多
已通过一致性评价品种:
药品名称企业名称规格阿奇霉素胶囊上海海虹实业(集团)巢湖今辰药业有限公司0.25g吡嗪酰胺片卓和药业集团有限公司0.25g吡嗪酰胺片卓和药业集团有限公司0.5g吡嗪酰胺片成都锦华药业有限责任公司0.25g吡嗪酰胺片成都锦华药业有限责任公司0.5g醋酸钙片沈阳福宁药业有限公司0.667g碘克沙醇注射液扬子江药业集团有限公司100ml:32g(I)碘克沙醇注射液扬子江药业集团有限公司100ml:27g(I)厄贝沙坦片深圳市海滨制药有限公司0.15g厄贝沙坦片修正药业集团股份有限公司0.15g呋塞米片上海朝晖药业有限公司20mg伏立康唑片北京博康健基因科技有限公司50mg氟康唑氯化钠注射液扬子江药业集团有限公司100ml:0.2g枸橼酸莫沙必利片成都康弘药业集团股份有限公司5mg甲钴胺注射液扬子江药业集团南京海陵药业有限公司1ml:0.5mg甲硝唑片昆明全新生物制药有限公司0.2g硫辛酸注射液成都倍特药业有限公司12ml:0.3g马来酸氯苯那敏片华中药业股份有限公司4mg马来酸伊索拉定片齐鲁制药有限公司2mg马来酸伊索拉定片齐鲁制药有限公司4mg吗替麦考酚酯胶囊邛崃天银制药有限公司0.25g咪达唑仑注射液江苏恩华药业股份有限公司1ml:5mg咪达唑仑注射液江苏恩华药业股份有限公司2ml:2mg咪达唑仑注射液江苏恩华药业股份有限公司5ml:5mg咪达唑仑注射液江苏恩华药业股份有限公司10ml:50mg米非司酮片湖北葛店人福药业有限责任公司10mg替米沙坦片江苏亚邦爱普森药业有限公司40mg替米沙坦片江苏万邦生化医药集团有限责任公司40mg头孢氨苄胶囊哈药集团制药总厂0.125g;0.125g头孢氨苄胶囊广州白云山医药集团股份有限公司白云山制药总厂0.125g头孢氨苄片山东新华制药股份有限公司0.125g头孢氨苄片山东新华制药股份有限公司0.25g维生素B2片华中药业股份有限公司5mg硝酸甘油片山东信谊制药有限公司0.5mg硝酸甘油片北京益民药业有限公司0.5mg盐酸氨溴索注射液云南龙海天然植物药业有限公司2ml:15mg盐酸氨溴索注射液云南龙海天然植物药业有限公司4ml:30mg盐酸氨溴索注射液山东罗欣药业集团股份有限公司1ml:7.5mg盐酸氨溴索注射液山东罗欣药业集团股份有限公司4ml:30mg盐酸氨溴索注射液山东罗欣药业集团股份有限公司2ml:15mg盐酸氨溴索注射液海南全星制药有限公司2ml:15mg盐酸氨溴索注射液湖北科伦药业有限公司2ml:15mg盐酸氨溴索注射液成都倍特药业有限公司2ml:15mg盐酸二甲双胍缓释片山东齐都药业有限公司0.5g盐酸二甲双胍缓释片成都恒瑞制药有限公司0.5g盐酸二甲双胍片上海上药信谊药厂有限公司0.25g盐酸二甲双胍片浙江国光生物制药有限公司0.25g盐酸二甲双胍片北京中新药业股份有限公司0.25g盐酸氟桂利嗪胶囊山东方明药业集团股份有限公司5mg盐酸拉贝洛尔注射液江苏迪赛诺制药有限公司5ml:50mg;10ml:50mg;2ml:25mg盐酸特比萘芬片保定天浩制药有限公司0.125g脂肪乳氨基酸(17)葡萄糖(19)注射液四川科伦药业股份有限公司2053ml注射用艾司奥美拉唑钠正大天晴药业集团股份有限公司40mg注射用更昔洛韦钠海南普利制药股份有限公司0.5g注射用兰索拉唑江苏奥赛康药业股份有限公司30mg注射用兰索拉唑山东罗欣药业集团股份有限公司30mg注射用帕瑞昔布钠浙江海正药业股份有限公司40mg注射用泮托拉唑钠江苏奥赛康药业股份有限公司60mg注射用泮托拉唑钠江苏奥赛康药业股份有限公司80mg注射用培美曲塞二钠扬子江药业集团有限公司0.5g注射用培美曲塞二钠扬子江药业集团有限公司0.5g注射用培美曲塞二钠扬子江药业集团有限公司0.5g注射用头孢呋辛钠山东润泽制药有限公司0.75g注射用头孢呋辛钠山东润泽制药有限公司1.0g注射用头孢呋辛钠山东润泽制药有限公司1.5g注射用头孢呋辛钠山东润泽制药有限公司2.0g注射用头孢呋辛钠浙江惠迪森药业有限公司1.5g注射用头孢他啶韩美药品株式会社;北京韩美药品有限公司0.5g注射用头孢他啶韩美药品株式会社;北京韩美药品有限公司0.5g注射用头孢他啶韩美药品株式会社;北京韩美药品有限公司1.0g注射用头孢他啶韩美药品株式会社;北京韩美药品有限公司1.0g注射用胸腺法新海南双成药业股份有限公司1.6mg注射用盐酸吉西他滨江苏豪森药业集团有限公司1.0g注射用盐酸吉西他滨江苏豪森药业集团有限公司0.2g注射用盐酸瑞芬太尼宜昌人福药业有限责任公司1mg注射用盐酸瑞芬太尼宜昌人福药业有限责任公司2mg注射用盐酸瑞芬太尼宜昌人福药业有限责任公司5mg紫杉醇注射液扬子江药业集团有限公司16.7ml:0.1g紫杉醇注射液扬子江药业集团有限公司5ml:30mg
注:不包括按一致性评价审评获批的仿制药
四、一致性评价申报
推荐关注品种:
药品名称企业名称受理号碘解磷定注射液上海旭东海普药业有限公司CYHB2050764甲磺酸帕珠沙星氯化钠注射液四川美大康佳乐药业有限公司CYHB2050791利奈唑胺葡萄糖注射液浙江医药股份有限公司新昌制药厂CYHB2050780马尿酸乌洛托品片湖南明瑞制药有限公司CYHB2050747盐酸右美托咪定注射液成都倍特药业股份有限公司CYHB2050761注射用甲泼尼龙琥珀酸钠重庆莱美药业股份有限公司CYHB2040052注射用替加环素扬子江药业集团有限公司CYHB2050778左乙拉西坦注射用浓溶液成都天台山制药有限公司CYHB2050779
药事纵横投稿须知:稿费已上调,欢迎投稿
图片广告:
药事纵横是一个开放,由自愿者组成的团体,由以下成员组成:Voyager88,雷道安,Herman,梅希,文竹,duke,子炎,ZMJ和曾文亮。欢迎有志之士加入我们团队。投稿、合作、加专业群请加微信437180999,药事纵横二千人QQ群22711855
仿制药一致性评价疫苗抗体
100 项与 湖南明瑞医药有限责任公司 相关的药物交易
登录后查看更多信息
100 项与 湖南明瑞医药有限责任公司 相关的转化医学
登录后查看更多信息
组织架构
使用我们的机构树数据加速您的研究。
登录
或

管线布局
2026年06月10日管线快照
管线布局中药物为当前组织机构及其子机构作为药物机构进行统计,早期临床1期并入临床1期,临床1/2期并入临床2期,临床2/3期并入临床3期
批准上市
2
1
其他
登录后查看更多信息
当前项目
| 药物(靶点) | 适应症 | 全球最高研发状态 |
|---|---|---|
甘草酸苷 ( HMGB1 ) | 慢性肝病 更多 | 批准上市 |
马尿酸乌洛托品 | 下尿路症状 更多 | 批准上市 |
雷贝拉唑钠 ( Proton pump ) | Zollinger-Ellison综合征 更多 | 无进展 |
登录后查看更多信息
药物交易
使用我们的药物交易数据加速您的研究。
登录
或

转化医学
使用我们的转化医学数据加速您的研究。
登录
或

营收
使用 Synapse 探索超过 36 万个组织的财务状况。
登录
或

科研基金(NIH)
访问超过 200 万项资助和基金信息,以提升您的研究之旅。
登录
或

投资
深入了解从初创企业到成熟企业的最新公司投资动态。
登录
或

融资
发掘融资趋势以验证和推进您的投资机会。
登录
或

生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用


