首仿!正大天晴依维莫司片获得中国国家药品监督管理局的上市批准
2024年1月3日,中国生物制药宣布,集团子公司正大天晴开发的依维莫司片(商标名:晴维时 )已获得中国国家药品监督管理局的上市批准,是我国实施药品专利纠纷早期解决机制(药品专利链接制度)以来,首个因首仿获批+首个挑战专利成功获得 12 个月市场独占期的产品。
依维莫司原研企业是诺华,该药一种新的靶向治疗药物,为哺乳动物雷帕霉素靶蛋白(mTOR)的选择性抑制剂,通过与胞内蛋白FKBP12结合形成抑制性的复合物,从而抑制mTOR激酶的活性,降低mTOR的下游效应物S6核糖体蛋白激酶(S6K1)和真核生物延伸因子4E-结合蛋白(4E-BP)的活性,从而干扰癌细胞的生长、分化和代谢,发挥抗肿瘤效应。依维莫司对多种恶性肿瘤治疗效果确切,其临床价值得到充分肯定。目前,国内尚无国产依维莫司片上市,原研药售价较高,且医保报销存在限制。正大天晴依维莫司片的上市,一方面为患者提供了更多的用药选择,另一方面可极大程度地降低患者的用药负担,提高药物可及性,造福更多肿瘤患者。
正大天晴依维莫司片此次获批适应症为:
(1)既往接受舒尼替尼或索拉非尼治疗失败的晚期肾细胞癌成人患者。
(2)不可切除的、局部晚期或转移性的、分化良好的(中度分化或高度分化)进展期胰腺神经内分泌瘤成人患者。
(3)无法手术切除的、局部晚期或转移性的、分化良好的、进展期非功能性胃肠道或肺源神经内分泌肿瘤(NET)成人患者。
(4)需要治疗干预但不适于手术切除的结节性硬化症(TSC)相关的室管膜下巨细胞星形细胞瘤(SEGA)成人和儿童患者。依维莫司的有效性主要通过可持续的客观缓解(即SEGA肿瘤体积的缩小)来证明。尚未证明结节性硬化症相关的室管膜下巨细胞星形细胞瘤的患者能否获得疾病相关症状改善和总生存期延长。
(5)用于治疗不需立即手术治疗的结节性硬化症相关的肾血管平滑肌脂肪瘤(TSC-AML)成人患者。
(6)联合依西美坦用于治疗来曲唑或阿那曲唑治疗失败后的激素受体阳性、表皮生长因子受体-2阴性、绝经后晚期女性乳腺癌患者。
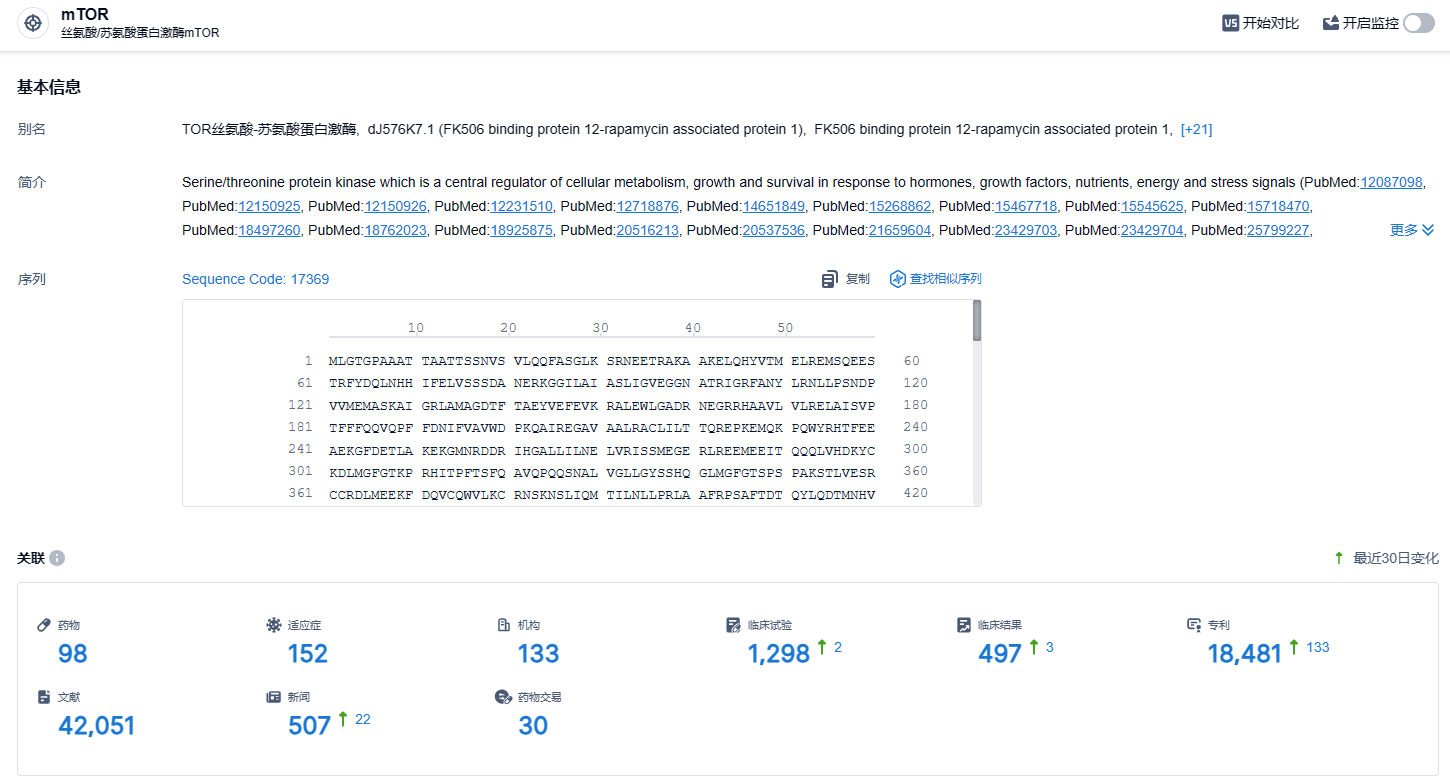
根据智慧芽新药情报库所披露的信息 (点击下方图片直达mTOR靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2024年1月4日,mTOR靶点共有在研药物98个,包含的适应症有152种,在研机构133家,涉及相关的临床试验1298件,专利多达18481件……正大天晴依维莫司片是国内药品专利链接制度实施以来,首个以“首仿获批+首个挑战专利成功”的身份获得12个月市场独占期的产品。晴维时“市场独占期”权益的获得,意味着我国药品专利链接制度实施迎来又一里程碑,为国内仿制药企起到了良好的示范作用,也推动了国内仿制药生态积极发展。