强生IL-23抑制剂古塞奇尤单抗拟纳入优先审评,治疗克罗恩病
2024年3月6日,中国国家药监局药品审评中心(CDE)官网公示,由强生(Johnson & Johnson)旗下强生创新制药(Johnson & Johnson Innovative Medicine)申请的古塞奇尤单抗注射液拟纳入优先审评,适用于治疗中重度活动性克罗恩病成人患者。
古塞奇尤单抗(Guselkumab,Tremfya)是强生旗下杨森制药研发的一款靶向IL-23的p19亚基的的单克隆抗体。目前,guselkumab已在美国、加拿大、日本和许多其他国家/地区获得批准,用于治疗中重度斑块状银屑病,以及银屑病关节炎。2019年,古塞奇尤单抗在中国获批,用于适合全身性治疗的中重度斑块状银屑病成人患者。本次古塞奇尤单抗拟纳入优先审评针对的适应症为克罗恩病。这是一种慢性的全身性疾病,表现为胃肠道或消化道内炎症,发作时会引起持续性腹泻、腹痛和直肠出血。它是一种进行性疾病,会随着时间的推移而恶化。由于克罗恩病的症状不可预测,它给患者带来了身体、情感、经济上的多重负担。针对克罗恩病适应症,古塞奇尤单抗此前已经被CDE纳入突破性治疗品种。
古塞奇尤单抗早先已经在针对中重度克罗恩病的2期GALAXI 1研究中取得积极结果。这项2期临床试验入组对传统疗法或生物制品应答不足或者不耐受的克罗恩病患者。试验结果显示,接受不同剂量古塞奇尤单抗治疗的患者组中,47.5%~66.7%的患者获得临床-生物标志物应答(定义为临床应答并且C反应蛋白或粪便钙卫蛋白水平比基线降低50%)。此外,达到内镜缓解的患者比例在44.3%~46%之间;达到临床缓解并且C反应蛋白或粪便钙卫蛋白水平正常化的患者比例在39.3~66.7%之间。研究人员认为,与安慰剂相比,古塞奇尤单抗所有3种剂量方案均诱导了更大的临床和内镜改善,并具有良好的安全性。
根据中国药物临床试验登记与信息公示平台,针对克罗恩病适应症,强生公司正在开展两项国际多中心(含中国)3期临床研究:一项为3期临床,旨在中重度活动性克罗恩病受试者中评价古塞奇尤单抗皮下给药诱导治疗的疗效和安全性;另一项为2/3期临床研究,旨在中重度活动性克罗恩病受试者中评价古塞奇尤单抗疗效和安全性。
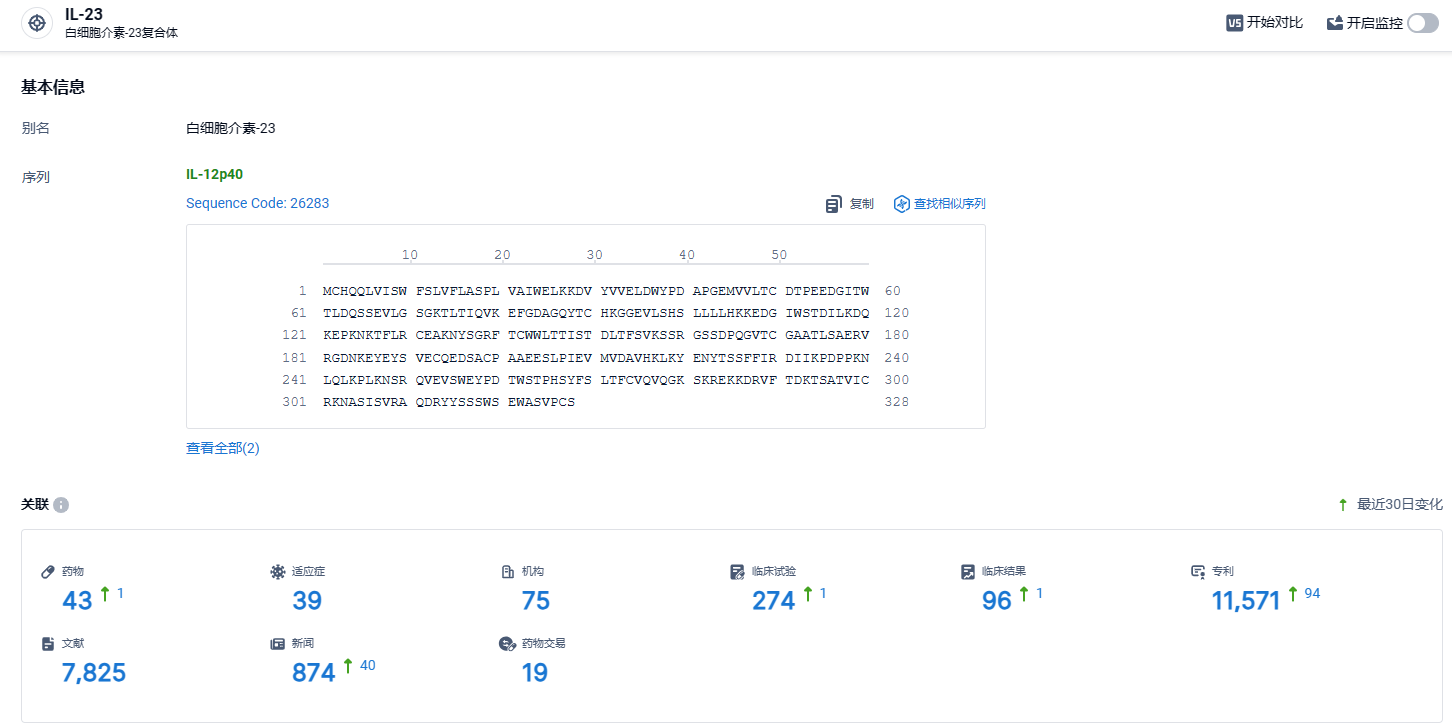
根据智慧芽新药情报库所披露的信息 (点击下方图片直达 IL-23 靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2024 年3月6日,IL-23 靶点共有在研药物43个,包含的适应症有39种,在研机构75家,涉及相关的临床试验274件,专利多达11571件……白细胞介素是一个很大的家族,有多种亚型,功能各异,有些与自身免疫疾病相关,也有些与肿瘤疾病相关。靶向IL-12/23的乌司奴单抗、靶向IL-23的瑞莎珠单抗和古塞奇尤单抗、靶向IL-4的度普利尤单抗、靶向IL-17的司库奇尤单抗和依奇珠单抗和靶向IL-6的托珠单抗,这些药物主要用于治疗自身免疫相关的疾病,如斑块状银屑病、银屑病关节炎、克罗恩病、溃疡性结肠炎和风湿性关节炎等。期待古塞奇尤单抗在竞争中脱颖而出。