迈威生物自研新药8MW0511白细胞减少症III期研究达到主要终点,即将申报上市
2023年10月16日,迈威生物发布公告,将在ESCO大会上报告注射用重组(酵母分泌型)人血清白蛋白-人粒细胞集落刺激因子融合蛋白8MW0511的一项III期研究成果,同时宣布公司正推进8MW0511的上市许可申请工作,预计于年内申报NDA。
8MW0511为迈威生物具有自主知识产权的新一代长效G-CSF(高活性改构细胞因子),拟用于成年非髓性恶性肿瘤患者在接受容易引起发热性中性粒细胞减少症的骨髓抑制性抗癌药物治疗时,降低以发热性中性粒细胞减少症为表现的感染发生率。8MW0511 应用基因融合技术将改构的 G-CSF 突变体基因的 N 端与人血清白蛋白的 C 端融合,可明显抑制 G-CSF受体介导的清除途径,延长半衰期,在临床使用中可以降低给药频率,减少患者痛苦,提高治疗的依从性。同时,8MW0511 采用酵母表达系统进行生产,均一性较好;制备过程避免了复杂的 PEG 化学修饰反应,生产工艺简单、有望降低生产成本。8MW0511 现已完成 III 期临床研究,目前正推进上市许可申请准备工作。
这项III期临床研究方案为:乳腺癌患者接受多西他赛联合环磷酰胺联合/不联合多柔比星的化疗方案,在每个化疗周期化疗药给药结束后接受8MW0511或阳性对照药津优力®治疗。本试验共入组492例受试者,其中8MW0511组328例,对照组164例。试验结果显示,在第1化疗周期中,8MW0511和津优力®的4级中性粒细胞减少的持续时间(DSN)分别为0.24天和0.25天,即8MW0511非劣效于对照药。第2-4化疗周期的DSN结果与第1周期一致。在第1-4化疗周期中,8MW0511组4级中性粒细胞减少的发生率均低于对照组,分别为16.5% vs 19.5%、3.0% vs 9.8%、2.7% vs 6.7%、3.4% vs 6.1%。在所有化疗周期中观察到8MW0511和对照药发热性中性粒细胞减少症(FN)的发生率均较低,8MW0511组为2.1%,对照组为3.7%,两组之间没有显著差异。以上研究结果表明,8MW0511的疗效和安全性均非劣效于对照药津优力®,8MW0511作为一款经人血清白蛋白修饰的新型长效人粒细胞集落刺激因子,可有效缩短化疗导致的4级中性粒细胞减少的持续时间,并可降低发热性中性粒细胞减少症和重度中性粒细胞减少症的发生率。
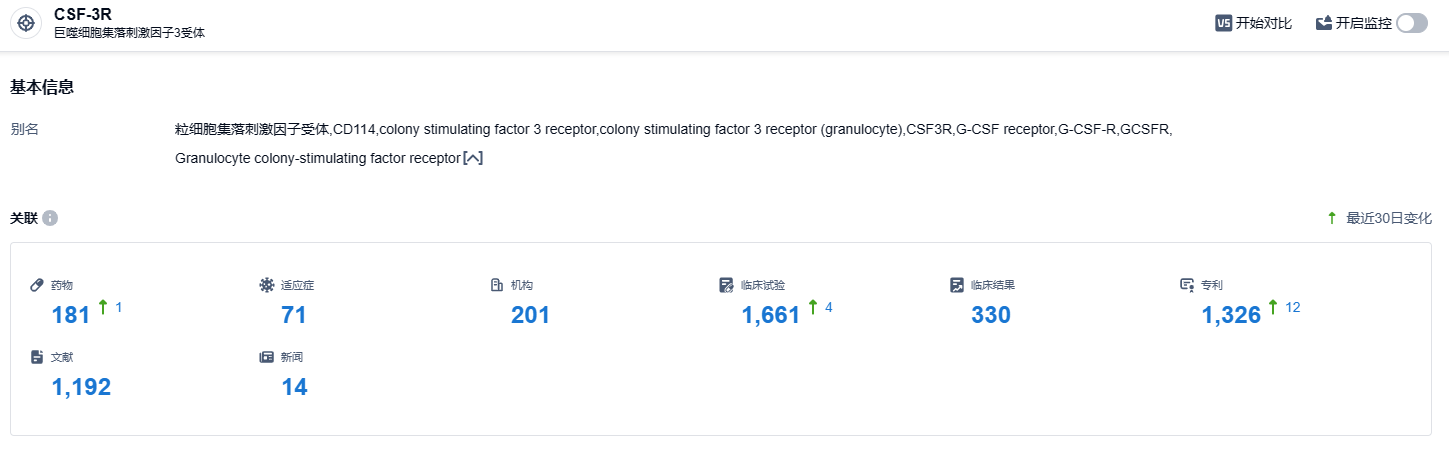
根据智慧芽新药情报库所披露的信息 (点击下方图片直达CSF-3R靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2023 年10月17日,CSF-3R受体 靶点共有在研药物181个,包含的适应症有71种,在研机构201家,涉及相关的临床试验1661件,专利多达1326件……迈威生物招股书中表示,8MW0511预计为第4~7家上市的长效G-CSF产品,不具有先发优势,预估2025年的市场占有率约为2%~4%。红海市场,期待8MW0511能够脱颖而出。