精准生物CAR-T细胞疗法普基仑赛注射液有望加速获批,针对急性淋巴细胞白血病
8月7日,中国国家药监局(NMPA)药品审评中心(CDE)官网公示,重庆精准生物的普基仑赛注射液(pCAR-19B细胞自体回输制剂)的新药上市申请拟纳入优先审评,用于治疗3~21岁CD19阳性的复发或难治性B细胞急性淋巴细胞白血病患者。这意味着,这款创新CAR-T疗法有望在中国加速获批上市。
普基仑赛(pCAR-19B)是由精准生物自主研发,是针对CD19阳性B细胞起源的恶性血液系统疾病开发的细胞免疫治疗产品。2019年2月该疗法获NMPA一类生物新药临床试验默示许可。2023年11月被CDE认定为突破性治疗品种,主要针对3至21岁患有CD19阳性复发性或难治性急性淋巴细胞白血病(ALL)的患者。2023年6月末拟纳入优先审评,是国内首款进入临床II期用于治疗儿童和青少年急性白血病的CAR-T疗法。就在上个月(7月),普基仑赛注射液针对这一白血病适应症的新药上市申请获得了CDE受理。
pCAR-19B作为国内首款该适应症进入关键性临床研究的CAR-T产品,此次被纳入突破性治疗审评程序,基于其注册临床研究突出的临床疗效和患者获益,相较已有治疗手段,显著提高了客观缓解率。当前,pCAR-19B关键临床研究已达到主要终点,期待其更有意义的相关结果公开,为儿童、青少年复发/难治性B细胞急性淋巴细胞白血病患者提供有效的新选择。普基仑赛注射液用于儿童、青少年B细胞急性淋巴细胞白血病(B-ALL)适应症于2019年在中国获批开展注册临床研究。根据早前公布的1期注册临床数据,入组的9例患者均获得完全缓解(CR),总体缓解率达100%,且首次达到完全缓解(CR)的患者微小残留病变也均为阴性,且总体安全性和耐受性良好。
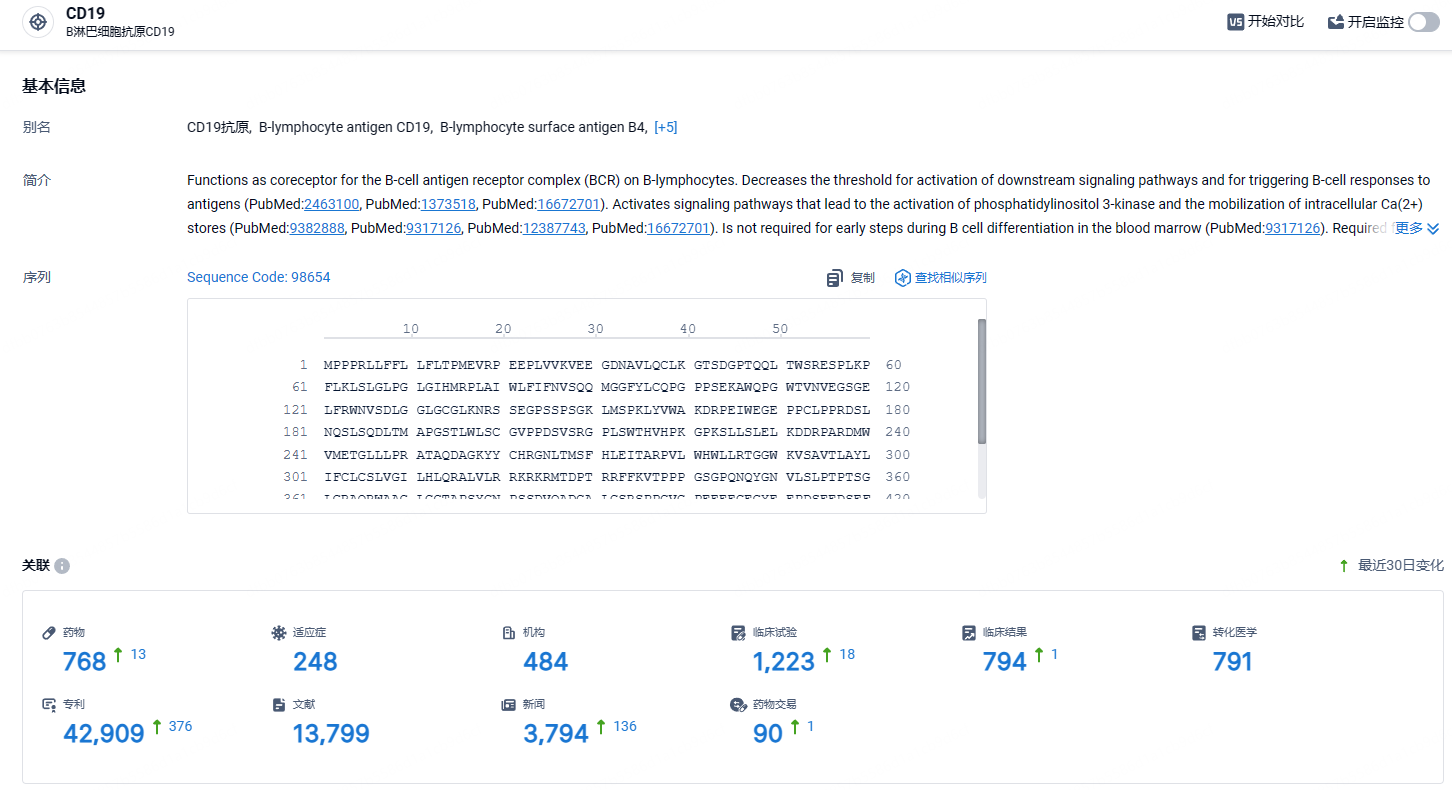
根据智慧芽新药情报库所披露的信息 (点击下方卡片直达CD19靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2024 年8月9日,CD19靶点共有在研药物768个,包含的适应症有248种,在研机构484家,涉及相关的临床试验1223件,专利多达42909件……根据中国临床试验登记与信息公示平台的公示,pCAR-19B细胞自体回输制剂正在开展两项2期临床研究,分别用于治疗3-21岁患有CD19阳性复发难治性急性淋巴细胞白血病患者,以及22-70岁患有CD19阳性复发/难治性B细胞急性淋巴细胞白血病患者。该两项研究的计划招募200名患者,每项研究100名。除了白血病,普基仑赛注射液也在开展用于治疗弥漫大B细胞淋巴瘤、滤泡性淋巴瘤、套细胞淋巴瘤的研究。期待普基仑赛(pCAR-19B)早日获批上市。