荣昌生物靶向HER2 ADC产品维迪西妥单抗3期临床达研究终点,治疗肝转移乳腺癌!
2024年6月13日,荣昌生物宣布,靶向HER2的抗体偶联药物(ADC)维迪西妥单抗治疗HER2阳性存在肝转移的晚期乳腺癌患者的3期临床取得阳性结果,达到主要研究终点。荣昌生物计划近期向中国国家药监局药品审评中心(CDE)递交上市申请。针对该适应症,维迪西妥单抗此前已于2021年6月被CDE纳入突破性治疗品种。
维迪西妥单抗是由荣昌生物研发的中国首个原创靶向HER2抗体偶联(ADC)药物,是我国首个获得美国 FDA、中国药监局突破性疗法双重认定的 ADC 药物。其胃癌、尿路上皮癌适应症分别于2021年6月、2021年12月获中国药监局批准上市销售,并分别于2022年1月、2023年1月进入国家医保目录。
本次维迪西妥单抗达主要终点的是一项在中国开展的、开放、平行对照、多中心的3期临床研究(RC48-C006),旨在评价注射用维迪西妥单抗对比拉帕替尼联合卡培他滨用于治疗HER2阳性晚期乳腺癌患者的有效性及安全性。根据本研究最终分析结果显示,与拉帕替尼联合卡培他滨相比,注射用维迪西妥单抗可显著延长患者的无进展生存期(PFS)。注射用维迪西妥单抗安全性数据与已知风险相似,未发现新的安全性信号。在今年刚刚结束的美国临床肿瘤学会(ASCO)大会上,荣昌生物以线上摘要的形式公布了维迪西妥单抗治疗HER2阳性晚期乳腺癌的中国真实世界经验数据。研究结果显示,患者中位PFS为7.85个月。总客观缓解率(ORR)和疾病控制率DCR分别为26.8%和73.2%。客观缓解的15例中位缓解持续时间(DOR)为5.78个月。在亚组分析中,与单药治疗相比,维迪西妥单抗联合其他靶向治疗/抗血管生成治疗的中位无进展生存期(mPFS)明显更长(NE vs 4.99个月)。研究认为,维迪西妥单抗在HER2阳性晚期乳腺癌患者群体中显示出有希望的抗肿瘤活性和可接受的耐受性。
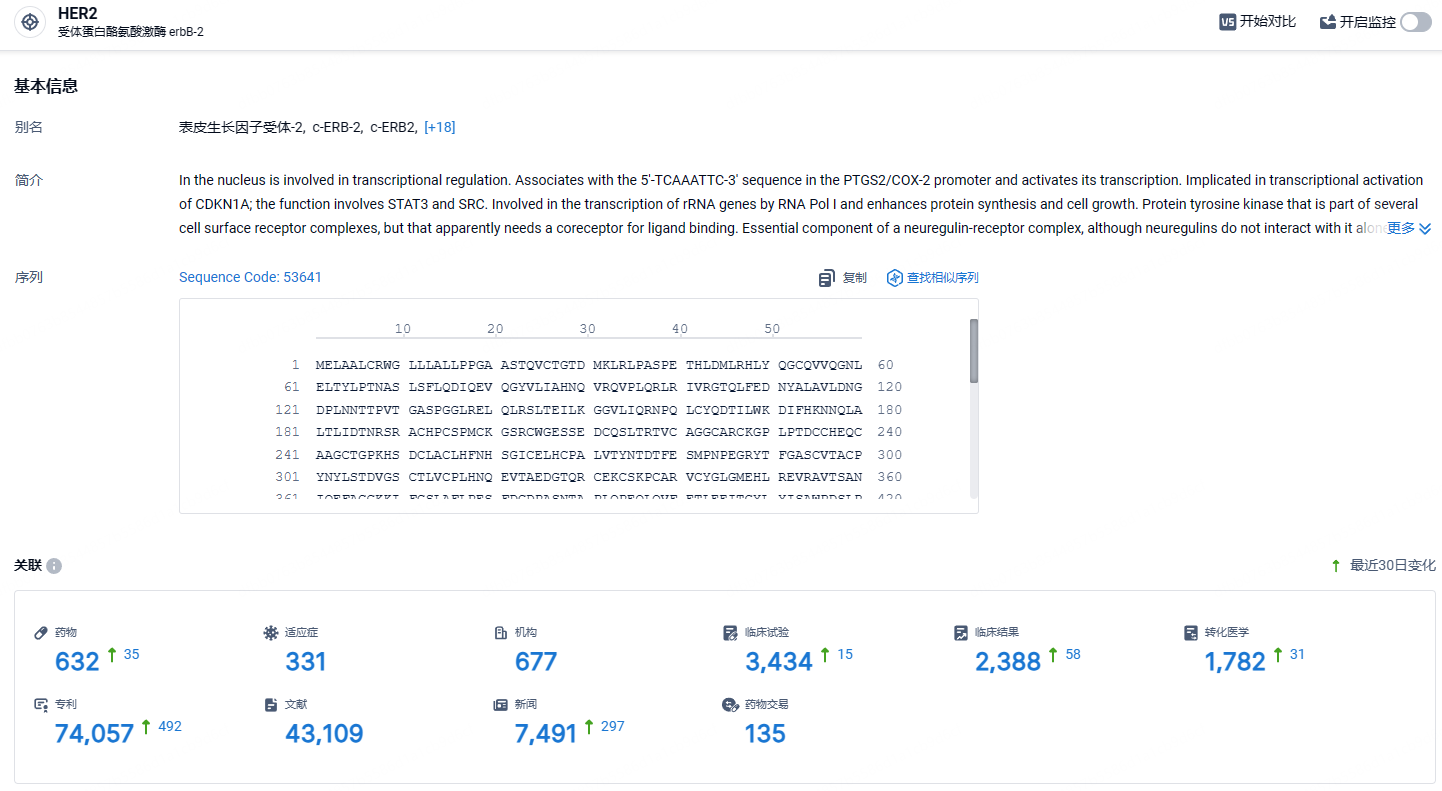
根据智慧芽新药情报库所披露的信息 (点击下方图片直达HER2靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2024 年6月15日,HER2靶点共有在研药物632个,包含的适应症有331种,在研机构677家,涉及相关的临床试验3434件,专利多达74057件……根据GLOBOCAN 2022数据,全球乳腺癌的年新发病例数达230万,死亡病例数达66万,为女性发病率最高的癌症。在中国,乳腺癌发病率和死亡率在恶性肿瘤中分别居第6位和第7位。年新发病例数达36万,死亡病例数达7万。HER2阳性乳腺癌肝转移发生率为44.5%,如果不积极治疗,中位生存期仅为4-8个月,但目前尚缺乏特异性的治疗方案。期待维迪西妥单抗肝转移乳腺癌适应症早日获批。