赛诺菲新型CD38单抗艾沙妥昔单抗在中国申报上市,治疗多发性骨髓瘤
2023年12月12日,中国国家药监局药品审评中心(CDE)官网公示,赛诺菲(Sanofi)申报了艾沙妥昔单抗注射液的上市申请,并获得受理。公开资料显示,艾沙妥昔单抗(isatuximab,商品名为:Sarclisa)是一款新型靶向CD38的单克隆抗体,用于治疗复发性或难治性多发性骨髓瘤(R/R MM)成人患者。
Isatuximab是一种单克隆抗体,靶向多发性骨髓瘤细胞上CD38受体的特异性表位,可触发多种不同的作用机制,包括程序性肿瘤细胞死亡(凋亡)和机体免疫反应调节。CD38在MM细胞表面呈高水平表达,它是细胞表面的潜在受体靶点。目前,Isatuximab注射液已在美国、欧盟、亚太等全球多个国家和地区获批。同时,赛诺菲正在进行的III期临床试验,将继续评估Isatuximab注射液联合现行标准方案治疗多发性骨髓瘤。Isatuximab注射液用于治疗其他血液恶性肿瘤和实体瘤的研究也在进行中。
此次申报上市基于III期临床IKEMA研究,IKEMA是一项随机、开放式、多国、平行组III期研究,比较Isa-Kd(Isatuximab联合泊马度胺+地塞米松)和Kd(泊马度胺+地塞米松)治疗接受过1-3种治疗的复发MM的疗效,通过无进展生存期(PFS)、完全缓解率(CRR)、总缓解率(ORR)等指标进行评估。研究结果显示,与Kd治疗组相比,Isa-Kd治疗组患者的中位PFS达到35个月,降低复发与死亡风险42%,同时显著改善了R/R MM患者的缓解深度(CRR≥44.1%);可显著延长中位PFS(11.53个月vs 6.47个月),同时显著提高了ORR(60.4% vs 35.3%)。
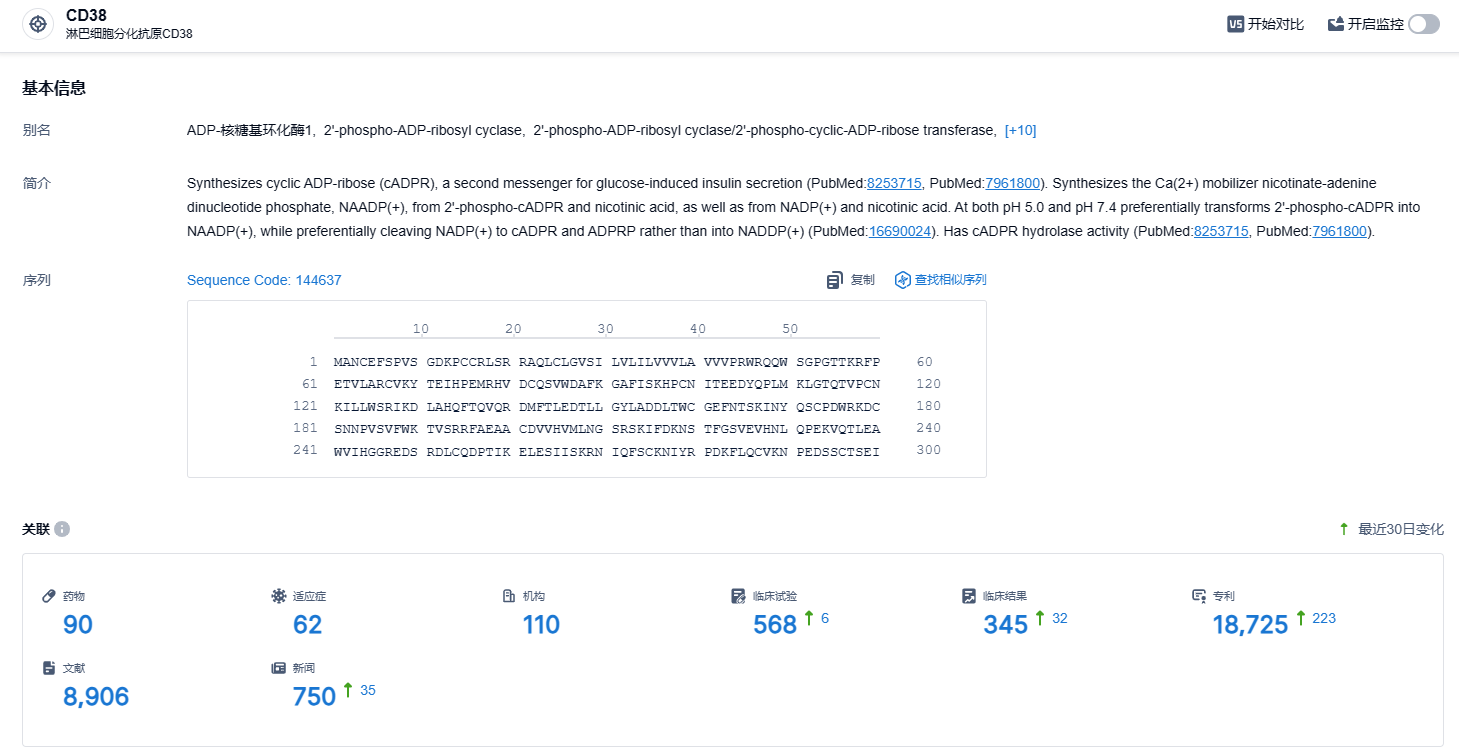
根据智慧芽新药情报库所披露的信息(点击下方卡片直达CD38靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到2023年12月13日,CD38靶点共有在研药物90个,包含的适应症有62种,在研机构110家,涉及相关的临床试验568件,专利多达18725件……在中国,目前CD38抗体只有强生的达雷妥尤单抗(Daratumumab)获批上市,天境生物/HI-Bio的菲泽妥单抗正处于III期临床,康诺亚自主研发的CM313目前正处于II期试验;此外,国内进入临床的还有尚健生物、凯信远达/天石同达、康缘药业、友芝友生物等。期待艾沙妥昔单抗顺利获批上市。




