和誉医药FGFR4抑制剂ABSK012获FDA临床试验许可,治疗晚期实体瘤
2023年11月8日,和誉医药宣布,其自主研发的抗耐药突变小分子成纤维细胞生长因子受体4(FGFR4)抑制剂ABSK012获美国FDA批淮可开展其单药在晚期实体瘤患者中的首次人体(FIH)I期临床试验。
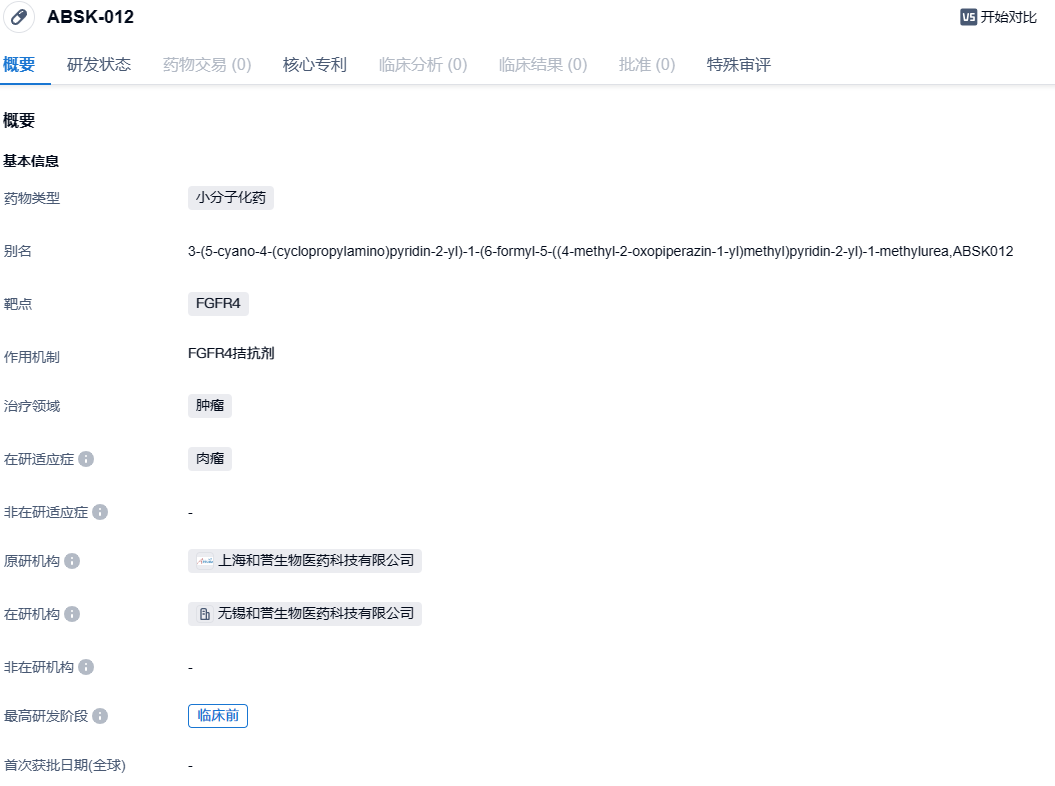
ABSK012是一款具有高选择性的新一代小分子FGFR4抑制剂,可克服对第一代抑制剂的FGFR4耐药突变。FGFR4信号通路是实体瘤(如HCC、RMS)分子靶向治疗开发的一个很有前景的方向。在临床前研究中,ABSK012显示出抗肿瘤活性,并具有良好的药物代谢和药代动力学特性。2023年4月,ABSK012获得美FDA授予的孤儿药资格认定,用于治疗软组织肉瘤(Soft Tissue Sarcoma简称STS)。
此次获批的研究是一项开放的评价ABSK012在晚期实体瘤患者中的安全性、耐受性与药代动力学I期临床研究。研究人群为具有特定基因改变的晚期实体瘤、FGF19过表达肝细胞癌(HCC)、FGFR4突变横纹肌肉瘤(RMS)等疾病患者。
成纤维细胞生长因子(FGFs)及其受体( FGFRs)在人类胚胎发生,血管生成,细胞增殖和分化中起重要作用,随着FGFRs 的异常活化,FGF/FGFRs 信号通路几乎参与所有恶性肿瘤的发生和发展。FGF19 与其受体 FGFR4 的过表达,通过激活无数下游信号通路,调控细胞的生存、增殖、侵袭和迁移等,诱发癌变。在人类肝癌标本中,发现异常表达的FGF19 和FGFR4 与不良预后相关,过表达的FGF19 参与肝癌的发展。在小鼠实验中,过表达的 FGF19 促进肝细胞增殖,导致肝细胞发育不良,诱发肝癌。使用FGFR4 单克隆抗体,能抑制过表达FGF19 小鼠中肝癌的形成和发展。
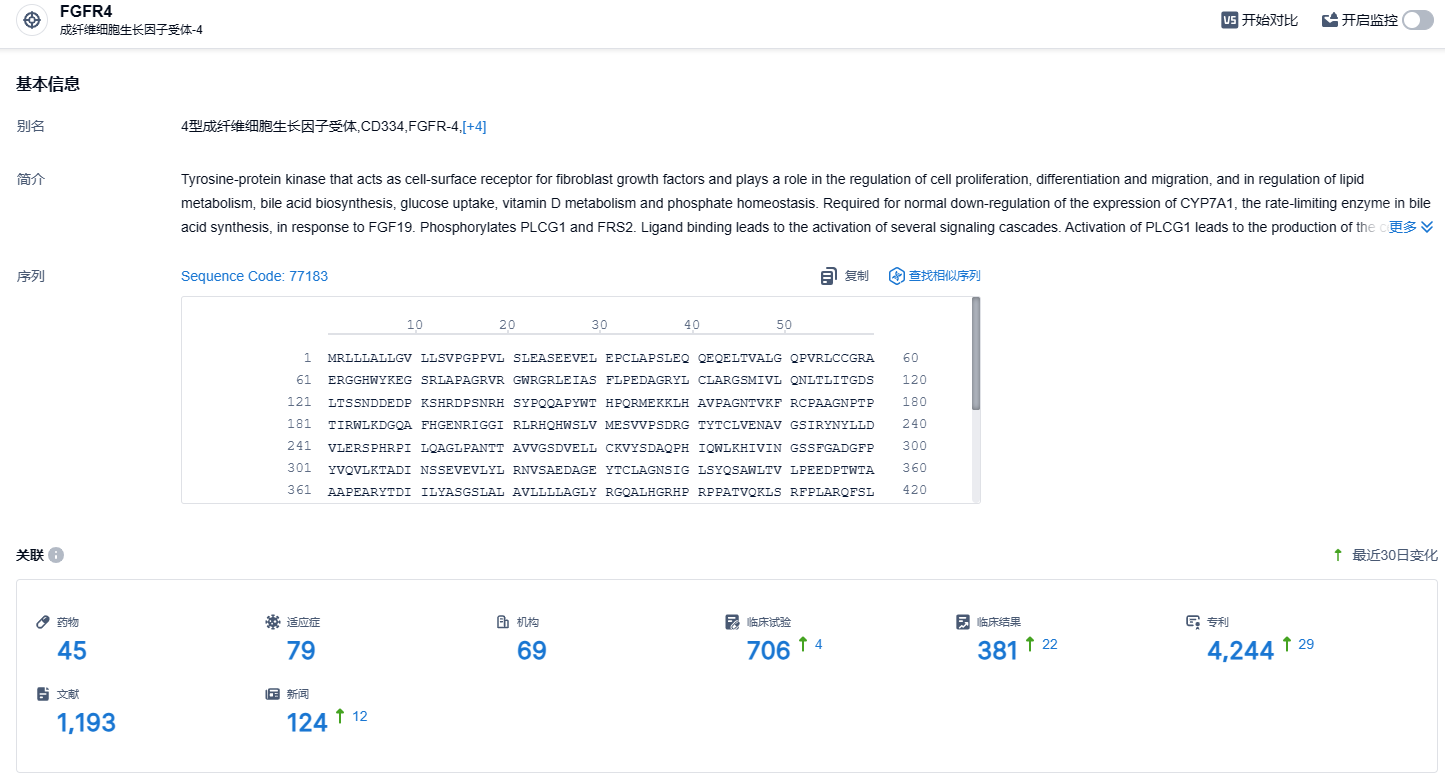
根据智慧芽新药情报库所披露的信息 (点击下方卡片直达 FGFR4 靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2023 年11月9日,FGFR4 靶点共有在研药物45个,包含的适应症有79种,在研机构69家,涉及相关的临床试验706件,专利多达4244件……据弗若斯特沙利文预测,中国和全球FGFR4药物市场在2025-2030年的复合年增长率分别为50.9%和60.1%,2026年中国和全球的FGFR4药物市场分别为2.08亿美元和5.55亿美元,2030年分别为7.40亿美元和24.35亿美元。期待ABSK012能够在FGFR4靶点赛道脱颖而出。