总缓解率达100%!Arcellx创新BCMA靶向性CAR-T疗法anito-cel展现长期疗效
近日,Arcellx公布了旗下细胞治疗产品CART-ddBCMA(现名为anitocabtagene autoleucel,anito-cel)1期扩展研究的最新临床数据。根据国际骨髓瘤工作组(IMWG)标准,所有受试者的总缓解率(ORR)达到100%,并且带有预后不良因素的患者出现了深入而持久的缓解。
anito-cel是一款靶向BCMA的CAR-T,其应用了一种名为D域(D-Domain)新的合成结合域来代替传统的scFv作为胞外抗原结合区。其与靶细胞上的抗原接触后,ddCAR能激活T细胞以杀死靶细胞,目前Arcellx正用于治疗复发性或难治性多发性骨髓瘤患者。anito-cel目前正在进行2期临床研究,它已被美国FDA授予快速通道资格、孤儿药资格和再生医学先进疗法认定。值得注意的是,anito-cel是吉利德/Kite看中的管线,通过与Arcellx公司合作授权,吉利德/Kite已经获得anito-cel在美国的独家权益。
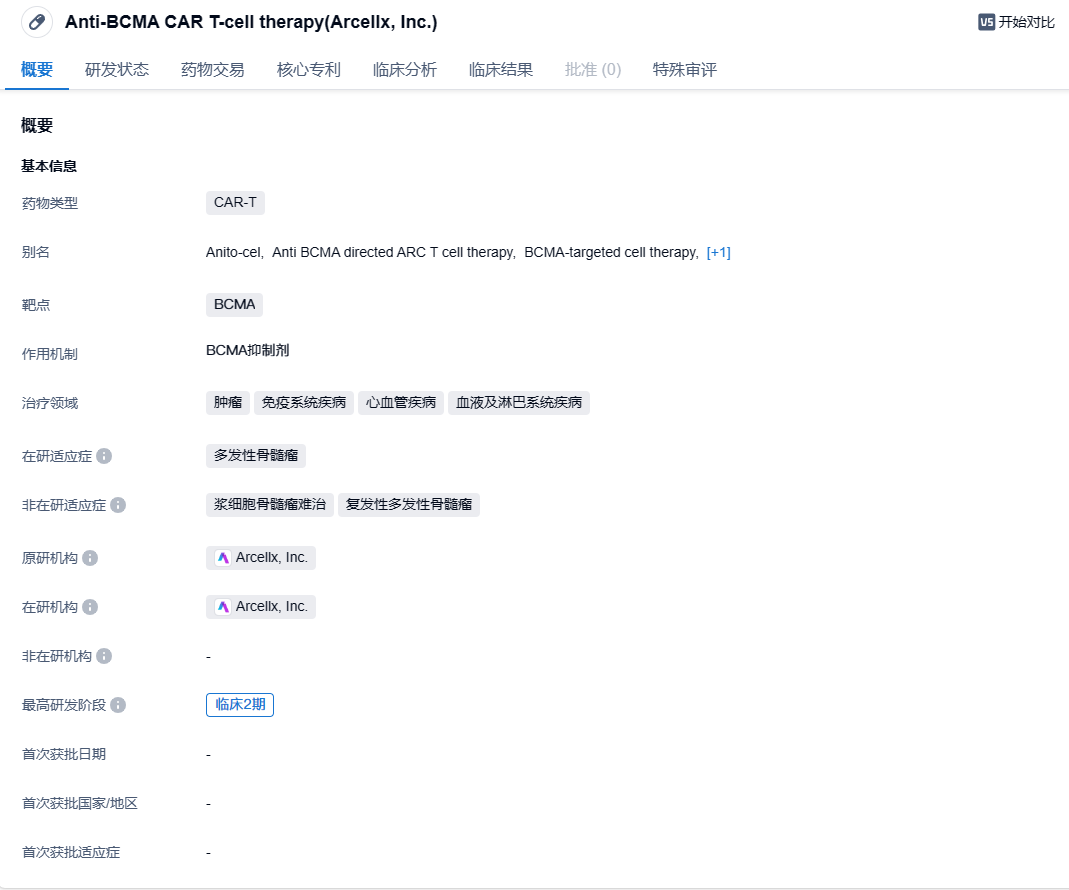 Anito-cel目前正在进行2期临床研究,它已被美国FDA授予快速通道资格、孤儿药资格和再生医学先进疗法认定。在2023年10月15日数据截止时,剂量为1.15亿(+/-10)个CAR+ T细胞的给药方案仍然耐受良好。使用anito-cel出现的不良反应,包括细胞因子释放综合征(CRS)和免疫效应细胞相关神经毒性综合征(ICANS),均在可控范围内。试验过程中无3级(或以上)CRS病例,仅有一例(3%)3级ICANS病例,此前未报告其他不良反应病例。试验中未观察到组织靶向毒性,未发现迟发性神经毒性事件或帕金森病症状。
Anito-cel目前正在进行2期临床研究,它已被美国FDA授予快速通道资格、孤儿药资格和再生医学先进疗法认定。在2023年10月15日数据截止时,剂量为1.15亿(+/-10)个CAR+ T细胞的给药方案仍然耐受良好。使用anito-cel出现的不良反应,包括细胞因子释放综合征(CRS)和免疫效应细胞相关神经毒性综合征(ICANS),均在可控范围内。试验过程中无3级(或以上)CRS病例,仅有一例(3%)3级ICANS病例,此前未报告其他不良反应病例。试验中未观察到组织靶向毒性,未发现迟发性神经毒性事件或帕金森病症状。
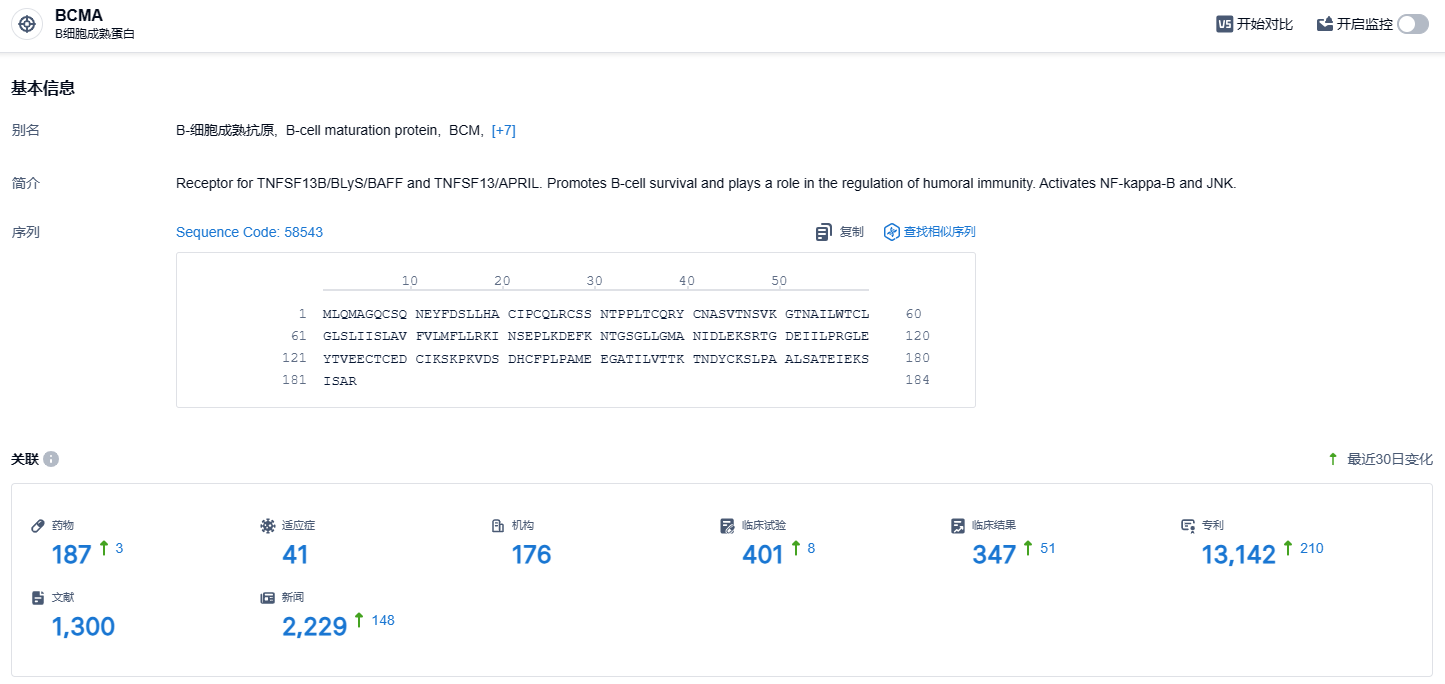
根据智慧芽新药情报库所披露的信息 (点击下方卡片直达BCMA靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2023 年12月15日,BCMA靶点共有在研药物187个,包含的适应症有41种,在研机构176家,涉及相关的临床试验401件,专利多达13142件……CAR-T细胞疗法的出现对于血液肿瘤治疗具有革命性意义,为血液肿瘤患者带来了新的治疗选择和希望,尤其用于后线骨髓瘤患者可显著提高缓解率并延长生存期,改善了患者治疗效果和生存质量。期待anito-cel后续研发一切顺利。