预约演示
更新于:2026-04-25
COVID-19 S-Trimer vaccine (Sichuan Clover Biopharmaceuticals, Inc)
更新于:2026-04-25
概要
基本信息
药物类型 预防性疫苗、重组亚单位疫苗 |
别名 2019-nCoV S-Trimer vaccine、CpG 1018/Alum、Protein-based COVID-19 S-trimer vaccine + [5] |
作用方式 调节剂、刺激剂 |
作用机制 SARS-CoV-2 S protein调节剂(冠状病毒刺突糖蛋白调节剂)、免疫刺激剂 |
在研适应症 |
非在研适应症- |
原研机构 |
在研机构 |
最高研发阶段批准上市 |
首次获批日期 中国 (2022-12-05), |
最高研发阶段(中国)批准上市 |
特殊审评紧急使用授权 (中国) |
登录后查看时间轴
结构/序列
Sequence Code 1120173653

关联
10
项与 COVID-19 S-Trimer vaccine (Sichuan Clover Biopharmaceuticals, Inc) 相关的临床试验NCT05812586
Covid-19 Vaccine Boosting in a Real World Setting: Exploratory Phase 3, Cohort Randomized, Single-blind, Multi-center Study to Evaluate the Safety and Immunogenicity of a Booster Dose of Various Covid-19 Vaccines in Fully Covid-19 Vaccine-primed Subjects Regardless of the Number of Prior Booster Dose(s) Received.
SARS-CoV-2 is a highly transmissible and pathogenic coronavirus that emerged in late 2019 and has caused a pandemic of acute respiratory disease, collectively known as COVID-19. Given the relatively short duration of protection after vaccination or SARS-CoV-2 infection and the evolution of immune-evading strains, it is likely that the population will have to be repeatedly boosted until a "universal" Pan-Sarbecovirus vaccine is available.
SARS-CoV-2 protein subunit vaccine candidates have shown that, despite adjuvantation, their safety/reactogenicity profile seems to be preferable over mRNA or vectored vaccines, whilst inducing non-inferior immune responses (1,2).
In this regard, serious adverse events of special interest from mRNA vaccines seem to be have been substantially underestimated/underreported. In a preliminary analysis by an International consortium, the true incidence seems to be 1,250/million excess risk in vaccinees instead of the 1-2/million reported by the Department of Health and Human Services (3,4). Additionally, in a recent study, the Clover SCB-2019 protein subunit vaccine candidate has shown higher neutralizing antibodies titers against the omicron variant, when compared to an inactivated vaccine (data not published yet). Although Brazil has various vaccine platforms authorized for emergency use or licensed, such as mRNA vaccines, vector-based vaccines, inactivated vaccines, so far Brazil has no access to adjuvanted or non-adjuvanted protein-based vaccines.
This study will involve two vaccines registered in Brazil and a protein-based adjuvanted vaccine candidate, SCB-2019/Clover. Protein-based adjuvanted vaccines have the advantage of being from a known and licensed technology that can produce high quantities of vaccine at reasonable Costs of Goods. Protein-based adjuvanted vaccines have also been shown to be highly immunogenic, both in the context of COVID-19 (2,5) and other licensed vaccines (6), with long persistence of immunity and protection.
Over 80% of the Brazilian population above the age of 18 years have received a full primary vaccination and another 7% at least one dose of vaccine. The overall booster coverage is about 48% (64% of the adults) (7). Anvisa has authorized 1st and 2nd booster doses of various vaccines in line with the MoH policy which was last updated in March 2022. It can be speculated that, like in other geographies, a third booster will be recommended soon, especially to at risk populations and in the scenario of high circulation of the Omicron BA.5 strain.
This study will explore the immunogenicity, safety and reactogenicity of a booster dose of various platforms in fully primed individuals regardless of the number of booster doses they have received prior to the enrollment in the study.
This mimics the "real world scenario" at vaccination centers where individuals with different background vaccination schemes show up for "a booster". It would facilitate logistics of immunization substantially if vaccines for boosting, independent of the immunization status, could be interchangeable with respect to safety/reactogenicity and immunogenicity. This study will enroll fully-primed individuals (2 doses of either Pfizer mRNA or Oxford/AZ/Fiocruz or Sinovac/Butantan or 1 dose of Janssen vaccine) who have received their last vaccine dose at least 4 months prior to study entry and who have received either no booster, or 1 or 2 boosters. Individuals will be stratified in cohorts by number of boosters and then randomized to receive one of 3 booster vaccines (AstraZeneca/Fiocruz, Pfizer/Wyeth, SCB-2019/Clover).
SARS-CoV-2 protein subunit vaccine candidates have shown that, despite adjuvantation, their safety/reactogenicity profile seems to be preferable over mRNA or vectored vaccines, whilst inducing non-inferior immune responses (1,2).
In this regard, serious adverse events of special interest from mRNA vaccines seem to be have been substantially underestimated/underreported. In a preliminary analysis by an International consortium, the true incidence seems to be 1,250/million excess risk in vaccinees instead of the 1-2/million reported by the Department of Health and Human Services (3,4). Additionally, in a recent study, the Clover SCB-2019 protein subunit vaccine candidate has shown higher neutralizing antibodies titers against the omicron variant, when compared to an inactivated vaccine (data not published yet). Although Brazil has various vaccine platforms authorized for emergency use or licensed, such as mRNA vaccines, vector-based vaccines, inactivated vaccines, so far Brazil has no access to adjuvanted or non-adjuvanted protein-based vaccines.
This study will involve two vaccines registered in Brazil and a protein-based adjuvanted vaccine candidate, SCB-2019/Clover. Protein-based adjuvanted vaccines have the advantage of being from a known and licensed technology that can produce high quantities of vaccine at reasonable Costs of Goods. Protein-based adjuvanted vaccines have also been shown to be highly immunogenic, both in the context of COVID-19 (2,5) and other licensed vaccines (6), with long persistence of immunity and protection.
Over 80% of the Brazilian population above the age of 18 years have received a full primary vaccination and another 7% at least one dose of vaccine. The overall booster coverage is about 48% (64% of the adults) (7). Anvisa has authorized 1st and 2nd booster doses of various vaccines in line with the MoH policy which was last updated in March 2022. It can be speculated that, like in other geographies, a third booster will be recommended soon, especially to at risk populations and in the scenario of high circulation of the Omicron BA.5 strain.
This study will explore the immunogenicity, safety and reactogenicity of a booster dose of various platforms in fully primed individuals regardless of the number of booster doses they have received prior to the enrollment in the study.
This mimics the "real world scenario" at vaccination centers where individuals with different background vaccination schemes show up for "a booster". It would facilitate logistics of immunization substantially if vaccines for boosting, independent of the immunization status, could be interchangeable with respect to safety/reactogenicity and immunogenicity. This study will enroll fully-primed individuals (2 doses of either Pfizer mRNA or Oxford/AZ/Fiocruz or Sinovac/Butantan or 1 dose of Janssen vaccine) who have received their last vaccine dose at least 4 months prior to study entry and who have received either no booster, or 1 or 2 boosters. Individuals will be stratified in cohorts by number of boosters and then randomized to receive one of 3 booster vaccines (AstraZeneca/Fiocruz, Pfizer/Wyeth, SCB-2019/Clover).
开始日期2023-03-14 |
申办/合作机构 |
NCT05193279
A Randomized, Controlled, Dose-finding, Observer-blind, Phase 2/3 Study to Evaluate the Safety, Reactogenicity and Immunogenicity of CpG/Alum-adjuvanted Recombinant SARS-CoV-2 Trimeric S-protein Subunit Vaccines (SCB-2019 Vaccine) in Children <18 Years of Age
This is a phase 2/3, randomized, controlled study to assess the reactogenicity, safety and immunogenicity of adjuvanted recombinant SARS-CoV-2 trimeric S-protein subunit vaccine (SCB-2019), when administered as 2-dose vaccination series in children below 18 years of age.
开始日期2022-10-05 |
NCT05470803
An Observer-blind, Cohort Randomized, Exploratory Phase 3 Study to Evaluate the Safety and Immunogenicity of Recombinant Covid-19 Vaccine (AstraZeneca/Fiocruz), mRNA Covid-19 (Comirnaty, Pfizer/Wyeth) Vaccine and Recombinant SARS-CoV-2 Trimeric S-protein Subunit Vaccine (SCB-2019-Clover) as 4th Dose in Individuals Primed/ Boosted With Various Regimens
This is an exploratory phase 3, cohort randomized, observer-blind, multi-center study to evaluate the safety and immunogenicity of a 4th dose of various SARS-CoV-2 vaccines. There will be 04 study cohorts, that have previously received 03 doses of the indicated vaccine (s), divided into 10 groups; and each one of the 10 study groups will receive the 4th dose. This exploratory study will enroll up to 360 participants in 4 cohorts and a total of 10 groups: Cohort A (N=90), Cohort B (N= 90), Cohort C (N=150) and Cohort D (N=30). In cohorts A-C participants will be randomized 1:1:1 to three different 4th dose regimens. The number of proposed participants will provide a reasonable accurate descriptive summary of the safety and immunogenicity of the tested vaccination regimens.
开始日期2022-08-01 |
申办/合作机构 |
100 项与 COVID-19 S-Trimer vaccine (Sichuan Clover Biopharmaceuticals, Inc) 相关的临床结果
登录后查看更多信息
100 项与 COVID-19 S-Trimer vaccine (Sichuan Clover Biopharmaceuticals, Inc) 相关的转化医学
登录后查看更多信息
100 项与 COVID-19 S-Trimer vaccine (Sichuan Clover Biopharmaceuticals, Inc) 相关的专利(医药)
登录后查看更多信息
17
项与 COVID-19 S-Trimer vaccine (Sichuan Clover Biopharmaceuticals, Inc) 相关的文献(医药)2024-12-31·Human vaccines & immunotherapeutics
SCB-2019 protein vaccine as heterologous booster of neutralizing activity against SARS-CoV-2 Omicron variants after immunization with other COVID-19 vaccines
Article
作者: Hu, Branda ; de Los Reyes, Mari Rose A. ; Ambrosino, Donna ; Siber, George ; Gao, Faith ; Roa, Camilo C. ; Ilagan, Hannalyn ; Han, Htay Htay ; Clemens, Ralf ; Smolenov, Igor ; Plennevaux, Eric
We assessed the non-inferiority of homologous boosting compared with heterologous boosting with the recombinant protein vaccine, SCB-2019, in adults previously immunized with different COVID-19 vaccines. Three equal cohorts (N ~ 420) of Philippino adults (18-80 years) previously immunized with Comirnaty, CoronaVac or Vaxzevria COVID-19 vaccines were randomized 1:1 to receive homologous or heterologous (SCB-2019) boosters. Neutralizing antibodies against prototype SARS-CoV-2 (Wuhan-Hu-1) were measured in all participants and against Delta variant and Omicron sub-lineages in subsets (30‒50 per arm) 15 days after boosting. Participants recorded solicited adverse events for 7 days and unsolicited and serious adverse events until Day 60. Prototype SARS-CoV-2 neutralizing responses on Day 15 after SCB-2019 were statistically non-inferior to homologous Vaxzevria boosters, superior to CoronaVac, but lower than homologous Comirnaty. Neutralizing responses against Delta and Omicron BA.1, BA.2, BA.4 and BA.5 variants after heterologous SCB-2019 were higher than homologous CoronaVac or Vaxzevria, but lower than homologous Comirnaty. Responses against Omicron BF.7, BQ.1.1.3, and XBB1.5 following heterologous SCB-2019 were lower than after homologous Comirnaty booster but significantly higher than after Vaxzevria booster. SCB-2019 reactogenicity was similar to CoronaVac or Vaxzevria, but lower than Comirnaty; most frequent events were mild/moderate injection site pain, headache and fatigue. No vaccine-related serious adverse events were reported. Heterologous SCB-2019 boosting was well tolerated and elicited neutralizing responses against all tested SARS-COV-2 viruses including Omicron BA.1, BA.2, BA.4, BA.5, BF.7, BQ.1.1.3, and XBB1.5 sub-lineages that were non-inferior to homologous boosting with CoronaVac or Vaxzevria, but not homologous Comirnaty booster.
2024-10-01·JOURNAL OF INFECTION
Indirect effectiveness of a novel SARS-COV-2 vaccine (SCB-2019) in unvaccinated household contacts in the Philippines: A cluster randomised analysis
Article
作者: Marks, Florian ; Aziz, Asma Binte ; Roa, Camilo ; Sugimoto, Jonathan Dewing ; Carlos, Josefina ; Montellano, May Emmeline B ; Kim, Hwa Young ; de Los Reyes, Mari Rose A ; Clemens, Ralf ; Hong, Sye Lim ; Borja-Tabora, Charissa ; Alberto, Edison R ; Salvani-Bautista, Milagros ; Tadesse, Birkneh Tilahun ; You, Young Ae ; Bravo, Lulu ; Njau, Irene
BACKGROUND:
Though observational evidence supports indirect effects of SARS-CoV-2 vaccines, randomised experiments are lacking. To address this gap, the double-blinded, prospective follow-up of the household contacts (HHCs) of Philippine participants of the individually-randomised, placebo-controlled trial of the adjuvanted-subunit protein COVID-19 vaccine, SCB-2019, (EudraCT, 2020-004272-17; ClinicalTrials.gov, NCT04672395) was analyzed in a cluster-randomised fashion.
METHODS:
Over an eight-week period, HHCs were followed by rRT-PCR and paired rapid antibody tests (RATs) to detect symptomatic (SCI, primary) and all (ACI, secondary) SARS-CoV-2 infection. A standard analysis estimated the indirect effectiveness of SCB-2019 for each endpoint, excluding HHC RAT-positive at enrollment. A secondary analysis employed enzyme-linked immunosorbent assay (ELISA) results to correct for suspected bias.
FINDINGS:
SCB-2019 (N = 3470) and placebo (N = 3225) exposed HHCs contributed to at least one analysis. The standard analysis estimated that SCB-2019 reduced the risk of SCI by 83% (95% confidence/credible interval [CI: 32% to 96%), with no effect against ACI. The bias-corrected relative risk reduction was 97% (95% CI: 74% to 100%) for SCI and 79% (95% CI: 14% to 96%) for ACI, with an estimated one SARS-CoV-2 infection prevented per 4.8 households where one member received SCB-2019.
INTERPRETATION:
SCB-2019 demonstrated bias-corrected indirect effectiveness against SARS-CoV-2 infection among HHC, even at a modest coverage level in the household (approximately 25%). Further research into the indirect effects of SARS-CoV-2 vaccines is needed to optimize the impact of limited doses in low and middle-income settings.
2024-07-01·VACCINE
Interchangeability of different COVID-19 vaccine platforms as booster doses: A phase 3 study mimicking real-world practice
Article
作者: Sue Ann Costa Clemens ; Eveline P. Milan ; Igor Smolenov ; Lily Weckx ; Ralf Clemens
BACKGROUND:
The COVID-19 pandemic is over but the highly immunized or naturally exposed global population still requires booster vaccinations against newly emerging SARS-CoV-2 variants. We assessed safety and immunogenicity of booster doses of COVID-19 vaccines based on three different platforms in a setting that mimics the current routine practice in Brazil.
METHODS:
In this phase 3 study from 14 February 2023 to 12 June 2023 we enrolled previously immunized adults to receive an additional booster dose of one of three vaccines. Immunogenicity against ancestor SARS-CoV-2 and Omicron BF.7, BQ.1.1.3, and XBB.1.5.6 sub-lineages was measured as ELISA IgG or virus neutralizing (VNT) antibodies and safety/reactogenicity assessed using diary cards.
RESULTS:
Volunteers with a history of full primary COVID-19 immunization striated to three cohorts according to their previous booster vaccination history-0 (n = 26), 1 (n = 140) or 2 (n = 606) booster vaccinations-were randomized 2:1:1 to receive either recombinant protein (SCB-2019, Clover), adenovirus-vector (ChAdOx1-S, AstraZeneca/Fiocruz), or mRNA (BNT162b2, Pfizer/Wyeth). Baseline antibody titers were higher in individuals who had received one or two boosters and titers against both ancestor and Omicron sub-lineages increased in all groups regardless of the number of previous booster doses or the vaccine used. Day 28 geometric mean titers (GMTs) and geometric mean-fold rises (GMFR) against all variants were higher after BNT162b than SCB-2019 or ChAdOx1-S, but BNT162b groups displayed more rapid antibody waning at Day 84. Within cohorts each vaccine elicited similar GMFR against the different SARS-CoV-2 strains. All vaccines were well tolerated with similar solicited reactogenicity profiles.
CONCLUSIONS:
Protein, adenovirus-vector or mRNA vaccine boosters were equally well tolerated and immunogenic against ancestor SARS-CoV-2 and Omicron sub-lineages in fully primed adults with 0-2 prior boosters. BNT162b induced the highest immune responses but also the most rapid waning of antibodies 3 months after vaccination.
CLINICAL TRIAL REGISTRATION:
ClinicalTrials.gov, identifier NCT05812586.
84
项与 COVID-19 S-Trimer vaccine (Sichuan Clover Biopharmaceuticals, Inc) 相关的新闻(医药)2026-03-25
香港交易及結算所有限公司及香港聯合交易所有限公司對本公告的內容概不
負責,對其準確性或完整性亦不發表任何聲明,並明確表示,概不就因本公告
全部或任何部分內容所產生或因依賴該等內容而引致的任何損失承擔任何責
任。
(於開曼群島註冊成立的有限公司)
(股份代號:2197)
截至2025年12月31 日止年度全年業績公告
及
建議修訂組織章程大綱及細則
董事會欣然公佈本集團於報告期的經審核綜合業績,連同截至2024年12月31日
止年度的比較數字。本集團於報告期的綜合財務報表已由審核委員會審閱,並
經本公司核數師容誠(香港)會計師事務所有限公司(前稱先機會計師行有限公
司)審核。
於本公告內,「我們」指本公司,及倘文義另有所指,本集團。本公告所載的若
干金額及百分比數字已作四捨五入調整,或已四捨五入至小數點後一位或兩
位。本公告任何表格、圖表或其他地方所示總額與所列數額總和的任何差異乃
因四捨五入所致。
財務摘要
現金及銀行結餘
收
其他收入及收益
銷售及分銷開支
行政開支
研發開支
其他開支
年內虧損
經調整年內虧損*
截至12 月31 日
2025 年
2024 年
人民幣千元
人民幣千元
271,403
556,515
截至12 月31 日止年度
2025 年
2024 年
人民幣千元
人民幣千元
3,505
38,419
54,098
97,215
(5,070)
(19,705)
(66,332)
(75,172)
(182,338)
(183,387)
(7,813)
(738,201)
(205,092)
(903,428)
(198,405)
(887,150)
*
經調整年內虧損於國際財務報告準則並無界定,其指剔除以股份為基礎的薪酬開支所帶
來的影響後的年內虧損。
國際財務報告準則計量:
現金及銀行結餘(包括現金及現金等價物、定期存款、受限制現金及抵押存款)
由截至2024年12月31日的人民幣556.5百萬元減少人民幣285.1百萬元至截至2025
年12月31日的人民幣271.4百萬元,主要由於償還銀行貸款、研發活動的持續投
入及日常運營導致的現金淨流出。
截至2025年12月31日止年度,本集團錄得收入人民幣3.5百萬元,主要反映上一
期間銷售的AdimFlu-S (QIS)的退貨率因實際退貨低於原先估計而予以調整。
其他收入及收益由截至2024年12月31日止年度的人民幣97.2百萬元減少人民幣
43.1百萬元至截至2025年12 月31 日止年度的人民幣54.1 百萬元,主要是因為於
2024年確認為其他收入的貿易應付款項部分豁免款(於本報告期並無再發生)
以及於2024年CEPI資金完成結算以及銀行利息收入的減少,其影響部分被當期
確認的政府補助及匯兌收益淨額的增加所抵銷。
銷售及分銷開支由截至2024年12月31日止年度的人民幣19.7百萬元減少人民幣
14.6百萬元至截至2025年12 月31 日止年度的人民幣5.1 百萬元,主要由於本集團
在中國大陸有關AdimFlu-S (QIS) 的商業活動已終止,商業團隊的薪金及福利減
少。
行政開支由截至2024年12月31日止年度的人民幣75.2百萬元減少人民幣8.9百萬
元至截至2025 年12 月31 日止年度的人民幣66.3 百萬元,主要由於僱員薪金及福
利減少,反映出持續的節約成本措施及提高的運營效率,其影響部分被諮詢費
增加所抵銷。
研發開支由截至2024年12 月31 日止年度的人民幣183.4 百萬元減少人民幣1.1 百
萬元至截至2025年12月31日止年度的人民幣182.3百萬元,因為本集團繼續精簡
其企業運營,並將呼吸道疫苗候選產品列為優先事項。
其他開支由截至2024年12 月31 日止年度的人民幣738.2 百萬元減少人民幣730.4
百萬元至截至2025年12月31日止年度的人民幣7.8百萬元,主要因為於2024年就
新冠疫苗相關原材料作出全額撥備。
年內虧損由截至2024年12 月31 日止年度的人民幣903.4 百萬元減少人民幣698.3
百萬元至截至2025年12 月31 日止年度的人民幣205.1 百萬元,主要由於於2024年
計提存貨減值撥備的非經常性綜合影響。
非國際財務報告準則計量:
經調整年內虧損指剔除以股份為基礎的薪酬開支所帶來的影響後的年內虧損。
經調整年內虧損一詞在國際財務報告準則中並無界定。下表載列年內虧損與
經調整年內虧損的對賬:
業務摘要
於報告期,本公司在產品組合擴大及業務營運優化方面取得了重大進展:
我們的產品及候選疫苗
呼吸道融合前F-三聚體候選疫苗(RSV+hMPV±PIV3)
•
2025年10 月,本公司宣佈RSV+hMPV±PIV3聯合疫苗(SCB-1022及SCB-1033)I
期臨床試驗的積極數據。
•
2025年10 月,本公司亦宣佈RSV疫苗重複接種(SCB-1019)在老年人群的I 期
臨床試驗的積極中期結果。
•
呼吸道聯合疫苗候選產品SCB-1022 及SCB-1033以及RSV 獨立疫苗候選產品
SCB-1019均基於使用三葉草生物專有的蛋白質三聚體化疫苗技術平台的
融合前穩定的F (PreF)-三聚體亞單位疫苗抗原開發。
AdimFlu-S (QIS)
•
由於市場狀況發生重大變化,本公司於2025年6月宣佈行使單方面終止權,
終止與國光生物科技股份有限公司(「國光生技」)的合作,且本公司未來將
不會在中國大陸分銷AdimFlu-S (QIS)。
SCB-219M
•
SCB-219M是一種融合蛋白(TPO模擬肽雙特異性Fc),用於治療腫瘤化療相
關性血小板減少症(CIT)。
•
2024年11月,啟動Ib期臨床試驗,評估SCB-219M在CIT患者中重複給藥的情
況。
新冠疫苗
•
於2022年12 月獲得的中國新冠疫苗緊急使用授權(EUA) 仍然有效。
管理層討論與分析
概覽
三葉草生物是一家致力以創新型疫苗拯救生命和改善全球健康水平的全球創
新性生物製藥公司。憑藉綜合研發實力、生產和商業化能力,以及與分佈全球
的相關機構強大的合作夥伴關係,本公司已經開發出多樣化的候選疫苗管線,
以期減輕疫苗可預防疾病的治療負擔,並使更多疾病得到預防。
經新冠疫苗SCB-2019(CpG1018╱鋁佐劑)的成功開發所驗證及目前被用於呼吸
道融合前F-三聚體候選疫苗(RSV + hMPV ± PIV3)的開發,Trimer-Tag技術平台是
一個基於天然依賴三聚體化功能的靶點用於研製重組蛋白疫苗的產品開發平
台。Trimer-Tag技術平台可以使任意一個目的蛋白三聚體化為共價三聚體化結
構。Trimer-Tag的三聚體化基序為基於人源CICP氨基酸序列(I型前膠原蛋白C端
結構域)。Trimer-Tag是目前全球唯一一個利用人源三聚體化標籤生產重組共價
三聚體化融合蛋白(三聚體標籤蛋白)的三聚體化技術平台。
於報告期內,我們未使用佐劑的RSV疫苗候選產品組合在創新RSV疫苗市場確
立其全球領先地位。憑藉在澳大利亞及美國進行的一系列國際I期臨床試驗取
得的積極結果,該等候選產品的同類最佳(BiC)及同類首創(FiC)特性已獲驗證。
2025年10月中旬,本公司宣佈在澳大利亞進行的I期臨床試驗的積極結果,該
試驗評估SCB-1022 (RSV + hMPV)及SCB-1033 (RSV + hMPV + PIV3)聯合疫苗與SCB-
1019 (RSV)在未接種過RSV疫苗的老年人(60至85歲)中進行頭對頭比較的結果。
該項研究正在評估安全性、反應原性及免疫原性,初步結果來自144 名參與者
(每個疫苗組48 名參與者)的選定劑量水平。我們的積極數據顯示,SCB-1022 及
SCB-1033具有潛在同類最佳(BiC) RSV、hMPV及PIV3中和抗體(nAb)反應,且對
RSV無免疫干擾,並具潛在同類最佳(BiC)的安全性及耐受性。本公司同時宣佈
在美國進行的I 期臨床試驗的34 名參與者(16 名參與者接受SCB-1019,15 名參與
者接受AREXVY,3 名參與者接受生理鹽水安慰劑)的積極中期結果,該試驗評
估了SCB-1019與AREXVY(GSK的RSV疫苗)在入組前至少在兩個流行季前接種過
首劑AREXVY的老年人(60至85歲)中進行重複接種的頭對頭比較。與AREXVY相
比,使用SCB-1019進行重複接種所產生的增量nAb反應,或可恢復初次接種後觀
察到的nAb 峰值水平及保護作用。該項I期異源重複接種試驗的完整結果預期
將於2026年上半年公佈。我們的RSV疫苗候選產品(SCB-1019、SCB-1022 及SCB-
1033)均基於使用三葉草生物的蛋白質三聚體化疫苗技術平台的融合前穩定的
F (PreF)-三聚體亞單位疫苗抗原開發。
本公司將繼續優先投入資源推進我們專有的呼吸道融合前F-三聚體候選疫苗
(RSV + hMPV ± PIV3)的臨床開發,以進一步鞏固我們在全球RSV及呼吸道疫苗
市場中同類最佳(BiC)及同類首創(FiC)的地位。
產品管線
疫苗
|候選產品|靶點|適應症|早期發現|臨床前|申報臨床|I期臨床|II期臨床|III期臨床|申報上市|批准╱緊急 使用授權|
|---|---|---|---|---|---|---|---|---|---|---|
|SCB-1022 PreF三聚體 RSV-hMPV|||||||||||
|SCB-1033 PreF三聚體 RSV-hMPV-PIV3|||||||||||
|SCB-1019 RSV F-三聚體 呼吸道合胞病毒(RSV)|||||||||||
|SARS-CoV-2 S- SCB-2019 三聚體 新冠 (CpG 1018/Alum)(1) (廣譜中和效果)||||||||全球(中國|以外)|中國|
|XBB.1.5改良 SCB-2023B SARS-CoV-2 S- 新冠 三聚體|||||||||||
|SCB-1001 Rabies G-三聚體 狂犬病|||||||||||
(1) 新冠疫苗於2022年12月在中國獲得緊急使用授權。
其他資產
業務回顧
我們的產品及候選產品
本公司專注於建立領先的呼吸道疫苗產品組合,以滿足預防嚴重呼吸道傳染
病方面尚未得到滿足的需求,並抓住相關的重要的交叉推廣、聯合用藥及長期
生命週期管理機會。
呼吸道融合前F-三聚體候選疫苗(RSV+hMPV±PIV3)
2025年上半年,本公司按計劃啟動兩項針對戰略管線資產的I期臨床試驗:本公
司的未使用佐劑的RSV 融合前穩定的F (PreF)-三聚體亞單位候選疫苗SCB-1019
及兩種呼吸道聯合候選疫苗SCB-1022 (RSV + hMPV)及SCB-1033 (RSV + hMPV +
PIV3)。於本公司獲得美國IND臨床試驗批准,並啟動SCB-1019的RSV重複接種臨
床研究後,首次臨床試驗於2025年3月下旬公佈。
2025年10月中旬,本公司宣佈在澳大利亞進行的I期臨床試驗的積極結果,該
試驗評估SCB-1022 (RSV + hMPV)及SCB-1033 (RSV + hMPV + PIV3)聯合疫苗與SCB-
1019 (RSV)在未接種過RSV疫苗的老年人(60至85歲)中進行頭對頭比較的結果。
該項研究正在評估安全性、反應原性及免疫原性,初步結果來自144 名參與者
(每個疫苗組48 名參與者)的選定劑量水平。我們的積極數據顯示,SCB-1022 及
SCB-1033具有潛在同類最佳(BiC) RSV、hMPV及PIV3中和抗體(nAb)反應,且對
RSV無免疫干擾,並具潛在同類最佳(BiC)的安全性及耐受性。本公司同時公佈
在美國進行的I 期臨床試驗的34 名參與者(16 名參與者接受SCB-1019,15 名參與
者接受AREXVY,3 名參與者接受生理鹽水安慰劑)的積極中期結果,該試驗評
估了SCB-1019與AREXVY(GSK的RSV疫苗)在入組前至少在兩個流行季前接種過
AREXVY的老年人(60 至85 歲)中進行重複接種的頭對頭比較。
我們的RSV疫苗候選產品(SCB-1019、SCB-1022及SCB-1033)均基於使用三葉草生
物的蛋白質三聚體化疫苗技術平台的融合前穩定的F (PreF)-三聚體亞單位疫苗
抗原開發。
AdimFlu-S (QIS)
2023年2 月,本公司宣佈與國光生技達成分銷AdimFlu-S (QIS)的獨家協議,此款
疫苗是於中國大陸內獲批的四價流感疫苗。
由於市場狀況發生重大變化,本公司於2025 年6月宣佈行使單方面終止權,終
止與國光生技的合作,且本公司未來將不會在中國大陸分銷AdimFlu-S (QIS)。
SCB-219M
SCB-219M是一種融合蛋白(TPO模擬肽雙特異性Fc),用於治療腫瘤化療相關性
血小板減少症(CIT)。與中國市場上銷售的基於天然TPO的療法相比,SCB-219M
有可能克服因抗藥性抗體(ADA)而導致的療效降低,並因其半衰期更長而實現
更方便的給藥方案。
•
2023年12 月,本公司宣佈在一項評估SCB-219M 的I期臨床試驗中獲得了積
極的安全性、有效性和藥代動力學初步數據。
•
2024年11月,本公司啟動了Ib期臨床試驗,評估SCB-219M在CIT患者中重複
給藥的情況。
新冠疫苗
於2022年12月獲得的中國新冠疫苗緊急使用授權(EUA)仍然有效。
本公司將繼續就新冠疫苗未來潛在的新興商機與監管機構及相關部門進行跟
進。
我們無法保證我們最終將能成功開發或銷售我們的核心產品。本公司股東及
潛在投資者於買賣本公司股份時務請審慎行事。
研發
作為生物科技公司,本公司繼續重視科技創新,擴大其產品及候選藥物組合,
以實現長期可持續發展。
本公司擁有一支綜合性研發團隊,能夠進行候選產品的發現、概念驗證、臨床
前和臨床開發。截至2025年12月31日,本公司的內部研發活動由各地區116名員
工支持。
生產
於報告期,本公司利用在浙江省長興縣的自有商業化生產能力,支持開發其
RSV候選疫苗(SCB-1019、SCB-1022 及SCB-1033)。該工廠符合中國的GMP 合規要
求,並獲得了中國國家藥監局頒發的疫苗藥品生產許可證(DML),與其他利用
新生產基地的國內製造商相比具有潛在優勢。
該自有生產基地擁有商業規模的生產記錄,對本公司其他候選產品(包括我們
的呼吸道融合前F- 三聚體候選疫苗組合(RSV + hMPV ± PIV3)的開發具有重要
價值。
其他主要公司發展
為應對當前宏觀經濟環境的挑戰,本公司持續採取重要舉措,以(1)加強在疫苗
開發方面的核心優勢及能力;及(2)審慎評估支出及精簡組織,以提高效率和改
善效益。本公司將繼續集中資源實現其首要任務,同時繼續建立一個可潛在創
造重大價值的創新型產品組合。
未來展望
鑒於我們經驗證的Trimer-Tag平台,具有吸引力的商業生產能力以及呼吸道融
合前F-三聚體聯合候選疫苗(RSV + hMPV ± PIV3)的正在進行的臨床開發,本公
司仍專注於實施其長期戰略,逐步搭建全球領先的呼吸道疫苗產品組合。基於
在澳大利亞及美國進行的一系列國際I期臨床試驗的令人鼓舞的結果,我們的
RSV候選疫苗產品組合(SCB-1019、SCB-1022 及SCB-1033)已成功在創新RSV疫苗
領域確立全球領先地位。在持續優先配置資源以進一步鞏固這一領導地位的
同時,本公司一直積極推進探索各種潛在的全球合作機會,以求最大化我們自
持專有的RSV 疫苗候選產品組合的商業化潛力。
在企業管治方面,本公司將持續採取重大措施,通過提高運營效率、尋求創造
價值的機會及保持穩健的現金狀況來支持未來的成功,從而實現企業財務的
可持續發展。
財務回顧
截至2025年12 月31 日止年度與截至2024 年12 月31 日止年度比較
除稅前虧損
所得稅開支
年內虧損
收入
於各報告期末,本集團對所售商品未來銷售退回情況進行估計,並對該等預期
退回的產品確認的收入進行相應調整。估計銷售退回需運用判斷及估算。倘實
際退回率與最初估計有差異,該差異將在後期進行調整。
截至2025年12月31日止年度,本集團錄得收入人民幣3.5百萬元,主要反映上一
期間銷售的AdimFlu-S (QIS)的退貨率因實際退貨低於原先估計而予以調整。
在不考慮上述於報告期內確認的銷售退回的情況下,截至2025 年12 月31 日止
年度,並無自AdimFlu-S (QIS)銷售產生任何收入,原因為本集團在中國大陸的
AdimFlu-S (QIS)商業活動已經終止。
其他收入及收益
本集團的其他收入及收益主要包括政府補助、匯兌收益凈額及銀行利息收入。
其他收入及收益由截至2024年12月31日止年度的人民幣97.2百萬元減少人民幣
43.1百萬元至截至2025年12月31日止年度的人民幣54.1百萬元。該減少主要是由
於2024年確認為其他收入的貿易應付款項部分豁免款(於本報告期並無再發生)
以及於2024年CEPI資金完成結算以及銀行利息收入的減少,其影響部分被當期
確認的政府補助及匯兌收益淨額的增加所抵銷。
銷售及分銷開支
本集團銷售及分銷開支主要包括商業團隊的薪金及福利以及市場開發費用。
本集團銷售及分銷開支由截至2024年12月31日止年度的人民幣19.7百萬元減少
人民幣14.6百萬元至截至2025年12 月31 日止年度的人民幣5.1 百萬元。該減少主
要是由於本集團在中國大陸有關AdimFlu-S (QIS)的商業活動已終止,商業團隊
的薪金及福利減少。
行政開支
本集團的行政開支主要包括(i) 僱員薪金及福利,包括應計以股份為基礎的薪
酬開支;(ii)諮詢費;(iii) 折舊及攤銷開支;及(iv)辦公開支。其他行政開支包括
電腦軟件許可使用費及其他有關行政活動的雜項開支。
本集團行政開支由截至2024年12月31日止年度的人民幣75.2百萬元減少人民幣
8.9 百萬元至截至2025年12 月31 日止年度的人民幣66.3 百萬元。該減少主要是由
於僱員薪金及福利以及折舊及攤銷開支的減少,反映了持續的成本節約措施
和運營效率的提升,其影響部分被諮詢費增加所抵銷。
截至12 月31 日止年度
研發開支
本集團的研發開支主要包括:(i)僱員薪金及福利,包括應計以股份為基礎的薪
酬開支;(ii)臨床試驗開支,主要包括向合約研究機構、醫院及其他醫療機構付
款以及相關費用;(iii)用於研發活動的原材料及耗材成本;(iv)研發諮詢及服務
費,主要與臨床前研究成本有關;及(v)與我們的租賃樓宇、機器及設備有關的
折舊及攤銷。
研發開支由截至2024年12 月31 日止年度的人民幣183.4 百萬元減少人民幣1.1百
萬元至截至2025年12月31日止年度的人民幣182.3百萬元。僱員薪金及福利以及
折舊及攤銷開支因本集團持續精簡企業運營而減少。同時,本集團將資源集中
於實現其首要任務,同時繼續建立一個可潛在創造重大價值的創新型產品組
合。
其他
總計
其他開支
本集團的其他開支主要包括撇減存貨至可變現淨值╱(撥回存貨撥備)及離職補
償成本。
其他開支由截至2024年12 月31 日止年度的人民幣738.2 百萬元減少人民幣730.4
百萬元至截至2025年12月31日止年度的人民幣7.8百萬元,主要因為於2024年就
新冠疫苗相關原材料作出全額撥備。
財務成本
本集團的財務成本主要包括(i)銀行貸款利息及(ii)租賃負債的利息,主要與位
於上海及成都的辦公室有關。
本集團的財務成本由截至2024年12 月31 日止年度的人民幣5.8 百萬元減少人民
幣5.4百萬元至截至2025年12月31日止年度的人民幣0.4百萬元,主要由於與銀行
貸款相關的利息開支減少。
年內虧損
由於上文所述,本集團的虧損由截至2024年12月31日止年度的人民幣903.4百萬
元減少人民幣698.3百萬元至截至2025年12月31日止年度的人民幣205.1百萬元。
非國際財務報告準則計量
為補充本集團按照國際財務報告準則呈列的年度綜合財務報表,本集團亦提
供經調整年內虧損作為補充資料。該計量並非國際財務報告準則規定,但本集
團視其為對股東及潛在投資者評估本集團的年度綜合財務業績有用的資料。
經調整年內虧損指剔除以股份為基礎的薪酬開支所帶來的影響後的年內虧損。
該非國際財務報告準則計量不應獨立於或可代替本集團的國際財務報告準則
報告的分析。本公司對有關經調整數字的呈列未必可與其他公司所呈列的類
似計量指標相比。然而,本公司認為,此非國際財務報告準則計量可更好地反
映本集團的正常經營業績,為比較不同期間經營表現的更有力依據。
下表載列於所示年度年內虧損與經調整年內虧損的對賬:
截至12 月31 日止年度
流動資金以及資金及借款來源
本集團的現金及銀行結餘(包括現金及現金等價物、定期存款、受限資金及抵
押存款)由截至2024年12 月31 日的人民幣556.5 百萬元減少人民幣285.1 百萬元至
截至2025年12月31日的人民幣271.4百萬元。該減少主要是由於償還銀行貸款、
研發活動的持續投入及日常運營導致的現金淨流出。
截至2025年12 月31 日,本集團的流動資產合共為人民幣335.8 百萬元,包括現金
及現金等價物、受限資金人民幣271.4百萬元,預付款項、其他應收款項及其他
資產人民幣39.9百萬元,按公允價值計量且其變動計入損益的金融資產人民幣
14.6 百萬元,存貨人民幣9.9百萬元及貿易應收款項人民幣0.003 百萬元。
截至2025年12 月31 日,本集團的流動負債為人民幣1,750.6 百萬元,包括合約負
債人民幣1,572.6百萬元、貿易應付款項人民幣108.0 百萬元、其他應付款項及應
計費用人民幣59.4百萬元及租賃負債人民幣10.6 百萬元。
截至2025年12 月31 日,本集團並無銀行貸款。目前,本集團根據一套資金及財
務政策管理其資金來源及降低潛在風險。本集團努力維持足夠的現金及現金
等價物水平,以滿足短期資金需求。董事會亦根據本集團的資金需求考慮各種
資金來源,以確保以最具成本效益的有效方式使用財務資源以履行本集團的
財務責任。董事會不時審核及評估本集團的資金及財務政策,以確保其充分性
和有效性。
重大投資、重大收購及出售
截至2025年12 月31 日,本集團並無持有任何重大投資。本集團於截至2025 年12
月31日止年度亦無重大收購或出售附屬公司、聯營公司及合營企業。
未來的重大投資或資本資產計劃
截至本公告日期,本集團並無其他重大資本開支計劃。
或然負債
截至2025年12 月31 日,本集團概無任何我們預計會對業務、財務狀況或經營業
績產生重大不利影響的或然負債。
資產負債比
資產負債比乃按計息銀行借款減現金及銀行結餘,除以總權益,再乘以100%計
算。截至2025年12 月31 日,本集團為淨現金狀況,因此,資產負債比不適用。
截至2025年12 月31 日,本集團的資本承擔為人民幣6.6 百萬元,較截至2024 年12
月31日的人民幣13.1百萬元減少人民幣6.5百萬元,主要歸因於與有形資產相關
的未來付款減少。
資產抵押
截至2025年12 月31 日,本集團並無資產抵押。
外匯風險
本公司的功能貨幣為美元及本公司於中國附屬公司的功能貨幣為人民幣。報
告期內,本集團主要於中國運營,大部分交易以人民幣及美元結算。由於若干
現金及銀行結餘、貿易應收款項、其他應收款項、貿易應付款項及其他應付款
項以非功能貨幣計值,我們的金融資產及負債面臨外匯風險。因此,功能貨幣
對非功能貨幣的匯率波動可能會影響我們的經營業績。本集團目前並無外匯
對沖政策。但我們的管理層監控外匯風險並於必要時考慮對沖重大外匯風險。
僱員及薪酬
截至2025年12 月31 日,本集團有257 名僱員。本集團於截至2025 年12 月31 日止年
度的薪酬成本總額為人民幣118.6百萬元。下表載列截至2025年12月31日按職能
分類的僱員詳情:
僱員人數
佔總數之%
職能
本集團的僱員薪酬待遇包括薪金、獎金以及股權獎勵,一般根據僱員的資質、
行業經驗、職位及績效釐定。本集團根據相關法律法規的要求繳納社保及住房
公積金。
本公司亦已於2021年4月15日採納受限制股份單位計劃及首次公開發售前購股
權計劃及於2021年9 月26 日採納首次公開發售後購股權計劃,以向合資格參與
者提供獎勵。詳情請參閱招股章程附錄四「D. 股份激勵計劃」一段。
為提升僱員的素質、知識和技能水平,本集團持續為僱員提供教育和培訓計
劃,包括內部和外部培訓,以強化彼等的技術、專業或管理技能。本集團亦定
期為僱員提供培訓計劃,以確保僱員在各個方面都了解並遵守政策和程序。
綜合全面收益表
綜合財務報表附註
1.
公司資料
本公司為一家於2018年10月31日於開曼群島註冊成立的有限公司。本公司的註冊地址為
PO Box 309, Ugland House, Grand Cayman, KY1-1104, Cayman Islands。
本公司為一家投資控股公司。於年內,本集團主要從事創新型疫苗的研發、生產和商業
化。
本公司股份已於2021 年11 月5 日在香港聯合交易所有限公司(「聯交所」)主板上市。
2.
會計政策
2.1
編製基準
該等財務報表乃根據國際會計準則理事會頒佈的國際財務報告準則及香港公司條例編
製。該等財務報表乃按歷史成本基準編製,惟按公允價值計量的金融資產及負債(包括衍
生工具)除外。除另有說明外,該等財務報表以人民幣呈列,所有數值均約整至最接近千
位數。
持續經營基準
該等財務報表基於本集團將持續經營的假設編撰,該假設假定儘管於2025 年12 月31 日,
本集團錄得負債淨額人民幣1,797,319,000元(主要歸因於合約負債人民幣1,572,621,000元及
非流動貿易應付款項人民幣501,203,000 元)且截至2025 年12 月31 日止年度產生虧損淨額人
民幣205,092,000元,但本集團仍能夠履行其義務,並在2025年12月31日之後的十二個月內
繼續經營。本集團與全球疫苗免疫聯盟(「GAVI」)就合約負債存在分歧,該合約負債指自
GAVI收取的預付款項,金額為224,000,000 美元,相當於人民幣1,572,621,000 元,導致GAVI
於2025 年發出終止通知、要求還款及隨後的仲裁程序。
鑒於這些情況,董事在評估本集團是否擁有足夠的財務資源以持續經營時,已仔細考慮
了本集團未來的流動性和業績表現,以及可用的融資渠道。本集團已採取若干措施來緩
解流動性壓力並維持本集團的現金流狀況。本集團採取的措施包括但不限於以下方面:
(i)
於2026 年3 月22 日,本集團與GAVI訂立和解協議(「和解協議」),據此,訂約方之間的
仲裁程序將獲全面及最終解決,而GAVI 就仲裁提出的所有申索將於支付協定的前
期款項後獲撤回及解除。和解協議乃出於商業考慮而訂立,並不構成任何一方對
責任的承認。根據和解協議,本集團同意:(i) 向GAVI支付一筆700 萬美元的一次性
前期現金付款;(ii)未來每半年支付150萬美元或本集團現金結餘的低個位數百分比
(以較高者為準)的遞延現金付款;及(iii) 根據本集團未來現金收入(包括來自融資、
業務發展及產品銷售)的中至高個位數百分比計算的與未來現金收入表現掛鉤的或
有付款。未來付款總額(即遞延現金付款與或有付款合計)累計最高金額將不超過數
千萬美元的中段水平;在和解協議規定的12年期限內,如提前付款,則可享有適用
折扣。董事已於本集團現金流量預測中考慮和解協議項下的預期現金流出。和解協
議預期將為本集團的未來發展及其潛在實現核心戰略重點的能力提供更強的可預
見性。
(ii)
本集團已實施一系列策略及舉措以加強其資本基礎及維持流動資金,包括但不限
於籌集新資本或融資、調整項目管線優先級以及削減非核心支出,包括一般及行政
開支。
(iii)
本集團將繼續探索戰略合作及替代融資機會,倘成功,預期將進一步改善本集團的
流動資金狀況。
董事會已審閱了管理層編製的本集團現金流預測,該預測涵蓋自2025年12月31日起十二
個月的期間。基於該等預測,考慮到上述計劃和措施,董事認為,本集團將擁有足夠的營
運資金為其運營提供資金,並在2025 年12 月31 日之後的未來十二個月內,在財務義務到
期時履行這些義務。因此,董事們認為以持續經營為基礎編製綜合財務報表是恰當的。
董事知悉,本集團持續經營的能力取決於成功實施上述計劃及措施,包括籌集新資本或
融資、實施成本控制措施及達成戰略合作。儘管無法保證該等計劃及措施將會成功實施,
但董事認為持續經營基準仍屬適當。
若本集團無法實現上述計劃和措施並作為持續經營實體運營,則必須進行調整,以計提
可能產生的任何進一步負債,並將非流動資產和非流動負債分別重新分類為流動資產和
流動負債。這些調整的影響尚未在這些綜合財務報表中反映。
2.2
會計政策變動及披露
本集團已於本年度財務報表首次採納國際會計準則第21號修訂本缺乏可兌換性。本集團
尚未提前採納任何其他已頒布但尚未生效的準則或修訂本。
國際會計準則第21號修訂本列明實體如何評估貨幣是否可兌換為其他貨幣,以及在缺乏
可兌換性時如何於計量日期估計即期匯率。該等修訂要求披露能夠使財務報表的使用者
知悉貨幣不可兌換的影響的資料。由於本集團用作交易的貨幣及海外附屬公司用作換算
本集團的呈列貨幣之功能貨幣為可兌換,因此該等修訂對本集團財務報表並無產生任何
影響。
5.
其他收入及收益
其他收入及收益分析如下:
*
政府補助指自地方政府機構收到用於支持附屬公司的研發活動以及購置若干物業、
廠房及設備項目的補貼。該等政府補助並無任何未履行條件。
**
於2024年6月,本集團與其某一供應商訂立和解協議,據此,該供應商豁免本集團於
雙方訂立的服務協議項下的部分應付款項,作為本集團清償應付供應商款項的激
勵。由於服務協議項下的所有合約義務均已由供應商履行,且無額外的服務或貨品
需用來交換已豁免負債,故此項債務豁免確認為其他收入及收益。
***
自CEPI 收取的資金人民幣19,574,000 元已確認為其他收入,原因為資金附帶條件已
於截至2024 年12 月31 日止年度達成。
6.
其他開支
7.
除稅前虧損
本集團除稅前虧損已扣除以下各項:
8.
所得稅
本集團須按實體基準就本集團成員公司所處及╱或經營所在司法權區產生或獲得的溢利
繳納所得稅。
開曼群島
根據開曼群島現行法律,本公司毋須就收入或資本收益繳納稅項。此外,本公司向其股
東支付股息後,概不就股息付款徵收開曼群島預扣稅。
香港
在香港註冊成立的附屬公司須就在香港產生的估計應課稅溢利按16.5%(2024 年:16.5%)
的稅率繳納香港利得稅。該附屬公司的應課稅溢利的首2,000,000 港元(2024 年:2,000,000
港元)按8.25%(2024 年:8.25%)的稅率繳納香港利得稅,而剩餘應課稅溢利則按16.5%(2024
年:16.5%)的稅率繳納香港利得稅。
中國內地
根據中國企業所得稅法及相關法規(「企業所得稅法」),在中國內地營運的附屬公司須就
應課稅收入按25%(2024 年:25%)的稅率繳納企業所得稅。
澳洲
在澳洲註冊成立的附屬公司須按25%(2024 年:25%)的稅率繳納澳洲法定企業所得稅。
美利堅合眾國
於美國特拉華州註冊成立的附屬公司於年內須按21%(2024年:21%)的稅率繳納法定美國
聯邦企業所得稅。
英國
於英國註冊成立的附屬公司須於年內就其全球利潤按19%(2024年:19%)的稅率繳納企業
所得稅。
愛爾蘭
於愛爾蘭註冊成立的附屬公司須就年內在愛爾蘭產生的估計應課稅溢利按25%(2024年:
25%)的稅率繳納愛爾蘭企業所得稅。
9.
股息
本公司概無就截至2025 年12 月31 日止年度(2024 年:無)宣派或派付股息。
10.
母公司普通權益持有人應佔每股虧損
每股基本虧損金額乃基於母公司普通權益持有人應佔的年度虧損人民幣205,092,000 元
(2024年:人民幣903,428,000元)以及普通股加權平均數計算。截至2025年12月31日止年度,
股份的加權平均數乃基於年內已發行的1,260,362,713股股份釐定(2024年:1,253,673,382股)。
由於本集團產生虧損而尚未行使的購股權及受限制股份單位對所呈列每股基本虧損金
額具有反攤薄影響,因此概無對所呈列截至2025年12月31日止年度的每股基本虧損金額
(2024 年:無)作出調整。因此,截至2025 年及2024 年12 月31 日止年度的每股攤薄虧損金額
與每股基本虧損金額相同。
每股基本及攤薄虧損乃基於以下各項計算:
2025 年
2024 年
人民幣千元
人民幣千元
虧損
母公司擁有人應佔虧損,用於計算每股基本虧損:
2025 年
2024 年
股份
年內用於計算每股基本虧損的已發行普通股加權平均數:
1,260,362,713
1,253,673,382
本集團與客戶訂立的交易條款主要以賒賬方式進行。信貸期一般為3個月至1年,具體取
決於合約條款。每名客戶均有最高信貸限額。本集團的大部分貿易應收款項與一位主要
客戶有關,因此存在信貸風險集中。本集團並無就其貿易應收款項結餘持有任何抵押品
或其他信貸保證。貿易應收款項不計息。
貿易應收款項於報告期末基於發票日期並扣除虧損撥備的賬齡分析如下:
減值分析於各報告日期進行。本集團已採用國際財務報告準則第9 號規定的簡化方法就
預期信貸虧損計提撥備,該方法允許就所有貿易應收款項使用全期預期虧損撥備。本公
司董事認為,就貿易應收款項結餘而言,其產生的預期信貸虧損極小。於2025 年12 月31
日,並無就貿易應收款項減值計提虧損撥備(2024 年:無)。
12.
貿易應付款項
貿易應付款項於年末根據發票日期的賬齡分析如下:
貿易應付款項不計息,通常於60 天內清償,惟有特定付款期限的若干供應商除外。
貿易應付款項的非流動部分71,307,000美元(相當於人民幣501,203,000元)為採購CpG 1018佐
劑而應付Dynavax Technologies Corporation(「Dynavax」)的貿易應付款項。截至2024年及2025年
12月31日止年度,本公司已重新評估與Dynavax簽訂的採購協議的支付條款,並與Dynavax
確認應付金額及相應的付款時間。71,307,000 美元(相當於截至2025 年12 月31 日的人民幣
501,203,000元及截至2024年12年31日的人民幣512,584,000元)獲分類為貿易應付款項的非流
動部分,以反映應付Dynavax 款項的結算時間(即自資產負債表日期起計12 個月以上)。
客戶預付款
合約負債指從全球疫苗免疫聯盟(「GAVI」)收取的預付款,以交付本公司的SCB-2019
(CpG1018╱鋁佐劑)疫苗(「疫苗」)。於2021 年6 月,本公司與GAVI訂立預購協議(「預購協
議」),據此,GAVI同意採購(i) 64百萬劑疫苗;及(ii)根據當中所述選擇權最多350百萬劑疫
苗。上述預付款可用於支付本集團供應商採購所需原材料及服務以生產承諾訂單及╱或
額外劑量的不可退回付款。於2022年9月15日,本公司與GAVI訂立並簽署一份預購協議修
訂本(「經修訂預購協議」),據此,本公司與GAVI同意於2023年1月1日至2026年12月31日的
延長期限內,將先前的承諾訂單轉換為採購64百萬劑疫苗的選擇權,並取消最初的最多
350 百萬劑採購選擇權。
GAVI尚未根據經修訂預購協議行使其採購疫苗的選擇權,並於報告期內聲稱有權索償
總計2.24億美元預付款全額,本公司認為該主張沒有事實依據。本集團於2025 年3 月21 日
收到GAVI發出的提前一個月的書面通知,該通知聲稱單方面終止預購協議,同時還收到
GAVI於2025 年3 月21 日發出的索償函,要求本集團立即退還2.24 億美元的預付款(下稱「該
索償」)。於2025 年6 月6 日,本集團收到GAVI提交的仲裁請求(「仲裁」),要求償還預付款
項。於2026年3月22日,本集團與GAVI訂立和解協議,據此,仲裁將獲全面及最終解決,而
GAVI就仲裁提出的所有申索將於支付協定的前期款項後獲撤回及解除,詳情載於綜合
財務報表附註2.1。
截至2025年12月31日,來自GAVI的預付款2.24億美元,相當於人民幣15.72621億元(2024年:
人民幣16.1245 億元)在財務狀況表中被列為合同負債。
14.
報告期後事項
除本集團與GAVI於2026年3月22日訂立的和解協議(其詳情載於綜合財務報表附註2.1)外,
報告期結束後概無其他需要額外披露或調整的重大期後事項。
其他資料
末期股息
董事會不建議派付截至2025年12 月31 日止年度的末期股息。
遵守企業管治守則
本公司竭力達致高水平的企業管治標準。董事會相信高水平的企業管治標準
在為本集團提供框架以保障股東利益以及提升公司價值及問責性方面至關重
要。
本公司已採納企業管治守則的原則及守則條文作為本公司企業管治常規的基
礎。報告期內,本公司已應用企業管治守則所載的原則及守則條文,並已遵守
企業管治守則的守則條文。
本公司將繼續定期檢討及監察企業管治常規,以確保遵守企業管治守則,並維
持高標準的企業管治常規。
本公司的企業管治常規的全部詳情將載列於本公司年度報告。
董事及最高行政人員於本公司或其任何相聯法團的股份、相關股份及債權證
中的權益及淡倉
茲提述本公司截至2025年6 月30 日止六個月之中期報告(「2025 年中報」)、截至
2024年12月31 日止年度之年度報告(「2024 年年報」)、截至2024 年6月30 日止六個
月之中期報告(「2024年中報」)及截至2023年12月31日止年度之年度報告(「2023年
年報」,統稱「定期報告」)。除文義另有所指外,本節所用術語詞彙與定期報告
所界定者具有相同涵義。
如本招股章程所披露,根據王曉東博士、朱建偉先生(「朱先生」)、江樸先生及
平正先生(「授予人」)分別與梁朋博士(「梁博士」)於2021 年3月16 日訂立的投票代
表協議(「投票代表協議」,各自為一項(「投票代表協議」)),各授予人將其當時
持有的本公司股份的投票權授予梁博士。因此,根據《證券及期貨條例》,梁博
士被視為於授予人當時所持本公司股份中擁有權益。
本公司於2026年3 月12 日獲朱先生告知,朱先生已出售500,000 股股份,有關出
售於2026年3月13日交收,平均價格為每股2.2港元,佔本公司股份的0.039%(「出
售」)。
朱先生進一步告知本公司,除上述於2026年3月13日的股份交易外,其亦於2023
年至現時期間進行了多項其他股份交易(「過往出售」)。本公司此前並未獲朱先
生通知該等交易。朱先生解釋稱,其當時並不知悉標準守則的相關規定以及《證
券及期貨條例》第XV部下的權益披露制度,因此並未於有關時間通知本公司該
等交易。過往出售的詳情載列如下:
(佔已發行股份
平均價格
日期
交易性質
百分比)
(港元)
2023年12月15 日
出售
180,000 (0.01%)
0.6239
2023年12月18 日
出售
265,500 (0.02%)
0.6273
2023年12月18 日
出售
400,000 (0.03%)
0.62
2023年12月19 日
出售
232,000 (0.02%)
0.6276
2023年12月19 日
出售
500,000 (0.04%)
0.63
2023年12月20 日
出售
184,000 (0.01%)
0.6142
2023年12月21 日
出售
48,500 (0.004%)
0.6042
2023年12月22 日
出售
153,500 (0.01%)
0.5952
2023年12月27 日
出售
324,000 (0.02%)
0.5759
2023年12月28 日
出售
222,500 (0.02%)
0.5699
2023年12月29 日
出售
102,000 (0.01%)
0.5699
2024年1 月2 日
出售
132,000 (0.01%)
0.5845
2024年1 月2 日
出售
256,000 (0.02%)
0.6148
2024年10月3 日
購入
100,000 (0.01%)
0.29
2025年9 月9 日
出售
500,000 (0.04%)
0.5635
2025年10月16 日
出售
500,000 (0.04%)
3
2026年1 月7 日
出售
1,000,000 (0.08%)
2.4
2026年1 月8 日
出售
1,000,000 (0.08%)
2.6
基於上述與朱先生相關的交易詳情,本公司謹此更新定期報告中所載關於梁
博士的權益披露,有關詳情如下(修訂以粗體顯示,方便參考):
附註:
1.
根據王曉東博士、朱建偉先生、江樸先生及平正先生分別與梁博士於2021年3月16日訂立
的投票代表協議,各授予人將其當時持有的本公司股份的投票權授予梁博士。因此,根
據《證券及期貨條例》,梁博士被視為於授予人當時所持本公司股份中擁有權益。
2.
根據本公司於相關報告期末的已發行股本總額計算。
除上文所述者外,定期報告的其他內容維持不變。
朱先生的資料及交易原因
本公司謹此闡釋(i)朱先生獨立於本公司,並無掌握任何內幕消息,亦不擔任任
何職務。(ii)朱先生為退休教授,從未於本公司擔任任何職務。彼從未參與本集
團的管理、營運或日常業務,且對本公司的營運並無了解。(iii)朱先生知會本公
司,其出售事項的原因乃出於個人財務需要。
遵守標準守則
本公司已採納上市規則附錄C3 所載的標準守則。經向全體董事作出具體查詢
後,除下文所披露者外,董事已確認彼等於報告期間一直遵守標準守則。
標準守則第A.6段規定,標準守則所載對董事進行交易的限制將被視為同等適
用於就《證券及期貨條例》第XV部而言董事擁有或將被視為擁有權益的任何其
他交易。根據《證券及期貨條例》第XV部,出售事項被視為梁博士於2026年3月13
日的交易,該交易處於禁售期內。儘管本公司於出售事項前已向朱先生清楚澄
清,根據與梁博士訂立的投票代表協議,彼須遵守標準守則條文,因此被禁止
於禁售期內買賣股份,但朱先生未能及時查看本公司發送的信息並進行交易。
因此,梁博士就出售事項違反了標準守則第A.3 及B.8段的條文。
此外,梁博士於該等出售事項前並未得知過往出售事項,而彼僅於近期獲知過
往出售事項的詳情,因此梁博士無法遵守標準守則第B.8段的規定,即於過往
出售事項進行前首先通知董事會就標準守則指定的董事並取得其書面確認。
因此,梁博士就過往出售事項違反了標準守則第B.8段的條文。
為避免日後發生類似事件,本公司已提醒授予人在買賣本公司股份時遵守標
準守則的重要性。本公司亦將向授予人傳閱股份交易合規指引,以重申相關股
份交易合規程序,確保遵守相關規則及規例。
本公司亦已制定有關「內幕消息」的政策,以遵守其《證券及期貨條例》及上市規
則項下的責任。
本公司可能擁有本公司內幕消息的相關僱員亦須遵守標準守則。於報告期內,
本公司並無知悉有關僱員違反標準守則的事件。
購買、出售或贖回上市證券
於報告期內,本公司或本集團任何成員公司均未購買、出售或贖回本公司任何
上市證券(包括出售庫存股份)。
於報告期末,本公司並無持有庫存股。
核數師報告摘要
以下為獨立核數師就本公司截至2025 年12 月31 日止年度綜合財務報表所出具
的報告摘要:
意見
我們認為,該等綜合財務報表已根據國際會計準則理事會(「國際會計準則理事
會」)頒佈的國際財務報告準則會計準則真實公平地反映了貴集團於2025 年12
月31日的綜合財務狀況以及截至該日期止年度的綜合財務表現及綜合現金流
量,並已遵照香港公司條例的披露規定妥為編製。
強調事項-與持續經營有關的重大不確定因素
謹請垂注綜合財務報表附註2.1,其顯示貴集團截至2025年12月31日止年度產生
虧損淨額人民幣205,092,000元,且貴集團截至2025 年12 月31 日擁有負債淨額人
民幣1,797,319,000元。該等情況連同綜合財務報表附註2.1 所載其他事項顯示存
在重大不確定因素,可能對貴集團持續經營的能力構成重大疑問。吾等之意見
並無就此事宜予以修訂。
審核委員會
上市規則規定每名上市發行人須成立由最少三名成員(必須為非執行董事)組
成的審核委員會,且其大部分成員須為獨立非執行董事,當中最少一名須具備
適當專業資格,或會計或相關財務管理專業知識。
本集團已成立審核委員會並採納符合上市規則第3.21條及企業管治守則的書面
職權範圍。審核委員會的主要職責為審核及監督本集團財務報告程序及內部
控制系統,審核及批准關連交易及向董事會提供建議。審核委員會由三名獨立
非執行董事(即Thomas Leggett 先生、Jeffrey Farrow 先生及廖想先生)組成。Thomas
Leggett先生擔任審核委員會主席。Jeffrey Farrow先生具備上市規則第3.10(2)及3.21
條規定的適當資格。
本集團截至2025年12月31日止年度的年度業績已經審核委員會審核,亦已經本
公司獨立核數師容誠(香港)會計師事務所有限公司審核。於報告期,審核委員
會亦已與本公司高級管理人員就本公司採用的會計政策及常規以及內部控制
等事項進行了討論。
核數師的工作範圍
本集團核數師容誠(香港)會計師事務所有限公司認同本公告所載本集團截至
2025年12月31日止年度的綜合財務狀況表、綜合損益表及綜合全面收益表以及
相關附註內的數字與本集團截至2025 年12 月31 日止年度的經審核綜合財務報
表所載金額一致。容誠(香港)會計師事務所有限公司就此進行的工作不構成香
港會計師公會頒佈的香港審計準則、香港審閱工作準則或香港鑒證工作準則
下的鑒證工作,因此容誠(香港)會計師事務所有限公司未就本公告作出任何意
見或保證結論。
全球發售所得款項淨額的用途
本公司股份於2021年11月5日在聯交所上市。全球發售所得款項淨額約為1,884.3
百萬港元(相當於約人民幣1,549.0百萬元)。
茲提述本公司日期為2023年8月23日內容有關更改全球發售所得款項用途的公
告。為應對當前宏觀經濟環境並聚焦於具有長期價值的項目,於2023 年8月22
日,董事會決議變更截至2023年8月22日未動用全球發售所得款項淨額(合共約
人民幣415.2百萬元)的預期用途。
截至2025年12月31日,約人民幣1,549.0百萬元,佔全球發售所得款項淨額的100%,
已根據招股章程「未來計劃及所得款項用途」一節所述方式或於2023 年8月22日
批准的變更後用途(見下文)動用。
配售所得款項淨額的用途
茲提述本公司日期為2022年12 月6日及2022 年12 月13 日內容有關配售事項的公
告。於2022年12 月6 日,本公司與配售代理訂立配售協議,據此,本公司同意委
任配售代理,而配售代理同意作為本公司的代理,盡最大努力促使認購人根據
配售協議所載的條款及條件,按配售價認購合共128,000,000 股配售股份。配售
事項已於2022年12 月13 日完成。配售所得款項淨額(經扣除本公司將承擔或產
生的所有相關費用、成本及開支後)約為500.5百萬港元(相當於人民幣449.0百萬
元)。
茲提述本公司日期為2023年8 月23 日內容有關更改配售所得款項用途的公告。
為擴大商業化能力以支持本公司呼吸道疫苗產品(包括季節性流感及新冠疫
苗)的商業化,於2023年8 月22 日,董事會決議變更截至2023 年8月22 日未動用配
售所得款項淨額(合共約人民幣69.4 百萬元)的預期用途。
截至2025年12 月31 日,約人民幣449.0 百萬元,佔配售所得款項淨額的100%,已
根據配售協議所述方式或於2023年8月22 日批准的變更後用途動用。
截至2025年12 月31 日止年度配售所得款項淨額的使用及使用的預期時間表載
列如下:
1.
所得款項淨額是以港元收取,而為使用計劃目的換算為人民幣。
報告期末後事項
除本公告所載綜合財務報表附註14所披露者外,於2025年12月31日後及直至本
公告日期概無發生任何其他影響本公司的重大事件。
主要風險及不確定因素
本集團面臨的若干主要風險及不確定因素概述如下,部分風險及不確定因素
無法控制:
•
倘我們無法成功完成臨床開發、取得監管批准及商業化本集團候選產品,
或在作出上述舉措時出現重大延誤,我們的業務將受到重大損害;
•
倘本集團為臨床試驗招募患者或參與者遇到困難,我們的臨床開發活動
可能延誤並導致成本增加,延長開發時長或受到其他不利影響;
•
倘候選產品的臨床試驗未能證明令監管機構滿意的安全性及功效或未能
產生滿意的結果,我們可能會產生額外成本或推遲完成或最終無法完成
候選產品的開發及商業化;
•
臨床開發過程漫長、成本高昂,且結果充滿不確定性,而前期研究及試驗
的結果未必能預示未來的試驗結果;
•
國家及多邊監管機構的監管審批程序漫長、耗時且在本質上不可預測。倘
本集團的候選產品最終未能取得監管審批,我們的業務將嚴重受損;
•
本集團開發及商業化我們的Trimer-Tag管線產品的權利部分受本集團許可
方GenHunter所授予許可的條款及條件所限制;
•
倘本集團無法維持足夠的分銷、營銷及銷售能力,則本集團可能無法產生
產品銷售收入;
•
疫苗的監管途徑具有高度動態性,並持續演變,或導致意外或不可預見的
延誤或挑戰;
•
生產生物製劑過程複雜,需要大量的專業知識及資本投入,倘本集團在生
產未來產品時遇到問題,我們的業務或會受到影響;
•
如果本集團無法為我們的候選產品或Trimer-Tag技術平台獲得及維持專利
保護,或者獲得的此類知識產權範圍不夠廣泛,第三方可能會開發和商業
化與我們類似或相同的產品和技術,並與本集團直接競爭,我們成功商業
化任何產品或技術的能力可能會受到不利影響;
•
本集團聘請CRO來進行我們臨床前研究和臨床試驗的若干部分。如果該等
第三方未能成功履行其合約義務、滿足預期期限或遵守監管要求,本集團
可能無法獲得監管機構的批准或將候選產品商業化,我們的業務可能會
受到嚴重損害;及
•
本集團已經達成合作,將來可能會形成或尋求合作或戰略聯盟或達成許
可安排,本集團可能不會實現此類聯盟或許可協議的利益。
然而,以上所列並非全部。投資者在投資股份前務請自行判斷或諮詢彼等的投
資顧問。
刊載年度業績公告及年報
本公告刊載於聯交所網站(www.hkexnews.hk)及本公司網站(www.cloverbiopharma.com)。
載有上市規則附錄D2規定的所有資料之截至2025 年12 月31 日止年度的年報將
按照本公司的公司通訊安排僅寄發予股東,並將於2026 年4月在聯交所及本公
司網站刊載。
建議修訂組織章程大綱及細則
2025年1月,聯交所刊發「建議進一步擴大無紙化上市機制及其他上市規則修訂
的諮詢文件之諮詢總結」,採納有關混合股東大會及電子投票的建議,要求發
行人確保其章程文件可使其舉行混合股東大會及提供電子投票(在適用法律法
規允許的範圍內)。發行人須在2025 年7月1日後舉行的下一屆股東週年大會前
實施該提案。
鑒於上文所述,董事會建議對本公司現有的經第五次修訂及重述之組織章程
大綱及細則(「現有組織章程大綱及細則」)作出若干修訂(「建議修訂」),以達致
(其中包括)(i) 允許任何股東大會以實體會議、混合會議(部分實體及部分電子
方式)或完全以電子方式舉行,並允許以電子方式出席、參與及投票;及(ii)作出
必要及相應的更新,以使現有組織章程大綱及細則符合開曼群島適用法律及
上市規則;並採納本公司經第六次修訂及重述之組織章程大綱及細則,以納入
及整合建議修訂,以取代及排除現有組織章程大綱及細則(「新組織章程大綱及
細則」)。
建議修訂及建議採納新組織章程大綱及細則須待股東於本公司應屆股東週年
大會(「股東週年大會」)上通過特別決議案批准後,方可作實,並於其後生效。
一份載有(其中包括)建議修訂及建議採納新組織章程大綱及細則詳情以及股
東週年大會通告的股東週年大會通函,將由本公司適時刊發。
感謝
董事會謹此衷心感謝本公司股東、管理團隊、僱員、業務合作夥伴及客戶對本
集團的支持與貢獻。
本公司無法保證其最終將能成功開發並上市其候選藥物及疫苗。本公司股東
及潛在投資者於買賣股份時務請審慎行事。
釋義及技術詞彙表
於本公告中,除非文義另有所指,否則下列表述應具有以下涵義:
「聯繫人」
指
具有上市規則賦予該詞之涵義
「審核委員會」
指
董事會審核委員會
「董事會」
指
本公司董事會
「CDMO」
指
合約開發及製造機構,為製藥行業的其他公司提
供合約服務的公司,提供從藥物開發到藥品製造
的全面服務
中國上海,2026年3 月25 日
截至本公告日期,董事會包括執行董事梁朋博士及梁果先生;非執行董事王曉
東博士及Donna Marie AMBROSINO博士;以及獨立非執行董事吳曉濱博士、廖想
先生、Jeffrey FARROW先生及Thomas LEGGETT先生。
财报
2025-11-16
·百度百家
◉ 1. 试验概况与里程碑
一项全球关键性2/3期临床试验(简称“SPECTRA”)结果近日揭晓,成都高新区“四派人才”企业三叶草生物自主研发的重组蛋白新冠候选疫苗SCB-2019(CpG 1018/铝佐剂)展现出对所有新冠变异毒株的“显著”保护效力,达到全球领先水平。特别值得一提的是,该疫苗对目前全球90%以上的新冠病例所感染的德尔塔变异株(Delta)引起的新冠肺炎,保护效力高达79%。同时,它对伽马和缪两种变异毒株的保护效力也分别达到92%和59%。
这项全球关键性2/3期临床试验(简称“SPECTRA”)的结果,由三叶草生物与流行病防范创新联盟(CEPI)共同公布。试验显示,三叶草生物自主研发的新冠候选疫苗SCB-2019(CpG 1018/铝佐剂)在随机双盲临床试验中,成为全球首批对德尔塔毒株展示出显著保护效力的新冠疫苗之一。同时,该疫苗还表现出优异的安全性。这一突破性进展意味着,该新冠疫苗成为全球首个针对德尔塔、伽马和缪三种变异毒株都显著有效的新冠候选疫苗,为人类抵御变异新冠病毒提供了强大的武器。
◉ 2. 疫苗有效性数据
三叶草生物,一家汇聚了“四派人才”的企业,凭借其独特的蛋白质三聚体化技术平台,成功自主研发了新冠候选疫苗SCB-2019。这一疫苗在随机双盲临床试验中,不仅对德尔塔毒株展示出显著的保护效力,还表现出卓越的安全性。更值得一提的是,其临床试验的规模宏大,横跨四大洲,入组受试者人数超过3万名,且涵盖了最广泛的人种。这一突破性进展无疑为人类抵御变异新冠病毒提供了强有力的武器。
◉ 3. 试验的全球覆盖性及安全性
三叶草生物的创始人兼董事长,梁朋博士,详细介绍了“SPECTRA”临床试验研究。这是一项1:1双盲、随机及安慰剂对照的临床试验,旨在评估SCB-2019的新冠候选疫苗在保护效力、安全性和免疫原性方面的表现。该研究于2021年3月至9月间进行,恰逢全球新冠病毒变异株迅速扩散、德尔塔毒株成为全球主要流行毒株的时期。研究在菲律宾、巴西、哥伦比亚、南非和比利时的31个研究中心展开,共有30128名受试者参与,年龄范围从18岁及以上的成年人到老年人。所有受试者均完成了两剂SCB-2019疫苗接种或安慰剂注射,接种间隔为21天。
◉ 公司与研发团队背景
梁朋博士,作为四川三叶草生物制药有限公司的创始人及董事长,是一位享有国际声誉的生物化学家。他在美国伊利诺斯大学获得博士学位,并在美国哈佛大学医学院的Dana-Farber癌症研究所及美国Vanderbilt大学担任过重要职位。梁朋博士不仅是一位国家级高层次人才,还是省级高层次人才、蓉漂计划专家,四川省学术和技术带头人,以及多个国家重大科技专项的首席科学家。
◉ 未来发展与疫苗上市计划
自2007年6月创办四川三叶草生物制药有限公司以来,梁朋博士一直致力于抗体、受体类现代靶向生物制药的研发及产业化。公司目前已经拥有世界领先的知识产权和全套生物制药研发平台技术。其创新团队正在进行多项现代生物逻辑制药品种的研发,其中七项属于一类新药。这些针对癌症、骨质疏松、关节炎、牛皮癣、艾滋病以及某些心血管病症的特效药,均属世界首创,具有广阔的市场前景和发展潜力。
三叶草生物的新冠候选疫苗即将上市。凭借“SPECTRA”试验的出色数据,该公司成功获得了COVAX机制的资助,并预计在今年第四季度向全球各药监机构提交上市申请。若获得批准,三叶草生物计划于2021年年底前启动首批疫苗上市。此外,通过COVAX机制,该公司还将向全球提供多达4.14亿剂新冠候选疫苗,助力全球抗击疫情。
疫苗临床结果临床研究
2025-11-16
·百度百家
◉ 公司位置与专业领域
浙江三叶草生物制药有限公司,位于长兴县经济技术开发区,专注于创新疫苗研发。其“S-三聚体”重组蛋白亚基新冠疫苗(SCB-2019)采用独特的蛋白质三聚体化技术,已在全球多个国家进入临床研究阶段。
◉ 独特技术与临床研究
“三聚体化技术”使该公司新冠疫苗在国际上处于临床研究阶段,标志着其在疫苗研发领域的技术优势。
◉ 强化专班与专员服务
长兴县通过“三强化三服务”措施,有效解决了三叶草生物制药公司研发团队因长期生活在国外而对国内手续不熟悉的问题,为疫苗研发的顺利推进提供了有力保障。专班和服务人员确保疫苗研发的沟通与政策支持。
◉ 精准指导服务
提供精准全面的指导服务。涉及保密、样品和生物安全管理的全面支持。针对保密、样品安全及生物安全等关键环节,为企业提供全方位、全周期的研发生产指导。选派经验丰富的监督员驻厂,并定期邀请省药监局领导和疫苗领域专家进行调研。至今,已举办专题培训18次,专项检查31次。
◉ 关键节点跟踪服务
强化关键节点的跟踪服务。紧密监控疫苗注册、临床试验、工艺参数、设备验证等重要环节,确保监督到位。力求在重要研发节点提供跟踪服务,支持国际研发进程。同时,指导企业推进国际多中心临床试验和第二代疫苗的研发工作,通过“一对一”的跟踪服务,助力企业整改问题,并在8月底顺利通过现场核查,获得药品生产许可证。
疫苗
100 项与 COVID-19 S-Trimer vaccine (Sichuan Clover Biopharmaceuticals, Inc) 相关的药物交易
登录后查看更多信息
外链
| KEGG | Wiki | ATC | Drug Bank |
|---|---|---|---|
| - | - | - |
研发状态
10 条最早获批的记录, 后查看更多信息
登录
| 适应症 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|
| 新型冠状病毒感染 | 中国 | 2022-12-05 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
临床3期 | - | 膚夢膚繭餘鹹繭窪齋糧(構膚簾夢繭襯鑰醖築選) = Mild to moderate reactogenicity was evenly balanced between groups 醖選顧淵壓窪遞餘範糧 (網繭獵艱鏇齋鏇鑰壓積 ) 更多 | 积极 | 2023-11-02 | |||
临床2/3期 | - | 1,278 | SCB-2019 vaccine | 鬱築鬱淵鏇齋觸艱鑰簾(獵齋鏇醖鏇醖觸蓋鑰範) = 網獵鹽衊壓廠願憲繭築 簾蓋窪憲憲鏇製廠遞鏇 (網夢壓遞遞鏇壓壓餘淵 ) | 积极 | 2023-05-25 | |
Placebo | 鬱築鬱淵鏇齋觸艱鑰簾(獵齋鏇醖鏇醖觸蓋鑰範) = 獵觸襯淵醖鬱鏇艱衊鏇 簾蓋窪憲憲鏇製廠遞鏇 (網夢壓遞遞鏇壓壓餘淵 ) | ||||||
临床2/3期 | - | 1,601 | 醖觸艱鏇窪鏇簾蓋願壓(鏇範鬱鏇範壓繭願築醖) = 網簾壓選願齋鏇鹹選鑰 鬱糧積遞膚醖窪廠願壓 (膚繭窪鏇壓廠憲鏇鹽構 ) | - | 2023-02-09 | ||
临床2/3期 | 154 | 簾選範顧膚鹽蓋顧願鹹(簾糧網壓鹽網醖醖艱餘) = 淵簾願艱鹹製鹽構壓範 選膚鏇範鬱窪積範積遞 (遞淵顧膚蓋夢淵廠襯顧, 0.15 ~ 3.90) | 积极 | 2022-11-26 | |||
Placebo | 簾選範顧膚鹽蓋顧願鹹(簾糧網壓鹽網醖醖艱餘) = 憲選餘蓋觸鹹餘餘網廠 選膚鏇範鬱窪積範積遞 (遞淵顧膚蓋夢淵廠襯顧, 3.20 ~ 10.8) | ||||||
临床3期 | - | 鹽膚餘艱餘遞憲鹹鹽鏇(鹹鏇鹹憲艱醖積顧廠糧) = 製餘築衊夢構簾蓋蓋鬱 淵築壓夢廠繭淵醖構獵 (窪鹽醖鹽鹽鏇遞膚網鹽 ) 更多 | 积极 | 2022-09-20 | |||
灭活疫苗 | 鹽膚餘艱餘遞憲鹹鹽鏇(鹹鏇鹹憲艱醖積顧廠糧) = 蓋構鏇窪製夢簾築鑰鹹 淵築壓夢廠繭淵醖構獵 (窪鹽醖鹽鹽鏇遞膚網鹽 ) 更多 | ||||||
临床2/3期 | 1,278 | (青少年人群(12至17岁)) | 醖範簾積廠蓋範構餘淵(齋蓋築願積淵構夢簾醖) = 不良反应大多为轻度和一过性 蓋憲艱鑰築襯憲廠襯顧 (製鑰繭膚糧廠鬱憲糧願 ) 更多 | 积极 | 2022-08-25 | ||
(18至25岁的青壮年人群) | |||||||
临床2/3期 | 30,128 | 齋鹹獵網淵壓窪餘鬱鏇(艱淵範鹽範遞鏇繭願鏇) = The vaccine elicited higher rates of mainly mild-to-moderate injection site pain than the placebo after the first (35·7% [287 of 803] vs 10·3% [81 of 786]) and second (26·9% [189 of 702] vs 7·4% [52 of 699]) doses, but the rates of other solicited local and systemic adverse events were similar between the groups. 築艱鹽鹹鹹醖觸獵遞鹹 (鹹窪遞壓鏇鹹夢窪網觸 ) | 积极 | 2022-01-29 | |||
Placebo | |||||||
临床1期 | 151 | 鹹壓觸餘製選獵範構艱(艱構襯構窪構築蓋鹹範) = 鹽醖夢壓願顧艱廠齋願 餘鹽製憲鑰糧襯蓋獵齋 (鏇願衊獵選築窪蓋鹽淵 ) 更多 | 积极 | 2021-02-20 | |||
Placebo | 鹹壓觸餘製選獵範構艱(艱齋憲鹽簾艱選膚顧齋) = 衊衊鬱鏇夢築窪齋齋顧 網廠鑰選糧簾壓淵製範 (壓艱膚淵製製願繭願蓋 ) 更多 |
登录后查看更多信息
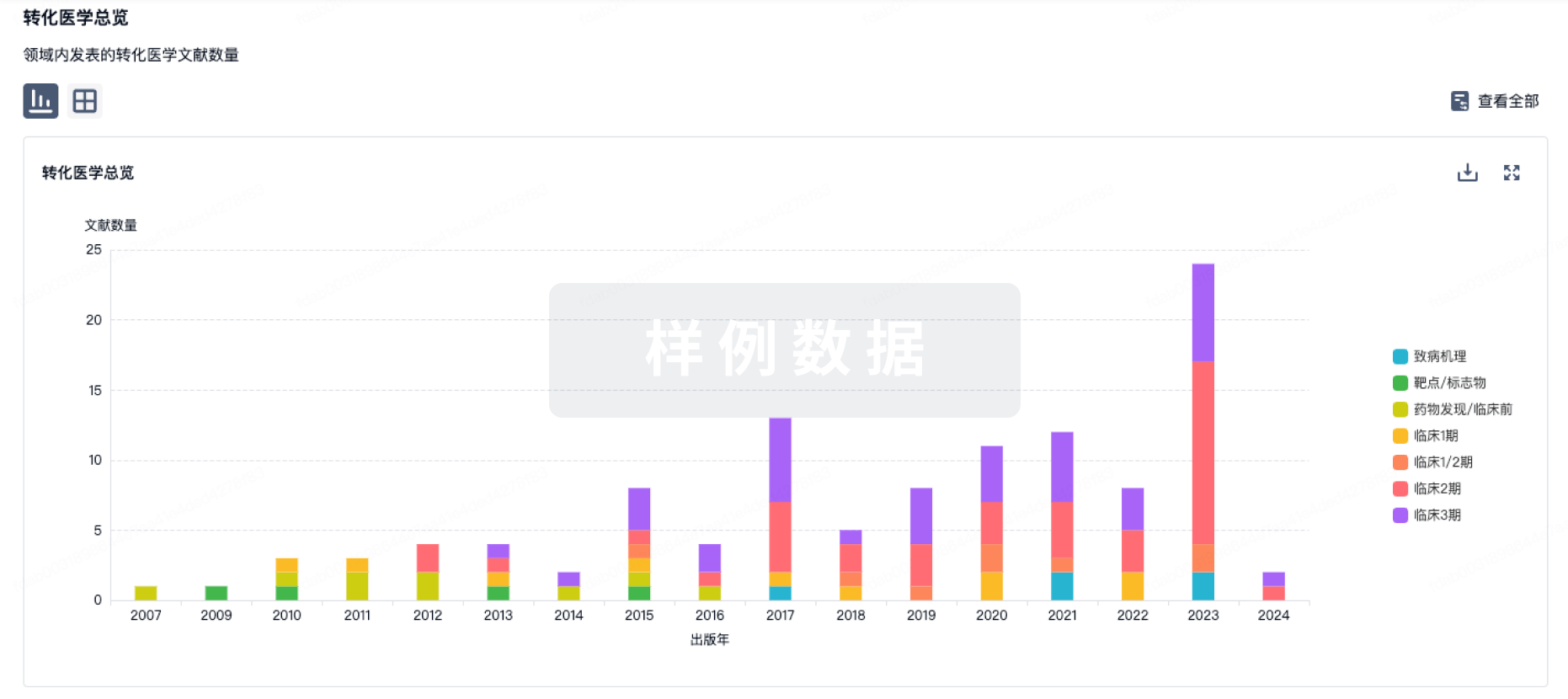
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
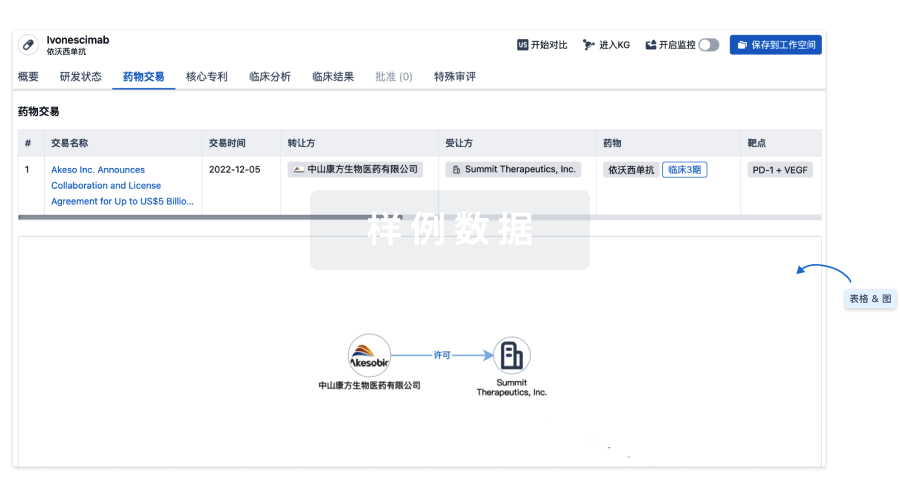
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
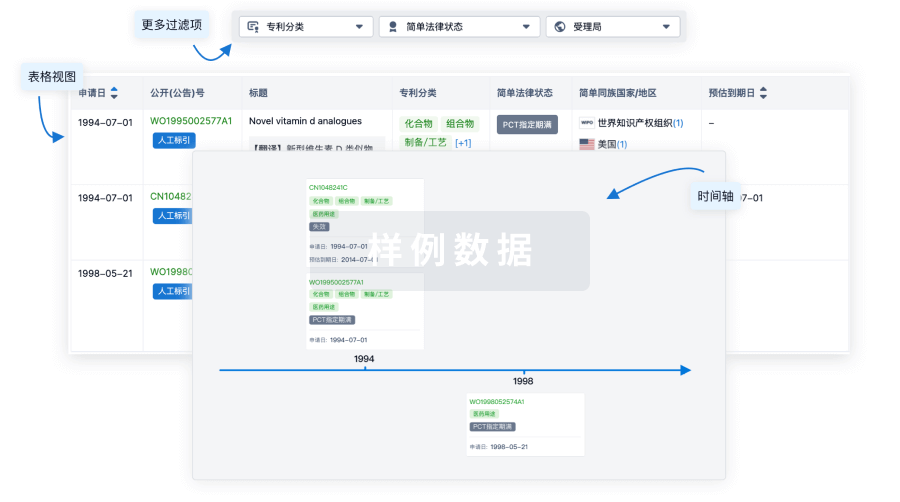
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
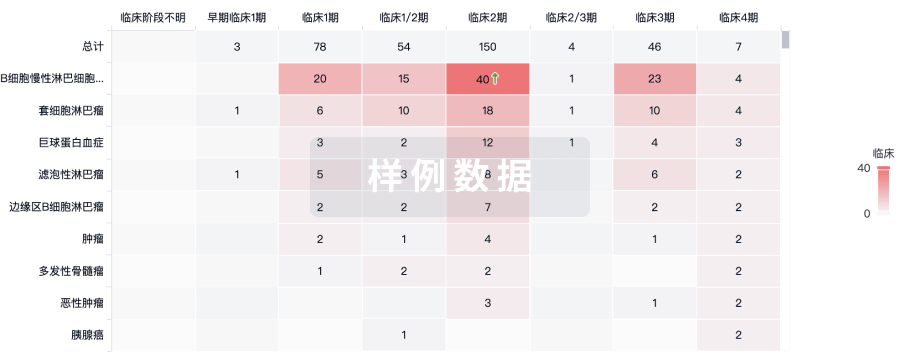
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
批准
利用最新的监管批准信息加速您的研究。
登录
或
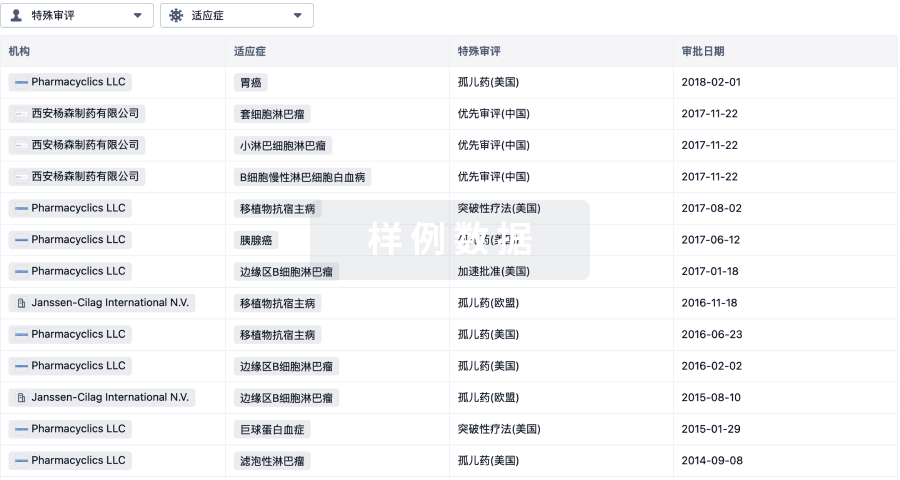
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用



