预约演示
更新于:2026-06-09

Sichuan Clover Biopharmaceuticals, Inc
更新于:2026-06-09
概览
标签
感染
呼吸系统疾病
肿瘤
预防性疫苗
Fc融合蛋白
肿瘤坏死因子
疾病领域得分
一眼洞穿机构专注的疾病领域
暂无数据
技术平台
公司药物应用最多的技术
暂无数据
靶点
公司最常开发的靶点
暂无数据
| 排名前五的药物类型 | 数量 |
|---|---|
| 预防性疫苗 | 8 |
| 重组亚单位疫苗 | 2 |
| Fc融合蛋白 | 1 |
| 重组蛋白 | 1 |
| 融合蛋白 | 1 |
关联
11
项与 四川三叶草生物制药有限公司 相关的药物作用机制 SARS-CoV-2 S protein调节剂 [+1] |
在研机构 |
原研机构 |
在研适应症 |
非在研适应症- |
最高研发阶段批准上市 |
首次获批国家/地区 中国 |
首次获批日期2022-12-05 |
作用机制 TPO receptor激动剂 |
在研机构 |
原研机构 |
非在研适应症- |
最高研发阶段临床1期 |
首次获批国家/地区- |
首次获批日期- |
作用机制 Respiratory syncytial virus F protein调节剂 |
在研机构 |
原研机构 |
在研适应症 |
非在研适应症- |
最高研发阶段临床1期 |
首次获批国家/地区- |
首次获批日期- |
11
项与 四川三叶草生物制药有限公司 相关的临床试验NCT05426369
A Phase I Clinical Study to Evaluate the Safety, Tolerability, Immunogenicity, Preliminary Efficacy and Pharmacokinetics of SCB-219M in the Patients With Chemotherapy-induced Thrombocytopenia
A Phase I Clinical Study to Evaluate the Safety, Tolerability, Immunogenicity, Preliminary Efficacy and Pharmacokinetics of SCB-219M in the patients with chemotherapy-induced thrombocytopenia (CIT)
开始日期2022-06-14 |
申办/合作机构 |
CTR20220602
评价SCB-219M 用于肿瘤化疗相关性血小板减少症(CIT)的安全性、耐受性、免疫原性、初步疗效和药代动力学的I 期临床试验
剂量递增阶段主要目的: 评估 SCB-219M 单次皮下注射的安全性和耐受性; 探索 SCB-219M 单次皮下注射的最大耐受剂量(MTD)及生物有效剂量(BED); 次要目的: 评估 SCB-219M 单次皮下注射的药代动力学(PK)特征; 评估 SCB-219M 单次皮下注射的免疫原性; 评估 SCB-219M 单次皮下注射后用于 CIT 的初步疗效。 剂量拓展阶段主要目的:
评估 SCB-219M 多次皮下注射的安全性和耐受性; 次要目的: 评估 SCB-219M 多次皮下注射的 PK 特征; 评估 SCB-219M 多次皮下注射的免疫原性; 评估 SCB-219M 每周一次和每两周一次皮下注射给药后用于 CIT 的初步疗效; 比较 SCB-219M 每周一次与每两周一次皮下注射给药用于 CIT 的初步疗效。
开始日期2022-06-10 |
申办/合作机构 |
NCT04954131
A Multi-center, Double-blind, Randomized, Controlled, Phase 2 Study to Evaluate the Immunogenicity and Safety of CpG 1018/Alum-adjuvanted Recombinant SARS-CoV-2 Trimeric S-protein Subunit Vaccine (SCB-2019) in Individuals Aged 18 Years and Older in China
The purpose of this clinical study, CLO-SCB-2019-010, is to assess the immunogenicity, reactogenicity and safety of the SCB-2019 vaccine in Chinese participants, and to show the comparability of the immune response versus randomly selected individuals who participated in the large-scale efficacy study with the SCB-2019 vaccine (Study CLO-SCB-2019-003).
开始日期2021-08-10 |
申办/合作机构 |
100 项与 四川三叶草生物制药有限公司 相关的临床结果
登录后查看更多信息
0 项与 四川三叶草生物制药有限公司 相关的专利(医药)
登录后查看更多信息
2,494
项与 四川三叶草生物制药有限公司 相关的新闻(医药)13 小时之前
·医药笔记
▎Armstrong
2026年6月8日,Incyte宣布以12.5亿美元预付款及7.5亿美元里程碑金额收购Vega Therapeutics。
Vega Therapeutics的核心管线VGA-39为一款Protein S调节剂,通过调控TFPI和aPC两条通路,让凝血酶产生过程正常化,同时不会驱动过度的凝血。
VGA039的资料可以让VWD患者年化出血率显著下降,全人群减少幅度为81%。
2029年初将读出三期临床顶线数据,预计销售峰值超过10亿美元。
VWD目前标准疗法需要每周静脉注射2-3次,VGA039仅需要每个月一次皮下注射。
GA039有望成为VWD的新标准疗法。
总结
新机制抗体疗法正在深刻改变凝血障碍疾病的治疗格局,FIX/FX双抗成为A型血友病的标准疗法,VGA039也有望彻底改变VWD的治疗格局。Hemlibra年销售额超过60亿美元,VGA039销售峰值也有望超过10亿美元。
Armstrong技术全梳理系列
GPRC5D靶点全梳理;
CD40靶点全梳理;
CD47靶点全梳理;
补体靶向药物技术全梳理;
补体药物:眼科治疗的重要方向;
Claudin 6靶点全梳理;
Claudin 18.2靶点全梳理;
靶点冷暖,行业自知;
中国大分子新药研发格局;
被炮轰的“me too”;
佐剂百年史;
胰岛素百年传奇;
CUSBEA:风雨四十载;
中国新药研发的焦虑;
中国生物医药企业的研发竞争;
中国双抗竞争格局;
中国ADC竞争格局;
中国双抗技术全梳理;
中国ADC技术全梳理;
Ambrx技术全梳理;
Vir Biotech技术全梳理;
Immune-Onc技术全梳理;
亘喜生物技术全梳理;
康哲药业技术全梳理;
科济药业技术全梳理;
恺佧生物技术全梳理;
同宜医药技术全梳理;
百奥赛图技术全梳理;
腾盛博药技术全梳理;
创胜集团技术全梳理;
永泰生物技术全梳理;
中国抗体技术全梳理;
德琪医药技术全梳理;
德琪医药技术全梳理2.0;
和铂医药技术全梳理;
荣昌生物技术全梳理;
再鼎医药技术全梳理;
药明生物技术全梳理;
恒瑞医药技术全梳理;
豪森药业技术全梳理;
正大天晴技术全梳理;
吉凯基因技术全梳理;
基石药业技术全梳理;
百济神州技术全梳理;
百济神州技术全梳理第2版;
信达生物技术全梳理;
信达生物技术全梳理第2版;
中山康方技术全梳理;
复宏汉霖技术全梳理;
先声药业技术全梳理;
君实生物技术全梳理;
嘉和生物技术全梳理;
志道生物技术全梳理;
道尔生物技术全梳理;
尚健生物技术全梳理;
康宁杰瑞技术全梳理;
科望医药技术全梳理;
岸迈生物技术全梳理;
礼进生物技术全梳理;
康桥资本技术全梳理;
余国良的抗体药布局;
荃信生物技术全梳理;
安源医药技术全梳理;
三生国健技术全梳理;
仁会生物技术全梳理;
乐普生物技术全梳理;
同润生物技术全梳理;
宜明昂科技术全梳理;
派格生物技术全梳理;
迈威生物技术全梳理;
Momenta技术全梳理;
NGM技术全梳理;
普米斯生物技术全梳理;
普米斯生物技术全梳理2.0;
三叶草生物技术全梳理;
贝达药业抗体药全梳理;
泽璟制药抗体药全梳理;
恒瑞医药抗体药全梳理;
齐鲁制药抗体药全梳理;
石药集团抗体药全梳理;
豪森药业抗体药全梳理;
华海药业抗体药全梳理;
科伦药业抗体药全梳理;
百奥泰技术全梳理;
凡恩世技术全梳理。
16 小时之前
·医药笔记
▎Armstrong
2026年6月8日,Nurix Therapeutics宣布与罗氏就BTK降解剂Bexobrutideg达成合作开发协议,开发成本罗氏与Nurix分别负担60%、40%,美国商业权益共担,美国之外的商业权益归罗氏所有,Nurix获得百分之十几的销售分成。根据协议,罗氏支付7亿美元预付款,交易总金额高达23亿美元。
受此消息影响,Nurix Therapeutics股价盘前大涨52%,目前市值超过22亿美元。
Bexobrutideg为Nurix Therapeutics的核心管线,B细胞恶性肿瘤处于关键临床阶段,自免适应症正在探索中。
Bexobrutideg具有成为BIC的潜力,在难治性B细胞恶性肿瘤中表现出优异疗效,r/r CLL的1a期临床中ORR为83.0%,mPFS长达22.1个月。
Bexobrutideg对于自免疾病也有很好的应用潜力。
总结
Nurix Therapeutics还在探索将BTK降解剂用于构建DAC,并与辉瑞达成34亿美元合作开发协议。
Armstrong技术全梳理系列
GPRC5D靶点全梳理;
CD40靶点全梳理;
CD47靶点全梳理;
补体靶向药物技术全梳理;
补体药物:眼科治疗的重要方向;
Claudin 6靶点全梳理;
Claudin 18.2靶点全梳理;
靶点冷暖,行业自知;
中国大分子新药研发格局;
被炮轰的“me too”;
佐剂百年史;
胰岛素百年传奇;
CUSBEA:风雨四十载;
中国新药研发的焦虑;
中国生物医药企业的研发竞争;
中国双抗竞争格局;
中国ADC竞争格局;
中国双抗技术全梳理;
中国ADC技术全梳理;
Ambrx技术全梳理;
Vir Biotech技术全梳理;
Immune-Onc技术全梳理;
亘喜生物技术全梳理;
康哲药业技术全梳理;
科济药业技术全梳理;
恺佧生物技术全梳理;
同宜医药技术全梳理;
百奥赛图技术全梳理;
腾盛博药技术全梳理;
创胜集团技术全梳理;
永泰生物技术全梳理;
中国抗体技术全梳理;
德琪医药技术全梳理;
德琪医药技术全梳理2.0;
和铂医药技术全梳理;
荣昌生物技术全梳理;
再鼎医药技术全梳理;
药明生物技术全梳理;
恒瑞医药技术全梳理;
豪森药业技术全梳理;
正大天晴技术全梳理;
吉凯基因技术全梳理;
基石药业技术全梳理;
百济神州技术全梳理;
百济神州技术全梳理第2版;
信达生物技术全梳理;
信达生物技术全梳理第2版;
中山康方技术全梳理;
复宏汉霖技术全梳理;
先声药业技术全梳理;
君实生物技术全梳理;
嘉和生物技术全梳理;
志道生物技术全梳理;
道尔生物技术全梳理;
尚健生物技术全梳理;
康宁杰瑞技术全梳理;
科望医药技术全梳理;
岸迈生物技术全梳理;
礼进生物技术全梳理;
康桥资本技术全梳理;
余国良的抗体药布局;
荃信生物技术全梳理;
安源医药技术全梳理;
三生国健技术全梳理;
仁会生物技术全梳理;
乐普生物技术全梳理;
同润生物技术全梳理;
宜明昂科技术全梳理;
派格生物技术全梳理;
迈威生物技术全梳理;
Momenta技术全梳理;
NGM技术全梳理;
普米斯生物技术全梳理;
普米斯生物技术全梳理2.0;
三叶草生物技术全梳理;
贝达药业抗体药全梳理;
泽璟制药抗体药全梳理;
恒瑞医药抗体药全梳理;
齐鲁制药抗体药全梳理;
石药集团抗体药全梳理;
豪森药业抗体药全梳理;
华海药业抗体药全梳理;
科伦药业抗体药全梳理;
百奥泰技术全梳理;
凡恩世技术全梳理。
2026-06-08
·医药笔记
▎Armstrong
2026年6月7日,诺和诺德宣布口服司美格鲁肽减重版Wegovy pill处方量超过300万张,平均5秒开出一张处方。今年1月5日,Wegovy pill在美国上市销售,12周即突破100万张处方。从3月23日到6月1日的10周时间里面,Wegovy pill又开出200万张处方。
口服版的上市,助力司美格鲁肽在减重市场反超替尔泊肽,重回第一的位置。Wegovy pill上市后快速放量,每周处方量已经超过22.5万张,并仍处于快速增长阶段。
诺和诺德围绕减重进行了广泛布局,后续产品管线包括Zenagamtide(GLP-1/Amylin)、UBT251(GLP-1/GIP/GCG)、Triple agonist(GLP-1/GIP/Amylin)、Efruxifermin(FGF21)等。
总结
肥胖人群基数大,口服场景临床需求旺盛,目前主要的竞品为口服司美格鲁肽、礼来的小分子GLP-1受体激动剂Orforglipron。在迭代研发方面,诺和诺德Zenagamtide口服版已经推进到三期临床,礼来则引进了英矽智能每周一次口服小分子GLP-1受体激动剂。
Armstrong技术全梳理系列
GPRC5D靶点全梳理;
CD40靶点全梳理;
CD47靶点全梳理;
补体靶向药物技术全梳理;
补体药物:眼科治疗的重要方向;
Claudin 6靶点全梳理;
Claudin 18.2靶点全梳理;
靶点冷暖,行业自知;
中国大分子新药研发格局;
被炮轰的“me too”;
佐剂百年史;
胰岛素百年传奇;
CUSBEA:风雨四十载;
中国新药研发的焦虑;
中国生物医药企业的研发竞争;
中国双抗竞争格局;
中国ADC竞争格局;
中国双抗技术全梳理;
中国ADC技术全梳理;
Ambrx技术全梳理;
Vir Biotech技术全梳理;
Immune-Onc技术全梳理;
亘喜生物技术全梳理;
康哲药业技术全梳理;
科济药业技术全梳理;
恺佧生物技术全梳理;
同宜医药技术全梳理;
百奥赛图技术全梳理;
腾盛博药技术全梳理;
创胜集团技术全梳理;
永泰生物技术全梳理;
中国抗体技术全梳理;
德琪医药技术全梳理;
德琪医药技术全梳理2.0;
和铂医药技术全梳理;
荣昌生物技术全梳理;
再鼎医药技术全梳理;
药明生物技术全梳理;
恒瑞医药技术全梳理;
豪森药业技术全梳理;
正大天晴技术全梳理;
吉凯基因技术全梳理;
基石药业技术全梳理;
百济神州技术全梳理;
百济神州技术全梳理第2版;
信达生物技术全梳理;
信达生物技术全梳理第2版;
中山康方技术全梳理;
复宏汉霖技术全梳理;
先声药业技术全梳理;
君实生物技术全梳理;
嘉和生物技术全梳理;
志道生物技术全梳理;
道尔生物技术全梳理;
尚健生物技术全梳理;
康宁杰瑞技术全梳理;
科望医药技术全梳理;
岸迈生物技术全梳理;
礼进生物技术全梳理;
康桥资本技术全梳理;
余国良的抗体药布局;
荃信生物技术全梳理;
安源医药技术全梳理;
三生国健技术全梳理;
仁会生物技术全梳理;
乐普生物技术全梳理;
同润生物技术全梳理;
宜明昂科技术全梳理;
派格生物技术全梳理;
迈威生物技术全梳理;
Momenta技术全梳理;
NGM技术全梳理;
普米斯生物技术全梳理;
普米斯生物技术全梳理2.0;
三叶草生物技术全梳理;
贝达药业抗体药全梳理;
泽璟制药抗体药全梳理;
恒瑞医药抗体药全梳理;
齐鲁制药抗体药全梳理;
石药集团抗体药全梳理;
豪森药业抗体药全梳理;
华海药业抗体药全梳理;
科伦药业抗体药全梳理;
百奥泰技术全梳理;
凡恩世技术全梳理。
100 项与 四川三叶草生物制药有限公司 相关的药物交易
登录后查看更多信息
100 项与 四川三叶草生物制药有限公司 相关的转化医学
登录后查看更多信息
组织架构
使用我们的机构树数据加速您的研究。
登录
或

管线布局
2026年06月09日管线快照
管线布局中药物为当前组织机构及其子机构作为药物机构进行统计,早期临床1期并入临床1期,临床1/2期并入临床2期,临床2/3期并入临床3期
药物发现
1
4
临床前
临床申请
1
1
临床申请批准
临床1期
4
1
批准上市
其他
10
登录后查看更多信息
当前项目
登录后查看更多信息
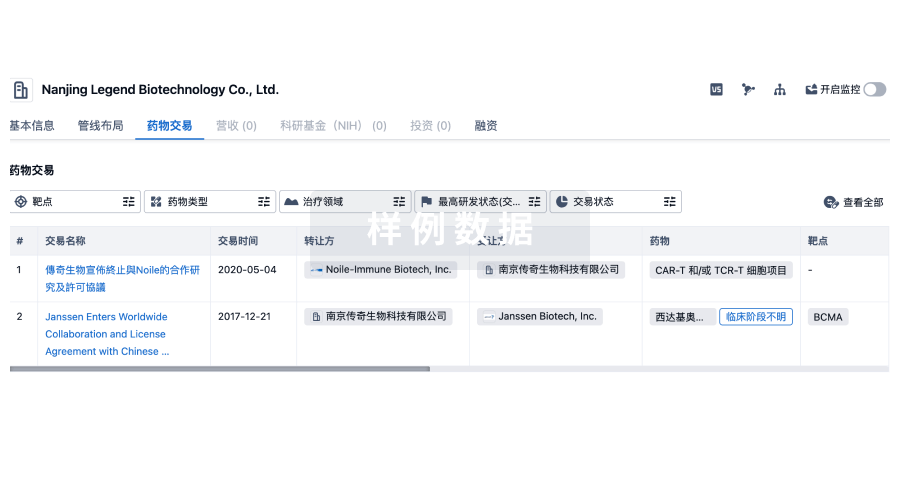
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
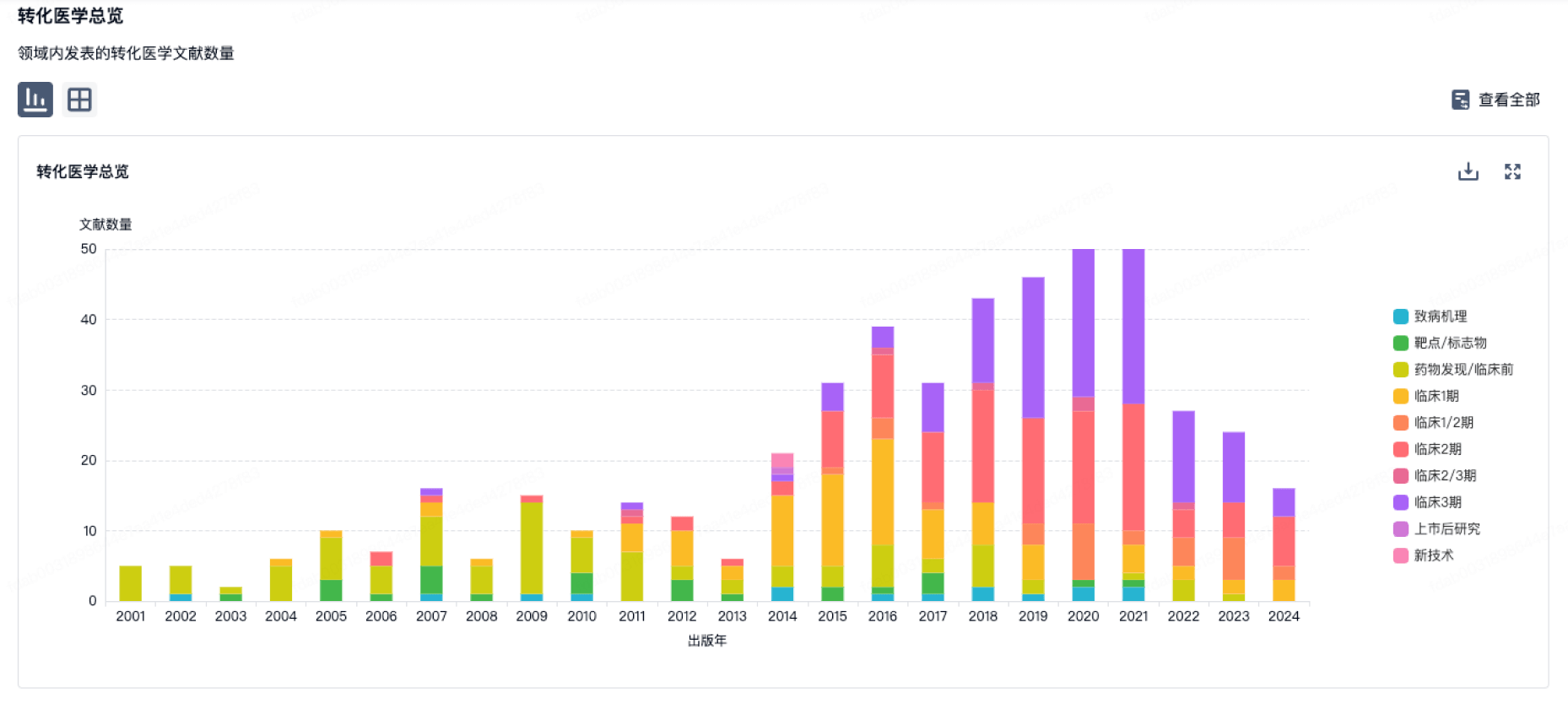
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
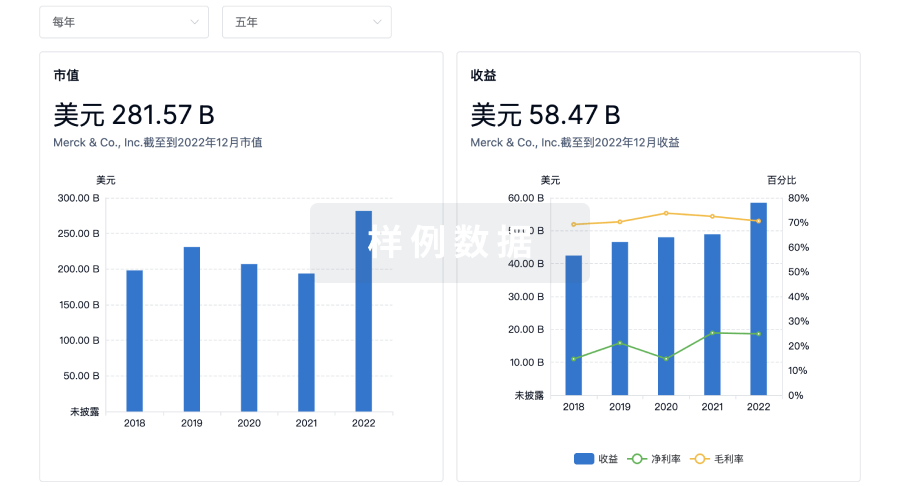
营收
使用 Synapse 探索超过 36 万个组织的财务状况。
登录
或
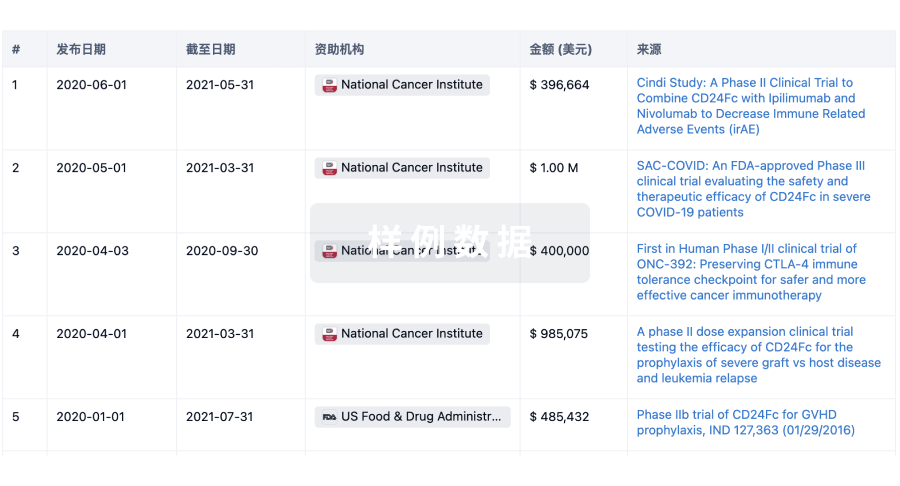
科研基金(NIH)
访问超过 200 万项资助和基金信息,以提升您的研究之旅。
登录
或
投资
深入了解从初创企业到成熟企业的最新公司投资动态。
登录
或
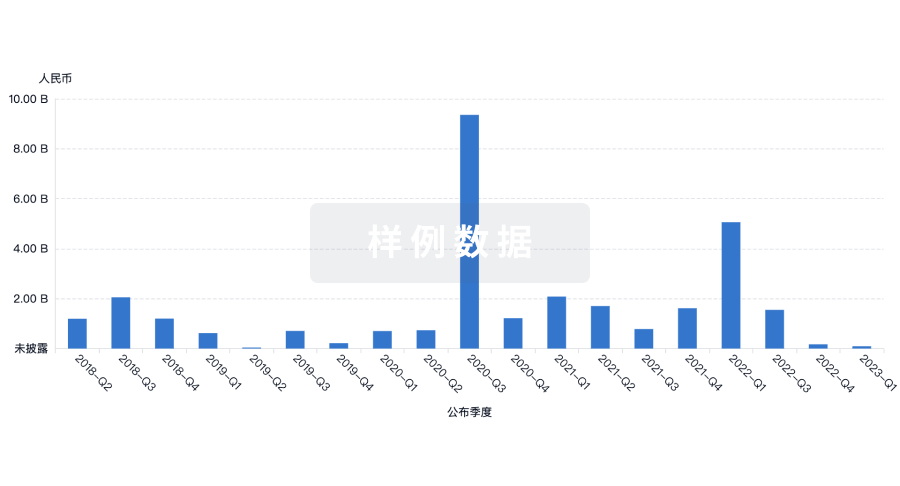
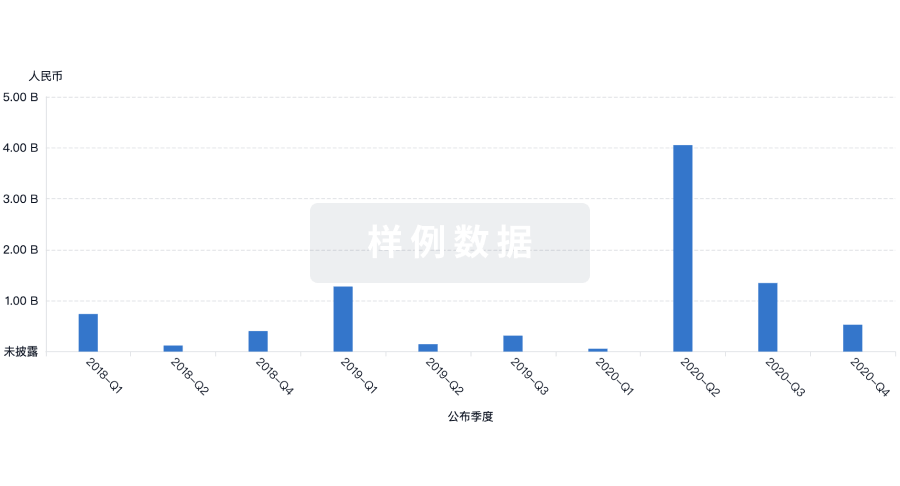
融资
发掘融资趋势以验证和推进您的投资机会。
登录
或
生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用