阿斯利康RSV长效单抗Nirsevimab在华获批上市,用于预防婴幼儿感染
2024年1月2日,阿斯利康宣布其Nirsevimab注射液已获中国国家药品监督管理局批准上市,用于预防新生儿和婴儿由呼吸道合胞病毒(RSV)引起的下呼吸道感染(LRTI)。RSV是引起婴儿下呼吸道感染最常见的病原,包括毛细支气管炎和肺炎。RSV也是导致全球婴儿住院的首要致病因素,且大多数住院发生在健康足月婴儿中。
Nirsevimab是赛诺菲/阿斯利康联合开发的一种针对RSV病毒F蛋白(RSV F protein)融合前构象的长效重组肌内注射中和人源IgG1ĸ单克隆抗体,其Fc结构与的三个氨基酸被替换(YTE突变)以延长其半衰期,因此nirsevimab能在整个RSV季节中维持有效浓度,注射一次即可,体重<5 kg的婴儿单次肌内注射50 mg,体重≥5 kg的婴儿单次肌内注射100 mg。2017年,赛诺菲和AZ达成合作协议,由AZ负责研发和生产,赛诺菲负责商业化和营收记录,两家公司在除美国以外的地区分享利益和营收,在美国的商业收益完全归赛诺菲。2022年10月,nirsevimab在欧盟首次获批,11月在英国获批;2023年2月在日本递交申请,4月在加拿大获批。2023年年5月,nirsevimab也在中国递交申请资料,被CDE纳入优先审评,于2024年1月初成功获批上市。2023年7月,Nirsevimab在美国获批。
本次Nirsevimab在国内获批,主要基于中国III期CHIMES研究、中国健康成人I期研究、全球III期MELODY/MEDLEY研究等多个临床试验结果。2023年4月20发布于顶刊《新英格兰医学杂志》的MELODY研究结果显示,对胎龄至少35周出生的婴儿,相比安慰剂组,Nirsevimab降低了76%因RSV引起下呼吸道感染导致的住院风险,针对严重的RSV下呼吸道感染总体疗效为78.6%。安全性方面,接种后的不良反应皮疹发生率为0.7%,发热发生率为0.5%,安全性与生理盐水相似。
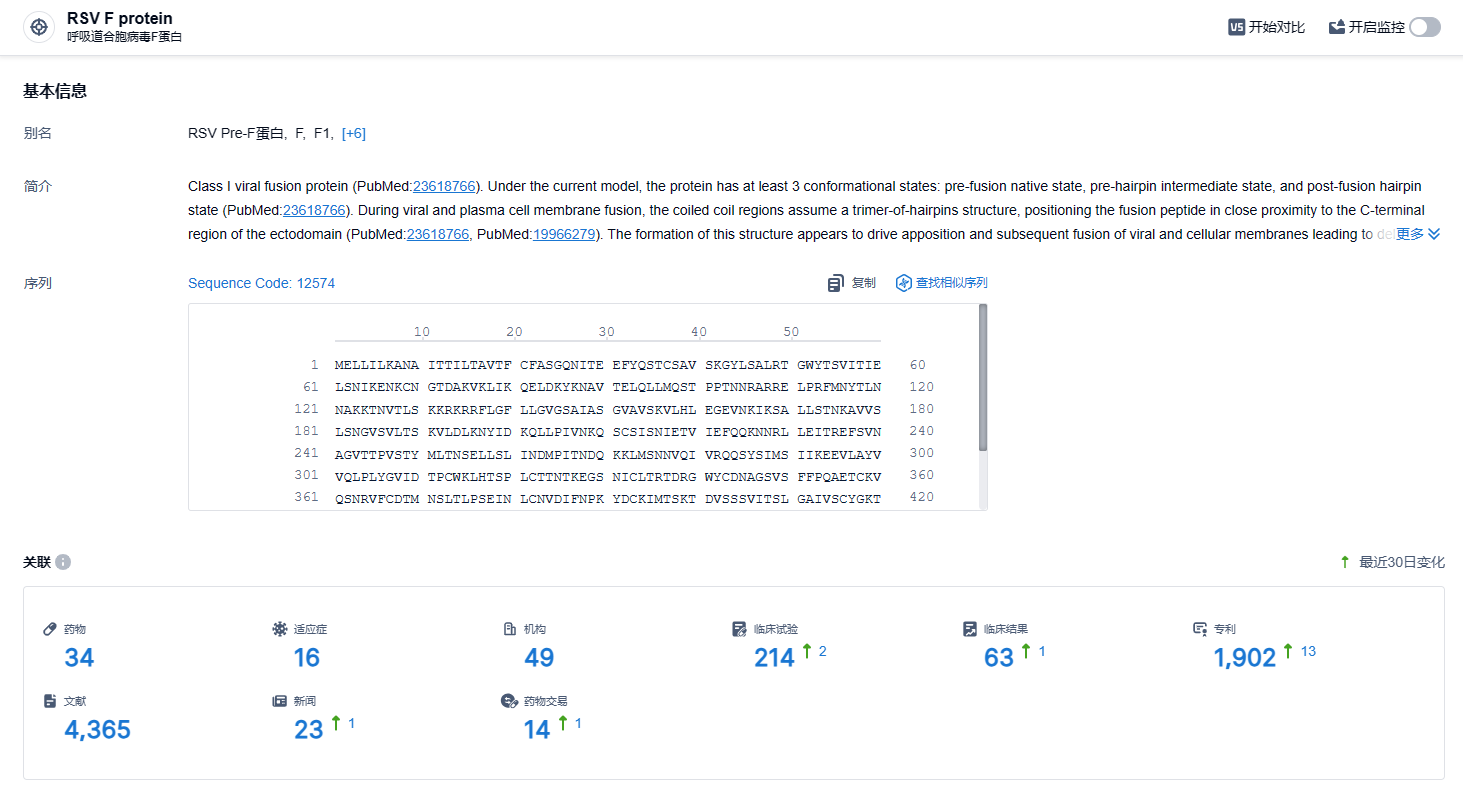
根据智慧芽新药情报库所披露的信息 (点击下方图片直达 RSV F protein 靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2024年1月3日,RSV F protein 靶点共有在研药物34个,包含的适应症有16种,在研机构49家,涉及相关的临床试验214件,专利多达1902件……nirsevimab具有广阔的市场空间,期待该药后续的表现。