丹擎医药PARG抑制剂DAT-2645片在美国获批临床,针对晚期实体瘤
2024年6月24日,丹擎医药(Danatlas Pharmaceuticals)宣布,该公司的PARG抑制剂DAT-2645片的新药临床试验申请(IND)已经于近日获得美国FDA批准。这是中国首个、全球前两名获得FDA批准进入临床的PARG抑制剂。
DAT-2645正是丹擎医药自主研发的一种全新结构的、高选择性的口服小分子PARG抑制剂。据丹擎医药新闻稿介绍,DAT-2645通过合成致死的机制特异性地杀伤携带特定DNA损伤修复缺陷的肿瘤细胞,其适应症包括乳腺癌、卵巢癌、胰腺癌、前列腺癌、子宫癌、胃癌、结直肠癌等多种常见癌症,并且有望拓展PARP抑制剂无效的适应症和解决PARP抑制剂耐药的痛点,具有潜在的“广谱治疗性”的临床应用前景。迄今为止,全球尚无PARG抑制剂获批上市。
丹擎医药将在中国和美国开展多中心,开放标签、剂量递增和剂量扩展的I期临床试验,于2024年下半年启动患者入组,用于评估DAT-2645单药治疗携带BRCA1/2功能缺失性突变和/或同源重组缺陷(HRD)的晚期或转移性实体瘤患者的安全性和有效性。
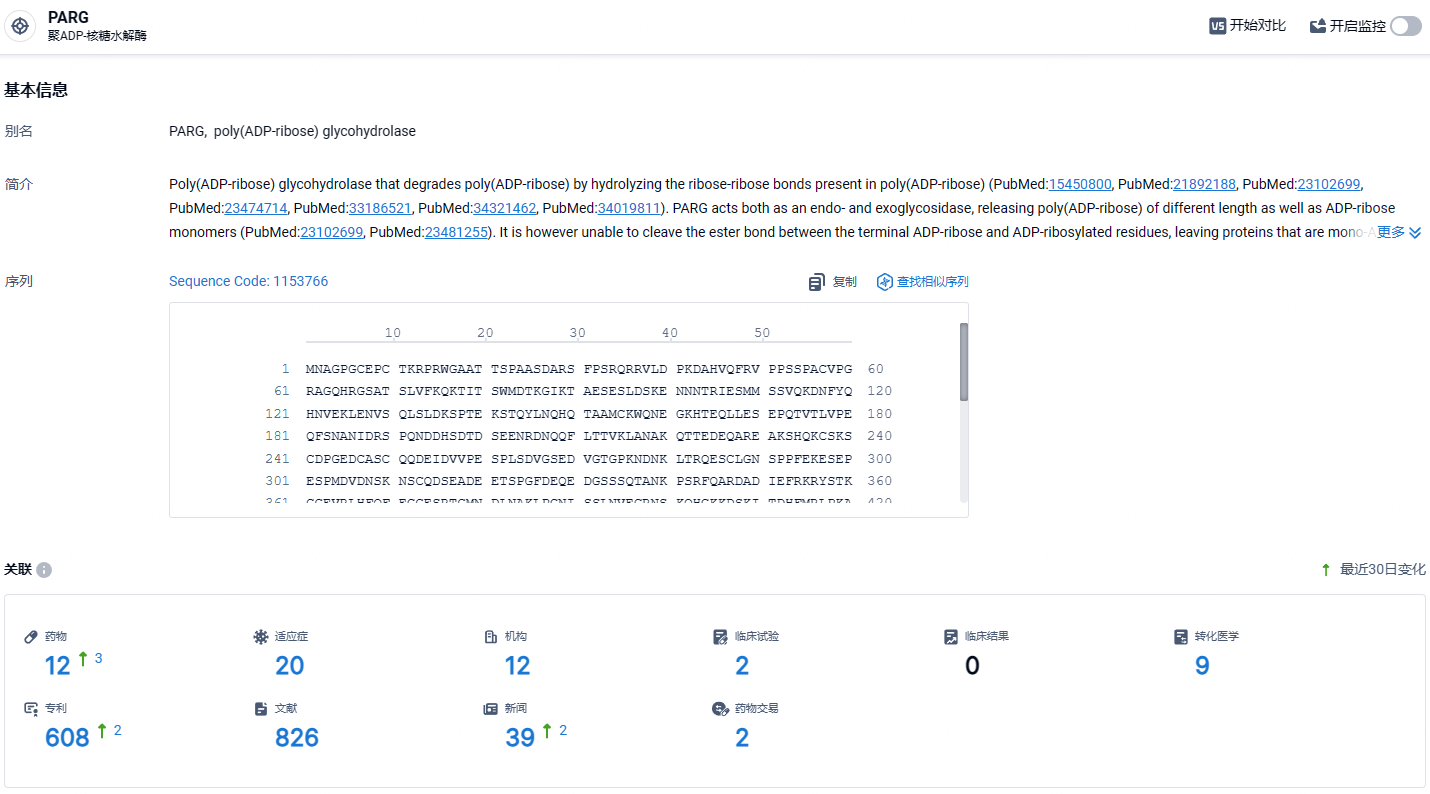
根据智慧芽新药情报库所披露的信息 (点击下方卡片直达PARG靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2024年6月26日,PARG靶点共有在研药物12个,包含的适应症有20种,在研机构12家,涉及相关的临床试验2件,专利多达608件……PARG在DNA修复过程中起着至关重要的作用,它通过从被聚腺苷二磷酸核糖多聚酶(PARPs)修饰的蛋白上移除聚腺苷二磷酸核糖,参与了DNA修复的过程。将PARG作为治疗靶点引起了广泛关注,作为一种潜在策略,可以使癌细胞对DNA损伤诱导剂产生敏感;抑制PARG可能会干扰DNA修复机制,导致细胞死亡。因此,开发PARG抑制剂是癌症治疗的一个新的有前景的方法。期待这款PARG抑制剂后续临床进展顺利。