云顶新耀引进S1PR1调节剂伊曲莫德在中国澳门申报上市,治疗溃疡性结肠炎
2024年3月11日,云顶新耀宣布,中国澳门特别行政区药物监督管理局已正式受理伊曲莫德治疗中重度活动性溃疡性结肠炎成人患者的新药上市许可申请。
伊曲莫德是Arena公司开发的一款口服选择性1-磷酸鞘氨醇受体(S1PR1)调节剂,采用优化的药理学设计,与S1P受体1、4和5结合,可用于治疗包括胃肠道和皮肤病在内的一系列免疫炎性疾病。2017年12月,云顶新耀从Arena获得了etrasimod和另一款产品ralinepag在大中华区的独家开发和商业化权益,首付款1200万美元,里程金2.12亿美元。2021年12月,辉瑞以约67亿美元收购Arena,同时获得了etrasimod。云顶新耀正在亚洲开展伊曲莫德(etrasimod)的多中心3期临床研究,该公司称争取尽早递交其在云顶授权范围的新药上市许可申请(NDA)。2023年10月,该产品已获FDA批准上市,用于治疗中度至重度活动性溃疡性结肠炎(UC)成人患者。2023年12月1日,云顶新耀宣布伊曲莫德(etrasimod)治疗中重度活动性溃疡性结肠炎(UC)的亚洲多中心III期临床研究诱导期取得积极结果。
此前云顶新耀公布的结果显示,诱导治疗期之后,etrasimod组在主要终点、所有关键次要终点以及其他次要终点(包括粘膜愈合、症状缓解和内镜改善)均达到了具有临床意义和统计学显著性的改善。此外,etrasimod 2mg治疗耐受性良好,未观察到新的安全性信号。
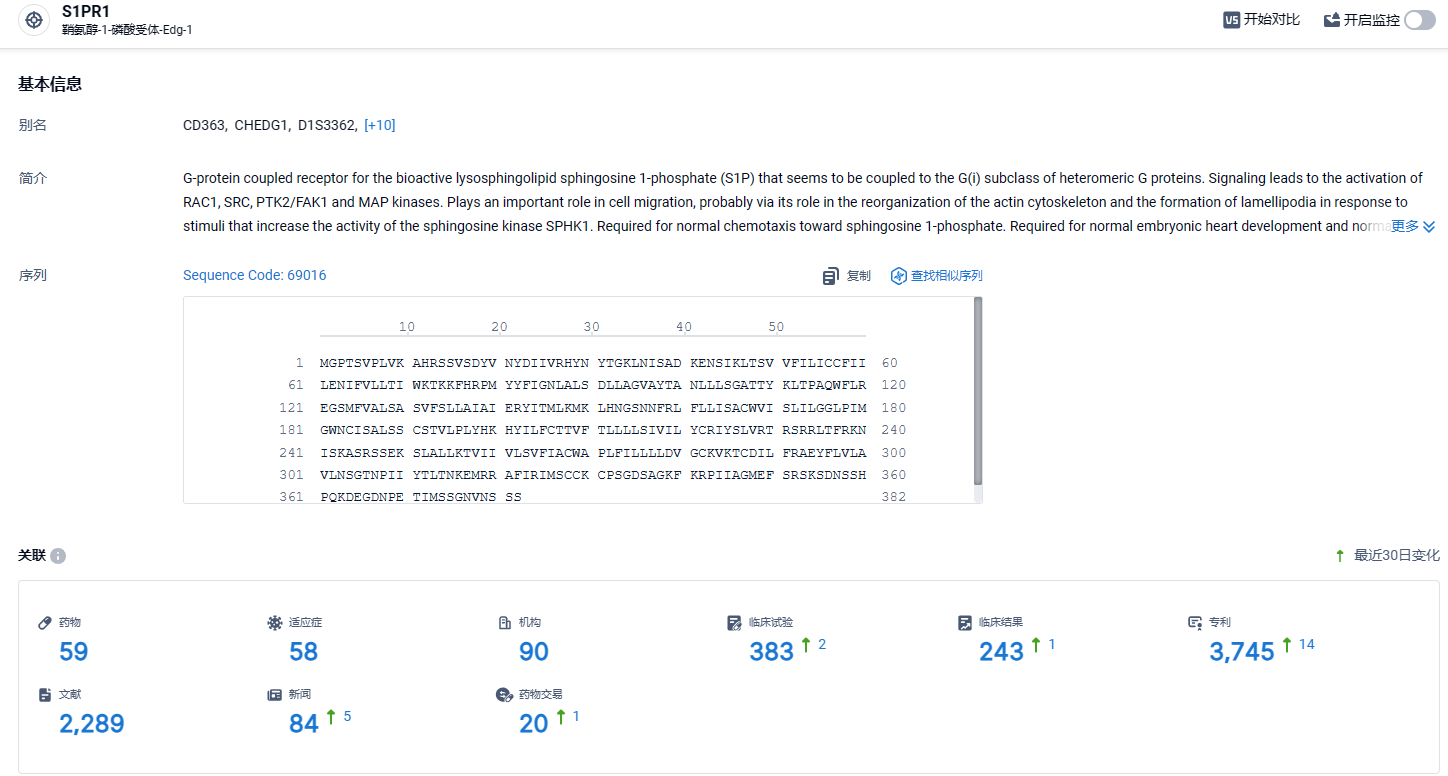
根据智慧芽新药情报库所披露的信息 (点击下方卡片直达S1PR1靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2024 年3月12日,S1PR1靶点共有在研药物59个,包含的适应症有58种,在研机构90家,涉及相关的临床试验383件,专利多达3745件……云顶新耀正在亚洲开展伊曲莫德(etrasimod)的多中心3期临床研究,期待云顶新耀尽早递交其在中国的新药上市许可申请(NDA)。