驯鹿生物靶向BCMA CAR-T产品伊基奥仑赛新适应症获批临床,针对多发性骨髓瘤
2024年3月28日,驯鹿生物宣布该公司自主研发的全人源靶向BCMA的CAR-T产品伊基奥仑赛注射液(研发代号CT103A)的一项新适应症临床试验申请获中国国家药品监督管理局(NMPA)批准,拟扩大适应症用于治疗既往经过1-2线治疗且来那度胺耐药的复发/难治性多发性骨髓瘤患者。
伊基奥仑赛注射液(驯鹿生物研发代号:CT103A;信达生物研发代号:IBI326)是一种靶向BCMA的CAR-T创新候选产品。该候选产品以慢病毒为基因载体转染自体T细胞,CAR包含全人源scFv、CD8a铰链和跨膜、4-1BB共刺激和CD3ζ激活结构域。此前,伊基奥仑赛注射液已被NMPA纳入突破性治疗品种,并获得FDA授予的孤儿药资格,用于治疗复发/难治性多发性骨髓瘤的申请。2023年2月,FDA再次授予该药再生医学先进疗法资格和快速通道资格,用于治疗复发/难治多发性骨髓瘤。2023年6月30日,中国国家药监局(NMPA)官网最新公示,驯鹿生物与信达生物联合开发的BCMA靶向CAR-T产品伊基奥仑赛注射液(曾用名:伊基仑赛注射液)已获批上市,用于治疗复发或难治性多发性骨髓瘤(MM)成人患者,既往经过至少3线治疗后进展(至少使用过一种蛋白酶体抑制剂及免疫调节剂)。2024年1月25日,中国国家药监局药品审评中心(CDE)官网公示,驯鹿生物递交的BCMA靶向CAR-T产品伊基奥仑赛注射液新适应症获批临床,拟用于治疗难治性全身型重症肌无力。
伊基奥仑赛注射液(商品名:福可苏®)于2023年6月30在中国上市,获批适应症为既往经过至少3线治疗后进展(至少使用过一种蛋白酶体抑制剂及免疫调节剂)的复发或难治性多发性骨髓瘤成人患者。末线治疗适应症的批准是基于一项评估伊基奥仑赛注射液治疗复发/难治性多发性骨髓瘤患者的中国多中心I/II期注册临床试验(CTR20192510, NCT05066646),FUMANBA-1的临床研究据。根据在2023年国际骨髓瘤学会(IMS)年会上公布的本研究最新长期随访数据,截至2022年12月31日,103例疗效可评估受试者中,总体缓解率(ORR)为96.1%,严格意义的完全缓解/完全缓解(sCR/CR)率为77.7%;91例既往无CAR-T治疗史的受试者中,ORR达98.9%,sCR/CR率达到 82.4%,12个月无进展生存(PFS)率为85.5%;94.2% (97/103) 受试者达到MRD阴性,所有CR/sCR受试者均达到MRD阴性。接受治疗的105例受试者中,仅一例受试者发生≥3级CRS,无≥3级ICANS。药代动力学数据显示,伊基奥仑赛注射液回输后能在体内长期存续,24个月时仍有40%的受试者能检测到基因拷贝数。
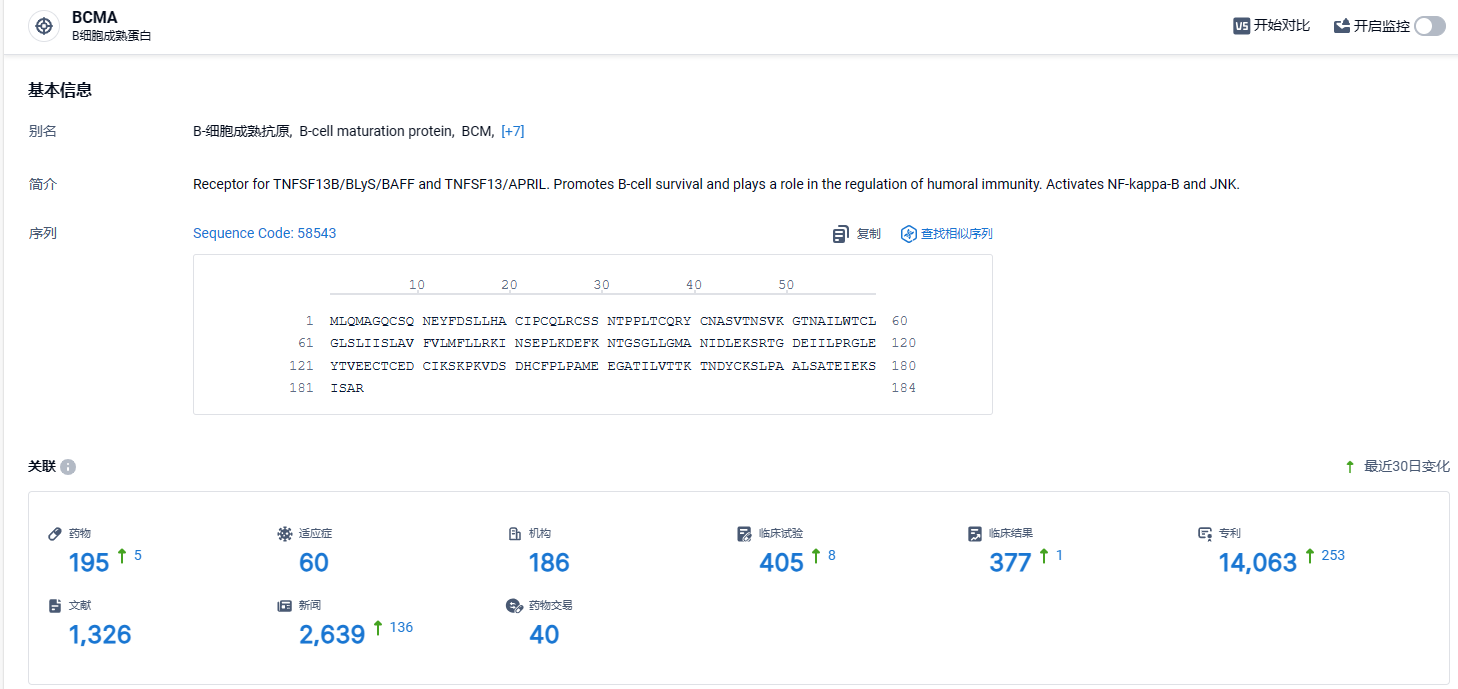
根据智慧芽新药情报库所披露的信息 (点击下方卡片直达BCMA靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2024年3月30日,BCMA靶点共有在研药物195个,包含的适应症有60种,在研机构186家,涉及相关的临床试验405件,专利多达14063件……CAR-T细胞疗法的出现对于血液肿瘤治疗具有革命性意义,为血液肿瘤患者带来了新的治疗选择和希望,尤其用于后线骨髓瘤患者可显著提高缓解率并延长生存期,改善了患者治疗效果和生存质量。期待伊基奥仑赛商业化一切顺利。