预约演示
最新资讯
强生EGFR/MET双抗Amivantamab递交sBLA申请,一线治疗非小细胞肺癌
2023-08-29
阅读时长 2分钟
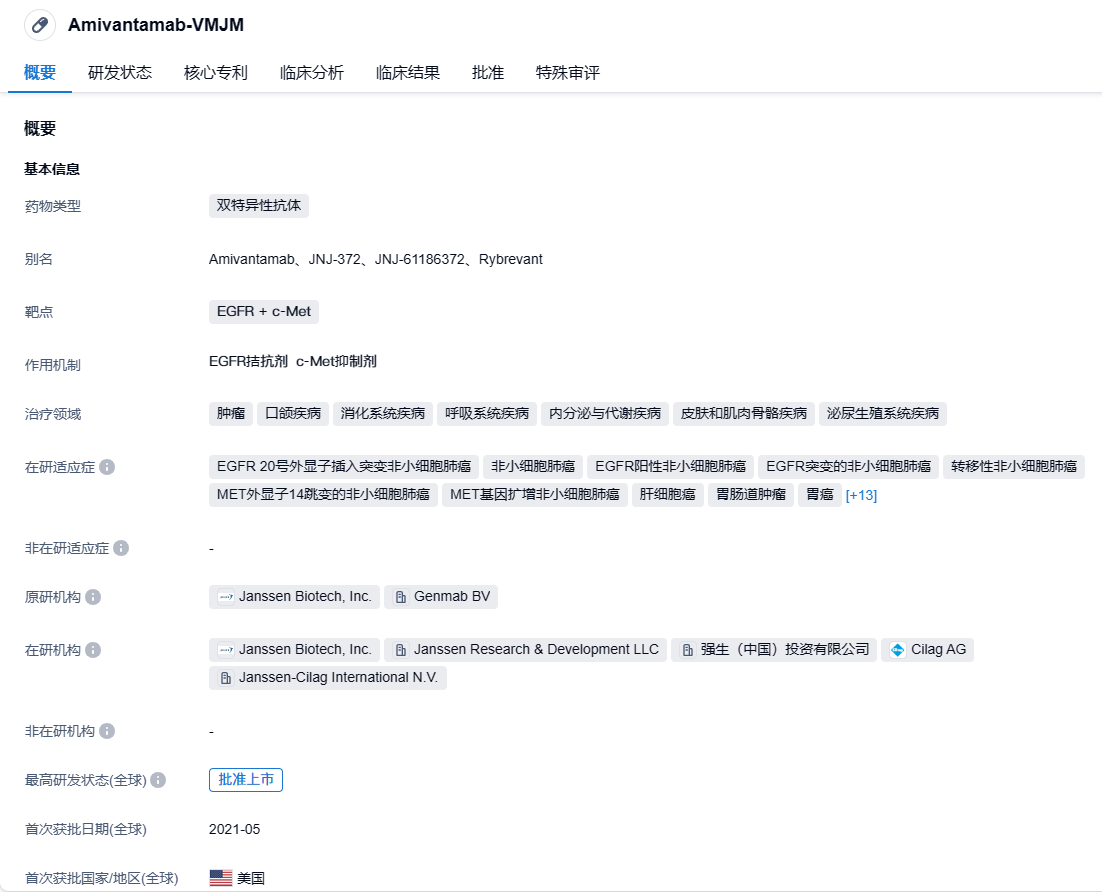
近日,强生旗下杨森(Janssen)公司宣布,已经向美国FDA递交补充生物制品许可申请(sBLA),寻求批准旗下EGFR/c-Met双特异性抗体疗法Rybrevant(Amivantamab)与化疗联用,一线治疗携带EGFR外显子20插入突变的局部晚期或转移性非小细胞肺癌(NSCLC)患者。
Amivantamab是一款人源化EGFR/c-Met双特异性抗体。它具有多重抗癌作用机制,不但能够阻断EGFR和MET介导的信号传导,还可以引导免疫细胞靶向携带激活性和抗性EGFR/MET突变和扩增的肿瘤。2021年5月,Amivantamab获得美国FDA批准上市,用于治疗铂类化疗期间或之后进展的EGFR外显子20插入突变NSCLC患者。
这一申请得到3期临床试验PAPILLON的支持。今年7月,杨森宣布PAPILLON研究达到了主要终点,接受Rybrevant联合化疗的患者与单独接受化疗的患者相比,无进展生存期有了显著统计学意义和临床意义的改善。Rybrevant与化疗联合治疗的安全性与单独治疗方案的安全性一致。
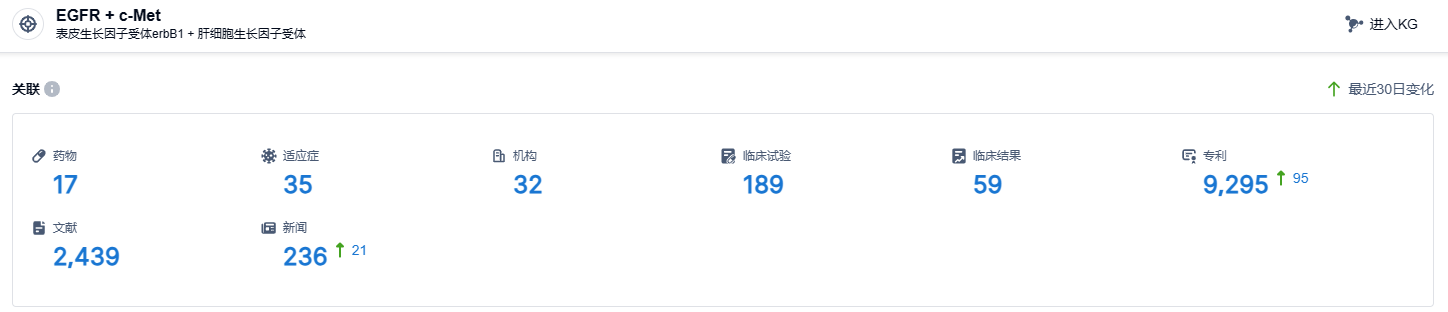
根据智慧芽新药情报库所披露的信息 (点击下方图片直达 EGFR/c-Met 靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2023 年8月29日, EGFR/c-Met 靶点共有在研药物17个,包含的适应症有35种,在研机构32家,涉及相关的临床试验189件,专利多达9295件……基于Amivantamab优异的数据,预计EGFR/c-Met双抗药物有望成为EGFR领域下一代重磅产品。国内企业中,岸迈生物、贝达药业、嘉和生物、和翰森制药等企业布局了EGFR/c-Met赛道,期待这些国产新药的后续表现。

生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
继续阅读
返回博客首页 →最新资讯
阅读时长 2分钟
诺和诺德GLP-1R激动剂司美格鲁肽心衰III期STEP HFpEF临床试验结果积极
2023-08-26
诺和诺德在欧洲心脏病学会(ESC)大会上宣布,在III期STEP HFpEF试验中,该公司的GLP-1R激动剂Wegovy(司美格鲁肽)除了显示出预期的体重减轻之外,还显示出心血管益处。
最新资讯
阅读时长 2分钟
科弈药业靶向BCMA/CD19自体 CAR-T产品在中国获批临床,治疗多发性骨髓瘤
2023-08-26
科弈药业全资子公司科棋药业申报的靶向BCMA/CD19细胞疗法KQ-2003自体嵌合抗原受体T细胞注射液获批临床,适应症为已经接受过三线或者更多线治疗的复发/难治性多发性骨髓瘤。
最新资讯
阅读时长 2分钟
阿斯利康FRα ADC新药AZD5335国内申报临床,针对实体瘤
2023-08-26
CDE 官网显示,阿斯利康的 FRα ADC 新药 AZD5335 首次在国内申报临床(受理号:JXSL2300158),这是阿斯利康自研 ADC(抗体偶联药物) 平台开发的第 3 款临床阶段新药。AZD5335 是阿斯利康开发的一款ADC药物,由FRα 抗体偶联其专有的 TOP1抑制剂 AZ14170132,DAR为8。
最新资讯
阅读时长 2分钟
罗氏KRAS G12C抑制剂divarasib 1期临床试验结果积极,持久产生临床缓解
2023-08-26
日前,《新英格兰医学杂志》发布了由罗氏(Roche)旗下基因泰克(Genentech)公司所研发的KRAS G12C抑制剂divarasib(RG6330/GDC-6036)在携带KRAS G12C突变实体瘤患者中的1期试验结果。论文指出,divarasib可以在KRAS G12C阳性肿瘤中,产生持久的临床缓解。
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。