Outlook Therapeutics眼用贝伐珠单抗ONS-5010三期研究失败,针对wAMD
11月27日,Outlook Therapeutics宣布眼用贝伐珠单抗ONS-5010治疗湿性年龄相关性黄斑变性(wAMD)的III期NORSE EIGHT研究未达到主要终点。
ONS-5010是一种Outlook Therapeutics开发的贝伐珠单抗研究性眼科制剂,将作为玻璃体内注射剂给药,用于治疗湿性AMD和其他已批准的视网膜疾病。贝伐珠单抗(Bevacizumab),原研药商品名安维汀(Avastin),是一种人源化单抗,通过阻断血管内皮生长因子(VEGF),抑制肿瘤的血管新生,从而诱导肿瘤细胞凋亡。贝伐珠单抗以高亲和力选择性结合人血管内皮生长因子(VEGF)的所有亚型,并通过空间阻断VEGF与其受体Flt-1(VEGFR-1)和KDR(VEGFR-2)的结合来中和VEGF的生物活性在内皮细胞表面。玻璃体内注射后,贝伐珠单抗与VEGF的结合阻止了VEGF与其在内皮细胞表面的受体的相互作用,从而减少了视网膜中内皮细胞增殖、血管渗漏和新血管的形成。
NORSE EIGHT研究是一项随机、盲法、阳性药物对照、非劣效性研究(n=400),旨在评估ONS-5010(1.25mg,每4周1次)对比雷珠单抗(0.5mg)治疗新诊断wAMD患者的疗效和安全性。研究的主要终点是最佳矫正视力(BCVA)从基线到第8周的平均变化。数据显示,治疗第8周,在意向性治疗(ITT)人群中,ONS-5010组和雷珠单抗组的BCVA平均值差异不显著(+4.2 vs +6.3个字母,差异为-2.257,95% CI: -4.044, -0.470;P=0.0863),未达到FDA在特殊方案评估(SPA)中预先指定的非劣效性范围下限(-3.5),也未达到P值要求(P>0.025)。Outlook Therapeutics表示,后续将继续随访患者,计划在2025年1月公布NORSE EIGHT研究的随访3个月的数据。
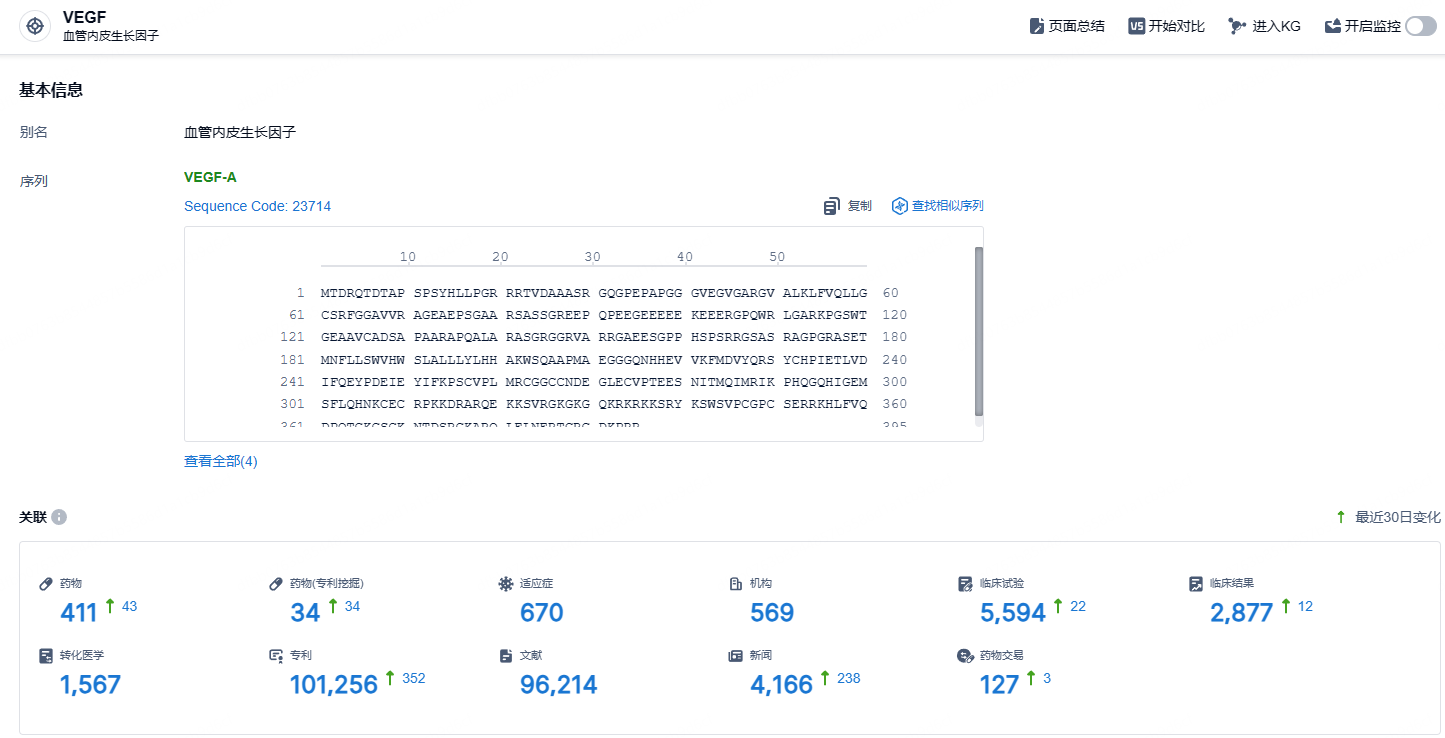
根据智慧芽新药情报库所披露的信息 (点击下方图片直达VEGF靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2024年11月29日,VEGF靶点共有在研药物411个,包含的适应症有670种,在研机构569家,涉及相关的临床试验5594件,专利多达101256件……随着本次临床试验的公布,市场对这一消息以大跌回应,Outlook股价在盘前交易中跌超79%。不过Outlook并未打算放弃,公司表示在完成对NORSE EIGHT的最终分析后,在2025年第一季度再次提交ONS-5010的上市申请(BLA)。期待该药的后续发展。