默沙东靶向ACVR2A新药Sotatercept 3期临床数据积极,试验将提前终止
11月26日,默沙东宣布,其“first-in-class”疗法Winrevair(sotatercept)在3期临床试验ZENITH的中期分析中达到主要终点。基于这一积极结果,试验将提前终止,让所有肺动脉高压(PAH)患者有机会接受Winrevair治疗。
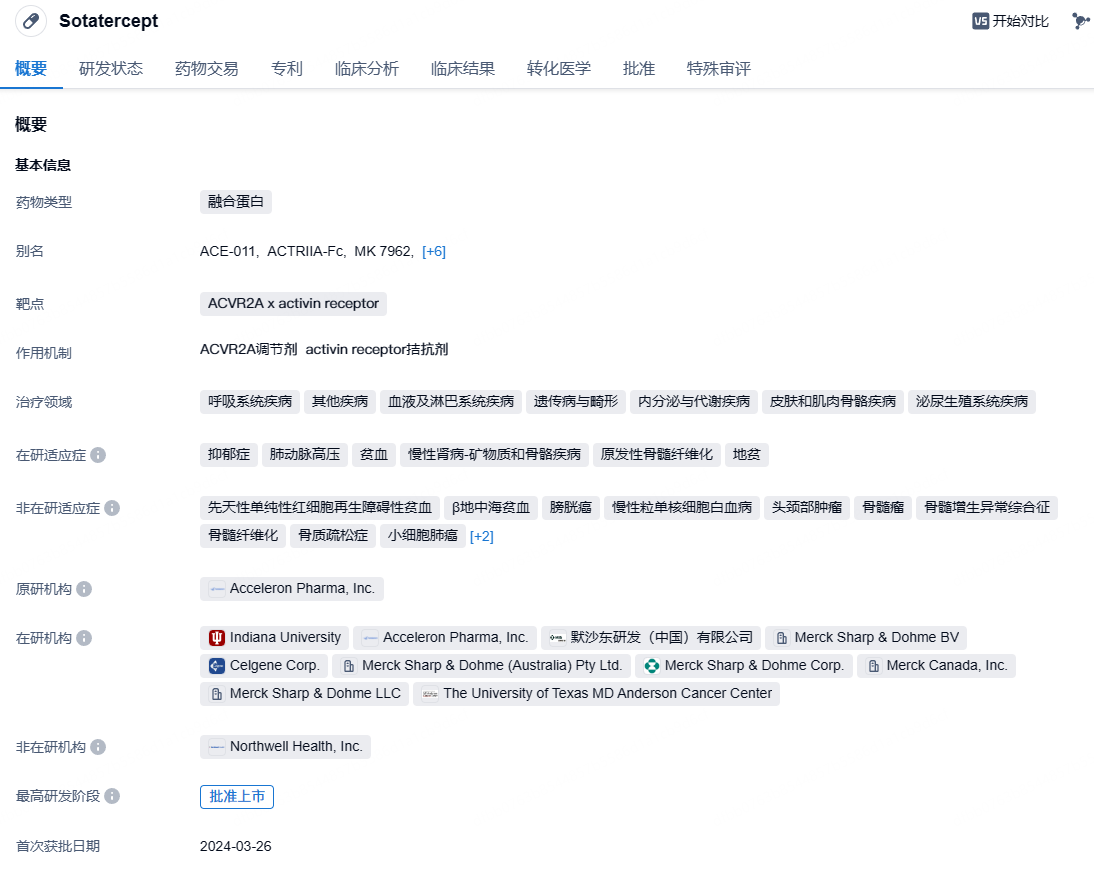
Sotatercept是Acceleron Pharma开发的一款first-in-class ACVR2A-Fc融合蛋白,可将ACVR2A经过改造的细胞外域与抗体的Fc端融合在一起,阻断激活素与细胞膜上的受体结合,从而降低激活素介导的信号传导。研究表明,转化生长因子β(TGF-β)超家族成员介导的细胞增殖和抗凋亡信号通路失衡是驱动PAH患者肺血管重塑的重要机制之一。激活素2A型受体(ACVR2A)便是TGF-β超家族的成员之一。因此,靶向ACVR2A的药物是逆转肺血管重塑的潜在有效途径。
2021年默沙东以115亿美元收购Acceleron获得Sotatercept。已经获得FDA授予的突破性疗法认定,这也是首款获得突破性疗法认定的肺动脉高压在研疗法。2023年8月1日,默沙东在公布2023年H1财报时表示,已向FDA提交Sotatercept(MK-7962)用于治疗肺动脉高压(PAH)的生物制品许可申请(BLA)。2024年3月,Sotatercept(商品名:Winrevair)凭借III期STELLAR研究的积极结果获FDA批准上市。2024年10月17日,CDE网站显示,默沙东的肺动脉高压(PAH)新药Sotatercept在国内申报上市。
ZENITH研究评估了Winrevair在肺动脉高压功能分级III或IV级且死亡风险较高的成人患者中的疗效和安全性。中期分析结果显示,Winrevair与安慰剂相比,显著降低了患者死亡或疾病恶化事件的风险(事件包括全因死亡、肺移植和因PAH恶化导致住院超过24小时)。这些患者均接受背景PAH治疗。基于这些结果,独立数据监察委员会建议ZENITH试验提前中止,所有参与者在开放标签扩展研究SOTERIA中均有机会接受Winrevair治疗。在初步评估中,不良事件和严重不良事件在不同治疗组之间的发生率保持均衡。
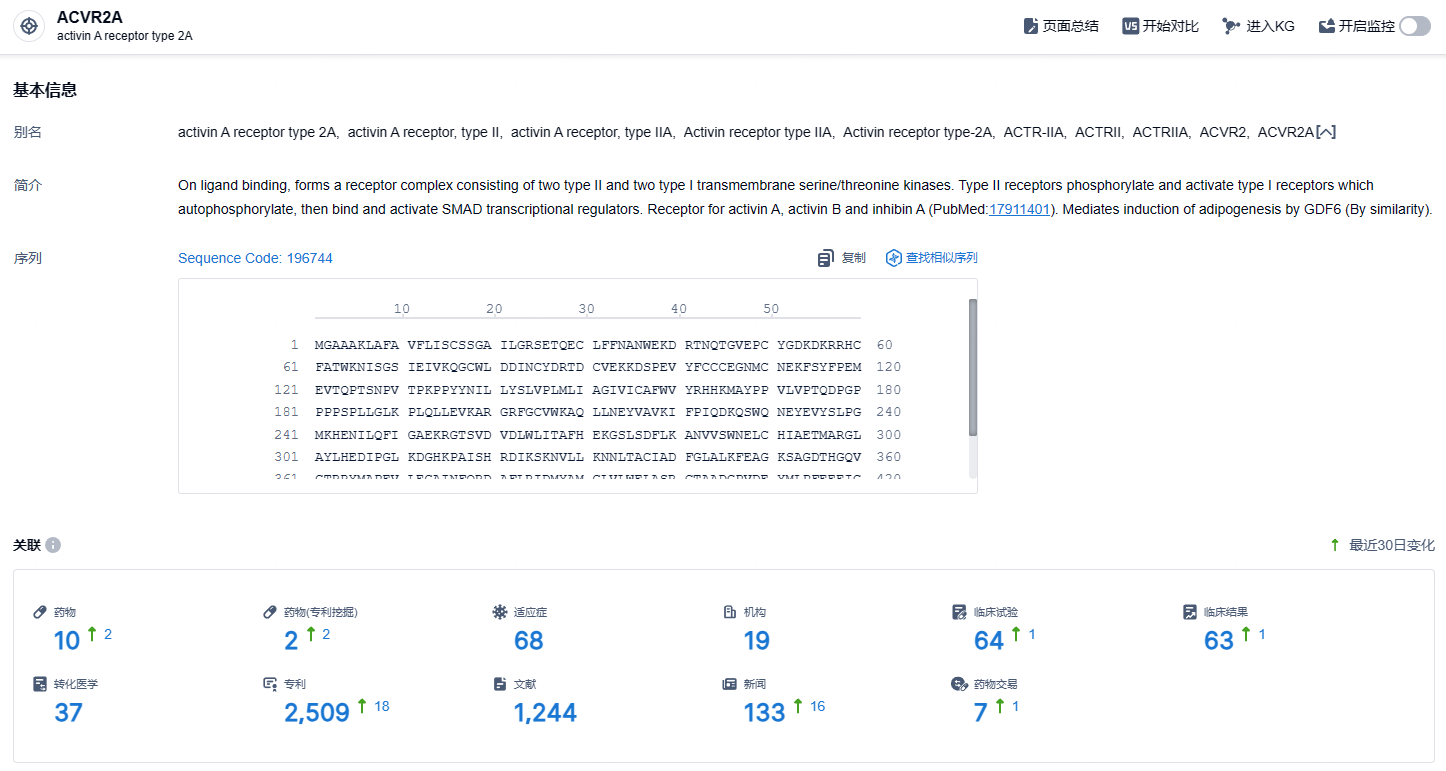
根据智慧芽新药情报库所披露的信息 (点击下方卡片直达ACVR2A靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2024 年11月27日,ACVR2A靶点共有在研药物10个,包含的适应症有68种,在研机构19家,涉及相关的临床试验64件,专利多达2509件……sotatercept在改善肺动脉高压患者运动能力和其他有意义的临床结局指标方面发挥了关键作用,且在稳定背景治疗的基础上,接受sotatercept治疗患者的死亡或临床恶化风险显著降低。这些结果彰显了sotatercept在肺动脉高压治疗领域的潜力,期待该药能够顺利在国内获批,为肺动脉高压患者带来新的治疗选择。