神州细胞CD20xCD3双抗SCTB35注射液获批临床,针对非霍奇金淋巴瘤
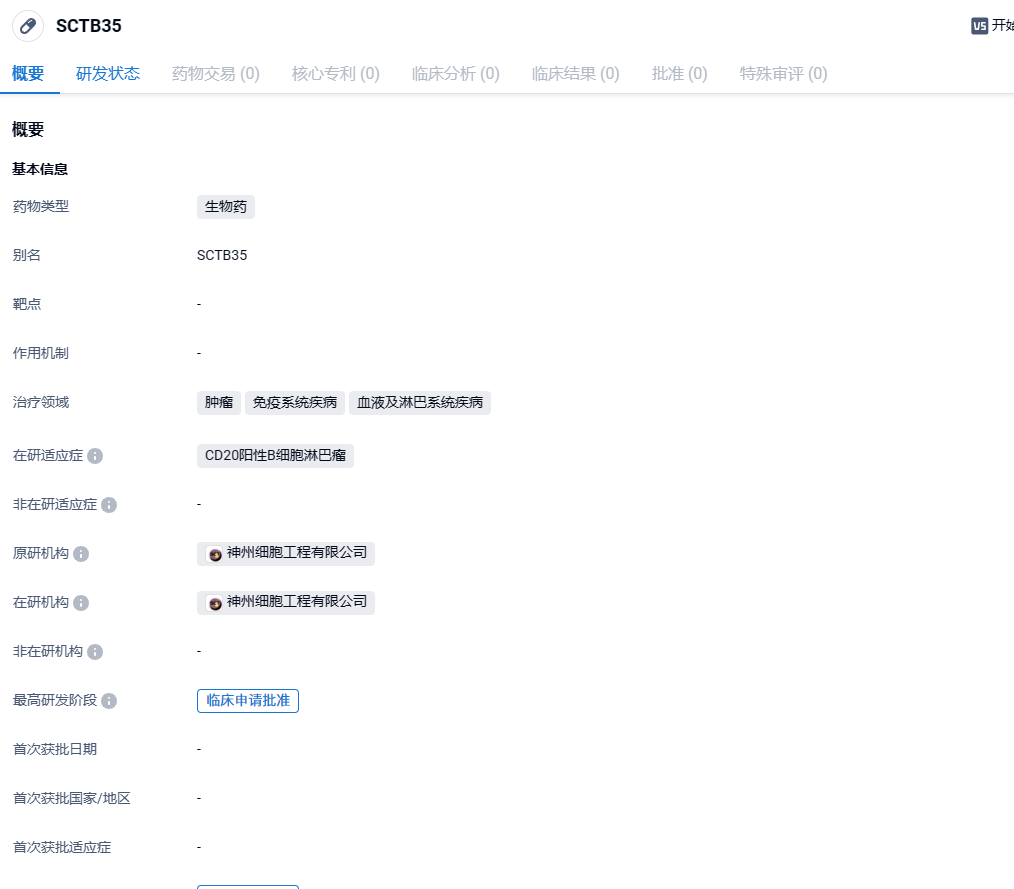
近日,中国国家药监局药品审评中心(CDE)官网公示,神州细胞1类新药SCTB35注射液获批临床,拟开发治疗复发/难治性CD20阳性B细胞非霍奇金淋巴瘤(B-NHL)。公开资料显示,SCTB35是神州细胞自主研发的一款CD20 x CD3双特异性抗体。
SCTB35是神州细胞自主研发的一款CD20 x CD3双特异性抗体注射液,可通过介导T细胞与肿瘤细胞的结合形成免疫突触,实现有效的T细胞激活及肿瘤细胞杀伤。本次提交的临床试验方案为一项评价SCTB35在复发/难治性CD20阳性B细胞非霍奇金淋巴瘤患者中的安全性、耐受性、药代动力学、初步有效性的I期临床研究。
非霍奇金淋巴瘤(NHL)是CD20+B细胞血液瘤的主要类型,包括弥漫性大B细胞淋巴瘤(DLBCL)、滤泡性淋巴瘤(FL)、套细胞淋巴瘤(MCL)、慢性淋巴细胞白血病/小淋巴细胞淋巴瘤(CLL/SLL)等。
2019年ASH(美国血液年会)年会,CD20/CD3双抗凭借惊艳临床数据一站成名,一度呈现比肩/赶超CAR-T之趋势。在几个主要玩家披露的临床数据中,经CAR-T细胞疗法治疗后进展/失效的患者仍可看到从中获益,令业备受鼓舞。该类靶点药物对非霍奇金淋巴瘤在内的血液瘤具有优秀的治疗潜力。
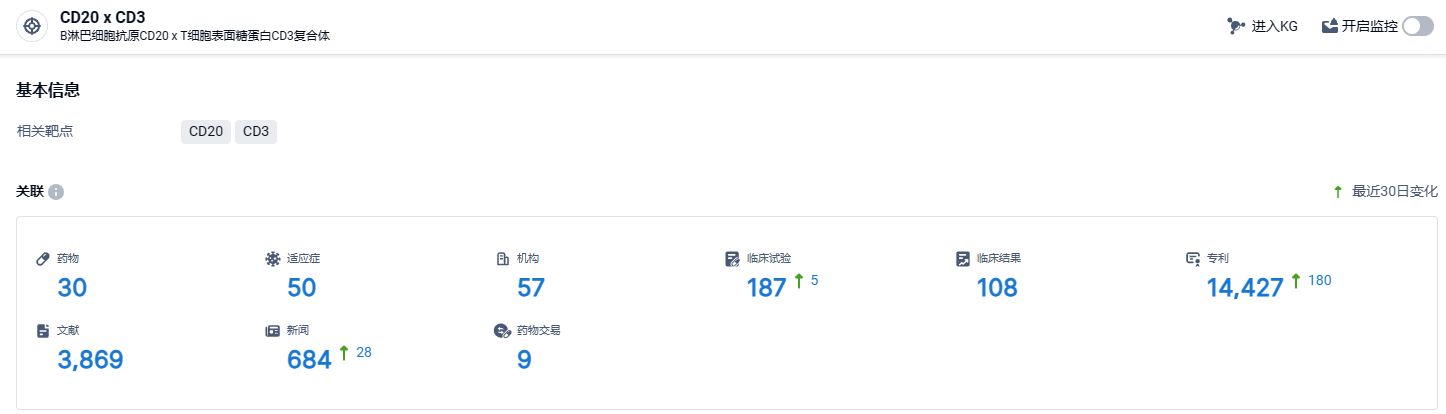
根据智慧芽新药情报库所披露的信息 (点击下方卡片直达CD20 x CD3靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2024 年3月15日,CD20 x CD3靶点共有在研药物30个,包含的适应症有50种,在研机构57家,涉及相关的临床试验187件,专利多达14427件……国内方面,爱思迈,正大天晴,康诺亚/诺诚健华,天广实,嘉和生物等快速跟进布局CD20 x CD3双抗研发。除了合作开发/引进的产品进展较快外,国内大多数CD20/CD3双抗都处于临床Ⅰ期。期待SCTB35能够研发顺利,在该赛道占据一席之地。