艾力斯医药KRAS G12D选择性抑制剂AST2169获批临床,针对晚期实体瘤
2024年3月13日,中国国家药监局药品审评中心(CDE)官网公示,艾力斯医药1类新药注射用AST2169脂质体获批临床,拟开发用于携带KRAS G12D突变的晚期实体瘤患者。
AST2169是艾力斯自主研发的具有全球知识产权的KRAS G12D选择性抑制剂。KRAS G12D突变是KRAS突变的一种常见的亚型,存在于非小细胞肺癌、结直肠癌、胰腺癌等多种类型癌症中。虽然KRAS突变在人类癌症中的作用已经为人所知几十年,但针对KRAS突变的抗癌疗法研发一直进展缓慢,目前全球范围内尚无KRAS G12D抑制剂获批上市,日益增长的临床需求无法得到满足。
KRAS是常见发生突变的驱动基因,KRAS G12D是KRAS突变中主要的突变亚型,在大约30%的胰腺癌、12%的结直肠癌和4%的非小细胞肺癌等多种类型癌症中可检测出。KRAS G12D突变的患者预后不佳,目前尚未有相关的靶向治疗获批上市,日益增长的临床需求无法得到满足。此次获批的1期临床研究旨在KRAS G12D突变晚期实体瘤患者中评估AST2169的安全性、耐受性、药代动力学及初步疗效。
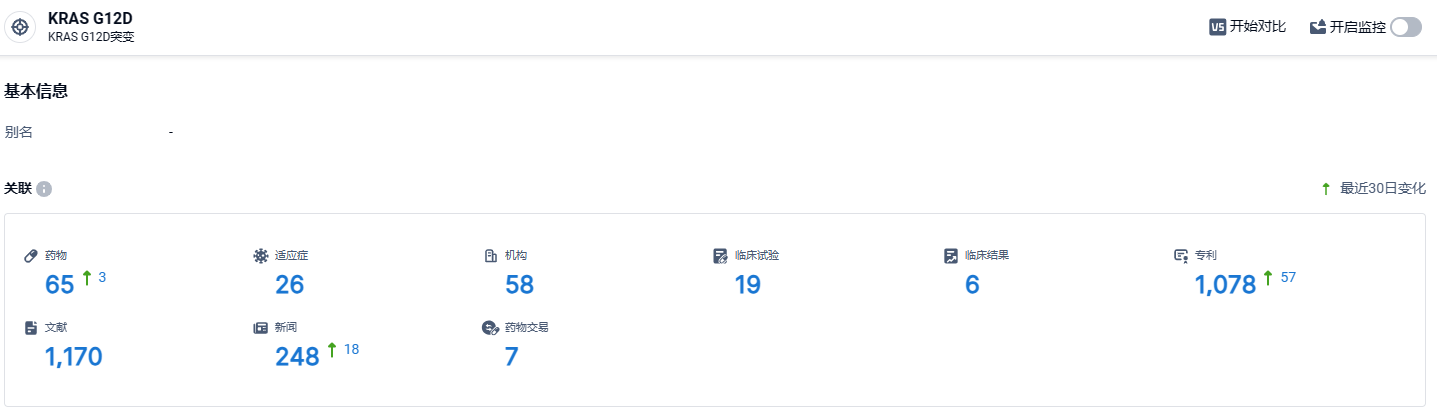
根据智慧芽新药情报库所披露的信息 (点击下方卡片直达KRAS G12D靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2024 年3月15日,KRAS G12D靶点共有在研药物65个,包含的适应症有26种,在研机构58家,涉及相关的临床试验19件,专利多达1078件……针对KRAS相关靶点,除了AST2169,艾力斯还开发了AST-NS1902(靶向KRAS G12C)、AST-NS2101(靶向KRAS G12D)、AST-NS2202(靶向 KRAS),这些候选药目前处于临床前研究阶段。期待AST2169这款KRAS G12D能够研发顺利。