Kymera旗下IRAK4降解剂KT-474 2期进展积极,加速挺进关键性临床开发
近日,Kymera Therapeutics宣布,在独立数据审查委员会对在研蛋白降解药物KT-474的初步安全性和有效性数据进行审查后,赛诺菲(Sanofi)公司已通知Kymera,计划扩大正在进行的化脓性汗腺炎(HS)和特应性皮炎(AD)的2期临床试验,以更快地将这款创新疗法推进至关键性临床研究阶段。
KT-474(SAR444656)是一款潜在“first-in-class”的IRAK4降解剂,正在开发用于治疗HS、AD等有显著患者需求的免疫炎症疾病,及其他潜在疾病。IRAK4是myddosome蛋白复合体中的关键组分,通过白细胞介素-1(IL-1)和toll样受体(TLR)参与调控免疫反应的信号传导过程。IL-1和toll样受体在启动针对入侵病原体的免疫反应中扮演着关键角色。IRAK4是一种支架激酶,处于先天性免疫反应与适应性免疫反应的交汇点,通过其激酶活性和支架功能执行多重作用。KT-474通过与IRAK4结合,募集E3泛素连接酶给IRAK4打上泛素的“标签”。这些“标签”会指引IRAK4蛋白被细胞的蛋白酶体降解。利用靶向蛋白降解完全消除IRAK4,会影响其激酶和支架功能,因此有可能实现广泛、耐受性良好的抗炎作用,提供多种免疫炎症疾病的新治疗途径。2020年7月,Kymera 曾与赛诺菲达成多项计划的战略合作,获得1.5亿美元的预付款,并可能获得超过20亿美元的潜在开发、监管和销售里程碑,以及可观的特许权使用费;赛诺菲承诺将共同推进KT-474到2期临床研究。
此前,在一项1 期随机、安慰剂对照、单次和多次递增剂量试验中,公司评估了KT-474的安全性、药代动力学、药效学和临床活性;其中105名健康志愿者 (HV) 被纳入安慰剂对照的单次和多次剂量递增队列(SAD 和 MAD),21 名 HS 和 AD 患者被纳入开放标签患者队列。结果显示:在 HV 血液中观察到 IRAK4 降解,单剂量 600-1600 mg后平均降低 ≥93%,14天后单剂量50-200 mg后平均降低 ≥95%。在接受75mg KT-474治疗的患者中,血液中也实现了类似的IRAK4降解。
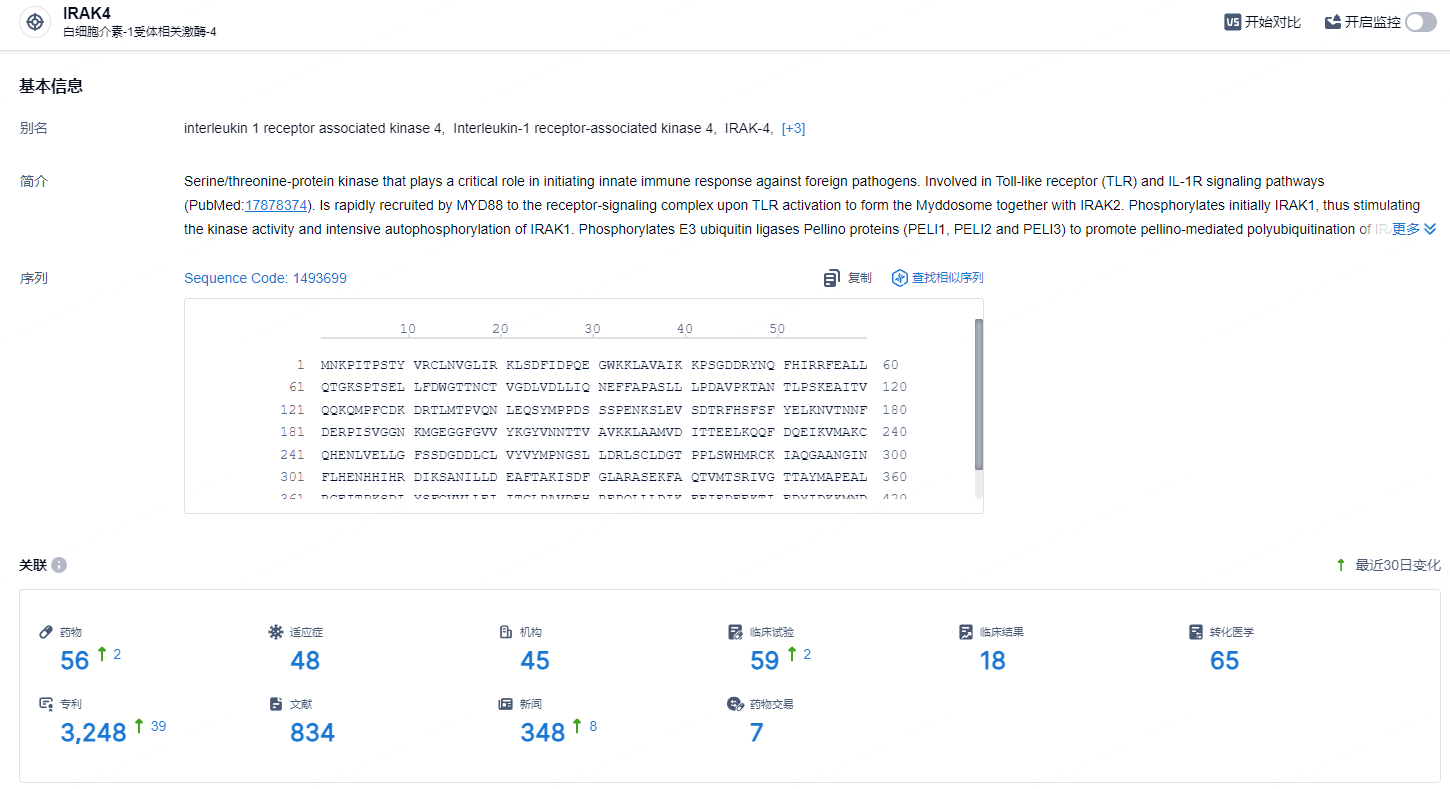
根据智慧芽新药情报库所披露的信息 (点击下方卡片直达IRAK4靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2024年7月11日,IRAK4靶点共有在研药物56个,包含的适应症有48种,在研机构45家,涉及相关的临床试验59件,专利多达3248件……特应性皮炎(AD)是一种慢性、复发性、炎症性皮肤病,好发于婴儿和儿童,也可发生于成人;由于患者常合并过敏性鼻炎、哮喘等其他特应性疾病,故被认为是一种系统性疾病。AD 最基本的特征是皮肤干燥、慢性湿疹样皮损和剧烈瘙痒,严重影响患者的生活质量。根据弗若斯特沙利文,全球特应性皮炎患者人数于2022 年达6.8 亿人,其中儿童/青少年达3.6 亿人。预计到2030 年达7.5 亿人,其中儿童/青少年达3.8 亿例。期待KT-474后续研发顺利。