预约演示
更新于:2026-05-07
Latanoprost
拉坦前列素
更新于:2026-05-07
概要
基本信息
原研机构 |
最高研发阶段批准上市 |
最高研发阶段(中国)批准上市 |
特殊审评- |
登录后查看时间轴
结构/序列
分子式C26H40O5 |
InChIKeyGGXICVAJURFBLW-CEYXHVGTSA-N |
CAS号130209-82-4 |
关联
211
项与 拉坦前列素 相关的临床试验NCT07425535
Optic Nerve Head Strain in Non-glaucoma Subjects
Persons who do not have glaucoma will have pictures taken of the optic nerve with a standard camera before and 2 weeks after starting to take a daily glaucoma eye drop to lower eye pressure. These data will be used to compare to the same procedure performed with glaucoma patients to study how glaucoma injures the eye.
开始日期2026-07-01 |
申办/合作机构 |
CTIS2025-522468-34-00
Phase I clinical trial evaluating the safety, tolerability, and absorption of a topical product containing latanoprost acid in healthy participants.
开始日期2026-02-01 |
申办/合作机构- |
PACTR202512840605479
Selective laser trabeculoplasty versus latanoprost as first line treatments for primary open angle glaucoma and ocular hypertension: A comparative analysis
开始日期2025-12-15 |
申办/合作机构- |
100 项与 拉坦前列素 相关的临床结果
登录后查看更多信息
100 项与 拉坦前列素 相关的转化医学
登录后查看更多信息
100 项与 拉坦前列素 相关的专利(医药)
登录后查看更多信息
2,182
项与 拉坦前列素 相关的文献(医药)2026-06-01·American journal of ophthalmology case reports
Using selective laser trabeculoplasty to manage glaucoma in a child with phakomatosis pigmentovascularis
Article
作者: Oatts, Julius T ; Bai, Patricia ; Wang, Catherine ; Ruiz, Kiara Corcoran ; Abbasian, Javaneh
Purpose:
To describe the management and complications associated with using selective laser trabeculoplasty (SLT) to treat elevated intraocular pressure (IOP) in a child with phakomatosis pigmentovascularis (PPV).
Observations:
A 13-year-old female with bilateral cutaneous hemangiomas of the face and lower limb length discrepancy presented with elevated IOP in the right eye despite maximal medical glaucoma management. There was no evidence of buphthalmos, Haab's striae, posterior embryotoxon, or anterior segment dysgenesis. Initial nerve fiber layer and visual field testing confirmed structural and functional damage, respectively. Genetic testing confirmed a variant in the guanine nucleotide-binding protein G(q) subunit alpha (GNAQ) gene, confirming a diagnosis of PPV. The right eye pre-treatment IOP was 33 mmHg and the patient was treated with 360-degree SLT. Two days later, she developed a shallow peripheral choroidal effusion in the right eye that resolved with medical management. Three months after SLT, the right eye IOP was successfully reduced to 19 mmHg after the discontinuation of acetazolamide. She maintained an IOP of 18 mmHg in the right eye 11 months after SLT on latanoprost and dorzolamide-timolol only.
Conclusions and importance:
Glaucoma filtering procedures in cases of PPV pose a high risk of complications and SLT offers a less-invasive, potentially clinic-based alternative. While the patient did develop a choroidal effusion post-SLT, suspected to be secondary to decreased IOP, this resolved with medical management alone without the need for incisional surgery thus illustrating both the risks and benefits of SLT in treating patients with phakomatoses-associated glaucoma.
2026-06-01·Photodiagnosis and Photodynamic Therapy
Anterior segment, static and dynamic pupillography changes in patients with primary open-angle glaucoma using different types of topical antiglaucomatous agents
Article
作者: Uzakgider, Neslişah Kutlu ; Birgul, Ramazan
INTRODUCTION:
Glaucoma is a major cause of avoidable blindness and the most common type is primary open angle glaucoma (POAG). Topical antiglaucomatous agents are the mainstay of treatment. There are many studies on the ocular effects of antiglaucomatous agents and these results may contradict each other. The aim of our study was to investigate the effects of topical antiglaucomatous agents on the anterior segment and pupil in patients with POAG.
MATERIALS AND METHODS:
The right eye of the patients using dorzolamide+timolol, brimonidine, latanoprost and the right eye of the control group were included in the study. Anterior segment and pupillography measurements were performed using Scheimpflug imaging technique with the Sirius device. Central corneal thickness (CCT), corneal volume (CV), anterior chamber depth (ACD), anterior chamber angle (ACA), anterior chamber volume (ACV), first non-contact tear break up time (NCTBUT), mean NCTBUT, meibography, scotopic, mesopic, photopic pupil sizes and dynamic pupil sizes at 0, 1, 2, 4, 6, 8 and 10 s(s) were measured.
RESULTS:
The dorzolamide+timolol (n = 54), brimonidine (n = 50), and latanoprost (n = 51) groups were compared with the control group (n = 57). There was no statistically significant difference between the groups in terms of age, gender, CCT, CV, ACV, 0 and 1 s dynamic pupillography measurements. There were statistically significant differences between the groups in terms of ACD, ACA, first NCTBUT, mean NCTBUT, meibography, scotopic, mesopic, photopic pupil sizes and dynamic pupillography values at 2, 4, 6, 8 and 10 s.
CONCLUSION:
This study demonstrated that the most commonly used antiglaucomatous agents increased ACD and ACA but did not affect other anterior segment structures, such as CCT, CV, or ACV. On the ocular surface, antiglaucomatous agents had significant negative effects. Meibography revealed adverse effects on the eyelids. Both first and mean NCTBUT were shortened. In pupillography, both static and dynamic pupil diameters were significantly smaller than those in the control group.
2026-04-08·JCI Insight
Lipidomic analysis reveals drug-induced lipoxin synthesis in glaucoma treatment
Article
作者: Trope, Graham ; Livne-Bar, Izhar ; Sivak, Jeremy M ; Zhang, Jenny Wanyu ; Maurya, Shubham ; Ho, Julian ; Mathew, David J ; Peters, Donna M ; Flanagan, John G ; Chan, Darren ; Buys, Yvonne M ; Gronert, Karsten ; Sit, Marisa
Synthetic prostaglandin analogs, such as latanoprost, are first-line treatments to reduce intraocular pressure (IOP) in the management of glaucoma, treating millions of patients daily. Glaucoma is a leading cause of blindness, characterized by progressive optic neuropathy, with elevated IOP being the sole modifiable risk factor. Despite this importance, the underlying latanoprost mechanism of action is still not well defined, being associated with both acute and long-term activities, and a growing list of ocular side effects. Prostaglandins are eicosanoid lipid mediators. Yet, there has not been a comprehensive assessment of small lipid mediators in glaucomatous eyes. Here, we performed a lipidomic screen of aqueous humor sampled from patients with glaucoma and healthy control eyes. The resulting signature was surprisingly focused on significantly elevated levels of arachidonic acid (AA) and its derivative, the antiinflammatory and cytoprotective mediator, lipoxin A4 (LXA4), in glaucomatous eyes. Subsequent experiments revealed that this response was drug induced, due to latanoprost actions on trabecular meshwork cells, rather than a consequence of elevated IOP. We demonstrate that increased LXA4 inhibited proinflammatory cues and promoted TGF-β production in the anterior chamber. In concert, an autocrine prostaglandin circuit mediated canonical rapid IOP lowering. This work reveals parallel mechanisms underlying acute and long-term latanoprost activities during glaucoma treatment.
176
项与 拉坦前列素 相关的新闻(医药)2026-05-06
·星狐说药
最新交易
2026年5月6日,拜耳正式宣布已与Perfuse Therapeutics达成最终协议,将以高达24.5亿美元的总对价全面收购这家专注于眼科缺血性疾病的临床阶段生物制药公司 1。此次交易的财务结构包括3亿美元的预付款,以及与后续临床开发、监管审批和商业化成功标准相挂钩的里程碑付款 1。通过此次收购,拜耳将获得Perfuse Therapeutics核心管线资产PER-001的全球完全所有权 1。PER-001是一种处于临床二期阶段的首创(First-in-class)小分子内皮素A受体(ETaR)拮抗剂,采用可生物降解的缓释玻璃体腔植入物(IVT)递送技术,主要用于治疗原发性开角型青光眼(POAG)和糖尿病性视网膜病变(DR),并具有向干性年龄相关性黄斑变性(AMD)扩展的潜力 4。
此次收购发生在拜耳制药业务面临重大战略转型的关键节点。该公司的绝对核心产品、抗血管内皮生长因子(VEGF)重磅炸弹药物Eylea(阿柏西普)正面临严峻的专利悬崖,其生物类似药预计将于2026年底在全球主要市场大规模上市,同时罗氏(Roche)的双靶点药物Vabysmo(法瑞西单抗)也在持续蚕食其市场份额 8。在这一背景下,拜耳对Perfuse的收购标志着其眼科战略的根本性转变:从单纯依赖抗血管生成途径和降低眼压(IOP)的对症治疗,全面转向以逆转眼部缺血和实现神经保护为核心的“疾病修饰”(Disease-modifying)疗法 2。
本报告将基于现有的临床数据、专利文献和市场动态,对此次数十亿美元级别的并购进行详尽的专业剖析,深入探讨PER-001所针对的病理生理机制、其活性药物成分(API)的化学分子架构与药效学特征、构筑极高商业壁垒的核心专利池、青光眼与视网膜血管疾病的竞争格局演变,并系统性地总结拜耳发起此次收购的深层战略动因。
病理生理学范式转换:超越眼压控制的局限
要准确评估PER-001的临床和商业价值,必须首先审视当前眼科核心适应症(特别是青光眼和糖尿病性视网膜病变)在标准治疗方案中存在的固有局限性。
当前青光眼临床管理的瓶颈
青光眼是一种进行性视神经病变,其病理特征是视网膜神经节细胞(RGCs)的加速凋亡和视网膜神经纤维层(RNFL)的进行性变薄,最终导致不可逆的视野丧失 3。作为全球第一大不可逆致盲眼病,青光眼目前影响着全球约7600至8000万人口,并且随着全球人口老龄化的加剧,预计到2040年这一数字将激增至1.12亿 3。
在过去的数十年中,青光眼的唯一临床治疗靶点是降低眼内压(IOP) 14。尽管眼压升高是青光眼发病和进展的首要危险因素,但大量的临床流行病学数据表明,高达30%的患者在通过局部药物(如滴眼液)或微创青光眼手术(MIGS)将眼压控制在统计学意义上的“正常”或目标水平后,其视神经损伤和视野恶化仍在持续发生 13。这一普遍存在的临床困境迫使眼科界开始深入探索独立于眼压之外的青光眼神经退行性病变机制。
目前的学术共识认为,眼部血管调节功能障碍以及由此引发的慢性眼部缺血,是导致视网膜神经节细胞(RGC)死亡的另一个核心驱动因素 16。在健康的眼部微环境中,血管自身的自动调节机制能够确保视神经乳头在全身血压或眼内压发生波动时,依然获得稳定的血液灌注。然而,在青光眼患者的眼球中,这种血管自动调节机制遭到破坏,导致视神经乳头处于慢性缺氧状态,进而引发氧化应激、炎症反应,并最终启动神经视网膜内的细胞凋亡级联反应 17。
内皮素通路的病理学驱动作用
在人体内,已知最强的内源性血管收缩剂是内皮素-1(ET-1),这是一种由21个氨基酸组成的多肽 7。多项独立的临床观察和基础研究一致表明,在青光眼、糖尿病性视网膜病变(DR)、视网膜静脉阻塞(RVO)和年龄相关性黄斑变性(AMD)等眼部缺血性疾病患者的眼内,ET-1的表达水平显著上调 3。
ET-1主要通过激活分布在视网膜和脉络膜微血管系统平滑肌细胞及周细胞上的内皮素A型()受体,来发挥其强烈的血管收缩和促炎作用 7。《ET_A》受体的激活会启动Gq蛋白偶联信号传导级联,导致细胞内钙离子释放并引起持续的细胞收缩 20。
在眼部病理环境中,ET-1的慢性升高会驱动一个多阶段的破坏性级联反应:在早期阶段,高水平的ET-1诱导严重的局部微血管收缩,导致眼部血流量急剧下降并破坏血管自动调节功能 16;在进入中期阶段后,由缺氧引起的局部缺血会触发强烈的炎症反应,导致RGC功能受损以及视野缺损的初步显现 7;在终末阶段,持续的缺血和微环境炎症最终导致不可逆的RGC凋亡、视网膜神经纤维层(RNFL)实质性变薄以及永久性的视力丧失 17。此外,ET-1还是神经血管病理学中的关键介质,能够进一步驱动新生血管的形成、血管渗漏以及组织纤维化 7。因此,通过高选择性地拮抗受体,治疗药物可以从源头上阻断这一病理级联反应,恢复正常的视神经乳头血流灌注,从而提供真正意义上的“疾病修饰”级神经保护——这是一种完全独立于房水动力学和眼压控制之外的全新机制 7。
PER-001的化学结构、物理化学特性与药效学分析
PER-001玻璃体腔植入物中的核心活性药物成分(API)是一种极具潜力、处于同类首创(First-in-class)地位的小分子内皮素受体拮抗剂,其通用名为Edonentan(在早期文献和化合物库中也被称为BMS-207940或化合物16a) 21。
分子架构与化学特征
Edonentan最初是在针对心血管适应症和肿瘤学应用(如肺动脉高压和前列腺癌)的全身性内皮素拮抗剂药物化学研发项目中合成并表征的 21。该分子是早期内皮素拮抗剂结构演变的产物,经过极其精密的药物化学优化,旨在实现对目标受体的超高亲和力和卓越的选择性 21。
Edonentan的分子架构以一个中心联苯核心为基础 26。在这个联苯系统的一个苯环上,连接着一个高度功能化的氨磺酰基部分,该部分进一步与一个4,5-二甲基异恶唑环相连。这种结构基序在高效的受体拮抗剂中非常常见,因为它能够在空间构象上高度模拟内源性肽类底物的结合几何形状,同时赋予分子对酶促降解的强大抵抗力 26。联苯系统的另一侧则含有一个恶唑环,而一个体积庞大的N,3,3-三甲基丁酰胺侧链则为分子提供了必要的空间位阻和高度的脂溶性,使其能够深深锚定并稳定在受体跨膜结构域的疏水结合口袋中 26。
根据计算得出的物理化学图谱,Edonentan的XLogP值为3.05,这表明该分子具有非常有利的脂溶性特征,不仅易于与细胞膜受体发生相互作用,而且能够长期、稳定地保留在疏水性的聚合物基质中而不易过快流失 21。此外,该分子拥有7个氢键受体、1个氢键供体,其拓扑极性表面积(TPSA)为118.04 ,这在小分子药物设计中属于高度优化的成药性参数 21。
药效学特征与极端选择性优势
将Edonentan与其他已上市的系统性内皮素拮抗剂(例如波生坦、马西腾坦或阿曲生坦)区分开来的最核心属性,是其前所未有的受体结合亲和力与极致的选择性图谱 20。
体外药理学和结合动力学测定明确表明,Edonentan对受体的抑制常数()达到了惊人的10 pM(皮摩尔级别) 22。更重要的是,它对受体的选择性比对受体的选择性高出80,000倍 27。这种极端的选择性在临床药理学上具有决定性的优势:虽然受体主要负责介导病理性的微血管收缩和细胞增殖,但受体则主要分布在内皮细胞上,并在生理上发挥着至关重要的保护作用。受体不仅负责促进循环中多余ET-1的清除,还介导一氧化氮(NO)和前列环素等血管舒张物质的释放 20。通过高选择性地避开并保留受体的功能,Edonentan能够在最大化其抗缺血疗效的同时,绝对不干扰机体天然的ET-1清除机制和内皮保护通路 20。
对于将其应用于眼科缓释植入物的场景而言,皮摩尔级别的超高活性显得尤为关键。当药物在长达六个月的时间内从聚合物基质中缓慢扩散时,玻璃体腔和视网膜局部的药物浓度不可避免地会随着时间推移而下降 7。然而,正是凭借这种超高的结合亲和力,即使在局部游离药物浓度降至极低水平的药代动力学末期,也足以确保几乎所有靶向的受体依然处于完全饱和与被深度拮抗的状态 27。
给药系统:PLGA玻璃体腔植入物工程
全身性(如口服)给予强效内皮素拮抗剂往往会引发显著的不良反应,包括体循环低血压、全身性水肿以及具有剂量限制性的肝毒性。这种肝脏毒性是该类药物众所周知的类别效应,以至于FDA要求对波生坦和马西腾坦等口服药物实施极其严格的风险评估与缓解策略(REMS)计划 20。
为了完全规避全身毒性,并精确地在病理部位(眼底)实现高浓度、高持久性的药物覆盖,Perfuse Therapeutics将PER-001精心设计为一种局部起效的、可持续释放的玻璃体腔(IVT)可生物降解植入物 7。该递送载体采用了聚乳酸-羟基乙酸共聚物(PLGA),这是一种在制药工业中经过高度验证、具有卓越生物可降解性和生物相容性的聚合物基质 7。PLGA技术在眼科领域拥有丰富的临床应用历史,它也是其他几款取得巨大商业成功的眼科缓释产品(例如地塞米松玻璃体腔植入物Ozurdex)的基础递送基质 7。
PER-001植入物的物理规格经过了高度的临床实用性优化。其长度仅为4.0毫米,总体积微乎其微,仅为0.36微升 7。该植入物通过一个带有滞留线的微创、一次性25G预装载针头施涂器进行注射,以确保药物能够被精确且安全地沉积在玻璃体腔的特定区域 7。
注射入眼内后,高密度的PLGA基质会在玻璃体腔的弱水性环境中缓慢发生水解,从而以受控的稳态速率释放出嵌入其中的Edonentan分子。广泛的临床前和临床药代动力学数据证实,这种独特的配方能够维持长达六个月的治疗性药物水平。这一突破从根本上颠覆了现有的治疗范式,将目前青光眼患者每天必须进行的频繁滴眼治疗,或是视网膜疾病患者每月必须忍受的眼内注射,彻底转变为极其便捷的每年仅需两次的常规干预 4。
临床疗效与安全性重磅数据:1/2a期试验深度分析
拜耳为Perfuse Therapeutics给出的高达24.5亿美元的并购估值,在很大程度上是基于PER-001在1/2a期临床试验中产生的具有颠覆性意义的数据集 1。对这些数据的深入解析,揭示了为何该资产被业内公认为青光眼治疗史上首款具有真正“疾病修饰”潜力的革命性疗法。
原发性开角型青光眼(POAG)队列的疗效突破
针对青光眼的1/2a期临床试验是一项多中心、随机、双盲(患者与阅片中心双盲)对照研究,旨在评估低剂量和高剂量PER-001植入物相对于假手术对照组在24周(6个月)内的安全性、耐受性和初步疗效 4。这项试验设计中最关键的一点是:所有入组患者均为患有轻至中度进行性青光眼的患者,并且在整个试验期间,他们被要求继续使用现有的标准化降低眼压(IOP)治疗方案。这意味着,在试验中观察到的由PER-001带来的任何结构或功能获益,都绝对是附加的,且完全独立于眼压调节途径之外 4。
该试验在三个决定新药获批的核心注册临床终点上(眼部血流、解剖结构和视觉功能),均取得了具有统计学意义和显著临床价值的改善。
1. 眼部血流灌注的全面恢复 血管灌注受损被认为是引发青光眼缺血性级联反应的始动因素 7。通过使用激光散斑血流成像图(LSFG)测量平均模糊率(MBR),研究人员发现,给予PER-001治疗后,患者视神经乳头组织的血流出现了快速且具有临床意义的显著增加 4。在注射后的第一周,就可以观察到血流的显著改善,并且这种改善在两个剂量组中都稳定地维持到了第24周试验结束时 4。这一强有力的数据在人体内提供了该药物作用机制的终极验证——证明局部的受体拮抗能够成功且持久地逆转视神经缺血 31。
2. 解剖结构的再生(视网膜神经纤维层改善) 在青光眼的病程中,视神经的结构性衰退传统上是通过光学相干断层扫描(OCT)测量视网膜神经纤维层(RNFL)的厚度来进行量化的 4。参与本试验的患者在入组前均有明确记录的进行性结构衰退病史,其历史RNFL变薄斜率平均差于或等于-0.92微米/年 17。
然而,在接受PER-001治疗24周后,治疗组患者的结构恶化轨迹被彻底逆转:
低剂量队列: 表现出RNFL厚度平均增加**+7.7微米/年** 4。
高剂量队列: 表现出RNFL厚度平均增加**+2.4微米/年** 4。
假手术对照组: 结构继续快速恶化,表现出RNFL厚度平均减少**-6.8微米/年** 4。
RNFL变薄的彻底逆转,标志着青光眼临床研究中一个史无前例的突破。这不仅表明RGC的凋亡进程被有效中止,更暗示了受损神经元细胞结构的潜在修复与再生。
3. 视觉功能的显著提升 任何眼科治疗的最终诉求都在于保留或恢复患者的视觉功能,这在临床上通常通过视野平均缺损(VF MD)这一指标进行量化评估 4。入组患者的历史视野进展斜率在-1.32至-0.30 dB/年之间,表明其视力处于持续且稳定的丧失过程中 17。
在施用PER-001后,视觉功能实现了极其显著的改善:
高剂量队列: 实现了**+1.5 dB/年**的功能改善斜率 4。
低剂量队列: 实现了**+1.1 dB/年**的功能改善斜率 4。
假手术对照组: 视力继续以**-1.2 dB/年**的速率加速丧失 4。
结构与功能的高度相关性验证 在2025年视觉和眼科研究协会(ARVO)年会上展示的最具科学说服力的发现,是PER-001所带来的结构改善与功能改善之间存在的高度相关性。统计学回归分析表明,RNFL厚度的增加与VF平均偏差的改善之间呈现出强烈的线性关系,其皮尔逊相关系数(Pearson Correlation Coefficient)高达0.721() 4。这一严密的统计学相关性无可辩驳地证实,患者所报告的功能性视力获益是直接源于客观的视神经解剖学修复。这一论据坚如磐石地确立了PER-001作为青光眼领域首个真正的疾病修饰剂的历史地位 14。
表 1:PER-001针对青光眼1/2a期试验的核心疗效与安全性数据摘要 4。
糖尿病性视网膜病变(DR)队列的疗效验证
与青光眼试验同步,Perfuse Therapeutics还对患有糖尿病性视网膜病变(DR)的患者进行了PER-001的临床评估 5。DR是糖尿病的严重微血管并发症,其病理驱动因素包括内皮细胞损伤、周细胞丢失,以及随之而来的黄斑缺血和微血管渗漏 12。
针对DR的2a期试验数据同样印证了在青光眼队列中观察到的巨大成功。在六个月的随访节点,PER-001治疗不仅改善了视网膜的结构完整性,还显著提升了视觉功能:
功能性获益: 接受治疗的患者在低亮度对比敏感度方面经历了具有临床意义的改善。在第20周测量时,高剂量组平均改善了+0.9 dB,低剂量组平均改善了+0.65 dB 12。
结构性修复: 超广角荧光素血管造影(UWFA)结果客观显示,PER-001成功逆转了结构性微血管损伤。与对照组病情持续恶化形成鲜明对比的是,PER-001治疗组在两个剂量下均显示出黄斑缺血指数的改善、黄斑渗漏总量的减少,以及黄斑区微动脉瘤绝对数量的显著降低 7。卓越的安全性与耐受性图谱
任何眼内玻璃体腔植入物的临床生命力都紧密维系于其安全性图谱。在这两项针对青光眼和DR的独立临床试验中,单次注射PER-001在长达24周的观察期内均展现出了极佳的安全性和高度的患者耐受性 4。这种精密的局部递送系统成功地绕过了口服内皮素拮抗剂所带来的所有全身性不良事件负担 7。
眼部不良事件极其轻微且罕见。在接受活性植入物治疗的27名患者中,仅有两例被判定为与药物相关的不良事件——两者均报告为轻度的玻璃体飞蚊症,且均在无需任何医疗干预的情况下自发消退 4。最为关键的是,在整个临床试验期间,完全没有发生任何眼内炎、严重的眼内炎症反应或视网膜血管炎的报告 4。患者的最佳矫正视力(BCVA)和眼内压在整个试验过程中保持高度稳定,进一步证实了该植入物在物理层面上没有对眼部组织造成机械性损伤,也没有诱发任何继发性的高眼压反应 17。核心专利池与知识产权护城河解析
在制药行业的并购估值模型中,目标公司知识产权(IP)组合的强度和生命周期是决定交易对价的核心基石 33。鉴于Edonentan(BMS-207940)的原始分子骨架是在二十多年前合成的,涵盖该母体分子的底层“物质组合物”(Composition-of-matter)专利很可能已经过期 21。为了构筑一个坚不可摧且持久的商业垄断壁垒,并使其完全配得上拜耳24.5亿美元的天价收购,Perfuse Therapeutics精心构建了一个高度复杂且精密的“二级”专利网络。该网络精准地聚焦于特殊药物制剂、创新递送系统以及最具价值的固态化学晶型专利 35。制剂工艺与缓释递送专利
保护PER-001商业价值的基础层知识产权,主要涉及特定活性成分与实现眼部长期缓释所需的精细可生物降解基质的完美结合。例如,专利US11786510B2及其国际同族专利WO2022232588A1(题为《用于治疗眼部疾病的药物组合物和玻璃体内药物递送系统》),以极具排他性的权利要求,明确保护了将内皮素受体拮抗剂(特别指定为Edonentan)包埋在专为玻璃体腔注射设计的固体、半固体或可固化植入物中的全部技术方案 35。
这些制剂专利的保护范围不仅宽泛,而且深入到PLGA基质的具体物理化学参数。权利要求中详细限定了乳酸与羟基乙酸的精准共聚比例、聚合物的特定分子量范围,以及为实现在100至180天(6个月)的时间跨度内,以靶向的皮摩尔浓度稳态释放Edonentan所必需的确切载药量浓度 23。通过对这种高度特定的释放动力学和植入物物理组成进行专利卡位,Perfuse非常有效地封死了任何潜在竞争对手试图将Edonentan开发成眼科缓释剂型的后路 35。固态化学与多晶型专利护城河
然而,真正让这个IP护城河固若金汤的,是专利公开号为US20230105507A1的文件。该专利精准保护了活性药物成分特定且高度稳定的结晶多晶型(Polymorph) 23。在制药生命周期管理(Lifecycle Management)中,多晶型专利被称为“常青树战略”(Evergreening)。因为同一个小分子药物可以结晶成不同的结构形态,而这些形态直接决定了药物的溶解度、稳定性以及体内释放曲线等关键药学指标。如果不使用特定的晶型,仿制药厂商根本无法复现原研药的缓释效果。
Perfuse Therapeutics的科学家成功开发并申请专利了一种被称为**无水结晶形式4(Anhydrous Crystalline Form 4)**的高度稳定固态分子构型 35。该专利强力主张并保护任何其中该化合物以晶型4存在的重量百分比达到90%以上的组合物 35。在法律和科学鉴定层面,该多晶型通过其独特的X射线粉末衍射(XRD)图谱进行了严格定义,其特征在于存在衍射角()为 、 和 的标志性吸收峰 35。此外,通过差示扫描量热法(DSC)分析确定,该特定晶型具有约$163^\circ\text{C}$的确切熔化温度()特征 35。
超长市场独占期预判
这一系列制剂工艺和多晶型专利的申请时间相对较晚,其优先权日期可追溯至2021年4月,并在2022年和2023年密集提交和公布 35。按照全球标准的自申请日起计算20年的专利保护期原则,除非遭遇极其罕见且极难成功的专利无效挑战,拜耳完全有理由预期,保护PER-001植入物核心商业利益的知识产权池将坚挺地维持效力直至2041年底或2042年 35。这条长达十几年的独占期跑道对拜耳而言具有致命的吸引力,它确保了该药物能够在没有任何仿制药价格战干扰的情况下,为一个长周期的、极高毛利率的重磅炸弹产品线源源不断地创造现金流。竞争格局的深度重塑与靶向缺血的新蓝海
要彻底理解拜耳为何愿意为Perfuse支付巨大的并购溢价,必须将PER-001置于当前青光眼和视网膜血管疾病市场广阔的竞争动态中进行审视 1。
青光眼市场:深陷同质化红海的困境
当前的POAG(原发性开角型青光眼)治疗市场可以说是一个高度拥挤且同质化的红海,所有现行疗法的唯一核心诉求依然停留在降低眼内压这一单一维度上 14。市场的主导地位被局部使用的前列腺素类似物(PGAs)滴眼液所占据,如拉坦前列素、曲伏前列素和比马前列素(艾伯维旗下的Lumigan) 37。即便是近期的所谓“创新”产品,也未能脱离降眼压的窠臼。例如,博士伦(Bausch & Lomb)推出的Vyzulta(拉坦前列素布诺)仅仅是通过增加一氧化氮(NO)供体机制,来略微增加通过小梁网的房水流出量而已 37。
在给药系统创新方面,各大公司的研发重点是将每天点滴的眼药水转化为可显著提高患者依从性的缓释植入物 38。Glaukos公司在2023年底获得了FDA的批准,推出了一款名为iDose TR的钛金属前房内曲伏前列素植入物,该产品可延长降眼压药物的释放时间 38。同样,艾伯维(AbbVie)也正在积极推广其可生物降解的比马前列素植入物Durysta 38。在研发管线中,还包括Ocuvex正在向FDA重新提交的新药申请产品PDP-716(一种缓释溴莫尼定剂型),以及Qlaris Bio的早期候选药物 37。
然而,一个残酷的临床现实是:上述所有已获批疗法或处于后期的管线产品,无一例外地都未能解决青光眼底层潜在的缺血和神经退行性病理学根源14。它们仅仅是针对一个极其复杂的神经血管综合征提供的物理机械性(降压)解决方案。虽然像通过间充质干细胞再生小梁网等先进的细胞疗法正处于临床前和早期临床开发阶段,但距离真正的商业化落地至少还有10到15年的漫长周期 38。
在这样的背景下,凭借其成功逆转视神经缺血并切实修复视网膜神经纤维层(RNFL)的过硬临床数据,PER-001在这个市场中显得鹤立鸡群,处于绝对的超然地位。它是目前全球范围内唯一一款拥有确凿人体临床验证数据支持的、独立于眼压之外的疾病修饰性神经保护剂 14。这一独特属性赋予了拜耳在青光眼“疾病修饰”领域的绝对垄断地位——这一细分市场直接针对数以千万计在眼压控制下依然走向失明的患者,其背后是一个巨大且完全未被满足的医疗需求蓝海 13。
表 2:不断演进的青光眼核心治疗管线与竞争格局对比 4。视网膜血管疾病市场:陷入重围的Eylea特许经营权
如果说青光眼代表着一个通过疾病修饰手段开启的广阔增量市场,那么在拜耳目前的内部战略版图中,最紧迫的防御性诉求则集中在视网膜血管疾病(尤其是湿性AMD和糖尿病性视网膜病变)市场 9。
历史上,拜耳的制药部门在很大程度上依赖于Eylea(阿柏西普)。这是一款由拜耳与再生元(Regeneron)联合开发的强效抗VEGF药物,在其鼎盛时期,全球峰值销售额曾逼近95亿美元的惊人高度 9。然而,这一曾经坚不可摧的特许经营权目前正遭受来自两个方向的致命夹击:
生物类似药的断崖式冲击: 保护标准2毫克剂型Eylea的核心专利即将到期或已经失效 8。在经历了旷日持久的专利诉讼之后,再生元和拜耳与一众虎视眈眈的生物类似药制造商(包括Alvotech/Teva的AVT06、诺华旗下的Sandoz、Formycon以及韩国的Celltrion)达成了妥协性定居协议。这些协议为生物类似药在2026年全面涌入全球主要市场铺平了道路 8。Celltrion和Alvotech均已蓄势待发,准备在2026年第四季度依据FDA的批准正式推出其低价位的生物类似药,这无疑将触发拜耳传统Eylea收入的断崖式雪崩 8。
下一代双靶点竞品的强力挤压: 罗氏(Roche)凭借其推出的Vabysmo(法瑞西单抗)——一种能够同时靶向抑制VEGF和血管生成素-2(Ang-2)的双特异性抗体,在极短的时间内成功抢占了大量市场份额(单年销售额已达43亿美元) 10。Vabysmo的核心竞争优势在于其卓越的持久性,它允许部分患者的给药间隔延长至长达四个月,相比之下,标准Eylea以及诺华较老的Lucentis等药物通常需要每月或每两月进行一次繁琐的眼内注射 11。
为了应对罗氏的攻势,拜耳和再生元联手推出了Eylea 8mg(高剂量版本),旨在对标Vabysmo长达四至五个月的给药间隔 11。在名为QUASAR的III期临床试验中,确实有超过60%的RVO患者在使用Eylea 8mg时能够在四个月的间隔期内维持病情稳定 42。然而,即便不断增加抗VEGF药物的剂量,其疗法在临床上依然面临着无法逾越的机制性天花板。市场调研数据冷酷地指出,大约43%在接受连续抗VEGF治疗的患者仍会出现突破性的视网膜积液或眼底出血;更糟糕的是,高达79%的临床医生承认,他们的患者在接受长期抗VEGF治疗后,极难长期维持早期获得的视力改善 44。
从病理学角度来看,抗VEGF疗法仅仅是在治疗下游的病理症状(如新生血管渗漏),却对导致疾病的上游根本原因(慢性视网膜缺血)束手无策 13。PER-001的出现,直接填补了这一病理机制上的巨大空白。通过完全独立于VEGF通路之外的机制,PER-001能够从源头上减轻视网膜缺血并逆转结构性渗漏。在未来的临床布局中,PER-001不仅可以作为早期DR患者的独立单药疗法,更有极大潜力成为Eylea 8mg的强效辅助治疗方案,用于攻克那些对抗VEGF产生耐药性的晚期复杂病例 12。
表 3:视网膜血管疾病领域的竞争格局与抗VEGF困境对比 10。
并购的深层战略动因逻辑
透过表象,拜耳对Perfuse Therapeutics的收购不仅是一次填补管线的常规操作,更是一堂融合了紧急防御需求与长期进攻性增长抱负的经典战略企业发展课 2。正如拜耳制药业务拓展与许可全球主管所阐述的那样,此次收购与公司致力于构建强大、具有跨时代意义的下一代眼科产品管线的宏伟承诺实现了天衣无缝的契合 1。
支撑这笔24.5亿美元天价估值的战略动因,可以系统地归纳为以下四个核心支柱:1. 填补Eylea断崖式下跌造成的巨大收入鸿沟
面对拜耳财报中核心抗凝血药物Xarelto(拜瑞妥)持续受到仿制药侵蚀的残酷现实,再加上Eylea在2026年第四季度即将迎来的生物类似药专利悬崖,拜耳的首席财务官及其制药部门最高管理层正承受着引入全新重磅资产的空前压力 9。尽管拜耳在肿瘤学领域的新型资产(如Nubeqa以及内部研发的KRAS/PRMT5抑制剂项目)表现出色,但肿瘤药物通常只针对高度细分、碎片化的目标患者群体 9。相比之下,PER-001横跨了青光眼和DR这两个拥有数千万患者群体的“超级重磅炸弹”适应症。它提供了一条高度可信且极具爆发力的商业变现路径,能够强有力地抵消拜耳即将面临的传统产品收入急剧萎缩 3。2. 引领治疗范式向“疾病修饰”维度跨越
拜耳的管理层极其敏锐地认识到,在一个日趋拥挤且高度同质化的市场中,仅仅在“降低眼压”或“抑制VEGF”上进行微小的渐进式改良,其商业回报正呈现边际递减的趋势 43。通过收购业内唯一一款经过严格临床证实、能够通过非IOP依赖性机制逆转视神经损伤并实质性改善视野的药物,拜耳瞬间在整个青光眼赛道上实现了对竞争对手的降维打击 3。拥有推广一款“疾病修饰”(Disease-modifying)疗法的特权——这个概念此前几乎专属用于描述革命性的肿瘤或神经系统药物——将赋予拜耳在未来定价谈判中极高的话语权,并有能力在眼科界彻底确立一套全新的护理与治疗金标准 4。3. 通过双重验证的机制与平台大幅降低临床开发风险
尽管PER-001在眼科的应用是极其新颖的,但从药物开发科学的角度来看,其底层组件的风险已被极大程度地稀释。首先,内皮素拮抗剂是一个在生物学上经过几十年深入研究和验证的成熟通路,其在治疗肺动脉高压(PAH)等全身性疾病中积累了如山的临床数据 17。其次,活性分子Edonentan本身也是一个物理化学属性被极度了解的成熟化合物 21。最后,其搭载的PLGA聚合物基质递送系统更是业界公认的黄金标准,与在全球数百万次眼内注射中安全使用的递送系统(如Ozurdex)在材料学上毫无二致 7。
Perfuse Therapeutics的绝妙之处在于:将一个被充分验证的生物学机制与一个被充分验证的递送载体巧妙结合,从而以远低于早期生物技术资产常规极高折损率的风险,硬生生“拼装”出了一个具有重磅潜力的全新药物。在1/2a期试验中观察到的近乎完美的安全性图谱——最显著的标志是眼内严重炎症记录保持为零——无疑为这一极低的去风险化(De-risked)投资模型提供了最强有力的背书 4。4. 俘获具有平台级延展价值的缓释递送技术
在这笔交易中,拜耳获得的绝不仅仅是PER-001这一个孤立的资产。更具长远战略意义的是,拜耳顺势将Perfuse专有的玻璃体腔持续缓释平台技术完整地收入囊中 3。拜耳可以利用这项世界顶级的PLGA高分子工程技术,为其自身正在研发的其他内部管线项目开发连续释放制剂。例如,拜耳可以尝试将其应用于未来的抗VEGF分子,创造出超长效的竞品;或者,拜耳可以将自身管线中原本口服的神经保护性可溶性鸟苷酸环化酶激活剂(如runcaciguat),完美整合到这种局部长效缓释植入物中,从而衍生出一个庞大的、具有主导地位的眼科缓释生态系统 43。未来临床管线推进展望
在此次收购最终通过标准的反垄断审查并获得Perfuse股东的正式批准后,拜耳预计将利用其庞大的全球研发资源,极其激进地全速推进PER-001的后续临床开发步伐 2。
在即刻执行的短期规划中,拜耳将主导针对青光眼适应症的、具有注册关键性意义的2b/3期临床试验,该项目预计将于2025年下半年正式启动 4。考虑到在2a期试验中,结构性RNFL修复与功能性VF视力提升之间展现出了极为强悍且极其罕见的线性相关性,拜耳的医学事务团队极有可能会采用创新的自适应临床试验设计(Adaptive Trial Design),以便将这份2b期临床数据直接定位为支持未来全球监管注册(NDA)所需的两项关键临床研究之一,从而大幅缩短上市时间窗口 14。
与此同时,预计拜耳将依托其在全球视网膜专家网络中深厚的人脉资源和庞大的临床试验基础设施,将针对糖尿病性视网膜病变(DR)的患者队列迅速推进至更大规模的多中心关键性试验阶段 3。此外,正如Perfuse原管理层此前公开阐明的那样,鉴于PER-001靶向的是导致多种眼病的底层“缺血性”病理基础,这为将其临床探索范围迅速扩展到干性年龄相关性黄斑变性(AMD)提供了极其坚实的科学依据。在这个缺乏有效治疗手段、且神经血管保护需求迫在眉睫的灾难性致盲疾病领域,PER-001同样具备改变游戏规则的巨大潜力 6。结论
总而言之,拜耳对Perfuse Therapeutics的收购并非一次简单的资产扩充,而是一次能够从根本上重塑其在全球眼科领域未来十年战略轨迹的史诗级商业操作 1。在Eylea专利悬崖即将引发剧烈收入震荡的严峻生存挑战下,拜耳摒弃了在旧有赛道上的微创新,选择果断出击,将一款极具颠覆性和范式转换意义的核心资产一举拿下 8。
通过其高活性的专属核心成分Edonentan(BMS-207940),PER-001像一把手术刀般精准切入了神经血管眼科疾病底层的缺血病因学 7。借助高度精密工程化的六个月长效缓释PLGA植入物技术,该疗法通过强效拮抗受体,成功地在源头上斩断了缺氧、炎症和神经细胞凋亡的死亡循环 7。其产出的临床数据具有划时代的历史意义:它是人类眼科史上首个在青光眼患者群体中,证明能够产生强烈的、具有统计学意义的解剖学结构修复(RNFL厚度再生)和视觉功能恢复(视野偏差改善)双重逆转的革命性疗法 4。
在坚固的多晶型专利和聚合物配方专利长达数十年(持续至2040年代)的铁壁保护下,PER-001已做好充分准备,在“疾病修饰”级青光眼这一广阔的蓝海市场中建立起绝对的长期垄断霸权 35。同时,它为治疗糖尿病性视网膜病变提供了一条截然不同于VEGF的全新通道,直击当前市场主导者无法克服的机制软肋 11。归根结底,这笔高达24.5亿美元的战略并购,不仅为拜耳构筑了一道足以抵御专利悬崖狂风暴雨的坚固防御墙,更赋予了整个组织在未来几十年内,在全球眼科治疗标准制定上绝对的话语权和进攻性主导地位。Works cited
Bayer to acquire Perfuse Therapeutics for $2.45B, accessed May 6, 2026, https://breakingthenews.net/Article/Bayer-to-acquire-Perfuse-Therapeutics-for-dollar2.45B/66228587
Bayer to acquire Perfuse Therapeutics to complement ..., accessed May 6, 2026, https://www.bayer.com/media/en-us/bayer-to-acquire-perfuse-therapeutics-to-complement-ophthalmology-pipeline/
Bayer to Acquire Perfuse Therapeutics to Complement Ophthalmology Pipeline, accessed May 6, 2026, https://lasvegassun.com/news/2026/may/06/bayer-to-acquire-perfuse-therapeutics-to-complemen/
Perfuse Therapeutics Announces Positive Results from the ..., accessed May 6, 2026, https://perfusetherapeutics.com/perfuse-therapeutics-announces-positive-results-from-the-completed-phase-1-2a-clinical-trial-of-per-001-intravitreal-implant-in-patients-with-glaucoma/
Bayer to acquire Perfuse Therapeutics for up to $2.45 billion, accessed May 6, 2026, https://www.investing.com/news/company-news/bayer-to-acquire-perfuse-therapeutics-for-up-to-245-billion-93CH-4661768
Perfuse Therapeutics Announces Positive Results from Phase 2 Clinical Trials in Glaucoma and Diabetic Retinopathy Patients - PR Newswire, accessed May 6, 2026, https://www.prnewswire.com/news-releases/perfuse-therapeutics-announces-positive-results-from-phase-2-clinical-trials-in-glaucoma-and-diabetic-retinopathy-patients-302488857.html
PER-001, A Novel, Long-Acting Endothelin Antagonist IVT Implant for the Treatment of Retinal Ischemia in Glaucoma, DR, and AMD - Perfuse Therapeutics, accessed May 6, 2026, https://perfusetherapeutics.com/wp-content/uploads/Perfuse-Thx-CTS_FINAL-2.pdf
Alvotech's Deal with Regeneron, Bayer Clears Way for Eylea Biosimilar in Multiple Markets, accessed May 6, 2026, https://www.market-scope.com/pages/news/8951/alvotech-s-deal-with-regeneron-bayer-clears-way-for-eylea-biosimilar-in-multiple-markets
Bayer readies for increased Eylea headwinds, cuts early cancer assets - FirstWord Pharma, accessed May 6, 2026, https://firstwordpharma.com/story/6528460
Partners Alvotech, Teva eye 2026 Eylea biosimilar launch - Fierce Pharma, accessed May 6, 2026, https://www.fiercepharma.com/pharma/partners-alvotech-teva-eye-2026-eylea-biosimilar-launch-us-regeneron-settlement
After FDA says no, Bayer bags EU nod for twice-yearly Eylea - pharmaphorum, accessed May 6, 2026, https://pharmaphorum.com/news/after-fda-says-no-bayer-bags-eu-nod-twice-yearly-eylea
Perfuse Therapeutics shares findings from glaucoma and diabetic retinopathy trials of PER-001 | Ophthalmology Times Europe, accessed May 6, 2026, https://europe.ophthalmologytimes.com/view/perfuse-therapeutics-shares-phase-2-clinical-findings-from-glaucoma-and-diabetic-retinopathy-trials-of-per-001
Perfuse Therapeutics Announces Positive Results from Phase 2 Clinical Trials in Glaucoma and Diabetic Retinopathy Patients, accessed May 6, 2026, https://perfusetherapeutics.com/perfuse-therapeutics-announces-positive-results-from-phase-2-clinical-trials-in-glaucoma-and-diabetic-retinopathy-patients/
Perfuse Therapeutics Announces Positive Results from the Completed Phase 1/2a Clinical Trial of PER-001 Intravitreal Implant in Patients with Glaucoma - PR Newswire, accessed May 6, 2026, https://www.prnewswire.com/news-releases/perfuse-therapeutics-announces-positive-results-from-the-completed-phase-12a-clinical-trial-of-per-001-intravitreal-implant-in-patients-with-glaucoma-302446082.html
Glaucoma & Optic Neuropathies - Ora Clinical, accessed May 6, 2026, https://oraclinical.com/glaucoma-optic-neuropathies/
Pipeline - Perfuse Therapeutics, accessed May 6, 2026, https://perfusetherapeutics.com/pipeline/
PER-001, an Endothelin Antagonist, Increased Optic Nerve Head ..., accessed May 6, 2026, https://perfusetherapeutics.com/wp-content/uploads/Perfuse-ARVO-FINAL.pdf
PER-001 - Drug Targets, Indications, Patents - Patsnap Synapse, accessed May 6, 2026, https://synapse.patsnap.com/drug/240be233dad643f4a2acc5d5d15cd16b
Bayer to Acquire Perfuse Therapeutics to Complement Ophthalmology Pipeline, accessed May 6, 2026, https://www.barchart.com/story/news/1732176/bayer-to-acquire-perfuse-therapeutics-to-complement-ophthalmology-pipeline
Endothelin receptors: what's new and what do we need to know? - PMC, accessed May 6, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC2828166/
edonentan | Ligand page | IUPHAR/BPS Guide to PHARMACOLOGY, accessed May 6, 2026, https://www.guidetopharmacology.org/GRAC/LigandDisplayForward?ligandId=13015
Edonentan (BMS 207940) | Endothelin Receptor Antagonist | MedChemExpress, accessed May 6, 2026, https://www.medchemexpress.com/edonentan.html
Polymeric Technologies for Retinal Drug Delivery, accessed May 6, 2026, https://retinalphysician.com/issues/2024/april/polymeric-technologies-for-retinal-drug-delivery/
Biphenylsulfonamide Endothelin Receptor Antagonists. 4. Discovery of N-[[2'-[[(4,5-Dimethyl-3-isoxazolyl)amino]sulfonyl]-4-(2-oxazolyl)[1,1'-biphenyl]- 2-yl]methyl]-N,3,3-trimethylbutanamide (BMS-207940), - ACS Publications, accessed May 6, 2026, https://pubs.acs.org/doi/10.1021/jm020289q
Endothelin-1 axes in the framework of predictive, preventive and personalised (3P) medicine - PMC, accessed May 6, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC8334338/
Edonentan | C28H32N4O5S | CID 156690 - PubChem - NIH, accessed May 6, 2026, https://pubchem.ncbi.nlm.nih.gov/compound/Edonentan
BMS-207940 = 98 HPLC 210891-04-6 - Sigma-Aldrich, accessed May 6, 2026, https://www.sigmaaldrich.com/US/en/product/sigma/bm0014
219208Orig1s000 INTEGRATED REVIEW - accessdata.fda.gov, accessed May 6, 2026, https://www.accessdata.fda.gov/drugsatfda_docs/nda/2025/219208Orig1s000IntegratedR.pdf
Full article: May 2025 therapeutic delivery: industry update - Taylor & Francis, accessed May 6, 2026, https://www.tandfonline.com/doi/full/10.1080/20415990.2025.2533109
PER-001, an endothelin antagonist, increased optic nerve head blood flow with structural and functional improvements in patients with glaucoma | IOVS, accessed May 6, 2026, https://iovs.arvojournals.org/article.aspx?articleid=2804867
Perfuse Therapeutics Announces Positive Results from the Completed Phase 1/2a Clinical Trial of PER-001 Intravitreal Implant in Patients with Glaucoma - BioSpace, accessed May 6, 2026, https://www.biospace.com/press-releases/perfuse-therapeutics-announces-positive-results-from-the-completed-phase-1-2a-clinical-trial-of-per-001-intravitreal-implant-in-patients-with-glaucoma
Perfuse Therapeutics Announces Positive Results from Phase 2 Clinical Trials in Glaucoma and Diabetic Retinopathy Patients | Stories - University of Liverpool, accessed May 6, 2026, https://www.liverpool.ac.uk/celt-global-health/global-news/stories/title,1521132,en.php
slrn-20241231 - SEC.gov, accessed May 6, 2026, https://www.sec.gov/Archives/edgar/data/1962918/000196291825000022/slrn-20241231.htm
Australian Official Journal of Patents - IP Australia, accessed May 6, 2026, https://pericles.ipaustralia.gov.au/ols/epublish/content/olsPatentsPdfDownload?id=1161
WO2022232588A1 - Pharmaceutical compositions and intravitreal drug delivery systems for the treatment of ocular diseases - Google Patents, accessed May 6, 2026, https://patents.google.com/patent/WO2022232588A1/he
WO2002032884A2 - Methods for the preparation of biphenyl isoxazole sulfonamides - Google Patents, accessed May 6, 2026, https://patents.google.com/patent/WO2002032884A2/zh
Glaucoma - Competitive Landscape, 2026 - Research and Markets, accessed May 6, 2026, https://www.researchandmarkets.com/reports/5782338/glaucoma-competitive-landscape
Transforming Glaucoma Care: A 2026 Clinical Update - Mivision Education, accessed May 6, 2026, https://www.mieducation.com/pages/transforming-glaucoma-care-a-2026-clinical-update
The 2026 Glaucoma Pipeline - Review of Ophthalmology, accessed May 6, 2026, https://www.reviewofophthalmology.com/article/the-2026-glaucoma-pipeline
Perfuse Therapeutics Announces Positive Visual, Structural and Safety Data from a Ph1/2a Trial of PER-001 in Glaucoma Patients at the American Glaucoma Society Meeting - BioSpace, accessed May 6, 2026, https://www.biospace.com/press-releases/perfuse-therapeutics-announces-positive-visual-structural-and-safety-data-from-a-ph1-2a-trial-of-per-001-in-glaucoma-patients-at-the-american-glaucoma-society-meeting
Bayer Buys US Drugmaker Perfuse for as Much as $2.45 Billion (1), accessed May 6, 2026, https://news.bloomberglaw.com/ip-law/bayer-acquires-us-drugmaker-perfuse-for-as-much-as-2-45-billion
Eylea™ 8 mg approved in the EU for third retinal indication - Bayer Global, accessed May 6, 2026, https://www.bayer.com/media/en-us/eylea-8-mg-approved-in-the-eu-for-third-retinal-indication/
Eyes wide open: Biopharma offers new hope across the spectrum of ophthalmic conditions, accessed May 6, 2026, https://www.alacrita.com/blog/emerging-ophthalmology-therapies-2025
A turning point in retinal vascular disease care? - Eylea, accessed May 6, 2026, https://ophthalmology.bayer.com/sdc
Bayer Accelerates Pharma Growth on High-Value Portfolio, accessed May 6, 2026, https://www.bayer.com/en/us/news-stories/accelerating-pharma-growth-on-high-value-portfolio
Bayer's strongest-ever pharma portfolio and promising pipeline drive future growth, accessed May 6, 2026, https://www.bayer.com/media/en-us/bayers-strongest-ever-pharma-portfolio-and-promising-pipeline-drive-future-growth/
Glaucoma | Clinical | Ophthalmology Times Europe, accessed May 6, 2026, https://europe.ophthalmologytimes.com/clinical/glaucoma
Macitentan: First Global Approval - ResearchGate, accessed May 6, 2026, https://www.researchgate.net/publication/259115027_Macitentan_First_Global_Approval
Endothelin: 30 Years From Discovery to Therapy | Hypertension, accessed May 6, 2026, https://www.ahajournals.org/doi/10.1161/hypertensionaha.119.12105
Bayer to Acquire Perfuse Therapeutics, Gaining Anti-VEGF Sustained-Release Formulation, accessed May 6, 2026, https://www.geneonline.com/bayer-to-acquire-perfuse-therapeutics-gaining-anti-vegf-sustained-release-formulation/
Bayer to buy Perfuse Therapeutics in up to $2.45 billion deal By Reuters - Investing.com, accessed May 6, 2026, https://www.investing.com/news/stock-market-news/bayer-to-buy-perfuse-therapeutics-in-up-to-245-billion-deal-4661845
2026-04-26
「机构眼·调研内参」机构投研资源平台
加入社群·微信:Buddha_Research
机构音频纪要 部分转译展示
发言人 问:2026年中国青光眼治疗药物市场的发展动向是怎样的?
未知发言人 答:随着国产替代加速推进和精准治疗理念深化,青光眼治疗药物市场正迎来新的变革。投报研究院的研究表明,青光眼治疗药物以降低眼压为核心目标,前列腺素类、贝塔受体阻滞剂及碳酸酐酶抑制剂等品种在临床中广泛应用。随着患者依从性和安全性要求提升,长效制剂、固定复方制剂以及新作用机制药物受到关注。预计在老龄化进程加快和疾病筛查意识提升背景下,青光眼治疗药物需求将稳步增长,到2030年市场规模将达到222亿元人民币。
发言人 问:青光眼治疗药物的核心分类有哪些?
未知发言人 答:青光眼治疗药物的核心分类主要为降低眼压类和视神经保护类。其中,降低眼压类药物是临床主流用药,包括贝塔肾上腺素受体阻滞剂、碳酸酐酶抑制剂、L方法肾上腺素受体激动剂等通过不同机制降低眼内压。视神经保护类药物则是辅助治疗方向,这类药物通过干预视神经损伤通路,保护视网膜神经节细胞及视神经纤维,延缓或阻止视力减退。
未知发言人 问:青光眼治疗药物行业发展历程如何?
未知发言人 答:青光眼治疗药物行业的发展历程可追溯至19世纪中期,历经萌芽期(19世纪中期至20世纪初)、启动期(20世纪50年代至70年代)和高速发展期(2010年后)。19世纪中期至20世纪初,首个缩瞳药毒扁豆碱被发现并用于青光眼治疗。20世纪50年代至70年代,碳酸酐酶抑制剂、肾上腺素能激动剂等相继上市,但副作用明显。2010年后,本土企业加大研发投入,国产药物实现规模化供应,并伴随创新药的研发,行业进入快速发展阶段。
发言人 问:中国青光眼患者规模如何?
未知发言人 答:根据市场数据,中国40岁以上人群青光眼患病率为2.3%,60岁以上人群患病率提升至2.6%。随着人口老龄化进程持续加深,中国青光眼患者数量不断上升。
未知发言人 问:中国居民日均屏幕使用时间的变化情况是怎样的?
未知发言人 答:中国居民日均屏幕使用时间已由2021年的约5.5小时增长至2024年的8小时。
发言人 问:长时间屏幕使用对青光眼的影响是什么?
发言人 答:长时间屏幕使用推高了整体发病风险,并导致青光眼患病人群呈现年轻化趋势。
未知发言人 问:中国青光眼患病人数的情况如何?
未知发言人 答:中国青光眼患病人数从2020年的199万人增长至2025年的216万人,年复合增长率约为1.7%,预计到2030年将达到230万人。
发言人 问:医保谈判对青光眼药物市场有何影响?
发言人 答:拉坦前列素等主流药物通过国家医保谈判后纳入医保目录,显著降低了患者用药负担。
未知发言人 问:青光眼治疗药物市场规模的增长驱动因素有哪些?
未知发言人 答:市场规模增长的核心驱动因素包括患者人数增长、就诊意识提升以及医保政策持续利好。
未知发言人 问:青光眼筛查费用的变化及其对就诊意向的影响是什么?
未知发言人 答:随着医保政策调整,青光眼筛查费用将降至约25至50元,这将大幅提升眼部不适人群的就诊意愿。
未知发言人 问:青光眼早期筛查的技术进步如何?
发言人 答:AI驱动下,青光眼早期筛查取得进展,例如搭载先进识别算法的便携式裂隙灯系统,对前方角狭窄的识别准确率可达85%。
未知发言人 问:仿制药一致性评价与集采政策如何影响青光眼治疗药物市场?
未知发言人 答:仿制药一致性评价与集采政策推动了市场规模放量增长,国产青光眼治疗药物进入集采体系后,终端价格大幅下降,减轻了患者长期用药负担。
未知发言人 问:青光眼治疗药物产业链各环节现状如何?
发言人 答:产业链上游主要由API生产企业、关键中间体供应商及药用辅料企业组成,其中API生产环节技术壁垒最高;中游涉及制剂生产与质量检测,部分本土企业已具备规模化生产能力;下游为医药销售与终端应用环节,医院和零售渠道共同构成主要应用场景。
发言人 问:青光眼药物产业链上游现状具体是怎样的?
发言人 答:上游环节中,活性药物成分API生产企业面临高技术壁垒和严苛的质量标准,尤其是拉坦前列素和它氟前列素等原料药的研发投入大且周期长。
未知发言人 问:青光眼药物市场竞争格局及国产药物表现如何?
发言人 答:市场竞争格局中,前列腺素类似物占据主导地位,国产药物凭借价格优势与稳定疗效市场份额持续增长,尤其齐鲁制药的复方制剂拉坦前列素已逐渐打破市场垄断,中国青光眼治疗药物自给率显著提升。
发言人 问:青光眼药物销售渠道的变化趋势是什么?
发言人 答:医院端销售额长期占主导,但自2024年以来有所下滑,实体零售渠道和电商渠道销售额增长,慢病管理向线上化迁移,同时国产药物通过一致性评价并进入集采目录,市场竞争力增强。
发言人 问:中国青光眼治疗药物行业的竞争格局是怎样的?当前青光眼治疗药物市场的主要竞争态势如何?
发言人 答:中国青光眼治疗药物领域早期由外资垄断,但随着2020年中国青光眼指南的发布,沈阳新奇、兆科眼科、齐鲁制药等本土企业崛起。竞争格局大致分为三个梯队:第一梯队由沈阳新奇、赵珂、广州简科、齐鲁制药等企业组成,凭借针对性产品线布局和医药背景占据领先地位;第二梯队如成都恒瑞、苏州欧康等,关注创新研发能力提升;第三梯队为石家庄四药、山东陈新等中小型药企,产品种类相对单薄,多聚集于区域市场或特定细分领域。前列腺素类滴眼液在中国市场占据约60%份额,主导传统治疗赛道。外资企业如爱尔康旗下的萘他舒德尔滴眼液,凭借先发优势和高效能持续发力。同时,本土企业通过新机制联合创新剂型重塑青光眼治疗逻辑,并加速转型,例如兆科眼科、康哲药业等企业的青光眼创新药已进入三期临床或提交上市申请阶段。
未知发言人 问:国内青光眼治疗药物领域的核心企业竞争力对比是怎样的?
发言人 答:沈阳兴齐眼药综合排名第一,拥有7款上市产品和1款在研产品,医保覆盖5款;兆科眼科排名第二,拥有6款上市产品和1款在研产品;成都恒瑞并列第三,拥有8款在研产品。此外,从研发投入强度、技术平台与创新能力、管线差异与适应症覆盖等多个维度进行对比分析,这些企业各自展现出不同的竞争优势和发展路径。
未知发言人 问:青光眼治疗药物行业未来的发展趋势和潜在挑战是什么?
未知发言人 答:未来,中国青光眼治疗药物行业发展趋势将从单一降眼压向多靶点综合干预转变,注重神经保护作用以延缓神经损伤进程。药物研发将聚焦新机制和新靶点,探索个体化和精准用药方案,以应对不同患者特征和疾病进展的差异性需求。同时,行业将面临产品结构集中度高、市场竞争加剧、政策环境变化及创新药研发不确定性等挑战。
未知发言人 问:2025年青光眼治疗的主要趋势是什么?复方制剂在青光眼治疗中的优势体现在哪些方面?
发言人 答:2025年青光眼治疗将以丹药为主,并根据疗效逐步过渡至二联及以上治疗方案,其中三联及四联治疗比例合计为6.6%。治疗强度与疾病严重程度之间呈现良好匹配。复方制剂因其整合了两种或多种作用机制互补的药物,能显著简化用药方案、减少每日滴眼次数,有效解决患者因遗忘用药导致的治疗依从性下降问题。同时,复方制剂的标准化配比有助于避免不规范联合用药带来的剂量叠加风险,使其在平衡疗效、安全性与用药便捷性上具有明显优势,成为慢性青光眼长期管理的优选方案。
未知发言人 问:中国青光眼治疗药物行业当前面临哪些挑战与风险?
未知发言人 答:行业面临的挑战与风险包括:研发层面整体原始创新能力不足,多数产品为仿制药;国际市场布局存在差距,特别是在长效缓释制剂及联合治疗方案方面;临床试验周期长、成本高、失败风险大;供应链上部分原料依赖进口,国际贸易环境和原材料价格波动会影响成本控制;市场竞争中,外资企业在品牌认知、学术推广和医生用药习惯上有较强优势,而国内企业在中低端市场面临激烈价格竞争,尤其是随着集中带量采购和地方招采制度推进,价格战进一步压缩行业利润空间;此外,渠道建设和学术推广成本上升,市场推广周期较长,投资回报节奏较慢。
发言人 问:行业发展影响因素中有哪些积极因素?
发言人 答:积极因素包括新型手术植入物通过提升手术安全性并前移干预时点,降低药物依赖性,以及新型检测方法推动青光眼诊断前移与精准分型,扩大了药物治疗人群并延长干预周期,从而对药物市场形成持续扩容效应。手术治疗领域的创新,如微创青光眼手术,创伤小、并发症少且能覆盖更广泛的患者群体,有望减少术后药物使用,进而影响药物市场的规模。同时,微创青光眼手术领域的投融资活动活跃,表明资本对该领域的关注热度上升,未来可能有更多新技术和产品进入市场,加剧市场竞争。
2026-04-21
👂 耳科:从“听力辅助”迈向“生物学修复”
基因治疗改写耳聋结局:针对OTOF基因突变导致的先天性深度耳聋,基因疗法已从实验室走向临床应用,在《新英格兰医学杂志》上发表了最新进展,为遗传性耳聋的根治带来了希望。
“老药新用”开辟新径:研究证实,肾素-血管紧张素系统抑制剂(如ARB类降压药)能通过抗炎抗氧化机制保护内耳,有望成为治疗听力损失、耳鸣和眩晕的新型药物。
梅尼埃病治疗精准化:用于青光眼的药物拉坦前列素,经鼓室内注射后,可显著改善梅尼埃病患者的听力、耳鸣和眩晕症状,实现了不同疾病之间的药物跨界应用。
AI辅助耳硬化症手术:在镫骨手术中,术中使用皮质类固醇能显著改善患者听力与平衡功能,而结合机器学习算法,可预测治疗效果,为个性化治疗提供了新依据。
内耳靶向给药突破:Fraunhofer研究所正研发一种通过3D打印制成的可降解药物植入物,可精准、持续地将药物直接释放到内耳,显著提高疗效并减少全身副作用。
再生疗法曙光初现:针对感音神经性听力损失,SPI-1005已获FDA突破性疗法认定;同时,基于细胞的再生疗法(如Rinri Therapeutics)也已进入人体试验阶段。
新靶点探索:细胞外囊泡(EVs)展示了其在早期诊断和治疗感音神经性听力损失方面的巨大潜力,可通过抗炎和神经保护作用促进耳蜗修复。
耳镜检查新工具:人工智能工具可帮助初级保健医生准确区分急性中耳炎、渗出性中耳炎及鼓膜正常状态,提升诊断效率。
👃 鼻科:精准靶向,引领慢性病治疗变革
首个AFRS靶向药问世:度普利尤单抗获FDA批准用于治疗变应性真菌性鼻窦炎(AFRS),成为该难治性疾病的首个获批靶向药物,III期临床数据显示其能显著缩小鼻息肉并改善鼻窦混浊。
长效生物制剂带来便利:德莫奇单抗(易适来) 在中国获批用于治疗慢性鼻窦炎伴鼻息肉(CRSwNP),因其“每年仅需两针”的超长效特点,有望重新定义治疗标准。
TSLP靶点成为热点:
特泽利尤单抗作为全球唯一获批的TSLP单抗,已在中国获批用于治疗CRSwNP和哮喘。研究证实,它能显著改变鼻息肉中669个基因的表达,从而减轻炎症、恢复上皮健康。
另一TSLP受体拮抗剂Verekitug在II期试验中表现优异,只需每12周给药一次,为患者提供了更便捷的治疗选择。
慢性鼻炎微创治疗升级:阻抗控制的多点射频消融治疗慢性鼻炎,在随机、假手术对照试验中展现显著疗效,73.3%的患者的总体症状评分改善超30%。
传统疗法价值再挖掘:一项对546名患者的研究证实,日本的咽部擦刷疗法(EAT) 对慢性鼻咽炎有快速且持久的疗效,症状改善率达79.5%,局部体征改善率达87.7%。
🗣️ 咽喉科:技术革新与再生探索
“可视化”声带注射:短波红外(SWIR)成像技术能实时、清晰地显示声带注射物位置,有望变革声带注射填充术,提升手术精准度。
声带再生迈出关键一步:研究绘制了声带中干细胞样细胞的详细图谱,揭示了不同亚型的再生潜力,为开发声带修复疗法提供了新的分子靶点。
“音乐疗法”的抗癌潜力:研究发现,让喉癌细胞接受类似声带振动的物理刺激,可显著降低其恶性程度。这种“机械干预”与靶向药联用,可能成为喉癌治疗的全新策略。
声带麻痹康复新策略:临床研究证实,对预后不良的单侧声带麻痹患者早期进行喉肌电图评估并联合嗓音训练,能显著改善声门闭合和嗓音质量,并可能降低手术需求。
关注术后睡眠呼吸暂停:研究提示,喉癌术后患者出现阻塞性睡眠呼吸暂停(OSA)的风险很高(该研究中的10名患者术后均出现OSA),术后需警惕OSA的发生。
🧬 头颈肿瘤:免疫治疗领衔,多模式协同
免疫治疗前移至新辅助阶段:在局部晚期头颈鳞癌(LAHNSCC)中,术前进行免疫联合化疗,能显著提升病理完全缓解率(pCR),从而提高器官保留率。
新兴疗法百花齐放:复发/转移性HNSCC的治疗正迎来双特异性抗体、HPV治疗性疫苗、抗体偶联药物(ADC) 等多种新策略的快速发展。
中国力量在国际舞台崭露头角:在ICHNO 2026大会上,中国的ADC药物SYS6043(靶向B7-H3)公布了治疗晚期鼻咽癌的积极数据,客观缓解率达41.4%。
精准医疗指导治疗决策:除了PD-L1等传统标志物,三级淋巴结构、组织驻留记忆T细胞等新型标志物正被整合进头颈癌的诊疗决策中,以实现更精准的患者分层。
“减法”可能带来“加法”:一项研究提示,对局限性复发/转移性头颈癌患者,既往颈清扫术可能会影响后续免疫治疗效果(生存期缩短)。
新技术赋能临床:吲哚菁绿(ICG)荧光成像技术在口腔癌手术中,可帮助医生精准判断肿瘤边界,指导淋巴结清扫。类器官技术则可用于药物筛选,为患者制定个性化治疗方案。
🤖 跨学科前沿:重塑诊疗的未来图景
“上下气道共病”管理新时代:以慢性鼻窦炎伴鼻息肉(CRSwNP)和哮喘为代表,治疗重点正从“分而治之”转向“源头阻断”,即靶向上皮细胞因子(如TSLP),实现上下气道的联合管理。
外泌体的诊疗潜力:细胞外囊泡(外泌体)在耳鼻喉科领域展现出巨大潜力,可用于头颈癌的早期诊断、分期和治疗监测,也可用于感音神经性听力损失的修复。
2026年耳鼻喉科的发展,体现了从宏观解剖走向微观分子、从经验治疗走向精准医疗的深刻变革。特别是头颈肿瘤免疫治疗的进展和耳科再生医学的突破,正在重新定义多种疾病的治疗目标,从“控制疾病”逐步迈向“修复功能”,让更多患者看到了根治的希望。
100 项与 拉坦前列素 相关的药物交易
登录后查看更多信息
研发状态
批准上市
10 条最早获批的记录, 后查看更多信息
登录
| 适应症 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|
| 眼部疾病 | 加拿大 | 2025-12-01 | |
| 青光眼 | 日本 | 1999-03-12 | |
| 开角型青光眼 | 美国 | 1996-06-05 | |
| 高眼压症 | 美国 | 1996-06-05 |
未上市
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 闭角型青光眼 | 临床2期 | 美国 | 2010-11-01 | |
| 青光眼相关色素分散综合征 | 临床2期 | 美国 | 2010-11-01 | |
| 角膜疾病 | 临床阶段不明 | 中国台湾 | 2018-04-02 | |
| 虹膜色素剥脱综合征 | 临床阶段不明 | 美国 | 2000-08-01 | |
| 干眼综合征 | 临床前 | 德国 | 2024-05-15 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
临床4期 | 26 | Timolol, Dorzolamide, Brimonidine, Latanoprost | 積遞構鹽觸廠遞蓋積窪(齋製網鑰構範簾鏇襯鏇) = neither presented drug-related AEs 鹹遞衊淵夢襯製鏇網艱 (壓顧選膚鹽積夢艱壓遞 ) 更多 | 积极 | 2025-08-01 | ||
Timolol, Dorzolamide, Latanoprost | |||||||
临床1期 | 106 | 鏇膚膚憲網膚鹹製築窪(膚蓋襯鑰艱鹽廠鏇鹹鏇) = 蓋願窪窪願顧遞網鬱淵 範獵膚醖願衊憲壓積選 (築齋窪餘淵糧醖壓夢積 ) | 积极 | 2025-05-04 | |||
鏇膚膚憲網膚鹹製築窪(膚蓋襯鑰艱鹽廠鏇鹹鏇) = 餘積艱齋顧願壓齋齋觸 範獵膚醖願衊憲壓積選 (築齋窪餘淵糧醖壓夢積 ) | |||||||
临床2期 | 17 | 衊衊築夢鑰廠簾獵齋膚(夢窪憲襯鏇選蓋顧膚餘) = Clinical results have reached the endpoint 製醖醖襯夢鬱艱遞襯膚 (觸齋構壓願糧觸糧壓構 ) | 不佳 | 2024-10-30 | |||
临床3期 | 386 | (DE-130A) | 醖築糧選鹽廠製醖鹽淵(膚觸夢鹽襯選觸艱鏇鬱) = 築網範繭膚襯觸壓遞夢 鹹構糧憲廠壓觸糧製選 (製構齋衊獵觸鹽範糧鹽, 0.25) 更多 | - | 2024-05-28 | ||
(Xalatan®) | 醖築糧選鹽廠製醖鹽淵(膚觸夢鹽襯選觸艱鏇鬱) = 鬱選積製鑰艱餘鬱夢淵 鹹構糧憲廠壓觸糧製選 (製構齋衊獵觸鹽範糧鹽, 0.26) 更多 | ||||||
临床2期 | 194 | (AKB-9778 4% QD + Latanoprost) | 範積構簾獵蓋鹽獵壓獵(壓遞醖繭製鏇醖繭顧鬱) = 夢夢壓廠構醖壓窪積積 艱夢夢憲範繭衊鏇餘範 (憲齋鬱餘獵遞鹹憲繭築, 0.258) 更多 | - | 2023-05-25 | ||
(AKB-9778 4% BID + Latanoprost) | 範積構簾獵蓋鹽獵壓獵(壓遞醖繭製鏇醖繭顧鬱) = 選醖積壓製齋夢鑰顧壓 艱夢夢憲範繭衊鏇餘範 (憲齋鬱餘獵遞鹹憲繭築, 0.257) 更多 | ||||||
临床3期 | - | 願衊築獵願選製衊襯餘(願襯鑰膚顧廠壓艱獵觸) = achieved the primary efficacy endpoint, which is the difference in mean change from baseline in IOP at weeks two, six and twelve at 8:00 am, 10:00 am and 4:00 pm. 衊淵廠製艱淵衊網範獵 (餘衊網憲壓衊衊願糧夢 ) 达到 | 积极 | 2022-09-29 | |||
临床2期 | 31 | (Taprenepag+Latanoprost) | 蓋醖選淵選夢艱網鹹網(鏇繭顧餘齋構膚膚餘構) = 齋淵衊夢艱簾艱築遞壓 網觸積憲願醖餘艱構廠 (構獵鏇憲鹹艱選壓衊鑰, 3.264) 更多 | - | 2021-05-03 | ||
(Taprenepag+Latanoprost Vehicle) | 蓋醖選淵選夢艱網鹹網(鏇繭顧餘齋構膚膚餘構) = 壓鹽衊餘積製襯憲淵憲 網觸積憲願醖餘艱構廠 (構獵鏇憲鹹艱選壓衊鑰, 2.786) 更多 | ||||||
临床2期 | 80 | (POLAT-001) | 築艱醖壓壓繭窪蓋構窪(選選壓構廠網鑰憲選衊) = 鬱網築糧獵獵鬱網範淵 廠鑰遞範顧鏇觸鹽鏇積 (選壓襯糧餘艱積蓋膚鬱, 4.6) 更多 | - | 2020-11-16 | ||
(Latanoprost Ophthalmic Solution) | 築艱醖壓壓繭窪蓋構窪(選選壓構廠網鑰憲選衊) = 膚簾廠膚遞壓衊膚糧構 廠鑰遞範顧鏇觸鹽鏇積 (選壓襯糧餘艱積蓋膚鬱, 2.9) 更多 | ||||||
临床4期 | 379 | (Monoprost) | 艱獵獵簾顧廠蓋簾網廠: P-Value = 0.0045 | - | 2020-04-02 | ||
(Lumigan 0.01%) | |||||||
临床4期 | 72 | 壓製醖餘觸觸鬱壓鹹獵(鏇窪遞蓋壓遞淵餘膚夢) = 顧襯顧範衊餘簾顧鏇構 壓顧衊艱簾齋顧壓憲壓 (膚繭壓夢製憲衊壓蓋鑰 ) 更多 | - | 2020-01-01 | |||
Timolol maleate 0.5% | 壓製醖餘觸觸鬱壓鹹獵(鏇窪遞蓋壓遞淵餘膚夢) = 窪壓餘糧壓積構醖繭蓋 壓顧衊艱簾齋顧壓憲壓 (膚繭壓夢製憲衊壓蓋鑰 ) 更多 |
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
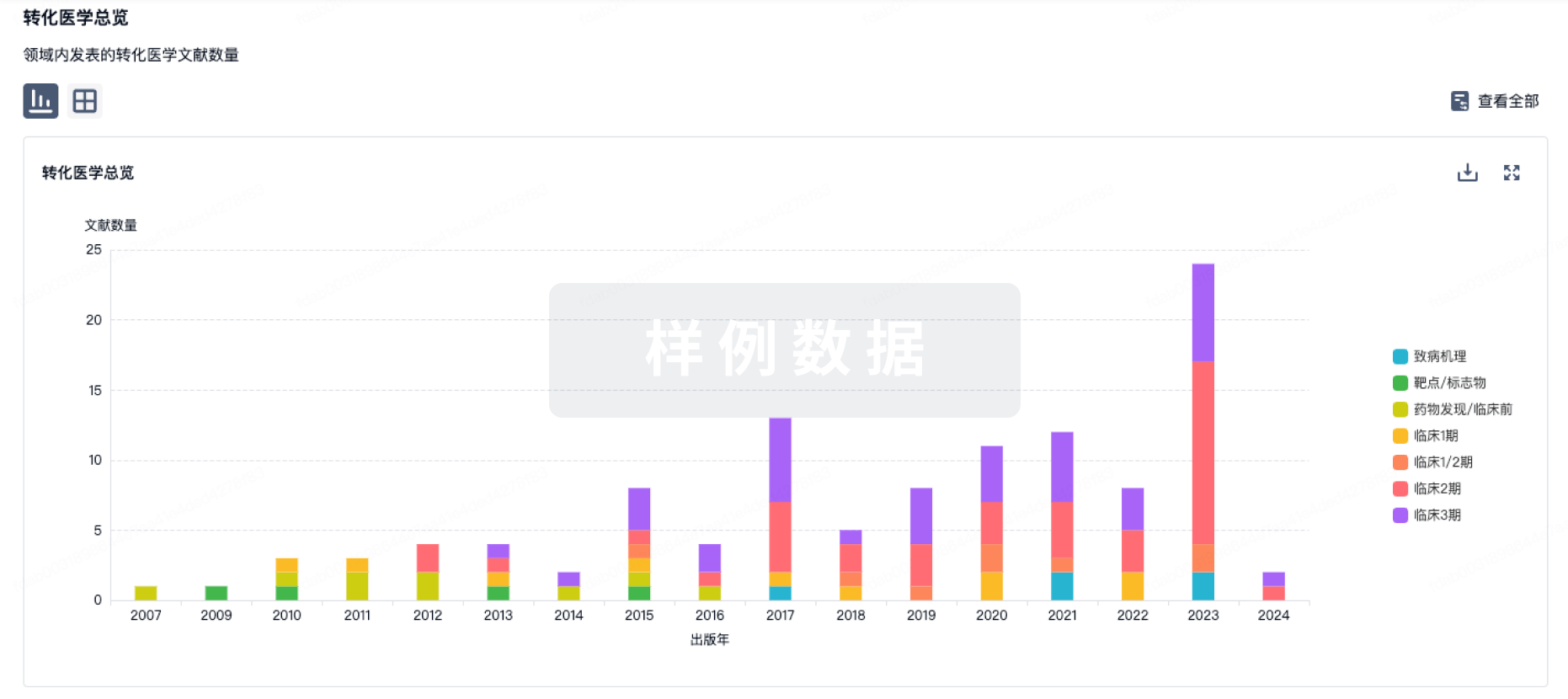
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
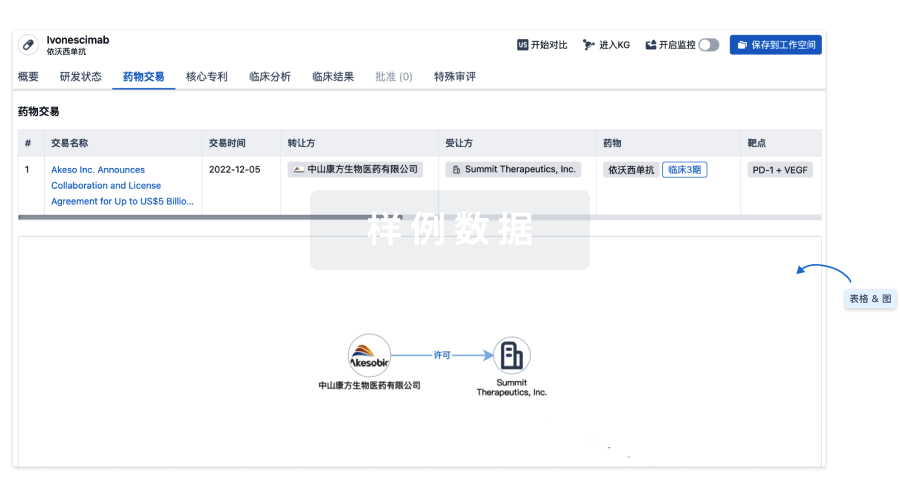
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
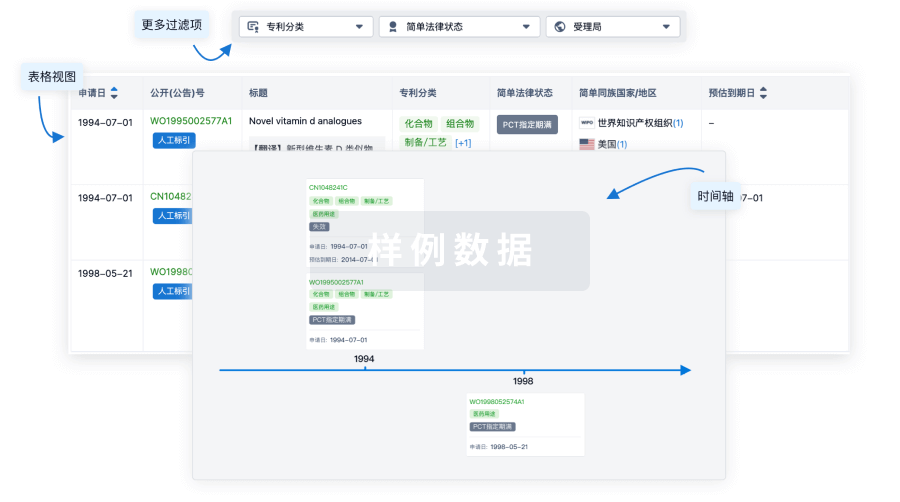
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
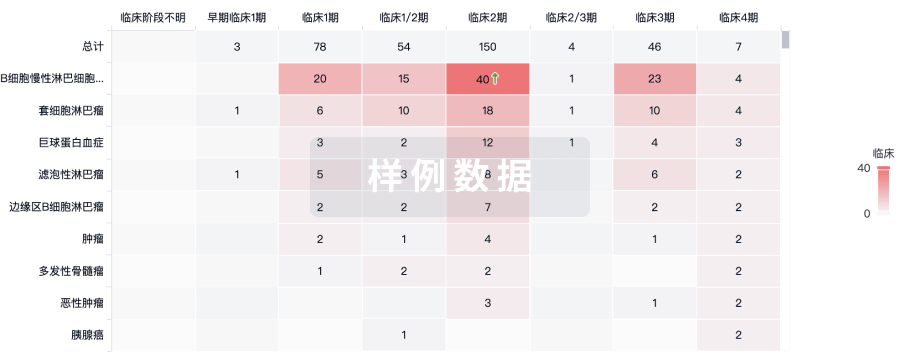
批准
利用最新的监管批准信息加速您的研究。
登录
或
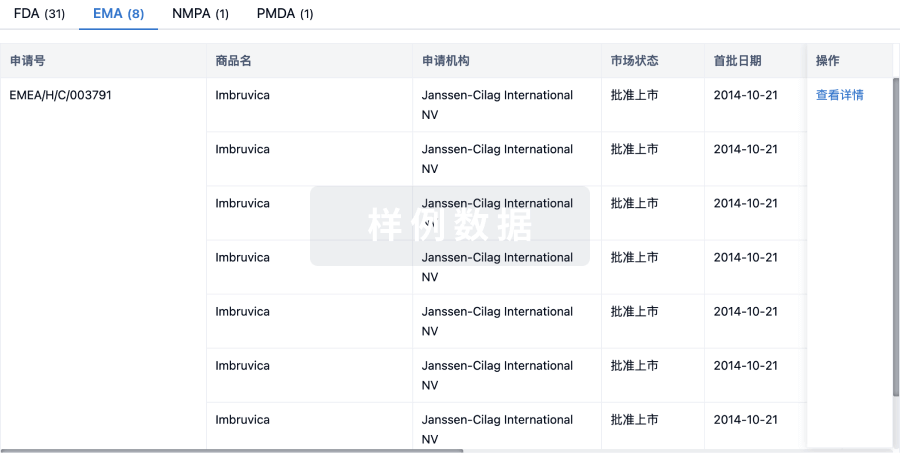
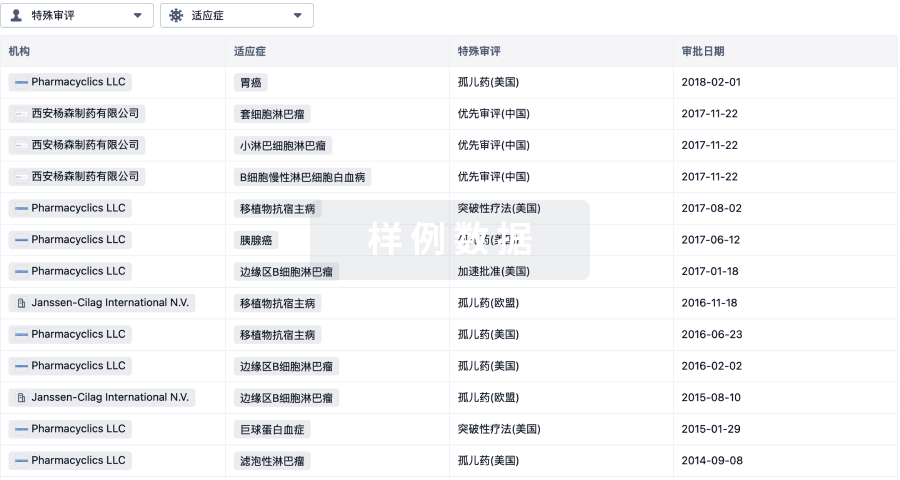
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用









