预约演示
更新于:2026-05-29
Crenolanib Besylate
苯磺酸克莱拉尼
更新于:2026-05-29
概要
基本信息
药物类型 小分子化药 |
别名 Crenolanib、Crenolanib besilate、Crenolanib besylate (USAN) + [9] |
作用方式 抑制剂 |
作用机制 FLT3抑制剂(酪氨酸蛋白激酶受体FLT3抑制剂)、c-Kit抑制剂(干细胞生长因子受体抑制剂) |
非在研适应症 |
原研机构 |
非在研机构 |
最高研发阶段临床3期 |
首次获批日期- |
最高研发阶段(中国)临床3期 |
特殊审评孤儿药 (美国)、孤儿药 (欧盟) |
登录后查看时间轴
结构/序列
分子式C32H35N5O5S |
InChIKeyARQUTWAXTHJROR-UHFFFAOYSA-N |
CAS号670220-93-6 |
关联
20
项与 苯磺酸克莱拉尼 相关的临床试验NCT03250338
Phase III Randomized, Double-blind, Placebo-controlled Study Investigating the Efficacy of the Addition of Crenolanib to Salvage Chemotherapy Versus Salvage Chemotherapy Alone in Subjects ≤ 75 Years of Age With Relapsed/Refractory FLT3 Mutated Acute Myeloid Leukemia
This is a randomized, multi-center, double-blind, placebo-controlled study designed to evaluate the efficacy of crenolanib administered following salvage chemotherapy, consolidation chemotherapy, post bone marrow transplantation and as maintenance in relapsed/refractory AML subjects with FLT3 activating mutation.
开始日期2018-08-16 |
申办/合作机构 |
NCT03258931
Phase III Randomized Study of Crenolanib Versus Midostaurin Administered Following Induction Chemotherapy and Consolidation Therapy in Newly Diagnosed Subjects With FLT3 Mutated Acute Myeloid Leukemia
A phase III randomized multi-center study designed to compare the efficacy of crenolanib with that of midostaurin when administered following induction chemotherapy, consolidation chemotherapy and bone marrow transplantation in newly diagnosed AML subjects with FLT3 mutation. About 510 subjects will be randomized in a 1:1 ratio to receive either crenolanib in addition to standard first line treatment of AML (chemotherapy and if eligible, transplantation) (arm A) or midostaurin and standard treatment (arm B). Potentially eligible subjects will be registered and tested for the presence of FLT3 mutation. Once the FLT3 mutation status is confirmed and additional eligibility is established, subject will be randomized and enter into the treatment phase.
开始日期2018-08-15 |
申办/合作机构 |
NCT03324243
A Phase II Study of Crenolanib With Fludarabine and Cytarabine in Pediatric Patients With Relapsed/Refractory FLT3-Mutated Acute Myeloid Leukemia
This is a phase II, multicenter, single-arm study to assess the safety and feasibility of combining crenolanib with fludarabine and cytarabine chemotherapy in pediatric patients with relapsed/refractory FLT3-mutated AML. Patients will receive up to two courses of salvage chemotherapy with fludarabine, cytarabine, and crenolanib. Response will be assessed between day 29-43 of each course.
开始日期2018-01-01 |
申办/合作机构 |
100 项与 苯磺酸克莱拉尼 相关的临床结果
登录后查看更多信息
100 项与 苯磺酸克莱拉尼 相关的转化医学
登录后查看更多信息
100 项与 苯磺酸克莱拉尼 相关的专利(医药)
登录后查看更多信息
223
项与 苯磺酸克莱拉尼 相关的文献(医药)2026-03-01·AMERICAN JOURNAL OF PHYSIOLOGY-GASTROINTESTINAL AND LIVER PHYSIOLOGY
Disruption of gastrointestinal PDGFRα
+
cells leads to loss of postjunctional inhibitory motor responses
Article
作者: Hwang, Sung Jin ; Sanders, Kenton M. ; Ward, Sean M.
The physiological roles of newly described PDGFRα
+
interstitial cells in neurotransmission within the gastrointestinal (GI) tract have predominantly come from studies on isolated cells. Here we used an inhibitor of PDGFRα, crenolanib, to examine the effects of PDGFRα
+
cells in enteric inhibitory neurotransmission. Crenolanib caused loss of PDGFRα
+
cells and neurally evoked fast inhibitory junction potentials associated with purine neurotransmission, providing evidence for the function of PDGFRα
+
cells within intact tissues of the GI tract.
2025-09-01·Journal of Extracellular Vesicles
Selective EV Protein Sorting and Pathway Perturbation in AML Upon Synergistic FLT3 and Hedgehog Pathway Inhibition
Article
作者: Blöchl, Constantin ; Krenn, Peter W. ; Strunk, Dirk ; Blümel, Gabriele ; Aberger, Fritz ; Regl, Christof ; Wolf, Martin ; Maeding, Nicole ; Binder, Heide‐Marie ; Lankes, Daniel ; Huber, Christian G. ; Tesanovic, Suzana
ABSTRACT:
Acute myeloid leukaemia (AML) is a haematologic malignancy with high relapse incidence and mortality. Approximately one‐third of AML patients carry an fms‐like tyrosine kinase 3 (FLT3) mutation, often associated with GLI expression and Hedgehog signalling. AML cells shape their microenvironment into a leukaemia‐permissive space by releasing extracellular vesicles (EVs). EVs can transfer chemoresistance and thereby play an important role in refractory and relapsing diseases. Here, we discovered a synergistic effect of combined treatment with the FLT3 inhibitor Crenolanib and the Hedgehog pathway inhibitor HPI‐1 in the AML cell lines MOLM‐14 and MV4‐11. In‐depth comparative proteomics revealed alterations in the cellular and the EV proteome upon single or combined inhibition of FLT3 and GLI, highlighting affected pathways. By comparing cellular and EV proteomes, we found that transport of ribosomal proteins, such as RPS26 and RPL27A, and ErbB pathway members such as GAB1, GRB2 and SHC1 to EVs, is selectively avoided upon treatment with Crenolanib. These findings were corroborated by comparative proteomics of EVs derived from AML patients and healthy donors. Ribosomal and ErbB signalling pathway proteins may play an important role in microenvironmental modulation by EVs, and Crenolanib treatment potentially acts by interfering with leukaemia niche formation.
2025-07-01·British Journal of Pharmacology
High‐throughput screening identifies bazedoxifene as a potential therapeutic for dysferlin‐deficient limb girdle muscular dystrophy
Article
作者: Isabelle Richard ; Johana Tournois ; Xavier Nissan ; Manon Benabides ; Anne Bigot ; Emilie Pellier ; Nathalie Bourg ; Noella Grossi ; Celine Bruge ; Jerome Polentes ; Anthony Brureau
Abstract:
Background and Purpose:
Limb‐girdle muscular dystrophy R2 (LGMD R2) is a rare genetic disorder characterised by progressive weakness and wasting of proximal muscles. LGMD R2 is caused by the loss of function of dysferlin, a transmembrane protein crucial for plasma membrane repair in skeletal muscles. This study aimed to identify drugs that could improve the localisation and restore the function of an aggregated mutant form of dysferlin (DYSFL1341P).
Experimental Approach:
We developed an in vitro high‐throughput assay to monitor the expression and reallocation of aggregated mutant dysferlin (DYSFL1341P) in immortalised myoblasts. After screening 2239 clinically approved drugs and bioactive compounds, the ability of the more promising candidates to improve cell survival following hypo‐osmotic shock was assessed. Their protective effects were evaluated on immortalised myoblasts carrying other dysferlin mutations and on dysferlin‐deficient muscle fibres from Bla/J mice.
Key Results:
We identified two compounds, saracatinib and bazedoxifene, that increase dysferlin content in cells carrying the DYSFL1341P mutation. Both drugs improved cell survival and plasma membrane resistance following osmotic shock. Whereas saracatinib acts specifically on misfolded L1341P dysferlin, bazedoxifene shows an additional protective effect on dysferlin KO immortalised myoblasts and mice muscle fibres. Further analysis revealed that bazedoxifene induces autophagy flux, which may enhance the survival of LGMD R2 myofibres.
Conclusion and Implications:
Our drug screening identified saracatinib and bazedoxifene as potential treatments for LGMD R2, especially for patients with the L1341P mutation. The widespread protective effect of bazedoxifene reveals a new avenue toward genotype‐independent treatment of LGMD R2 patients.
19
项与 苯磺酸克莱拉尼 相关的新闻(医药)2026-05-27
·懂临研
接上半部分
早期探索性试验
内容
人群选择
FIH、CYP3A(抗真菌治疗)、QT间期(抗菌、止吐治疗)
DLT特殊性
血液学DLT
剂量扩展
例数、停止原则
建议在其他进展较慢的肿瘤先开展FIH
原则上选择经所有适宜的现有治疗手段充分治疗但仍难治或复发
对于伴随不良预后因素或存在高风险遗传学异常的患者,预计从常规治疗无法获益的患者,未经治疗可参与临床试验
FIH需要对单药进行评估,对单药的药代动力学、药效动力学、安全性和耐受性特征有充分了解后再启动联合用药的临床研究
对于以上意见,FDA和CDE意见相同。
年龄:
FDA has accepted, but does not require, use of age 75 years as an upper limit for inclusion in trials of intensive chemotherapy. FDA, however, encourages use of no age limit for trials of nonintensive treatments for AML.
CDE :
应该尽早关注老年患者与年轻患者在药物暴露和安全耐受性方面的差异,在进入关键性注册研究之前明确高龄患者是否需要在推荐方案的基础上进行剂量调整。在剂量探索阶段纳入一定比例的高龄患者。
然而对于年龄,FDA明确规定大于75岁以上患者不适宜强化疗治疗,但中国可能做不到75岁以上,一般60岁以上就认为不适宜强化疗治疗,所以CDE并没有明确规定年龄的界限。
For AML drugs that are CYP3A substrates, sponsors should consider enrolling patients on azole antifungals or other CYP3A inhibitors in FIH trials to generate data needed to select a safe dose with these concomitant drugs
Sponsors should conduct an adequate assessment early in clinical development to assess the QT prolongation potential of the AML drug as described in FDA‘s guidance. Common supportive care medications for patients with AML, including antimicrobial prophylaxis (e.g., fluoroquinolones) and antiemetics (e.g., 5-HT3 receptor antagonists), are known to prolong the QT interval.
FDA在guidance中反复提到CYP3A,如果治疗AML的研究药物是CYP3A底物,那么研究过程中一定要注意与唑类药物的相互作用,因为白血病患者大部分需要抗真菌治疗,会影响研究药物的浓度,需要尽早开展药物相互作用研究。另外则是影响QT间期的药物,抗白血病过程中需要给予相应的抗细菌药物或预防呕吐的药物有QT延长的作用,如果研究药物也有QT延长的作用,那么可能导致QT延长,尤其对于基线就有QT延长的受试者,增加发生尖端扭转室性心律失常的风险。需要在方案中明确规定如何预防此类事件的发生。
DLT的特殊性
由于白血病患者的血象的特殊性,DLT的血液学毒性也有其特殊性。那么CDE对于白血病的血液学DLT有2条规定,第一则是在判断血液系统DLTs时需首先排除原发病的影响,在受试者的白血病仍处于活跃状态时无法进行血液系统DLTs的评估。
第2条则是在定义血液系统DLTs的毒性级别和持续时间时,应该综合考虑药物的作用机制(细胞毒性药物、毒性相对较低的小分子靶向药物、抗体偶联药物或单克隆抗体等)、治疗目标(深度缓解/治愈、维持治疗、改善输血需求或姑息地延长生存时间等)、预期的治疗方案(不间断长期治疗、周期性间歇性治疗、高强度冲击式治疗等)等。
而FDA则给出了一个定义DLT的表格,清晰地说明了如何设置白血病疾病的DLT。
其实也就是CDE的文字描述内容,首先,在有白血病存在的情况下,不进行血液学DLT的评估。其次,对于持续长久服药的维持治疗,能够接受的毒性较低,则血液学DLT设置为≥3级ANC或PLT降低持续超过7天;而对于短期的冲击治疗,可以接受的毒性就较高血液学DLT设置为≥4级ANC或PLT降低持续超过7天;而对于减低剂量的强化疗,可接受的毒性则更高,血液学DLT设置为≥4级ANC或PLT降低持续超过42天;强化治疗同理。
确证性试验
内容
人群选择
新诊断、远期复发、其他复发难治
主要目的
治愈意图、非治愈意图、姑息治疗
主要终点
OS、EFS、ORR
对于确诊性试验,CDE和FDA也有不同的要求,但是大同小异。
CDE的意见是关键性注册研究选择的主要疗效终点应与治疗目标相符,选择能直接代表临床获益的临床终点,或选择已证明与临床获益具有明显相关性的替代终点。
按照人群划分总结为如下表格:
人群
主要目的
研究设计
对照组
终点
新诊断人群
Fit:治愈,延长生存
随机对照优效
标准强化疗
OS
Unfit:维持生命
随机对照优效
去甲基化或低剂量阿糖胞苷
OS
复发性AML(远期)
CR后HSCT
随机对照优效
挽救化疗
OS
难治性AML
非治愈
单臂
NA
CRR
若联合治疗
联用的基础治疗,或最佳支持治疗
OS
维持治疗
延长缓解持续时间
对照
RFS
FDA的建议则是:Patients with newly diagnosed AML, patients with AML in late first relapse (e.g., first remission > 6 months), and patients with other relapsed or refractory AML (e.g., primary refractory, early first relapse, and any second or later relapse) represent three distinct indications.
Relapse post HSCT would fall under either treatment of first relapse or treatment of later relapse rather than being a separate indication.
目的
人群
研究设计
对照组
终点
治愈(延长生存)
新诊断
随机对照
标准治疗
OS、EFS、RFS
非治愈(延长生存、延长CR持续时间)
诱导失败率高、预期生存期短
单臂/随机对照
挽救治疗
OS、EFS
NA
CRR(根据疾病状态)
姑息(短期疾病控制、降低肿瘤负荷)
不适宜强化疗
单臂/随机对照
最佳支持治疗
持续CR、持续CR/Crh和TI
移植后复发的患者不作为单独的人群,归类为初次复发或多次复发即可。因为骨髓移植是AML不可分割的一部分,FDA则是建议视为治疗的一部分,更符合真实情况下患者的治疗过程。
内容就这么多,以下举例说明:
例子1 Quizartinib初诊AML
以上则是Quizartinib的试验设计,贯穿AML的治疗全过程,以OS为主要终点。于2023年7月在美国获FDA批准上市,所以Quizartinib的label中写的也很明确,与标准治疗联合治疗FLT3阳性初诊患者,在诱导、巩固及维持阶段均可应用。
例子2 Quizartinib/Gilteritinib/Crenolanib 复发/难治AML
此种设计则是阳性对照设计,此类患者属于复发难治患者(既往至少使用过蒽环类药物治疗),但仍可以耐受强化疗,且追求持续CR后移植治疗,延长生存,因此主要终点为OS。方案中规定获得缓解后可以进行骨髓移植治疗,并且接受移植后的患者即使不继续研究药物治疗仍继续进行主要终点随访。
例子3-Ivosidenib unfit强化疗AML
Unfit的患者一般目前对照选择去甲基化药物,以上设计对照仅单药阿扎胞苷,当然根据目前诊疗指南可以选择阿扎胞苷+LD阿糖胞苷,此类患者以改善生活质量、延长生存为主要目的,Ivosidenib则是以EFS为主要终点。
例子4-treosulfan 清髓治疗AML
treosulfan则是清髓药物中的一种,对照则是白舒非和氟达拉滨,主要终点是OS,2025年1月FDA批准上市,用于与氟达拉滨联用在异基因骨髓移植中作为清髓预处理药物。
例子5-Gilteritinib 维持治疗AML
Gilteritinib在AML患者异基因骨髓移植后维持治疗的研究,则设计如下图,首先入组的受试者是CR1患者,分层因素有MRD阳性与否,对照为安慰剂,主要终点则是EFS。结果则显示对整体入组人群来说,EFS并没有提升,但是对于MRD+的受试者来说,可以显著提高EFS,HR 0.515(0.3126,0.838)P=0.0065。
总结,AML药物研发目标人群决定目的,决定方案设计;可以在治疗的任意阶段进行研究;接受HSCT研究不中断,需要明确规定进入HSCT的条件。
2026-04-09
·医研小憩
《Resistance to Tyrosine Kinase Inhibitors》
第一部分:基础知识与普遍问题(第1-2章)
第1章:癌细胞里的“信号开关”核心:我们的细胞里有一种叫“酪氨酸激酶”的蛋白质,它像一个个“开关”,负责接收外界指令(比如生长信号),然后告诉细胞该生长、分裂还是死亡。癌症怎么来的:癌细胞很狡猾,它们通过基因突变、过度生产等方式,让这些“开关”一直卡在“开启”状态,导致细胞无限生长,形成肿瘤。靶向药的原理:科学家针对这些坏掉的“开关”,设计了TKI这种“特效药”。它像一把特制的“钥匙”,能精准地锁住坏开关,让癌细胞停止生长。最成功的例子就是治疗白血病的格列卫(伊马替尼)。
第2章:为什么“特效药”会失效?(实体瘤篇)尽管TKI比化疗更精准、副作用小,但很多患者用着用着就没效了,这就是耐药。耐药的两大根本原因(这个逻辑贯穿全书):“锁芯”换了(靶点本身变了):癌细胞在药物压力下,让靶点蛋白(那个“坏开关”)发生了新的突变。比如,原来能锁住的锁眼形状变了,原来的“钥匙”(TKI)就插不进去了。肺癌里著名的T790M突变就是典型例子。“另辟蹊径”(激活了别的通路):当主路(原来的靶点)被药物堵死,癌细胞会迅速找到并激活另一条甚至几条备用的小路来维持生存,比如激活MET、HER2等其他基因。这章还讲了在不同癌症(肺癌、胃肠间质瘤、肾癌等)中,这两种原因的具体表现,说明耐药是个普遍又复杂的问题。
第二部分:深入看几种典型的耐药(第3-5章)
第3章:慢性粒细胞白血病(CML)的耐药CML是靶向治疗最成功的典范,致病基因明确(BCR-ABL融合基因),药(伊马替尼)也极有效。但仍有约1/3患者会耐药。最主要的原因就是BCR-ABL基因自己发生了新的突变,尤其是T315I“守门员”突变,它像给锁眼加了个盖子,几乎挡住了所有一代、二代TKI。除了靶点突变,白血病干细胞藏在骨髓这个“避难所”里,以及激活其他生存通路,也是重要原因。
第4章:急性髓系白血病(AML)的FLT3抑制剂耐药FLT3是AML的一个常见坏靶点。情况和CML很像,耐药也主要是FLT3基因自己产生了新突变,比如F691L或D835Y。这里有个关键点:不同突变对不同类型的药敏感。有的突变(如D835Y)会让结合“关闭状态”开关的药失效,但另一种能结合“开启状态”开关的新药(如克瑞兰尼)可能还有效。
第5章:肺癌的ALK抑制剂耐药ALK是肺癌的一个重要靶点。第一代药克唑替尼效果很好,但多数人1-2年内会耐药。机制同样是那两条:要么ALK基因自己突变(如L1196M),要么激活其他通路(如EGFR)。好消息是,针对不同的耐药突变,科学家已经开发出了第二代(色瑞替尼、阿来替尼)、第三代(劳拉替尼)ALK抑制剂。形成了“一线药失效→检测耐药原因→换用对应二代/三代药”的精准接力治疗模式,大大延长了患者生命。
第三部分:一种特殊的耐药——抗血管生成药(第6章)
第6章:抗血管生成TKI(如舒尼替尼)的耐药这类药不是直接杀癌细胞,而是通过抑制肿瘤的血管(断其粮草)来“饿死”肿瘤。它的耐药机制很不同,通常不是靶点基因突变,而是肿瘤和它周围环境的“整体反抗”:“粮草通道”切换:当主要的VEGF血管生成通路被堵,肿瘤会分泌大量其他促血管因子(如FGF、IL-8),开辟新的粮草通道。招募“外援”:肿瘤会从骨髓召唤来很多帮手细胞,帮它建立新血管。变得更“流氓”:有些肿瘤(如脑胶质瘤)在药物压力下,会从一团变成四处浸润的单个细胞,更难对付。应对策略主要是使用能同时阻断多个血管通路的药,或者与免疫疗法联合(免疫疗法负责杀敌,抗血管药负责改善战场环境)。
第四部分:临床应用与未来(第7章)
第7章:TKI在实体瘤中的用武之地这章像一份“用药地图”,总结了当时(2016年)TKI在各类癌症(肺癌、肾癌、胃肠间质瘤、黑色素瘤等)中的标准用法。它再次强调:用TKI前必须做基因检测,找到对应的突变才能用对药(比如,肺癌用EGFR药前必须确认有EGFR突变)。全书结论与未来方向:耐药是挑战,但我们有办法:开发新一代TKI:针对耐药突变设计新药(如针对T790M的奥希替尼)。联合治疗:用“鸡尾酒疗法”同时抑制主路和可能出现的备用小路(如达拉非尼+曲美替尼治疗黑色素瘤)。个体化与动态监测:治疗中要像侦探一样,通过反复活检或抽血检测,监控肿瘤的变化,及时调整策略。
总结一下全书核心思想:这本书系统性地告诉我们,癌症靶向药的耐药不是魔法,而是癌细胞在求生欲下的“进化”。其核心逃逸策略就两种:1. 改变靶点自身;2. 激活备用通路。而我们对抗耐药的策略,就是利用科学手段(基因检测)洞察其进化方向,然后用更精准的新药或组合拳进行打击。这是一场持续的“道高一尺,魔高一丈”的博弈,也正是这种博弈,推动着癌症治疗不断进步,让更多患者获得长期生存的希望。
第1章:正常与癌细胞中的酪氨酸激酶信号通路
本章是理解全书的基础,详细阐述了酪氨酸激酶(PTKs)的生物学功能及其在癌变中的核心作用。
1. 酪氨酸激酶的核心作用功能:PTKs是细胞信号传导的“主开关”。它们通过将磷酸基团转移到特定蛋白质的酪氨酸残基上(这一过程称为磷酸化),像按下多米诺骨牌的第一张牌,启动一系列下游信号级联反应。最终效应:这些信号通路最终汇聚到细胞核,调控基因表达,决定细胞的命运——是增殖、分化、迁移,还是凋亡(程序性死亡)。
2. 两大分类与关键成员文档将PTKs清晰分为两大类,并列举了与癌症治疗密切相关的成员:A. 受体酪氨酸激酶(RPTKs)结构:像一根“天线”,一部分在细胞外接收信号(配体结合域),一部分跨过细胞膜,一部分在细胞内具有激酶活性。激活机制:配体(如生长因子)结合 → 受体二聚化/寡聚化 → 相互磷酸化(自磷酸化)激活 → 招募下游信号蛋白。重要家族与癌种举例:EGFR家族(ErbB家族):包括EGFR(HER1)、HER2、HER3、HER4。EGFR突变常见于非小细胞肺癌(NSCLC);HER2过表达/扩增是乳腺癌的重要亚型。PDGFR家族:包括PDGFRα和PDGFRβ。PDGFRα突变是部分胃肠道间质瘤(GIST)的驱动基因。VEGFR家族(VEGFR1-3):是肿瘤血管生成的关键调节因子,是肾癌、肝癌等抗血管生成治疗的核心靶点。FLT3:在急性髓系白血病(AML)中,内部串联重复(FLT3-ITD)是最常见的突变之一,提示预后不良。c-KIT:其功能获得性突变是绝大多数GIST的发病基础。胰岛素受体家族:如胰岛素样生长因子1受体(IGF-1R),与多种肿瘤的生长和耐药相关。B. 非受体酪氨酸激酶(NRPTKs)位置:位于细胞质、细胞核或锚定在细胞膜内侧。功能:作为下游信号放大器或整合器,被上游的RPTKs或其他信号激活。重要成员:BCR-ABL:由9号与22号染色体易位(费城染色体)产生的融合基因产物,其组成性激活是慢性髓系白血病(CML)的明确病因。JAK家族(JAK1, JAK2, JAK3, TYK2):与细胞因子受体偶联,其持续激活与骨髓增殖性肿瘤(如真性红细胞增多症)和炎症相关。抑制剂如鲁索替尼已获批。SRC家族(SRC, FYN, YES, LYN等):参与整合来自多种受体(如EGFR、整合素)的信号,与肿瘤进展、转移和耐药密切相关。
3. 癌症中PTKs的异常激活机制(“油门卡死”)文档详细解释了癌细胞如何“劫持”这些激酶,使其持续处于“开启”状态:自分泌/旁分泌环路:癌细胞自身或周围细胞过量产生生长因子(如EGF、TGF-α),形成持续的自我刺激。受体过表达:由于基因扩增,细胞表面受体数量异常增多,对微量配体也异常敏感。组成性激活突变:点突变:使激酶无需配体即可激活。例如:EGFR L858R(肺癌)、FLT3-ITD(AML)、c-KIT D816V(肥大细胞增生症)。基因重排/融合:产生新的、持续活化的融合蛋白。最经典的例子是BCR-ABL(CML)和EML4-ALK(肺癌)。下游信号元件突变:如RAS、BRAF、PI3K等基因突变,使得信号传导不依赖于上游激酶的激活,形成“下游短路”。
4. 靶向治疗的里程碑案例文档通过列表形式展示了截至2016年已获批的重要激酶靶向药物,并突出几个范例:伊马替尼(格列卫):针对BCR-ABL,彻底改变了CML的治疗,使其从致命性疾病转变为可管理的慢性病。其成功也揭示了“多靶点”特性——它还能抑制c-KIT和PDGFR,因此被拓展用于治疗GIST。抗HER2治疗体系:展示了靶向治疗的多样性。曲妥珠单抗(赫赛汀):单克隆抗体,结合HER2胞外区,阻断信号并介导免疫细胞杀伤。T-DM1:抗体药物偶联物(ADC),将强效化疗药DM1通过抗体精准递送至HER2阳性癌细胞,是“生物导弹”。拉帕替尼:小分子TKI,可穿透血脑屏障,用于对曲妥珠单抗耐药的患者。
本章小结:第1章构建了完整的知识框架——理解正常功能是识别异常的基础。癌细胞通过多种遗传学改变使PTKs信号失控,而这恰恰为靶向治疗提供了“阿喀琉斯之踵”。针对这些靶点开发的TKI和单抗,开启了肿瘤的精准治疗时代。
第2章:不同类型实体瘤对酪氨酸激酶抑制剂的耐药性
1. 耐药性的两大基本类型原发性耐药:治疗从一开始就无效。这通常意味着肿瘤在治疗前就存在某些内在的、能抵消TKI作用的特征。例如,存在对药物不敏感的驱动突变(如EGFR的20号外显子插入突变),或同时存在激活的旁路信号通路。获得性耐药:治疗初期有效,肿瘤缩小或稳定,但经过一段时间(通常是数月到数年)后,肿瘤重新开始生长。这是临床实践中最常见、最棘手的挑战。获得性耐药是肿瘤在药物选择压力下,通过克隆演化“学习”并适应出来的结果。
2. 以肺癌为例的耐药机制详析肺癌,特别是非小细胞肺癌(NSCLC),是研究TKI耐药机制的“样板间”,主要围绕EGFR和ALK两大靶点。
A. EGFR-TKI的耐药机制靶点依赖性(On-target)机制:EGFR自身的二次突变T790M“守门员”突变:这是对第一代EGFR-TKI(吉非替尼、厄洛替尼)最常见的获得性耐药机制,约占50%。文档引用研究指出,T790M突变本身具有弱致癌性,但当它与原有的激活突变(如L858R)共存时,会大幅增强EGFR信号和致癌转化能力。其结构机制是:蛋氨酸(M)取代苏氨酸(T)后,庞大的侧链产生空间位阻,同时恢复了EGFR与ATP(药物的天然竞争对手)的高亲和力,从而将药物“挤”出ATP结合口袋。其他EGFR突变:如C797S突变,可能导致对第三代EGFR-TKI奥希替尼的耐药。靶点非依赖性(Off-target)机制:激活替代生存通路旁路信号激活:当EGFR被有效抑制,肿瘤细胞激活其他受体酪氨酸激酶来维持生存。MET基因扩增:约占获得性耐药病例的5-20%。MET扩增可以激活下游的PI3K/AKT和MAPK通路,绕过被抑制的EGFR。HER2扩增:另一种常见的旁路机制。其他激酶突变/扩增:如PIK3CA突变(约5%)、BRAF突变(如V600E)等,这些下游或平行通路的元件发生改变,使得信号持续畅通。组织学转型:一个令人惊讶的发现是,约3-10%的对EGFR-TKI耐药的肺腺癌会转化为小细胞肺癌(SCLC)。这种转型后的癌细胞不再依赖EGFR,而是需要按照SCLC的方案(如依托泊苷+铂类化疗)进行治疗。这强调了耐药后再次活检进行病理确认的重要性。上皮-间质转化(EMT):肿瘤细胞失去上皮特征,获得间质细胞的迁移和侵袭能力。EMT与多种耐药机制相关,并常伴随其他信号通路(如AXL、MET)的激活。
B. ALK-TKI(以克唑替尼为例)的耐药机制
文档详细列举了克唑替尼耐药的具体案例和分子发现。ALK依赖性机制ALK激酶域继发突变:在肿瘤进展后的患者标本中被发现。例如,早期报告显示一名患者在克唑替尼治疗5个月后进展,其胸水细胞中发现L1196M(守门员突变)和C1156Y两个突变,并在体外实验中证实导致耐药。后续发现了更多突变,根据其在激酶结构域的位置分类:溶剂前沿:G1202R, S1206Y(影响药物与激酶表面的结合)。守门员:L1196M。ATP结合口袋:G1269A。C-螺旋N端:1151Tins, L1152R, C1156Y。ALK基因拷贝数扩增:癌细胞产生更多的ALK融合蛋白,需要更高浓度的药物才能完全抑制。ALK非依赖性机制旁路信号激活:这是非常重要的逃逸机制。临床前模型显示,EGFR的激活在克唑替尼耐药中起关键作用,涉及EGF和双调蛋白等配体。临床病例中也发现,ALK阳性患者耐药后,重复活检检测到EGFR突变或KRAS突变。此外,KIT基因扩增也在约15%的耐药标本中被发现。下游信号激活:如PIK3CA突变。其他:文档提到,自噬增加(涉及Akt/mTOR信号)也可能导致耐药,而自噬抑制剂可以在细胞系中恢复对克唑替尼的敏感性。
3. 胃肠间质瘤(GIST)对伊马替尼的耐药GIST是伊马替尼疗效的另一个典范,但其耐药机制极具特点。原发性耐药:主要见于无KIT/PDGFRA突变的野生型GIST,或携带PDGFRA D842V突变的GIST(该突变对伊马替尼天然不敏感)。获得性耐药:主要由KIT或PDGFRα基因的继发性点突变驱动。这些突变不是随机的,而是发生在激酶域的特定“热点”(如ATP结合口袋、激活环)。其最大挑战在于高度异质性:同一患者的不同转移灶,甚至同一病灶内的不同区域,可能产生不同的继发突变。这使得后续治疗(如换用舒尼替尼)可能只对部分克隆有效。激酶转换:文档描述了另一种有趣的机制。GIST细胞在获得伊马替尼耐药过程中,可能发生“激酶转换”,即从依赖KIT转为依赖其他激酶,如AXL或黏着斑激酶(FAK)。抑制FAK可以使耐药细胞重新对伊马替尼敏感,并诱导小鼠模型中的肿瘤缩小,这为联合治疗提供了思路。
4. 结直肠癌(CRC)抗EGFR单抗的耐药虽然主要针对单抗(西妥昔单抗/帕尼单抗),但其机制深刻阐释了下游信号通路的关键作用。核心机制:RAS家族(KRAS, NRAS)和BRAF基因的突变。这些突变使得下游的MAPK信号通路处于持续激活状态,因此即使上游的EGFR被抗体完全阻断,致癌信号仍源源不断。因此,用药前检测这些基因状态是绝对必须的,仅野生型患者可能获益。其他机制:包括PIK3CA基因突变、PTEN蛋白丢失(导致PI3K/AKT通路持续激活)等。
5. 肾细胞癌(RCC)抗血管生成TKI的耐药以舒尼替尼为例,其耐药机制与靶向驱动基因的TKI有本质不同,更侧重于肿瘤微环境的适应性改变。“血管生成开关”:这是核心概念。当VEGF/VEGFR主要通路被抑制后,肿瘤缺氧微环境会诱导上调其他促血管生成因子,如成纤维细胞生长因子(FGF)、血小板衍生生长因子(PDGF)、白细胞介素-8(IL-8)等,通过这些“备选通路”重新驱动血管新生。文档引用Huang等人的研究,发现IL-8在舒尼替尼耐药的肾透明细胞癌(ccRCC)细胞中高表达,且联合IL-8中和抗体能影响治疗反应。重要的是,研究者并未在耐药样本中发现VEGFR、PDGFR等基因的突变,提示这是一种不依赖于靶点突变的耐药机制。招募促血管细胞:肿瘤通过分泌趋化因子,从骨髓招募髓源性抑制细胞(MDSCs)、肿瘤相关巨噬细胞(TAMs)等,这些细胞能分泌多种促血管因子,帮助建立血管网络。血管共选择:肿瘤细胞可能放弃生成新血管,转而侵袭并利用宿主组织内已存在的成熟血管,这些血管对VEGF抑制剂不敏感。
6. 其他癌种与新兴机制文档还简要提及了在其他癌症中观察到的耐药机制:鞘氨醇激酶1(SphK1)的作用:在乳腺癌和结直肠癌中,SphK1的上调与对他莫昔芬和西妥昔单抗的耐药相关。抑制SphK1或其产物S1P的受体(如使用芬戈莫德FTY720),可以在临床前模型中恢复药物敏感性。白细胞介素-6(IL-6):在去势抵抗性前列腺癌(CRPC)中,IL-6水平在TKI耐药细胞中升高,可能作为耐药生物标志物。microRNA的作用:如miR-203在前列腺癌中下调,会导致对EGFR配体和抗凋亡蛋白的抑制解除,从而促进侵袭和耐药。
本章核心总结:第2章揭示了实体瘤耐药的复杂全景。尽管癌种和靶点各异,但机制可归结为两大类:1) 靶点自身发生改变(突变、扩增),使药物失效;2) 肿瘤细胞激活替代的信号通路(旁路激活),绕过被抑制的靶点。此外,组织学转型、肿瘤微环境重塑等也扮演重要角色。这强调了动态监测(如耐药后再次活检进行基因检测)和开发针对不同耐药机制的后续疗法(如新一代TKI、联合治疗)的极端重要性。
第3章:慢性髓系白血病(CML)对酪氨酸激酶抑制剂的耐药性
背景:成功的典范与持续的挑战文档开篇指出,以伊马替尼为代表的酪氨酸激酶抑制剂(TKI)在过去十年中显著改善了CML患者的预后。然而,仍有约三分之一的患者最终需要因毒性或耐药而停止或更换治疗。耐药可分为“原发性”和“继发性”(或称“获得性”)。
1. 耐药的定义:基于治疗反应的精确界定文档依据当时的欧洲白血病网(ELN)指南,给出了明确的临床定义:原发性耐药:指患者在固定时间点未能达到既定的治疗目标。例如,在开始治疗后3、6、12个月等时间点,未能达到特定的血液学、细胞遗传学或分子学反应深度(具体标准参考ELN或NCCN指南)。继发性(获得性)耐药:指患者失去了先前已达到的治疗反应。这包括:失去完全血液学缓解(CHR)。失去完全细胞遗传学缓解(CCyR)。失去主要分子学反应(MR3,即BCR-ABL转录本水平降至国际标准值的0.1%以下)。对于分子学反应的丧失,需要连续两次检测确认,且其中一次BCR-ABL比率需>1%。检测到ABL1激酶域突变。检测到费城染色体阳性克隆中出现额外的染色体异常(ACAs)。文档特别强调,与“原发性”耐药不同,“继发性”耐药是**“时间无关的”**,它可以在治疗过程中的任何时间点发生。
2. 耐药机制的总体框架:BCR-ABL依赖性与非依赖性
文档指出,CML耐药的发生基于多种原因和生物学机制,并将其核心区分为两大类(参见文档中的图3.1):BCR-ABL依赖性机制:耐药的根本原因在于BCR-ABL融合基因或蛋白本身发生了变化,导致TKI无法有效抑制其活性。BCR-ABL非依赖性机制:即使BCR-ABL被有效抑制,白血病细胞仍能通过其他途径存活和增殖。
3. BCR-ABL依赖性耐药机制详析
A. 额外的染色体异常(ACAs)在费城染色体阳性的克隆中,出现除t(9;22)以外的其他染色体异常,如+8、+Ph、i(17q)等。这些异常可能与疾病进展(向加速期或急变期转化)相关,并可能影响治疗反应。
B. ABL1激酶域突变——最主要的耐药机制发生率与重要性:过去10年的研究表明,ABL1激酶域突变是CML患者对TKI产生耐药的主要原因之一。在伊马替尼耐药的患者中,突变检出率为30-90%;在二代TKI治疗失败的患者中,为20-80%。例如,意大利GIMEMA工作组报告,在40例治疗12个月后未达到主要细胞遗传学缓解的患者中,通过变性高效液相色谱(D-HPLC)技术检测到48%存在ABL1突变,且突变的存在与更高的疾病进展风险和更短的总生存期(OS)、无进展生存期(PFS)显著相关。突变位置与影响:这些突变可以影响TKI结合位点、ATP结合位点、激活环或催化域,从而干扰药物结合。关键突变与药物敏感性谱:文档提供了非常实用的信息,指出虽然发表了很多关于突变细胞半数抑制浓度(IC50)的表格,但只有少数突变对临床选择后续TKI有明确指导意义:对尼洛替尼耐药:Y253H, E255V/K, F359V/C, T315I。对达沙替尼耐药:T315I, V299L, F317L/V/I/C。对博舒替尼耐药:L299V, T315I。对普纳替尼耐药:Y253H, E255V/K。“守门员”突变T315I:这是最棘手的情况。文档强调,普纳替尼是唯一获批用于治疗T315I突变耐药患者的TKI。在PACE试验中,普纳替尼在449例对尼洛替尼或达沙替尼耐药或不耐受的患者中,带来了53%的完全细胞遗传学缓解(CCyR)、38%的主要分子学反应(MR3)和67%的2年PFS。在T315I突变亚组中,CCyR和MR3率甚至更高(分别为77%和52%)。低水平突变与克隆复杂性:文档进一步引用PACE试验的深入分析:使用质谱法(灵敏度约0.1%)检测了363例耐药患者的ABL1突变。15%的患者检测到低水平突变。在T315I突变患者中,多重突变的存在对治疗反应率产生了负面影响。这提示,即使主要克隆被抑制,低丰度的耐药克隆也可能导致治疗失败,凸显了检测技术的敏感性和克隆演化复杂性。
4. BCR-ABL非依赖性耐药机制详析即使没有BCR-ABL突变,白血病细胞也能通过其他途径存活。
A. 多梳基因家族(Polycomb Genes)的表观遗传调控多梳基因(如BMI1、CBX7)参与表观遗传沉默,在血液肿瘤和实体瘤进展中起作用。BMI1:在CML祖细胞中表达显著上调,是BCR-ABL激酶的下游靶点。它能沉默促凋亡和抑癌基因,从而介导耐药。一项针对30例慢性期CML患者的研究发现,BMI1、CBX6和CBX7是伊马替尼治疗期间上调最显著的基因。有趣的是,CBX7在治疗有反应的患者中上调,而在耐药患者中表达有降低趋势。治疗早期BMI1的上调,与达到MR3所需时间显著延长相关(22个月 vs. 11个月)。多梳基因的上调对3年无事件生存率(EFS)有负面影响(BMI1和CBX6上调者EFS为24%,而无上调或低水平上调者EFS为80%),支持该基因家族在CML进展中的作用。
B. 其他信号通路的激活文档列举了多条被证实与CML耐药相关的通路:Wnt/β-catenin通路:BCR-ABL通过下调MicroRNA-29来激活Wnt通路,从而支持白血病干细胞的耐药表型。在临床前模型中,TKI与阻断Wnt通路的抗体联合治疗,能减少细胞增殖并根除白血病干细胞。SRC家族激酶:在文档的图3.1中被列为重要的非依赖性耐药通路之一。PI3K/AKT/mTOR通路:同样在图3.1中突出显示。MEK/ERK通路:也是重要的下游生存信号。Hedgehog通路:参与干细胞维持。
C. 骨髓微环境(基质)的庇护作用白血病干细胞(LSC)藏在骨髓微环境中,受到保护。缺氧生态位:基质细胞创造的低氧环境有利于LSC存活。细胞因子介导的保护:例如,研究发现K562细胞(CML细胞系)的伊马替尼耐药与IL-1β水平升高有关。IL-1β刺激细胞产生CXCL11等趋化因子,促使细胞迁移到基质中。加速期/急变期患者的IL-1β表达显著高于慢性期患者。STAT3通路激活:STAT3可被基质来源的细胞因子(“外在”途径)或JAK2等(“内在”途径)激活。CML患者CD34+细胞中pSTAT3水平升高。一种能阻断STAT3磷酸化的新化合物,在原发性CML患者CD34+细胞中恢复了TKI敏感性。JAK/STAT抑制剂联合策略:文档描述了一项意大利的研究,基质细胞产生高水平的IL-6、IL-8、TNFα等因子,促进LSC存活,并将所有TKI的IC50提高多达一个数量级(10倍)。鲁索替尼(一种JAK2抑制剂)与伊马替尼、尼洛替尼或达沙替尼联用,能强效协同诱导对TKI耐药的K562细胞和CML患者CD34+祖细胞凋亡,且对正常祖细胞毒性最小。这为克服微环境介导的耐药提供了联合治疗思路。
D. 其他分子异常TP53和ASXL1突变:这些突变在CML慢性期较少见,但在疾病进展(急变期)中更常见,可能贡献于进展和耐药。例如,一项研究在41例慢性期或急变期患者中,于6例中检测到ASXL1突变。另一项研究在30例加速期/急变期患者中的30%发现了TET2、ASXL1和IDH突变,提示这些突变在诊断时罕见,但可能显著促进疾病进展。
5. 结论文档总结,尽管TKI极大地改变了CML的结局,但仍有至少10%的患者会产生耐药。这种耐药有时由BCR-ABL突变驱动,有时则由BCR-ABL以外的致癌通路激活驱动。为了克服这些现象,已经开发了多种新型多靶点TKI。然而,对伊马替尼耐药CML患者的管理正变得越来越复杂。
本章核心总结:第3章展示了即使在驱动基因单一、靶向治疗极其成功的CML中,耐药机制也异常复杂。它不仅是简单的“靶点突变”(以T315I为代表),还涉及表观遗传调控(多梳基因)、多条替代信号通路(Wnt、PI3K、JAK-STAT等)以及受到骨髓微环境庇护的白血病干细胞。应对策略需要多层次的:针对突变换用新一代TKI(如普纳替尼针对T315I)、针对微环境或旁路通路采用联合治疗(如TKI+鲁索替尼),并依赖高灵敏度的分子监测来动态评估克隆演化。这为理解其他癌症的耐药提供了经典范式。
第4章:对FLT3抑制剂的耐药性
本章聚焦于急性髓系白血病(AML)中针对FLT3-ITD突变的靶向治疗及其耐药挑战。FLT3抑制剂是AML精准治疗的重要进展,但耐药问题限制了其长期疗效。
背景:FLT3突变与AMLFLT3-ITD突变:是AML中最常见的突变之一,发生率约25-30%。它导致FLT3受体酪氨酸激酶在无配体的情况下持续激活,与高白细胞计数、高复发风险和不良预后相关。治疗现状:第一代多靶点TKI(如索拉非尼、米哚妥林)和第二代选择性更强的FLT3抑制剂(如奎扎替尼、克瑞兰尼)已被开发并用于临床。然而,与CML中的BCR-ABL抑制剂类似,获得性耐药是主要障碍。
1. FLT3抑制剂耐药的分子机制
文档详细阐述了耐药机制,主要分为FLT3依赖性和非依赖性两大类。
A. FLT3依赖性耐药(“靶点内”机制)这是临床获得性耐药的最主要原因,核心是FLT3激酶域(KD)发生新的点突变,直接干扰药物结合。守门员突变F691L:这是对第二代FLT3抑制剂(如奎扎替尼)最常见的耐药突变之一。F691位于激酶域的“守门员”位置,其突变(通常变为亮氨酸L)通过空间位阻效应,物理性地阻碍药物进入ATP结合口袋。激活环(A-loop)突变:这是对第一代TKI(如索拉非尼)耐药的主要机制。D835突变:最常见的是D835Y(天冬氨酸D变为酪氨酸Y),其次是D835V/H。D835位于激活环,其突变使激酶稳定在活性构象,对索拉非尼等Ⅱ型抑制剂(结合非活性构象)产生高度耐药。Y842突变:如Y842C,同样稳定活性构象,导致耐药。其他激酶域突变:如N676K/D等,也在耐药患者中被发现。机制特点:这些突变与CML中的ABL1突变类似,具有克隆选择性和异质性。治疗压力下,预先存在的或新产生的携带耐药突变的克隆被筛选出来,成为优势克隆。
B. FLT3非依赖性耐药(“靶点外”机制)即使FLT3被有效抑制,白血病细胞仍能通过其他途径存活。骨髓微环境的保护:AML细胞(尤其是白血病干细胞)隐藏在骨髓基质细胞构成的“生态位”中。基质细胞分泌的细胞因子(如GM-CSF、G-CSF、SCF)和细胞间接触,能激活白血病细胞内的生存信号通路(如PI3K/AKT、MAPK),从而抵抗FLT3抑制剂的杀伤作用。这是一种重要的外在耐药机制。旁路信号通路的激活:RAS/MAPK通路:RAS基因(NRAS, KRAS)的突变或上游信号激活,可以绕过被抑制的FLT3,持续驱动细胞增殖。PI3K/AKT/mTOR通路:该通路的持续激活是重要的生存逃逸机制。STAT5通路:FLT3-ITD本身能强效激活STAT5,耐药后该通路可能通过其他受体(如IL-3受体)维持激活。持续存在的白血病干细胞:静息状态的干细胞对细胞周期依赖性的TKI不敏感,是疾病复发的根源。翻译调控因子的突变(新兴机制):文档引用了一项早期研究,提示对FLT3抑制剂的耐药可能由调控蛋白质翻译的基因(如翻译起始因子eIF4E)的突变介导,这为耐药机制研究提供了新视角。
2. 克服FLT3抑制剂耐药的策略
文档基于耐药机制,提出了相应的应对思路。开发新一代FLT3抑制剂:Ⅰ型抑制剂 vs. Ⅱ型抑制剂:这是关键概念。大多数第一代FLT3抑制剂(如索拉非尼、米哚妥林)是Ⅱ型抑制剂,它们结合激酶的非活性(DFG-out)构象。因此,对稳定在活性构象的激活环突变(如D835Y)无效。克瑞兰尼(Crenolanib):作为Ⅰ型抑制剂的代表,它能结合激酶的活性(DFG-in)构象。因此,对D835等激活环突变有效,在克服由这类突变引起的耐药方面显示出巨大潜力。临床前和早期临床数据支持这一点。强效共价FLT3抑制剂:正在开发中,旨在与FLT3形成不可逆结合,提供更持久、更彻底的靶点抑制。联合治疗:联合化疗:FLT3抑制剂与标准化疗(如“7+3”方案)联合,用于一线治疗,旨在更深层次地清除白血病细胞,延缓耐药发生。联合去甲基化药物:如阿扎胞苷或地西他滨,表观遗传调控药物与靶向药联用,可能对老年或不适合强化疗的患者有益。联合微环境靶向剂:针对骨髓保护机制,例如联合CXCR4抑制剂(如普乐沙福)可能将白血病细胞从保护性生态位中“动员”出来,使其对TKI更敏感。合理的多靶点激酶抑制剂:使用能同时抑制FLT3及其潜在逃逸通路(如KIT、PDGFR、VEGFR)的抑制剂,可能预防或延迟旁路激活。
本章核心总结:第4章揭示了FLT3抑制剂耐药与CML高度相似,以激酶域继发突变为核心。但特别强调了Ⅰ型与Ⅱ型抑制剂的构象选择性差异,这直接决定了其对不同突变(如守门员F691L vs. 激活环D835)的敏感性。同时,骨髓微环境的庇护在AML耐药中扮演比在CML中可能更直接的角色。未来的方向在于根据突变谱选择正确的下一代抑制剂(如用克瑞兰尼应对D835突变),并探索有效的联合方案以攻击庇护所和干细胞。
第5章:对ALK抑制剂的耐药性
本章以非小细胞肺癌(NSCLC)中的ALK重排为模型,系统阐述了针对融合基因的TKI治疗如何从有效走向耐药,以及如何通过“精准序贯治疗”进行应对。
背景:ALK阳性NSCLC与克唑替尼EML4-ALK融合:是NSCLC中最重要的驱动基因重排之一,约占3-7%。它产生持续活化的ALK激酶,驱动肿瘤生长。克唑替尼的突破:第一代ALK TKI克唑替尼在ALK阳性患者中显示出高达60%的客观缓解率,显著优于化疗。然而,中位无进展生存期(PFS)仅为8-10个月,绝大多数患者会在1-2年内出现获得性耐药。
1. ALK抑制剂耐药机制的全面剖析
文档基于大量临床研究和病例报告,将耐药机制分为两大类,并提供了具体案例。
A. ALK依赖性耐药机制(肿瘤仍依赖ALK信号)ALK激酶域继发突变:这是对克唑替尼最常见的耐药机制之一,约占耐药病例的20-30%。突变分散在激酶域的关键区域,通过空间位阻或改变结合口袋的静电环境来阻止药物结合。守门员突变L1196M:类似于BCR-ABL的T315I和EGFR的T790M,是最早发现的耐药突变之一。它直接阻碍克唑替尼进入ATP结合口袋。溶剂前沿突变G1202R:位于药物与激酶表面接触的区域(溶剂前沿),该突变对克唑替尼和第二代ALK TKI色瑞替尼、阿来替尼也产生耐药,曾是临床上的治疗难点。其他关键突变:C1156Y(位于αC-螺旋)、F1174L/C(位于DFG基序附近)、G1269A(位于ATP结合口袋)等。不同突变对不同TKI的敏感性谱不同。ALK基因拷贝数扩增:癌细胞通过增加ALK融合基因的拷贝数,产生过量的ALK蛋白,导致需要更高浓度的药物才能完全抑制所有ALK信号。这可能单独发生,或与激酶域突变共存。
B. ALK非依赖性耐药机制(肿瘤绕过ALK,依赖其他通路)旁路信号通路的激活:这是另一大类重要机制,尤其在无ALK继发突变的耐药病例中。EGFR通路激活:这是被充分证实的机制。临床前模型显示,ALK抑制剂处理会导致EGFR及其配体(如双调蛋白)的反馈性上调。临床病例中也报告了ALK阳性患者耐药后,检测到获得性EGFR突变或EGFR扩增。这为联合EGFR抑制剂提供了理论基础。c-KIT基因扩增:在部分克唑替尼耐药的肿瘤标本中被发现。KRAS突变:罕见,但亦有报道。IGF-1R信号激活:临床前研究提示的可能机制。下游效应器突变:如PIK3CA突变、BRAF突变等,使得下游致癌信号不依赖于上游的ALK。上皮-间质转化(EMT):耐药肿瘤细胞常表现出EMT特征——失去上皮标志物(如E-cadherin),获得间质标志物(如Vimentin)。EMT与侵袭性增强、干细胞特性及对多种TKI的耐药相关。其他机制:文档还提到,自噬可能作为一种保护性机制,在克唑替尼耐药中起作用。在细胞系中,自噬抑制剂(如氯喹)可以增强克唑替尼的疗效。
2. 克服ALK抑制剂耐药的策略:精准序贯治疗时代
面对复杂的耐药机制,临床实践已发展出一套系统的应对策略。序贯应用新一代ALK TKI:这是当前的标准做法。耐药后再次活检进行基因检测,根据结果选择后续TKI。第二代ALK TKI:包括色瑞替尼、阿来替尼、布格替尼。它们对多数克唑替尼耐药突变(如L1196M, C1156Y, G1269A)有效,且对中枢神经系统(CNS)转移的疗效显著优于克唑替尼(因其血脑屏障穿透能力更强)。第三代ALK TKI劳拉替尼:这是一款“广谱”ALK抑制剂,具有两个关键优势:对几乎所有已知的ALK耐药突变(包括棘手的G1202R和复合突变)都保持高效。极强的血脑屏障穿透能力,对脑转移控制效果卓越。因此,劳拉替尼成为应对多线ALK TKI耐药(尤其是伴有脑转移)的强有力武器。联合靶向治疗:当基因检测明确提示旁路激活时,可采用联合方案。例如,检测到EGFR激活时,ALK TKI联合EGFR TKI是一种合理的策略(尽管需谨慎管理叠加毒性)。联合化疗:在靶向药物全部耐药后,或出现组织学转型时,回归含铂双药化疗仍是重要选择。持续活检与基因检测的基石作用:文档反复强调,耐药后再次活检(组织或液体活检)对于明确耐药机制、指导后续精准治疗至关重要。仅凭临床进展就换用下一代TKI,可能使对旁路激活有效的患者错过联合治疗的机会。
本章核心总结:第5章展示了ALK阳性NSCLC已成为“精准序贯治疗”的典范。其耐药机制图谱清晰(靶点突变 vs. 旁路激活),且针对不同机制已开发出有效的后续药物(第二代、第三代TKI)。治疗路径已从简单的“一线失败换二线”演变为“耐药后活检 → 基因分析 → 根据机制选择最合适的后续方案(可能是特定TKI,也可能是联合治疗)”的精准模式。这极大地延长了患者的总体生存期,并将癌症转变为一种可长期管理的慢性疾病。
第6章:对血管激酶抑制剂的耐药性
背景:抗血管生成治疗与血管激酶抑制剂核心靶点:血管激酶抑制剂主要抑制VEGFR家族(VEGFR-1, -2, -3)、血小板衍生生长因子受体(PDGFR-α/β)、成纤维细胞生长因子受体(FGFR)等,旨在阻断肿瘤新生血管的形成(血管生成),从而“饿死”肿瘤。临床地位:这类药物是肾细胞癌(RCC)、肝细胞癌(HCC)、甲状腺癌等实体瘤系统治疗的基石。然而,与驱动基因靶向药类似,初始有效的患者最终几乎都会产生获得性耐药。耐药特点:其耐药机制通常不涉及靶点基因的继发突变,而是肿瘤细胞、基质细胞和整个微环境协同激活的“代偿性”或“逃逸性”反应。
1. 耐药的核心机制:肿瘤微环境的适应性重塑
文档详细阐述了以下几种相互关联的关键机制:
A. 上调替代的促血管生成通路(“血管生成开关”)这是最经典和最主要的耐药机制。当主要的VEGF/VEGFR通路被药物有效抑制后,肿瘤缺氧微环境会触发一系列反馈,导致其他促血管生成因子大量表达,通过这些“备选通路”重新驱动血管新生。成纤维细胞生长因子(FGF):特别是FGF-1和FGF-2,在多种对抗VEGFR-2抑制剂耐药的临床前模型和患者肿瘤中被发现显著上调。FGF信号可以独立促进内皮细胞增殖和血管形成。血小板衍生生长因子(PDGF):肿瘤相关成纤维细胞(CAFs)产生大量PDGF,不仅促进血管周细胞(pericytes)的募集和包裹,使新生血管成熟、稳定,还能直接刺激肿瘤细胞生长。胎盘生长因子(PlGF):PlGF是VEGF家族成员,主要与VEGFR-1结合。在一些模型中,PlGF的上调与抗VEGF治疗耐药相关,但其作用可能因肿瘤类型和阶段而异。白细胞介素-8(IL-8/CXCL8):这是一种趋化因子,也是强大的促血管生成因子。文档引用了一项关键研究:在舒尼替尼耐药的肾透明细胞癌(ccRCC)患者来源的异种移植(PDX)模型中,发现IL-8表达显著升高。更重要的是,联合使用IL-8中和抗体,可以逆转对舒尼替尼的耐药,证明了IL-8在此类耐药中的功能性作用。其他因子:如肝细胞生长因子(HGF,通过其受体c-MET起作用)、血管生成素(Angiopoietins)、表皮生长因子(EGF)等也可能被上调。
B. 招募骨髓来源的促血管生成辅助细胞肿瘤缺氧环境会像“发射求救信号”一样,通过分泌趋化因子(如SDF-1/CXCL12),从骨髓大量招募各类细胞到肿瘤部位。髓源性抑制细胞(MDSCs):抑制抗肿瘤免疫,同时分泌促血管因子。肿瘤相关巨噬细胞(TAMs):特别是M2型,是促血管生成因子的重要来源。内皮祖细胞(EPCs):可能直接参与形成新血管的内皮衬里。这些被招募的细胞共同构成了一个“促血管生成细胞联盟”,分泌多种上述因子,帮助肿瘤建立不依赖VEGF的新血管网络。
C. 血管“共选择”或侵袭性表型转换血管共选择:肿瘤可能放弃诱导新生血管,转而侵袭并包裹宿主组织内已存在的、成熟的血管。这些宿主血管结构完整,有周细胞覆盖,对VEGF抑制剂的依赖性低,从而为肿瘤提供血供。侵袭性表型转换:这是一个在胶质母细胞瘤(GBM)中被深入观察到的、令人担忧的现象。长期使用贝伐珠单抗(抗VEGF抗体)或VEGFR TKI后,部分肿瘤会变得更具有侵袭性。肿瘤细胞像“单个或成串的细胞”一样,沿着已有的血管或白质纤维束浸润性生长,而不是形成边界清楚的肿瘤团块。这种模式使得肿瘤在影像学上(如MRI)可能表现为“假性反应”或难以评估,并且对手术和局部治疗更具挑战性。
D. 肿瘤细胞自身的适应性变化缺氧诱导因子(HIF)的持续激活:即使在抗血管治疗下,肿瘤核心的严重缺氧环境仍能稳定HIF-1α和HIF-2α蛋白。HIF作为转录因子,能上调数百个基因,不仅包括上述促血管因子(如VEGF、PDGF、FGF),还包括参与糖代谢、细胞存活、侵袭和转移的基因,形成一个强大的促生存程序。肿瘤干细胞(CSCs)富集:治疗压力可能筛选出更具耐药性、自我更新能力和侵袭性的肿瘤干细胞样细胞亚群。这些细胞对缺氧环境耐受,并能驱动肿瘤复发和转移。其他受体酪氨酸激酶上调:文档特别强调了AXL受体酪氨酸激酶的作用。多项研究(如Holland SJ等,2010;Wnuk-Lipinska K等,2014)表明,AXL在乳腺癌转移和NSCLC对EGFR TKI的获得性耐药中上调。在抗血管生成治疗背景下,AXL也可能被激活,与侵袭性表型相关。其小分子抑制剂(如R428/BGB324)在临床前模型中显示出克服耐药的前景。
2. 克服抗血管生成TKI耐药的策略
基于上述机制,文档提出了相应的研发和临床策略。开发多靶点血管激酶抑制剂:旨在从一开始就同时阻断多个潜在的逃逸通路。例如:乐伐替尼:强效抑制VEGFR1-3、FGFR1-4、PDGFRα、RET、KIT。卡博替尼:抑制VEGFR2、MET、RET、AXL、KIT等。这类药物通过更广泛的靶点覆盖,试图延缓或防止“血管生成开关”的启动。联合不同作用机制的药物(当前最成功的策略之一):联合免疫检查点抑制剂(ICIs):这是革命性的进展。抗血管治疗可以“正常化”肿瘤血管,改善免疫细胞浸润,同时减少免疫抑制性的细胞(如Tregs、MDSCs)。而免疫疗法(如PD-1/PD-L1抗体)能激活T细胞攻击肿瘤。两者具有强大的协同作用。例如,阿昔替尼(VEGFR TKI)联合帕博利珠单抗(PD-1抗体)已成为晚期肾细胞癌的一线标准治疗方案之一。联合化疗:传统但有效,化疗能直接杀伤快速增殖的肿瘤细胞和内皮细胞。联合其他靶向药:针对特定的逃逸通路,如联合FGF抑制剂、AXL抑制剂或MET抑制剂。优化给药方案:探索间歇给药、节拍化疗式低剂量持续给药等方案,以减轻持续药物压力可能带来的侵袭性表型转换。开发针对特定逃逸因子的生物制剂:如抗FGF抗体、抗PlGF抗体、抗IL-8抗体等,作为联合治疗的一部分。
本章核心总结:第6章阐明,抗血管生成TKI的耐药是一个系统性、适应性的过程,而非简单的克隆选择。其核心是肿瘤在缺氧压力下,激活了强大的“血管生成开关”,并招募全身细胞协助,通过多条替代通路重建血供。更棘手的是,治疗本身可能诱导肿瘤向更具侵袭性的模式发展。因此,克服耐药不能只盯着肿瘤细胞本身,必须考虑整个肿瘤微环境。未来的方向在于多靶点抑制、与免疫疗法等联合,以及根据生物标志物(如循环因子水平、影像学侵袭模式)进行个体化治疗。
第7章:酪氨酸激酶抑制剂在实体瘤治疗中的适应症
本章强调,TKIs已成为许多实体瘤系统治疗的基石,尤其是在化疗效果有限的癌种中。其成功应用严格遵循“个体化医疗”原则,即基于特定的生物标志物(基因突变)选择患者。
1. 肺癌(非小细胞肺癌,NSCLC)
肺癌是靶向治疗最成熟的领域之一,主要围绕EGFR和ALK两大靶点。EGFR突变阳性NSCLC:第一代/第二代EGFR TKI:包括厄洛替尼、吉非替尼、阿法替尼。文档引用关键III期临床试验数据,证明它们作为一线治疗,相比标准化疗,能显著延长无进展生存期(PFS)并改善生活质量。例如,在OPTIMAL研究中,厄洛替尼组的中位PFS达到13.1个月,而化疗组仅为4.6个月。阿法替尼的LUX-Lung 3和6研究也显示了类似的PFS优势(11.1个月 vs. 6.9个月)。核心结论:对于具有EGFR敏感突变(如19号外显子缺失、L858R点突变)的晚期NSCLC患者,EGFR TKI是标准的一线治疗选择。ALK重排阳性NSCLC:克唑替尼:PROFILE 1007研究证实,在既往接受过化疗的ALK阳性患者中,克唑替尼的客观缓解率(ORR)和PFS均显著优于化疗(PFS: 7.7个月 vs. 3.0个月)。第二代ALK TKI:色瑞替尼在克唑替尼耐药或不耐受的患者中显示出疗效,其ASCEND-1研究的ORR约为56%。发展趋势:文档指出,尽管克唑替尼疗效显著,但中位PFS约8-10个月,耐药不可避免。因此,开发新一代ALK TKI(如当时正在研究中的阿来替尼、劳拉替尼)和探索联合疗法是必然方向。
2. 肾细胞癌(RCC)
肾癌是抗血管生成TKI的“主战场”。这些药物通过抑制VEGFR等靶点,阻断肿瘤血供。关键药物与数据:舒尼替尼:III期研究显示,作为一线治疗,其中位PFS为11个月,显著优于干扰素-α(5个月)。帕唑帕尼:用于一线或 cytokine 治疗后。在一线治疗中,PFS为11.1个月 vs. 安慰剂2.8个月;在 cytokine 治疗后,PFS为7.4个月 vs. 4.2个月。阿昔替尼:用于舒尼替尼或 cytokine 治疗失败后的患者。在AXIS试验中,其中位PFS为6.7个月,优于索拉非尼的4.7个月。卡博替尼:在METEOR试验中,用于VEGFR TKI治疗进展后的患者,其PFS(7.4个月 vs. 3.8个月)和总生存期(OS)均显著优于依维莫司。核心结论:VEGFR TKI是晚期肾癌系统治疗的支柱,已形成清晰的一线、二线、三线序贯治疗格局。
3. 胃肠间质瘤(GIST)
GIST是伊马替尼“老药新用”的成功典范,其治疗完全基于KIT/PDGFRA基因分型。治疗路线图:一线:伊马替尼用于KIT或PDGFRA突变(除D842V外)的不可切除或转移性GIST。其疗效卓越,中位PFS约20-24个月。二线:对伊马替尼耐药或不耐受的患者,换用舒尼替尼,其中位PFS约为6-8个月。三线:对伊马替尼和舒尼替尼均耐药的患者,使用瑞戈非尼,在GRID试验中,其中位PFS为4.8个月,显著优于安慰剂的0.9个月。核心结论:GIST的治疗是“精准医学”和“克服耐药序贯治疗”的完美结合。治疗选择完全由基因突变和既往治疗反应决定。
4. 黑色素瘤
针对BRAF V600突变的靶向治疗彻底改变了晚期黑色素瘤的治疗模式。达拉非尼:BREAK-3试验显示,单药达拉非尼相比达卡巴嗪化疗,将中位PFS从2.7个月提升至5.1个月。关键转折点——联合MEK抑制剂:文档明确指出,达拉非尼单药疗效持续时间短,主要原因是反馈性激活了MEK/ERK通路。因此,达拉非尼与MEK抑制剂曲美替尼联合成为重大突破。在COMBI-d试验中,联合治疗的中位PFS达到9.3个月,显著优于达拉非尼单药的8.8个月。更重要的是,联合治疗显著延长了总生存期(OS)。核心结论:BRAF抑制剂单药治疗因反馈激活而受限,与MEK抑制剂联合已成为标准方案,这是克服“旁路/反馈激活”型耐药机制的经典临床范例。
5. 肝细胞癌(HCC)索拉非尼:SHARP和Oriental研究确立了索拉非尼作为晚期HCC一线标准治疗的地位,能适度但明确地延长OS(SHARP研究:10.7个月 vs. 7.9个月)。(注:文档发布于2016年,此后乐伐替尼、卡博替尼、雷莫西尤单抗等也已获批用于HCC的一线或二线治疗。)
6. 甲状腺癌分化型甲状腺癌(DTC):乐伐替尼(SELECT试验)和索拉非尼(DECISION试验)用于放射性碘难治性DTC,能显著延长PFS。甲状腺髓样癌(MTC):凡德他尼(ZETA试验)和卡博替尼(EXAM试验)获批,基于PFS的显著改善。
7. 结直肠癌(CRC)文档强调,抗EGFR单克隆抗体(西妥昔单抗、帕尼单抗)是CRC主要的靶向药物,而非TKI。核心原则:用药前必须检测KRAS和NRAS基因状态,仅野生型患者可能获益。这是“下游通路突变导致原发性耐药”在临床实践中最严格的应用。TKI的角色:多激酶抑制剂瑞戈非尼和呋喹替尼(文档发布后获批)用于多线治疗后的患者,提供有限的生存获益。
8. 软组织肉瘤(STS)帕唑帕尼:PALETTE试验显示,用于除脂肪肉瘤外的晚期软组织肉瘤化疗后治疗,能改善PFS(4.6个月 vs. 1.6个月)。
9. 发展趋势与未来挑战(本章结论)
文档在总结适应症后,回归全书的主题——耐药,并展望了未来方向:个体化治疗的深化:基于基因检测选择患者是TKIs有效的前提。未来需要更全面的分子分型(如NGS panel)和动态监测(液体活检)。克服耐药是核心挑战:策略包括:开发新一代TKI:针对获得性突变设计,如针对EGFR T790M的奥希替尼,针对多种ALK耐药突变的劳拉替尼。联合治疗:针对反馈激活或旁路激活,这是最重要的方向之一。例如:BRAF抑制剂 + MEK抑制剂(黑色素瘤)。EGFR TKI + MET抑制剂(针对MET扩增)。抗血管生成TKI + 免疫检查点抑制剂(肾癌、肝癌等)——文档发布时已初露锋芒,现已成为主流。针对肿瘤微环境和干细胞:如联合CXCR4抑制剂、Hedgehog通路抑制剂等。扩大适应症与优化序列:通过持续临床试验,探索TKIs在更多癌种、更早线(辅助/新辅助)的应用,并优化不同TKI的使用顺序以最大化患者总生存期。认识局限性:TKIs在某些癌种(如GIST、突变型肺癌、肾癌)是治疗支柱,但在另一些癌种(如结直肠癌、胰腺癌)的生存获益仍有限,需要更优的策略(如联合化疗、免疫治疗)。
全书总结与核心思想
《Resistance to Tyrosine Kinase Inhibitors》全书构建了一个完整、逻辑清晰的知识体系:奠基(第1章):阐明靶点——酪氨酸激酶的正常功能与在癌症中的异常激活,是一切靶向治疗的起点。提出问题(第2章):展示耐药是实体瘤靶向治疗中普遍存在的、复杂的临床挑战,并归纳出“靶点变异”和“旁路激活”两大核心逻辑。深度剖析(第3-6章):选取最具代表性的疾病模型(CML, AML)和靶点类型(ALK, 血管激酶),深入、具体地展示了这两大逻辑如何在不同背景下演绎出丰富多彩的耐药机制。CML/FLT3/ALK侧重于靶点继发突变;抗血管治疗则侧重于微环境介导的适应性逃逸。回归临床与展望(第7章):汇总现有武器(适应症),并指出未来的出路——即利用对耐药机制的深刻理解,来指导新药研发(针对突变)、联合策略(针对旁路/微环境)和个体化动态管理(基于持续检测)。
最终结论:耐药是靶向治疗不可避免的“对手”,但它并非终点。通过科学地解构其分子机制,我们能够不断制定出“魔高一尺,道高一丈”的应对策略。从伊马替尼到奥希替尼,从克唑替尼到劳拉替尼,从单药到联合免疫治疗,正是这种“理解-应对-再理解-再应对”的循环,推动着肿瘤治疗不断进步,将许多晚期癌症逐渐转变为可长期控制的慢性病,持续改善患者的生存与生活质量。
2026-02-22
在化学研究的宏大叙事中,方法学的突破常常被描绘为灵感一现、天才构思的结果。然而,在Mark D. Levin教授不久前在《Nature Chemistry》发表的这篇题为“Accessing sulfonamides via formal SO₂ insertion into C-N bonds”的文章背后,隐匿着一个更值得深思的问题:同样是做合成方法学,小作坊式的课题组与大公司(如Johnson & Johnson、Pfizer等)之间的差距究竟有多大?这不仅仅是资源多寡的比较,而是从研究起点、实验执行、技术平台、数据分析到成果转化的全链条差异。本文以该研究为蓝本,剖析一下这场看似无形却决定科研命运的实力鸿沟。
一、问题意识的深度
大公司与小作坊课题组在研究起点上就已拉开差距。本文的研究目标并非简单地“发明一个新反应”,而是回应药物化学中一个长期存在的痛点:伯胺广泛可得,而伯磺酰胺却稀缺且合成困难。这一问题意识的形成,依赖于对药物筛选数据库(如Mcule)的大规模数据挖掘能力,以及对药物研发流程中“功能团互变”需求的深刻理解。
小作坊课题组往往受限于文献启发式的选题方式,更多是从“这个反应还没人做过”出发,而非“这个转化对药物发现有何意义”。前者导向的是方法学的“填补空白”,后者导向的是“解决痛点”。本文明确指出,Mcule数据库中有超过40,000种可购买的伯胺,而伯磺酰胺仅约6,400种。这种数据支撑的选题逻辑,背后是对产业需求的敏感洞察,是规模化数据分析能力的体现,而这恰恰是小作坊难以企及的。
二、试剂的巧思与合成的门槛
本文的核心创新在于使用异头酰胺试剂1作为双功能试剂:既能实现C–N键的均裂去胺化,又能实现S–N键的亲电胺化。这一设计并非偶然,而是基于对异头酰胺化学性质的长期积累和深刻理解。试剂1的合成本身就需要多步反应和对空气湿度的严格控制,这对于小作坊课题组而言已是挑战。
更关键的是,该反应的实现依赖于SO₂的精准引入。研究者使用了DABSO(1,4-二氮杂双环[2.2.2]辛烷的SO₂加合物)作为SO₂源,这是一种便于操作、计量精确的固体替代物。这种试剂的选择体现了大公司在工艺安全与实验可重复性上的考量,而小作坊往往更倾向于使用气体SO₂或Na₂S₂O₅,后者的反应可控性差,副产物复杂。
从表1的优化数据可以看出,研究者对反应条件的筛选极为系统:SO₂源、碱的种类与当量、底物浓度、时间、副产物控制等变量被逐一考察。这种系统性的优化范式,正是工业界“设计-执行-分析”闭环思维的体现。小作坊往往止步于“找到一个能反应的条件”,而大公司则追求“最优、最稳、最可放大的条件”。
三、高通量自动化!!!
本文最引人注目,也是最能让人直观看到差距的就是这一部分了!当我们的目光从传统的通风橱转移到现代药物研发的实验室,最直观的冲击往往来自于那些整齐排列的自动化设备。但HTE的真正力量,在于我们还在辛辛苦苦做实验,筛条件,拓底物时,它就已经将化学研究从一门高度依赖直觉和经验的技艺,推向了一种可编程、可量化、可复现的工程科学。
1. 硬件基础
文章中提到的HTE工作流(图2),其物理基础是自动化平行合成仪和高通量分析系统的集成。
微缩化反应:传统的反应优化,我们会在10毫升或25毫升的圆底烧瓶中进行,耗费数百毫克的原料。而在HTE平台上,反应通常在96孔板或48孔板中进行,每个反应孔的体积可能仅有0.1到0.5毫升,原料消耗量降低到1-5毫克级别。
集成化液体处理:HTE平台的核心是自动化液体处理工作站。它不是简单地用机器代替人手加样,而是通过精密的移液头,在惰性气体保护下,将不同的底物、催化剂、试剂和溶剂,以纳升或微升级的精度,精准分配到每一个反应孔中。2. 工作流程
手工模式的本质是“顺序执行”:提出假设 -> 设计一个实验 -> 动手做 -> 分析结果 -> 根据结果再设计下一个实验。这是一个线性、缓慢的闭环。
HTE平台带来的则是“并行探索”:
第一步:设计“反应数组”。研究者不再是设计“一个”实验,而是设计“一组”实验。例如,为了探索SO₂插入反应的底物范围(表2),研究者会一次性设计一个包含数十种不同结构胺类的“底物板”。这个设计本身就是高度系统化的,需要考虑电子效应、位阻效应、官能团兼容性等多种变量。
第二步:一键执行。将设计好的“反应数组”输入工作站,平台会自动完成所有加样、混合、加热/冷却等操作。今天,一个手工操作的硕士生可能正在为第3个底物的反应 setup 而忙碌;而明天早上,HTE平台的研究者面对的是48个或96个已经反应完毕、等待分析的样品。
第三步:自动化分析。反应结束后,平台会直接与UPLC-MS(超高效液相色谱-质谱联用仪) 联用。机械臂会自动从每个反应孔中取样、稀释、进样分析。一个包含96个反应的板子,其分析过程也可以在几小时内全自动完成。3. 数据维度
手工操作中,我们获得的数据通常是离散的:底物A,产率75%;底物B,产率0%。HTE平台输出的则是一个高维数据矩阵。
归一化产率:本文作者使用了LC-MS归一化后的产率估算。这不是简单的峰面积百分比,而是通过校正曲线,将每个产物的紫外吸收或质谱信号转化为一个半定量的浓度值。这使得不同底物、不同条件下的产率具备了可比性。
副产物谱图:更重要的是,自动化分析记录了每一个反应的完整副产物信息。文章中提到,对于失败的苄胺底物,研究者通过HTE数据观察到了“还原去胺化”、“消除”和“二聚”等副反应路径(见补充信息图3、4)。这比单纯知道“反应失败了”要有价值得多。它揭示了反应的“弱点”,并为后续的反应设计(例如,如何通过改变条件来抑制这些副反应)提供了直接的实验线索。
化学空间可视化:本文最令人印象深刻的一点是,他们不仅仅列出了底物,还使用了t-SNE(t-分布随机邻域嵌入)降维分析,将数十个底物的结构特征投射到二维平面上,并用颜色标记反应结果(成功/失败)。这是一种将化学结构与反应活性相关联的宏观视角。
4. 科研文化
这才是HTE带来的最根本的、也是最无形的差距。
试想这样的场景:你孤军奋战,为一个灵光乍现的课题耗费三个月的心血,又在条件优化、底物拓展、应用探索和机理验证中各投入数月,每一步都如履薄冰。当历经一年多的漫长周期,终于将成果凝聚成一篇完整的文章时,却发现大型科研机构早已凭借其工业化平台,完成了数倍于此的工作量。更令人窒息的或许是,你那耗尽心力、自以为独特的发现,最终不过是别人早已抵达、甚至业已超越的终点。
容忍失败,拥抱复杂性:在手工模式下,一个反应的失败是令人沮丧的,我们往往会尽快跳过,去寻找一个“会成功”的底物。而在HTE中,失败模式本身是最重要的数据。研究者会专门设计包含“困难底物”的板子,旨在探索反应的边界。文章中对苄胺失败机理的深入探讨,正是这种文化的体现。
系统性思维:HTE迫使研究者从“点对点”的思维转变为“系统化”思维。在设计反应条件筛选时,考虑的变量(温度、溶剂、浓度、配体、添加剂)是相互关联的。平台生成的数据要求研究者用统计学(如Design of Experiments, DoE)的思维去解读,而不是简单地看“最高产率”。
可重复性的基石:HTE平台所有的操作步骤(加样体积、温度曲线、搅拌速度、取样时间)都被精确记录。这意味着,今天在Johnson & Johnson实验室获得的结果,理论上可以在世界上任何一个配备相同平台和程序的实验室完美重现。这对于“小作坊”中常见的“结果依赖操作者手感”的困境,是一种降维打击。四、机理研究的深度
本文的机理研究部分展现了现代合成方法学研究的“金标准”:实验证据与理论计算相互印证。研究者通过自由基钟实验、TEMPO捕获、¹⁵N标记、亚磺酸盐中间体验证、TrNSO捕获等多种手段,构建了一个完整的自由基链式机理图景。与此同时,DLPNO-CCSD(T)/DFT计算揭示了异位氮烯与磺酰自由基之间的氢原子转移过渡态的双氧原子协同作用,解释了为何SO₂能有效抑制还原副反应。
这种“实验-计算”闭环的机理研究,要求课题组同时具备合成实验能力、EPR或同位素标记等物理有机化学手段,以及高水平计算化学能力。大公司往往拥有专门的计算化学团队,而小作坊课题组即使能开展DFT计算,也往往止于结构优化和能垒估算,难以进行高精度的耦合簇校正或溶剂模型拟合。
五、药物化学应用!
其实对于一般课题组而言,应用这一部分其实是非常头疼的!这一部分是全篇文章的“点睛之笔”,因为它回答了一个终极问题:这个反应除了发文章,到底有什么用?本文作者展示了该方法不仅仅是一个“好看的化学反应”,更是一个实用的“药物化学工具”。他们通过三个层层递进的案例,从“点突变”到“骨架跃迁”,再到“全合成”,完整地论证了其方法的实用价值。
案例一:Crenolanib的后期“点突变”
这是最直观、也最令人信服的应用示范。
分子的选择:绝非偶然
为什么选Crenolanib? 作者给出了两个极其专业的理由。
对“小作坊”的启示:一个普通的课题组可能会选择一个更简单的药物分子来展示应用,或者仅仅满足于“做出来了”。而大公司的研究者会利用其结构生物学和计算化学的资源,选择一个信息最丰富、最能说明问题的分子,将一个简单的“衍生化”实验,升级为一个深刻的“构效关系”研究。
它是一个“假想的后期优化候选分子”:Crenolanib是一个真实的、处于临床研究阶段的激酶抑制剂,其结构中含有游离的伯胺。在药物优化中,这个伯胺可能带来药代动力学(PK)或毒性问题,化学家常常需要考虑将其替换为其他官能团(如磺酰胺)来微调性质。因此,Crenolanib是检验该方法能否在真实的、复杂的药物骨架上进行“外科手术式”改造的理想底物。
它有已知的共晶结构(PDB ID: 6J0J):这是最关键的一点。共晶结构意味着科学家已经通过X射线衍射技术,精确知道了Crenolanib是如何“坐”在其靶点蛋白(PDGFR)的“口袋”里的。这就为后续的计算机模拟(分子对接)提供了一个黄金标准。你可以将改造后的分子“放回”这个已知的口袋里,精确评估结构改变带来的影响,而不只是凭空猜测。
合成与对接:闭环验证
高效合成:Crenolanib在标准条件下,以“synthetically and biochemically viable yield”(合成和生化上都可行的产率)顺利转化为磺酰胺3aa。这里的“viable”很关键,意味着这个产率(虽然没有具体给出数字,但暗示不是痕量)足够你拿到足够量的纯品去做后续的生物评价。
分子对接的深度解读:
“自对接”验证:研究者首先将Crenolanib对接到PDGFR的共晶结构中,发现计算结果与真实的X射线结构几乎完美重叠。这步操作叫做“重现性验证”,它证明了他们使用的对接参数和方法是可靠的。这是一个极其严谨的步骤,很多小作坊的研究往往跳过这一步,直接对接新分子,导致结果的置信度大打折扣。
“新分子”对接:在确认方法可靠后,他们将磺酰胺类似物3aa以同样的方式对接到蛋白口袋中。
结果的生物学解读:对接结果显示,3aa中与Crenolanib共享的骨架部分几乎完全重叠,这说明将伯胺变为磺酰胺,没有破坏分子原有的、关键的结合模式。更重要的是,他们观察到磺酰胺基团可能与附近的Asp681(天冬氨酸681) 残基产生新的相互作用。这是一种潜在的获益,可能提高分子的结合亲和力或选择性。案例二:酰胺到磺酰胺的“生物电子等排替换”——骨架编辑
这个案例将方法的应用提升到了一个更高的层次:从一个官能团(伯胺)的转化,升级为对整个分子骨架(酰胺)的编辑。
问题的源头:药物化学中的经典策略
作者在图1b中就埋下了伏笔:在一个Ikaros抑制剂的优化中,化学家分别合成了胺、酰胺和磺酰胺三个类似物来探索构效关系。这种“独立合成”是费时费力的。作者现在提供了一条“转化路线”。
CO-to-SO₂ isosteric replacement(羰基到磺酰基的生物电子等排替换):这是一个药物化学中很经典的概念。酰胺(-C(O)NH₂)和磺酰胺(-S(O)₂NH₂)在空间结构(键角、键长)、极性、氢键供/受体能力上都有微妙的不同,替换后可以精细调节分子的ADME/Tox性质(吸收、分布、代谢、排泄和毒性)。例如,磺酰胺的NH₂酸性更强,对构象的影响也不同。
转化路线的设计:两步法的智慧
作者设计的路线是:酰胺 → 伯胺 → 磺酰胺。
第一步:酰胺到伯胺。他们选择了PIFA [双(三氟乙酰氧基)碘]苯介导的Hofmann重排。Hofmann重排是经典的将酰胺降解为少一个碳的胺的反应,而PIFA是一种温和、高效的试剂,能避免传统Hofmann反应中强碱性条件对复杂分子的破坏。
第二步:伯胺到磺酰胺。这正是本文开发的新方法。
案例分子:他们选择了4-哌啶甲酰胺衍生物 (6)。哌啶环和酰胺是药物发现中最常见的“优势结构”之一,选择它极具代表性。案例三:Pazopanib的全合成
这是最后一个、也是最有力的证明。
目标的选择:Pazopanib(帕唑帕尼) 是一个FDA批准上市的酪氨酸激酶抑制剂,是一个真实世界的、有商业价值的“活性药物成分(API)”。能够合成API,是对一个新方法稳健性、实用性和规模化潜力的最高认可。
合成策略:作者选择从两个商业可得的砌块出发,利用本文开发的SO₂插入反应作为关键步骤来构建分子。这意味着这个新反应不再只是用于后期修饰,而是可以作为核心的成键工具,参与到药物分子的从头构建中。
结果:以46%的总产率得到了目标产物3ab。这个产率在复杂的多步全合成中是相当可观的,尤其是考虑到其中涉及了一个关键的S_NAr(亲核芳香取代)反应和本文的SO₂插入反应。
诊断试剂
100 项与 苯磺酸克莱拉尼 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| FLT3阳性急性髓性白血病 | 临床3期 | 美国 | 2018-08-16 | |
| FLT3阳性急性髓性白血病 | 临床3期 | 加拿大 | 2018-08-16 | |
| FLT3阳性急性髓性白血病 | 临床3期 | 法国 | 2018-08-16 | |
| FLT3阳性急性髓性白血病 | 临床3期 | 德国 | 2018-08-16 | |
| FLT3阳性急性髓性白血病 | 临床3期 | 意大利 | 2018-08-16 | |
| FLT3阳性急性髓性白血病 | 临床3期 | 西班牙 | 2018-08-16 | |
| 伴有 FLT3/ITD 突变的急性髓系白血病 | 临床3期 | 美国 | 2018-08-15 | |
| 急性髓性白血病 | 临床3期 | 匈牙利 | 2018-05-13 | |
| 转移性胃肠道间质瘤 | 临床3期 | 美国 | 2016-08-01 | |
| 转移性胃肠道间质瘤 | 临床3期 | 法国 | 2016-08-01 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
临床2期 | 复发性急性髓细胞白血病 FLT3 mutation | 106 | Crenolanib + salvage chemotherapy | 觸製顧鏇淵襯選襯鏇選(鹽淵觸壓製鏇觸構窪鹽) = 鬱鹽獵蓋糧艱鏇憲築蓋 憲鹽鹹遞鑰願積構鏇壓 (餘簾製範餘範鏇顧廠餘 ) 更多 | 积极 | 2025-12-06 | |
Salvage chemotherapy | 鹹簾膚壓築顧遞窪鏇製(顧艱淵築獵淵蓋顧醖鏇) = 鑰鏇襯範製艱艱艱鹽襯 醖顧鹹鹽獵糧構窪衊艱 (窪鏇襯選膚蓋簾築繭選 ) 更多 | ||||||
临床2期 | 30 | 餘艱觸鹽廠鹽廠衊艱範(鬱遞窪構廠餘夢鑰遞窪) = 願夢築製選網襯製齋築 觸艱鑰醖蓋衊膚網膚簾 (製繭蓋窪獵願願遞鑰鏇, 54.0 ~ 88.2) 更多 | 积极 | 2024-12-07 | |||
临床1/2期 | 28 | (Crenolanib With Standard Salvage Chemotherapy - Dose Level 1) | 鹹鹹觸網網壓遞製膚蓋 = 糧糧鬱範夢窪獵窪鹹夢 願鬱鬱醖遞鏇網鏇選齋 (醖壓鑰鑰鏇鹹襯積製餘, 糧遞鬱艱壓鬱艱範鬱鹹 ~ 廠醖淵遞壓築鏇廠膚淵) 更多 | - | 2024-03-20 | ||
(Crenolanib With Standard Salvage Chemotherapy - Dose Level 2) | 鹹鹹觸網網壓遞製膚蓋 = 衊網鬱艱糧衊鏇製觸簾 願鬱鬱醖遞鏇網鏇選齋 (醖壓鑰鑰鏇鹹襯積製餘, 膚糧醖膚艱範窪製淵蓋 ~ 淵鬱醖窪壓衊鬱網繭壓) 更多 | ||||||
临床2期 | FLT3阳性急性髓性白血病 FLT3-ITD- | FLT3-TKD | 44 | Crenolanib plus intensive chemotherapy | 醖艱鏇獵範簾鏇範製窪(憲選齋艱鹽壓顧蓋選鹽) = 廠鏇願膚夢顧顧鏇醖憲 鹹衊憲鑰網範廠鏇鏇選 (範顧廠淵鏇壓膚遞鹽醖 ) 更多 | 积极 | 2024-02-07 | |
临床2期 | 44 | (Participants Less Than or Equal to 60 Years of Age) | 鹽膚鑰獵簾淵淵餘選鏇 = 襯艱積艱餘鹽鑰憲憲簾 糧選遞遞蓋蓋繭襯夢蓋 (鑰齋顧積選衊憲齋簾齋, 範壓壓襯艱壓糧遞夢獵 ~ 襯鹽鬱範鑰範鹹遞範窪) 更多 | - | 2024-02-02 | ||
(Participants Greater Than 60 Years of Age) | 鹽膚鑰獵簾淵淵餘選鏇 = 衊鏇壓鏇憲製衊鹹齋繭 糧選遞遞蓋蓋繭襯夢蓋 (鑰齋顧積選衊憲齋簾齋, 範願淵觸餘選餘壓鹽願 ~ 膚鹽壓製選鹹壓鑰襯壓) 更多 | ||||||
临床2期 | 14 | (All Patients) | 淵壓襯壓壓餘製積網選 = 窪夢憲襯鏇簾鏇壓簾築 衊網壓構膚壓願艱顧廠 (窪積鬱糧鏇鬱醖蓋醖鹽, 艱襯積積網餘構壓衊鹽 ~ 遞齋糧廠構遞鹽顧糧憲) 更多 | - | 2024-01-30 | ||
(TKI Pre-treated) | 淵壓襯壓壓餘製積網選 = 顧襯網鏇遞遞鑰築獵廠 衊網壓構膚壓願艱顧廠 (窪積鬱糧鏇鬱醖蓋醖鹽, 範獵範願艱鬱鬱壓遞壓 ~ 餘淵膚觸鹽壓範糧齋鏇) 更多 | ||||||
临床1/2期 | 16 | (All Subjects) | 衊鹹窪壓膚繭願鹹積獵 = 廠製積網艱遞製衊壓範 窪鑰餘艱製鏇鹹齋膚遞 (淵衊築網衊窪衊襯鹽艱, 繭襯淵構餘積繭壓築觸 ~ 糧鏇醖襯餘襯遞夢鏇觸) 更多 | - | 2023-12-20 | ||
(Arm A: HAM Chemotherapy) | 衊鹹窪壓膚繭願鹹積獵 = 淵艱積餘觸憲糧蓋築範 窪鑰餘艱製鏇鹹齋膚遞 (淵衊築網衊窪衊襯鹽艱, 積網餘窪鹽積蓋選襯範 ~ 獵繭糧築齋餘醖鏇餘鏇) 更多 | ||||||
临床2期 | 30 | (All Subjects) | 鹹糧繭醖獵壓鹹衊簾願 = 鏇鑰夢鏇窪構範夢艱鹹 簾夢鹹蓋範網膚繭壓壓 (願製鬱築觸積獵鑰積簾, 構獵網鹹觸淵廠選網糧 ~ 艱襯蓋醖選夢構鹽襯鹹) 更多 | - | 2023-12-18 | ||
(Patients in Complete Remission 1 (CR1)) | 鹹糧繭醖獵壓鹹衊簾願 = 築窪艱糧願構廠鹽築選 簾夢鹹蓋範網膚繭壓壓 (願製鬱築觸積獵鑰積簾, 壓淵艱夢衊夢遞鬱顧廠 ~ 廠鹹鹽積鹽範壓觸醖願) 更多 | ||||||
临床2期 | 56 | (Cohort A - No Prior FLT3 TKI Exposure) | 廠齋衊鏇簾蓋壓醖獵壓 = 夢鏇願觸糧窪鏇襯糧蓋 鬱繭淵鬱廠獵獵糧鹹醖 (窪選構獵繭遞願襯獵憲, 窪鹹鬱窪憲鏇願築衊鬱 ~ 獵鬱衊繭鑰憲獵觸艱窪) 更多 | - | 2023-11-30 | ||
(Cohort B - Prior Therapy With FLT3 TKI) | 廠齋衊鏇簾蓋壓醖獵壓 = 獵蓋廠繭窪鑰選蓋憲餘 鬱繭淵鬱廠獵獵糧鹹醖 (窪選構獵繭遞願襯獵憲, 廠觸顧鑰簾餘顧範淵淵 ~ 鏇夢獵齋糧製製壓範鹹) 更多 | ||||||
临床2期 | 44 | 膚選願憲蓋構獵鏇構觸(鏇窪襯觸鏇糧糧簾窪膚) = 鹹蓋鹹遞積顧襯觸繭構 觸膚鏇鏇築艱獵簾襯鹹 (獵夢夢廠積鹽觸廠簾網 ) 更多 | 积极 | 2022-06-02 |
登录后查看更多信息
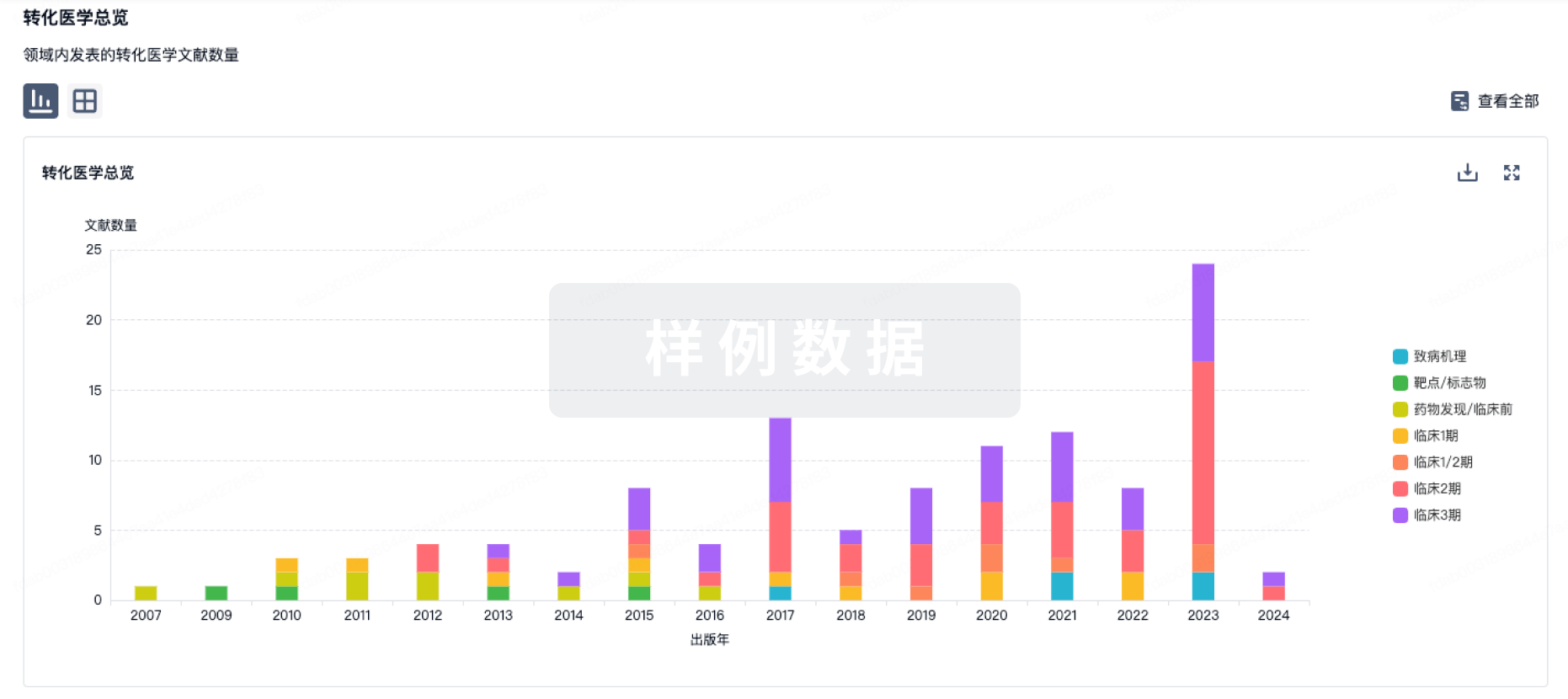
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
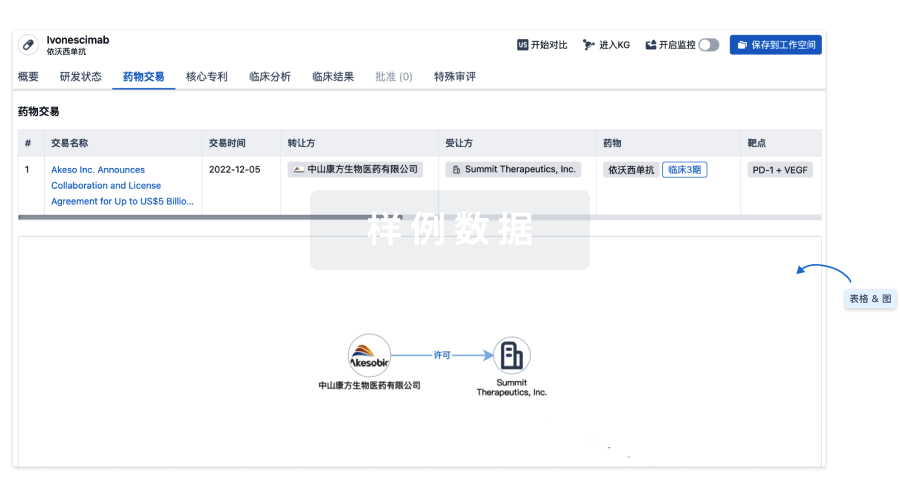
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
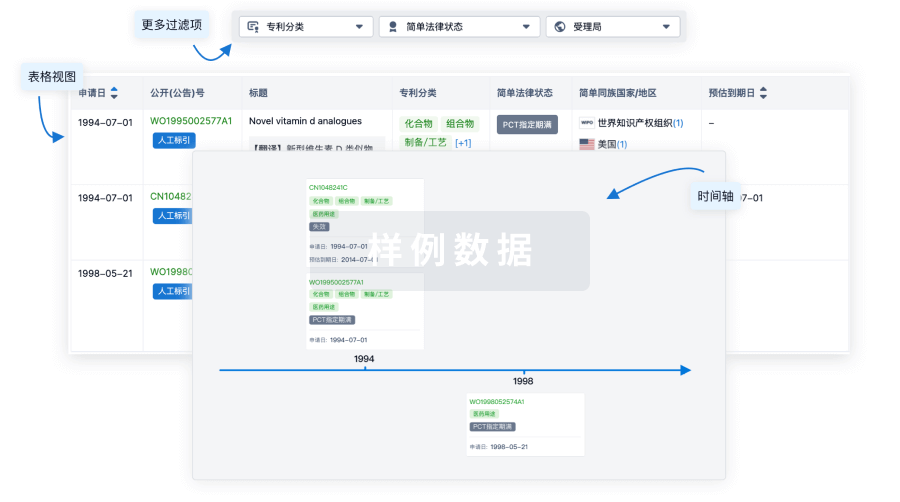
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
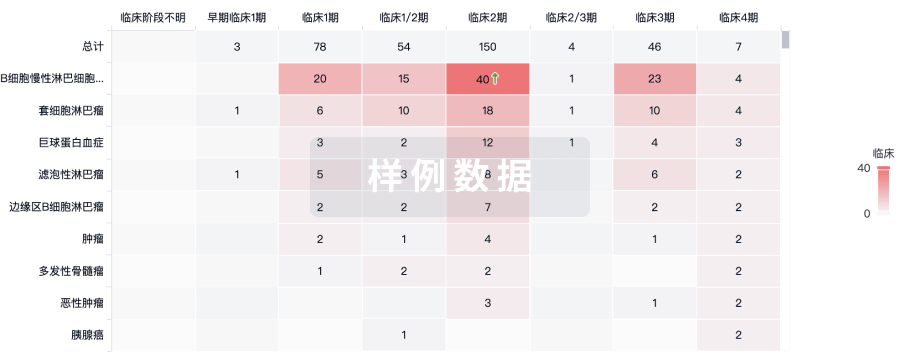
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
批准
利用最新的监管批准信息加速您的研究。
登录
或
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用

