安进/阿斯利康开发TSLP 单抗Tezepelumab获FDA突破性疗法认定,治疗COPD
近日,安进(Amgen)公司在2024年第二季度财报中表示,该公司与阿斯利康(AstraZeneca)合作开发的“first-in-class”单抗Tezspire(tezepelumab)获得FDA授予的突破性疗法认定,作为附加维持疗法,治疗中度至极重度慢性阻塞性肺病(COPD)患者,这些患者具有嗜酸性粒细胞表型。两家公司正在计划在COPD患者中启动3期临床试验。
Tezepelumab是一款“first-in-class”人源性、靶向抗胸腺基质淋巴细胞生成素(TSLP)的单克隆抗体。TSLP是位于许多炎症级联反应顶端的上皮细胞因子,能引发对过敏性、嗜酸性和其他类型气道炎症的过度免疫反应。该疗法在2021年12月获美国FDA批准作为附加维持疗法,治疗12岁以上儿童和成人严重哮喘患者。
突破性疗法认定的授予是基于2a期临床试验COURSE的结果,此前公布的数据显示,tezepelumab能够降低中度或重度COPD恶化的发生率。在第52周时,与安慰剂相比,tezepelumab治疗使中度或重度COPD急性发作的年发生率数值降低了17%,但统计学上并不显著(90% CI:-6,36;单侧p值=0.1042)。然而,重要的是,这项概念验证研究显示,在血液嗜酸性粒细胞计数(BEC)≥150细胞/µL的患者中,tezepelumab与安慰剂相比,中度或重度COPD恶化发生率在数值上减少了37%。研究显示,约65% COPD患者的BEC≥150细胞/μL。在BEC≥300细胞/μL的患者中,tezepelumab导致中度或重度COPD恶化的发生率在数值上减少了46%。
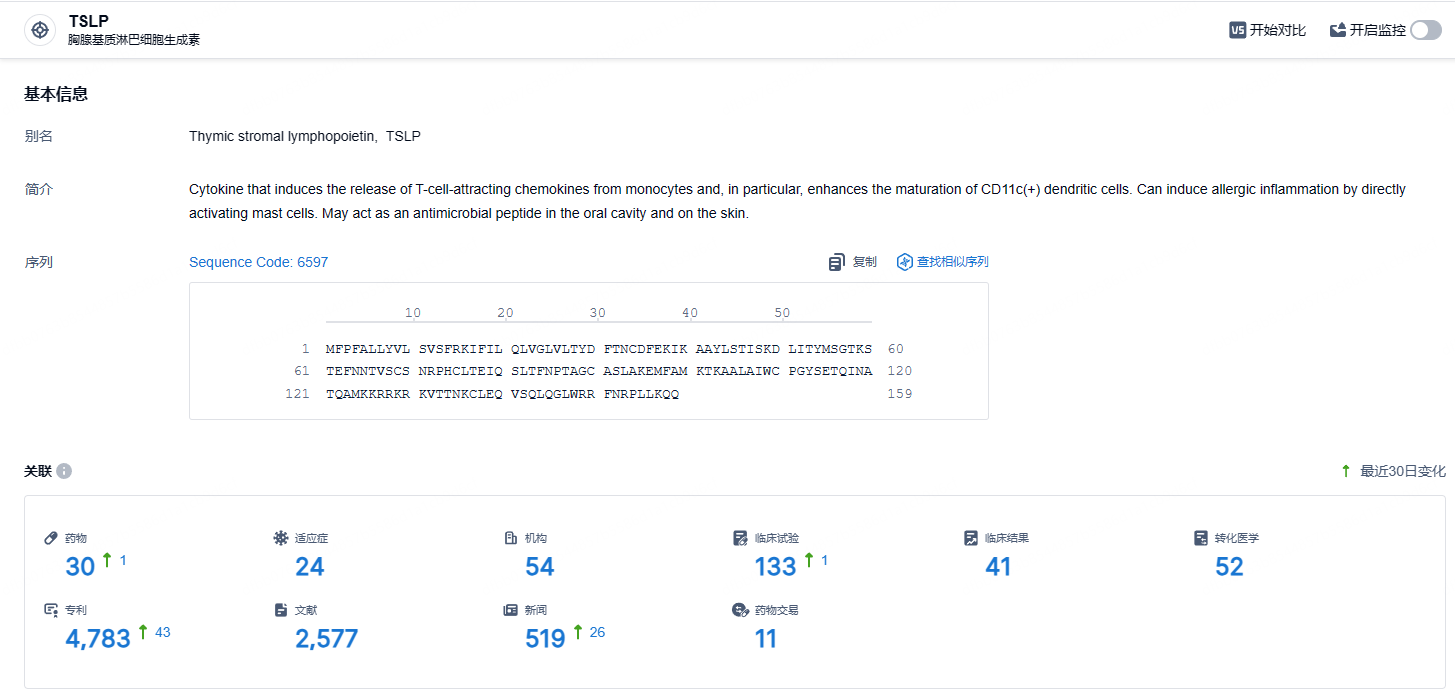
根据智慧芽新药情报库所披露的信息 (点击下方图片直达TSLP靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到2024年8月13日,TSLP靶点共有在研药物30个,包含的适应症有24种,在研机构54家,涉及相关的临床试验133件,专利多达4783件……Tezepelumab作为一种用于治疗严重哮喘的生物制剂,通过阻断TSLP-TSLPR相互作用发挥着治疗作用。对于药物依赖性哮喘患者,Tezepelumab也表现出了良好的耐受性。Tezepelumab在治疗未受控制的重度哮喘方面展现出了显著的临床疗效,为哮喘患者带来了新的治疗选择。