阿斯利康AKT抑制剂Capivasertib在华申报上市,治疗乳腺癌
2023年10月10日,CDE官网显示,阿斯利康AKT抑制剂Capivasertib上市申请获得受理。根据临床试验进展,推测适应症为联合Faslodex(氟维司群)治疗激素受体阳性(HR+)、人表皮生长因子受体2阴性(HER2-)局部晚期或转移性乳腺癌患者,这些患者在接受内分泌基础方案治疗过程中或之后疾病复发或进展。
Capivasertib 是一种新型、高效、选择性 ATP 竞争性泛 Akt 激酶抑制剂,在三种亚型 AKT1、AKT2 和 AKT3 中具有相似的活性。此药品在2023年1月获FDA授予快速通道资格。Capivasertib在早期试验中的结果便展现出不俗潜力,无论患者的 PIK3CA/AKT1/PTEN 突变状态如何,均可获得临床获益。氟维司群是一种雌激素受体拮抗剂、内分泌疗法。两者的联合疗法在临床试验中展现出对乳腺癌患者优秀的治疗效果。
Capivasertib的NDA得到了3期CAPItello-291试验(NCT04305496)数据的支持。该研究评估了Capivasertib加氟维司群对比安慰剂加氟维司群治疗芳香化酶抑制剂治疗期间或之后复发或进展的局部晚期(无法手术)或转移性HR+/HER2-乳腺癌患者(N=708)的疗效。研究受试者被随机分配接受Capivasertib加氟维司群(n=355)或安慰剂加氟维司群(n=353)。双主要终点是整个试验人群和AKT通路生物标志物改变人群的无进展生存期;AKT通路内的改变发生在高达50%的晚期HR阳性乳腺癌患者中。结果显示,在总体人群中,与安慰剂加氟维司群相比,Capivasertib和氟维司群的组合将疾病进展或死亡的风险降低了40%。联合用药的中位无进展生存期(PFS)为7.2个月,氟维司群单药为3.6个月。在AKT通路改变的肿瘤患者中,与安慰剂加氟维司群相比,Capivasertib加氟维司群将疾病进展或死亡的风险降低了50%。联合治疗组的中位PFS为7.3个月,而氟维司群单独治疗组为3.1个月。
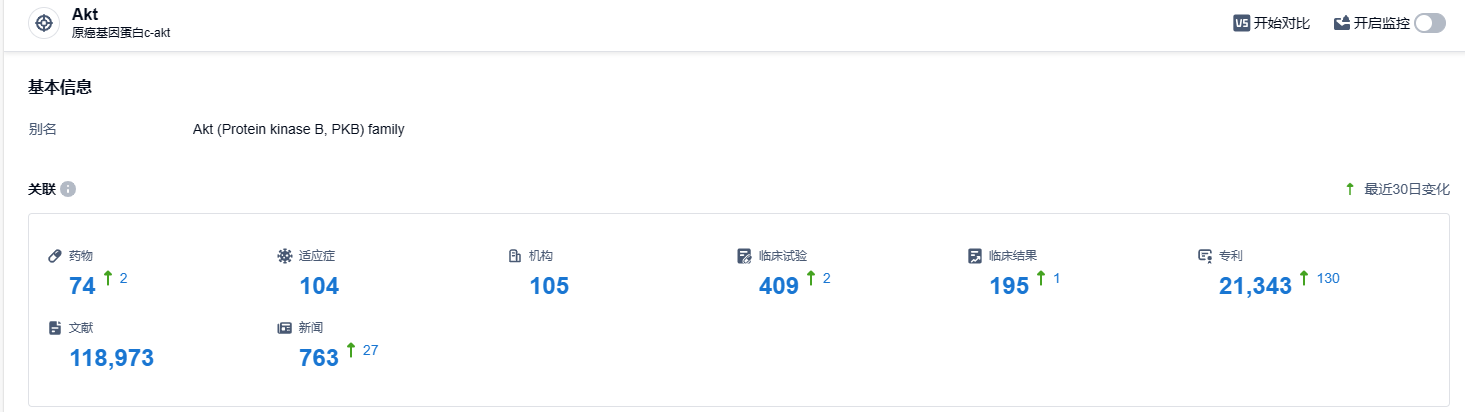
根据智慧芽新药情报库所披露的信息 (点击下方卡片直达 Akt靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2023 年10月11日,Akt靶点共有在研药物74个,包含的适应症有104种,在研机构105家,涉及相关的临床试验409件,专利多达21343件……期待Capivasertib能够顺利上市,这款潜在首创的AKT抑制剂有望给乳腺癌患者带来新的治疗选择。