百济神州PD-1制剂替雷利珠单抗获FDA批准上市,针对食管鳞状细胞癌
2024年3月15日,百济神州(BeiGene)宣布,美国FDA已批准其食管鳞状细胞癌PD-1抑制剂Tevimbra(tislelizumab,替雷利珠单抗)作为单药疗法,用于治疗既往接受过全身化疗,针对(不包括PD-1或PD-L1类疗法),患有不可切除或转移性食管鳞状细胞癌(ESCC)的成年患者。
百泽安®(替雷利珠单抗注射液)是一款人源化IgG4抗程序性死亡受体1(PD-1)单克隆抗体,设计目的旨在最大限度地减少与巨噬细胞中的Fcγ受体结合。临床前数据表明,巨噬细胞中的Fcγ受体结合之后会激活抗体依赖细胞介导杀伤T细胞,从而降低了PD-1抗体的抗肿瘤活性。百泽安®是第一款由百济神州的免疫肿瘤生物平台研发的药物,目前正进行单药及联合疗法临床试验,以开发一系列针对实体瘤和血液肿瘤的广泛适应症。2021年1月,百济神州曾与诺华就PD-1抗体替雷利珠单抗达成首付款6.5亿美元,总价超22亿美元的合作,百济神州瑞士授予诺华在美国、加拿大、墨西哥、欧盟成员国、英国、挪威、瑞士、冰岛、列支敦士登、俄罗斯和日本开发、生产和商业化替雷利珠单抗的权利。根据授权协议,诺华负责在授权国家的注册申请,并有权在获批后开展商业化活动。2023年9月19日晚间,百济神州宣布其自主研发抗PD-1抗体替雷利珠单抗(百泽安®)获得欧盟批准,作为单药用于治疗既往接受过含铂化疗的不可切除、局部晚期或转移性食管鳞状细胞癌(ESCC)的成人患者。同日,百济神州宣布,已与诺华签订了终止合作协议,即诺华退还PD-1药物替雷利珠单抗在美国、欧盟成员国等国家/地区的全球化开发、生产和商业化权益。2024年2月27日,百济神州宣布,美国食品和药物管理局(FDA)已经受理了替雷利珠单抗的生物制品许可申请(BLA),与含氟嘧啶和铂化疗联合治疗局部晚期不可切除或转移性胃或胃食管交界处(G/GEJ)腺癌患者。FDA预计将于2024 年12 月对该BLA作出决定。
FDA此次的批准主要基于RATIONALE 302临床3期试验的结果,该试验在意向治疗(ITT)人群中达到了主要终点。与化疗相比,Tevimbra对患者具有统计学和临床意义的生存获益。在ITT人群中,Tevimbra组的中位总生存期(OS)为8.6个月(95% CI:7.5,10.4),而化疗组为6.3个月(95% CI:5.3,7.0),两者具统计学差异(p=0.0001;HR=0.70;95% CI:0.57,0.85)。Tevimbra也展现优于化疗的安全性。Tevimbra最常见(≥20%)的不良反应,包括实验室异常、血糖升高、肝受损生物标志ALT与AST升高、肌肉骨骼疼痛、体重减轻和咳嗽。
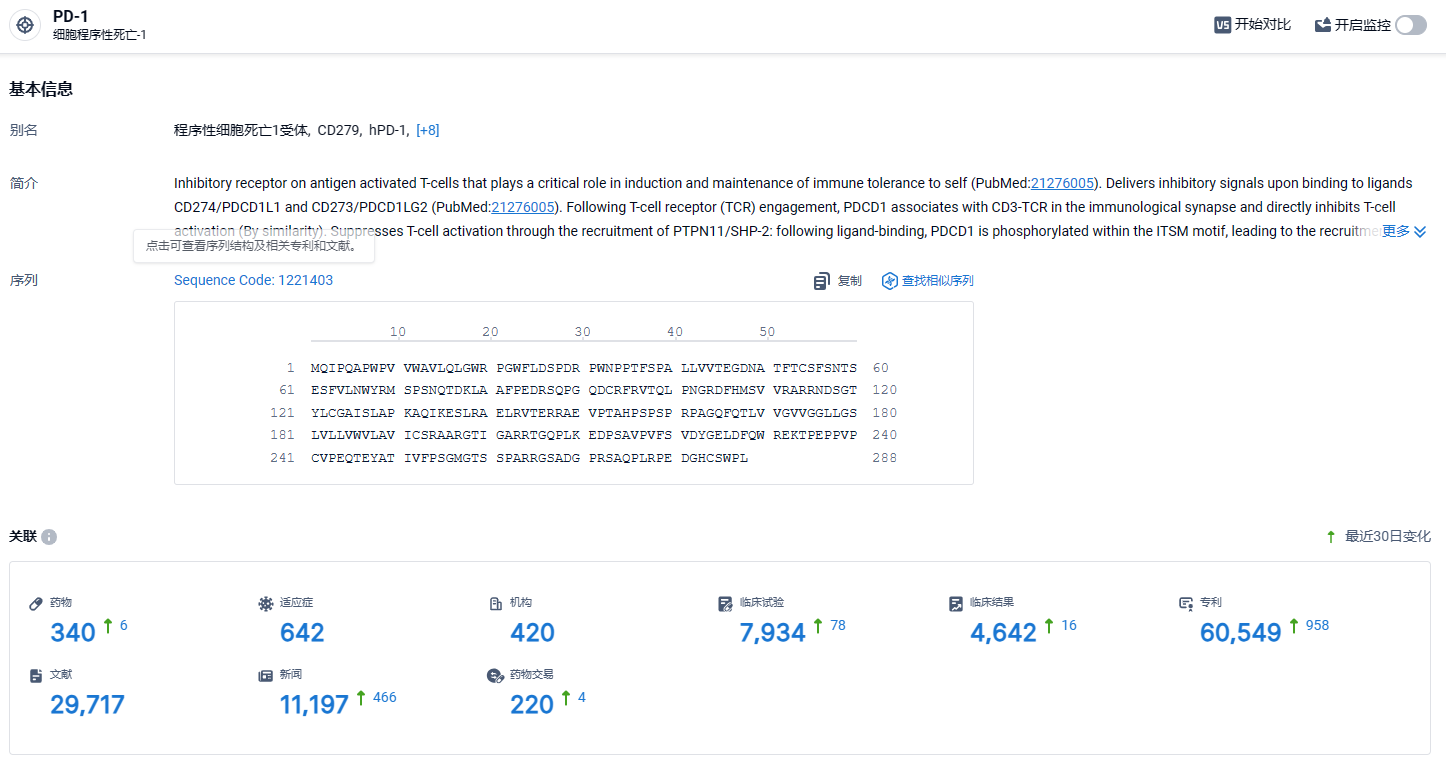
根据智慧芽新药情报库所披露的信息 (点击下方图片直达 PD-1 靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2024 年3月16日,PD-1 靶点共有在研药物340个,包含的适应症有642种,在研机构420家,涉及相关的临床试验7934件,专利多达60549件……PD-1/PD-L1靶点是研发非常火热的领域,国内目前已经有16款相关新药上市,替雷利珠单抗2022年在国内销售额高达18.36亿元。在这一红海市场,商业化与更进一步的临床推进成了药企pk的重中之重。作为首款在欧美均成功获批的国产PD-1单抗,替雷利珠单抗的商业化设计和临床设计非常值得国内PD-1/PD-L1新药企业的学习。期待有更多国产新药登陆欧美发达国家的医药市场。