勃林格殷格翰GCGR/GLP-1R双重激动剂Survodutide递交三项肥胖全球III期临床试验
2023年8月25日,勃林格殷格翰向中国NMPA递交了针对超重或肥胖人群的三项Survodutide(GCGR/GLP-1R双重激动剂)注册性III期国际多中心研究,此次递交与全球同步。这一决定是基于此前公布的一项针对超重或肥胖人群的2期剂量发现研究的数据。
Survodutide是勃林格殷格翰开发的一种GLP-1R/GCGR受体双重激动剂,可同时激活GLP-1和胰高血糖素受体。这两种受体在新陈代谢功能调控中起着至关重要的作用。 Survodutide由勃林格殷格翰和Zealand Pharma共同开发,是勃林格殷格翰在心-肾-代谢疾病领域研发产品组合的一部分。
此前公布的试验数据来自一项随机、平行组、剂量探索的2期临床试验,目的为评估与安慰剂相比,不患有2型糖尿病的超重或肥胖患者接受每周一次survodutide皮下注射达46周的疗效与安全性。分析显示,治疗46周后,接受最高或次高剂量survodutide治疗的患者中,40%体重减轻至少20%,而此数值在安慰剂组为0%。其中接受剂量达4.8 mg的survodutide治疗的患者中,有67%患者的体重减轻15%或以上,而此数值在安慰剂组仅为4.3%。患者的体重减轻在46周时尚未达到平台期,意味着接受治疗时间更长的话可能进一步减轻体重。
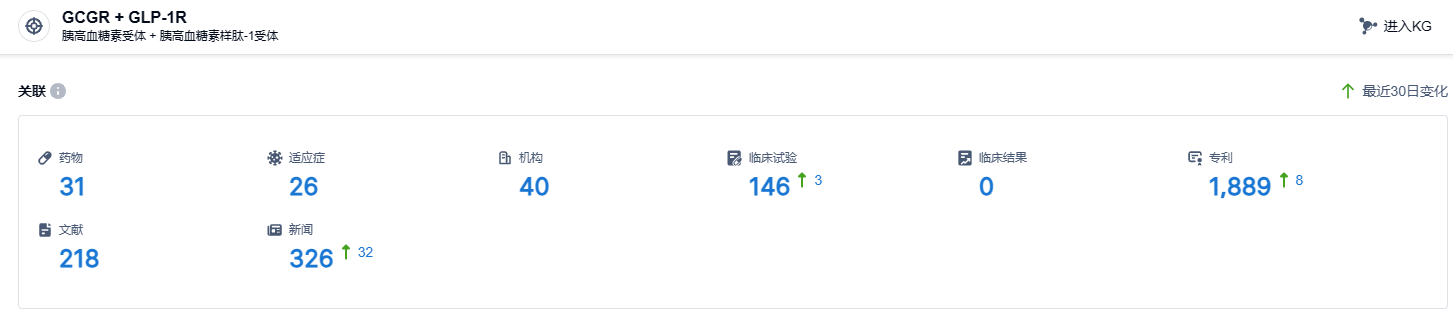
根据智慧芽新药情报库所披露的信息 (点击下方图片直达 GLP-1R/GCGR 靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2023 年8月29日,GLP-1R/GCGR 靶点共有在研药物31个,包含的适应症有26种,在研机构40家,涉及相关的临床试验146件,专利多达1889件……GLP-1R/GCGR双靶点新药在减肥、降糖、肝病等领域展现出优秀潜力,期待Survodutide的后续表现。