入选 “突破性研究”,药捷安康公布FGFR抑制剂tinengotinib最新研究结果
2024年4月12日,药捷安康宣布在2024年美国癌症研究协会(AACR)上公开核心产品tinengotinib针对携带FGFR1-3变异晚期泛实体瘤(单药)的最新研究成果。该项临床结果还入选了本次AACR会议的Late-Breaking Research(突破性研究)环节。
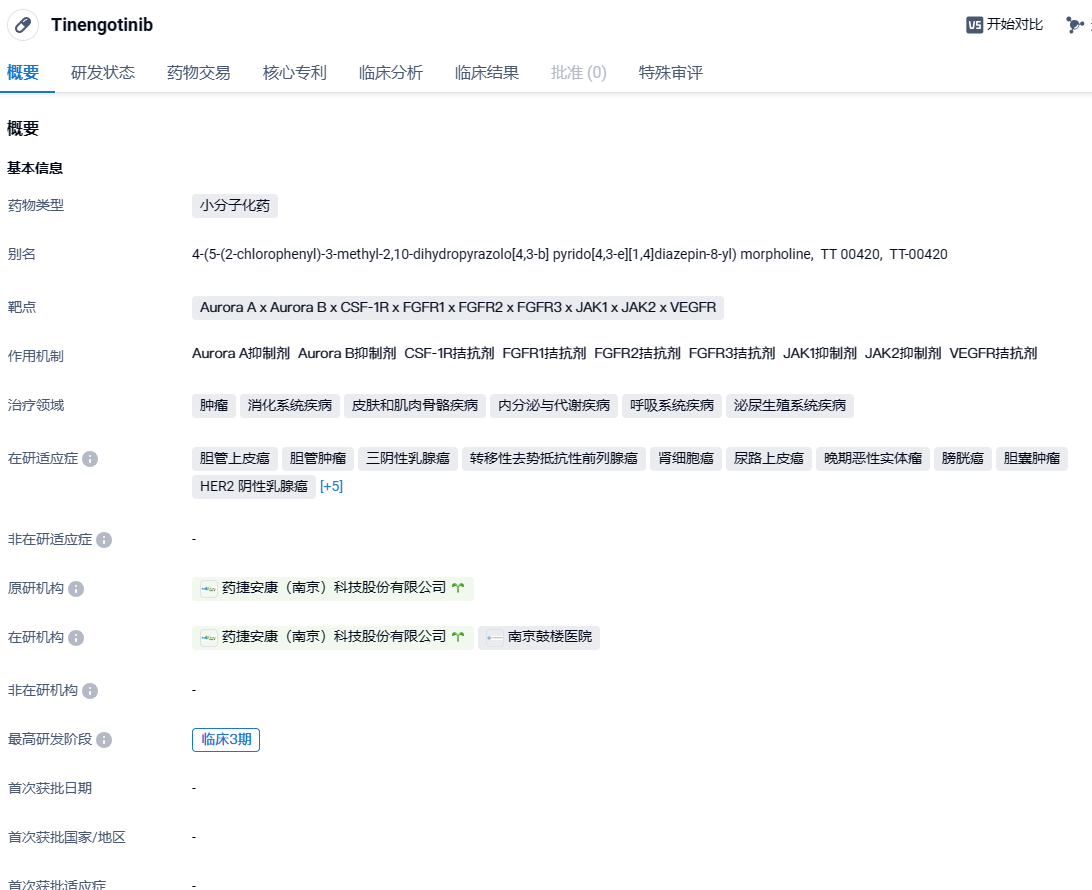
Tinengotinib是一款自主研发、全球3期临床阶段的创新激酶谱选择性小分子激酶抑制剂,通过靶向肿瘤细胞和改善肿瘤微环境发挥抗肿瘤作用。目前,tinengotinib已经在中美两地开展了多项针对胆管癌、前列腺癌、乳腺癌等实体瘤的临床试验,并获得了美国FDA授予的用于治疗胆管癌的“孤儿药认证”(Orphan Drug Designation)及“快速通道资格认证”(Fast Track Designation),中国NMPA批准纳入突破性治疗品种名单,欧洲 EMA 授予的用于治疗胆道癌的孤儿药认证(ODD)。
成纤维细胞生长因子受体(FGFRs)的变异广泛出现于多种恶性肿瘤中,是常见的致癌驱动因子。FGFR抑制剂已被证实对部分携带FGFR变异的肿瘤有效。tinengotinib和FGFR有非常特异性的结合模式,使得该产品对一系列FGFR 1-3的突变都保留了高活性。这些突变包括守门员突变、分子刹车突变、不可逆抑制剂结合位点突变等,这是该产品的差异化特点,也显示了tinengotinib针对FGFR变异的泛癌种治疗潜力。
在大会上,公司通过壁报形式展示了核心产品Tinengotinib针对携带FGFR1-3突变的晚期泛实体瘤患者的汇总研究数据。回顾性分析数据显示,Tinengotinib针对多种癌症都有疗效信号,包括胆管癌、乳腺癌、前列腺癌、尿路上皮癌、结肠癌及头颈癌。疗效为BOR 33.3%,DCR 88.2%,mPFS 6.90个月。这个积极的临床结果验证了Tinengotinib针对FGFR突变的潜力,以及针对晚期泛实体瘤患者的临床运用。
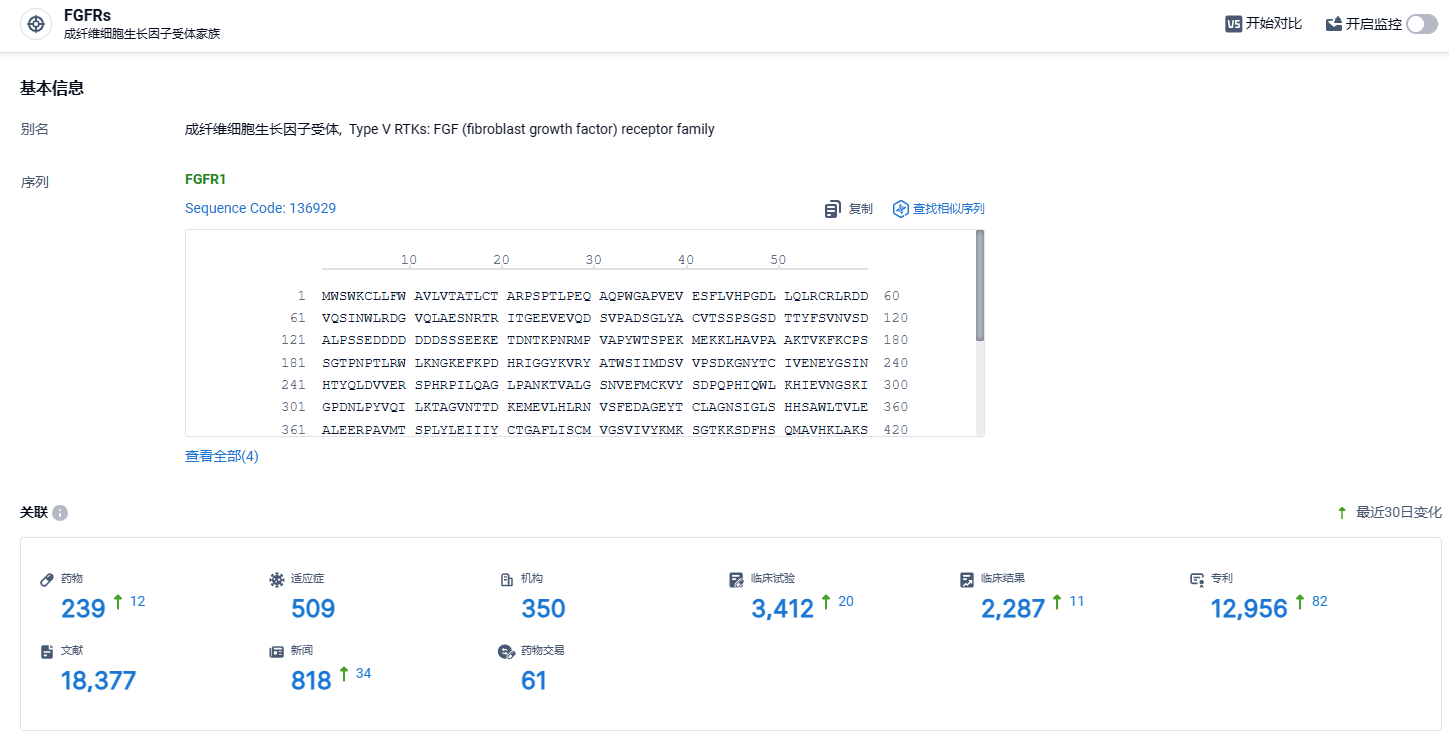
根据智慧芽新药情报库所披露的信息 (点击下方卡片直达FGFRs靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2024年4月13日,IL-5Rα靶点共有在研药物239个,包含的适应症有509种,在研机构350家,涉及相关的临床试验3412件,专利多达12956件……在全球范围内,尚无产品获批上市能够治疗携带FGFR1-3突变的晚期泛实体瘤。期待这款FGFR抑制剂能够早日在国内上市,给国内患者带来新的治疗选择。