预约演示
最新资讯
晖致/Mapi Pharma长效格拉替雷注射剂在美申报上市,治疗多发性硬化症
2023-08-09
阅读时长 2分钟
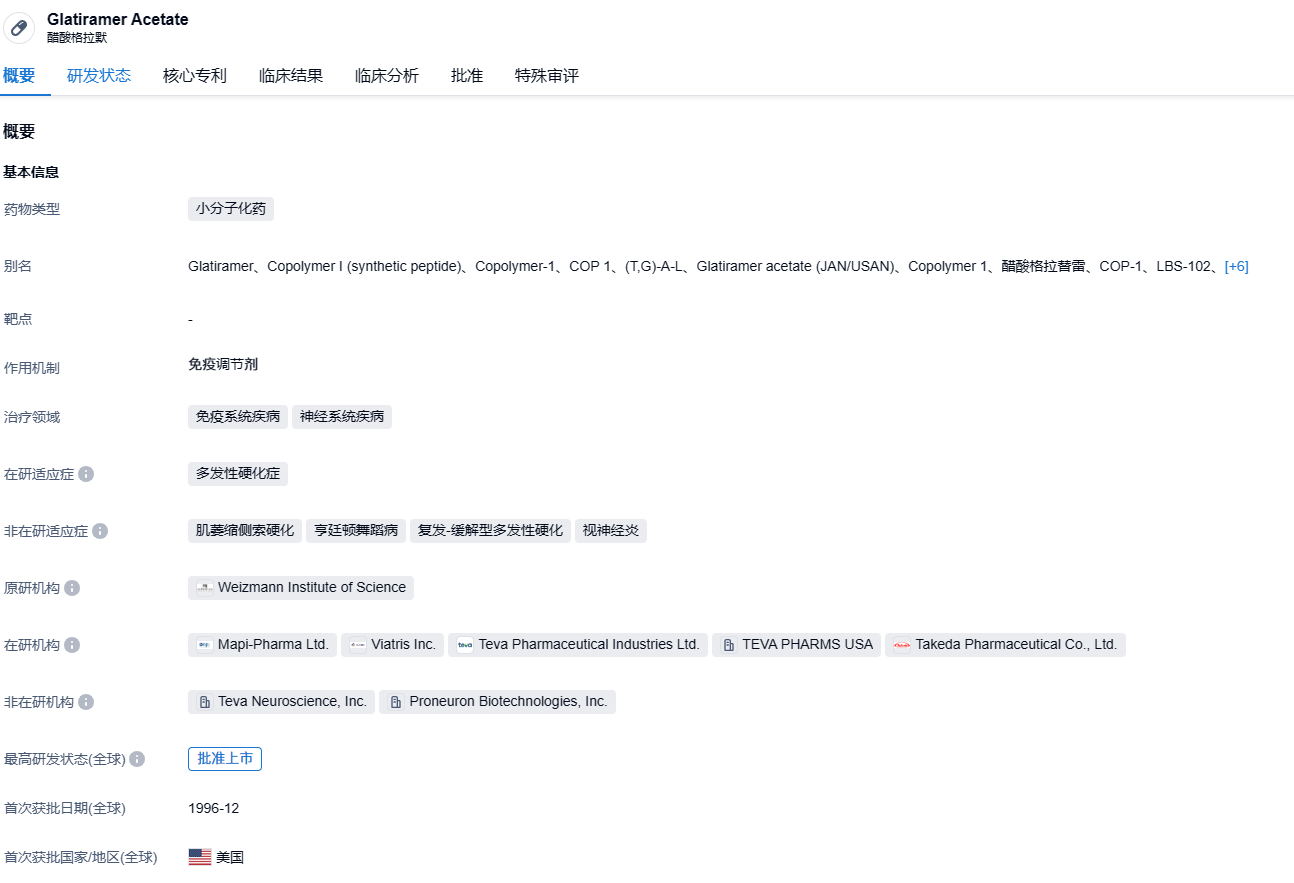
2023年8月7日,晖致(Viatris)和Mapi Pharma共同宣布GA Depot(醋酸格拉替雷,40mg)用于治疗复发型多发性硬化症的新药申请(NDA)获FDA受理,PDUFA日期定为2024年3月8日。GA Depot是一款长效注射剂,可将注射频率从每周3次降低至每月1次。
GA Depot是晖致和Mapi Pharma基于格拉替雷合作开发的长效注射制剂,只需每月肌肉注射一次。格拉替雷的一种MHC-II调节剂,原研企业是梯瓦。梯瓦的醋酸格拉替雷(商品名:Copaxone)有20mg和40mg两种版本,前者需每日注射,而后者也需每周注射3次。据梯瓦财报,Copaxone的年销售额曾连续7年维持在35-42亿美元之间。但是,自2017年超长效制剂奥瑞利珠单抗(Ocrevus)获批上市后,Copaxone的销售额便急转直下,2022年其销售额已跌至6.91亿美元。GA Depot长效制剂的开发,有望逆转格拉替雷销售额的下跌趋势。
GA Depot的NDA主要是基于一项III期研究的积极结果。该研究共纳入1016例患者,旨在评估GA Depot对比安慰剂治疗RMS患者的有效性、安全性和耐受性。结果显示,GA Depot组患者的年复发率相比安慰剂组降低了30.1%(P=0.0066)。
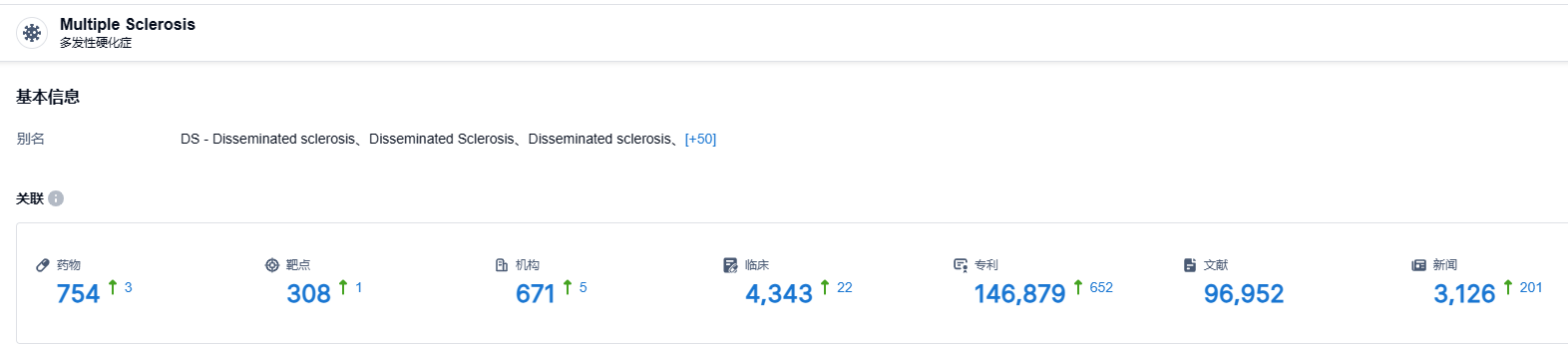
根据智慧芽新药情报库所披露的信息 (点击下方卡片直达 多发性硬化症 适应症注册登录后可免费获得该适应症下的在研药物、靶点、研发机构、临床试验等详细信息),截止2023年8月9日,多发性硬化症 适应症共有在研药物754个,包含的靶点有308种,在研机构671家,涉及相关的临床试验4343件,专利多达146879件……期待GA Depot能够早日获批,为多发性硬化症患者带来新的治疗选择。

生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
继续阅读
返回博客首页 →药物解读
阅读时长 2分钟
塞利尼索——靶向XPO1的小分子化药
2023-08-08
塞利尼索,英文名称Selinexor,商品名XPOVIO,是由Karyopharm Therapeutics, Inc.开发的一款靶向XPO1的小分子化药。该药物最早于2019年07月03日在美国获批,用于治疗多发性骨髓瘤。之后陆续在以色列、欧盟、英国、韩国等多个国家/地区获批。主要用于肿瘤领域,涉及三四十个细分瘤种,其中多个瘤种已停止开发。2023年07月17日,针对原发性骨髓纤维化、原发性血小板增多症后骨髓纤维化、真性红细胞增多症后骨髓纤维化三个适应症,美国FDA将Selinexor纳入快速通道程序。
最新资讯
阅读时长 2分钟
10:0投票结果!赛诺菲/阿斯利康RSV长效抗体nirsevimab获美国CDC一致推荐
2023-08-08
近日,美国疾病预防与控制中心(CDC)免疫实践咨询委员会(ACIP)以10:0的投票结果一致推荐赛诺菲/阿斯利康联合开发的Beyfortus(nirsevimab,尼塞韦单抗)用于预防婴儿由RSV引起的下呼吸道疾病;为即将进入或在第一个RSV流行季期间出生的新生儿和8个月以下婴儿提供保护。
药物解读
阅读时长 2分钟
佐妥昔单抗——靶向CLDN18.2的单克隆抗体
2023-08-08
佐妥昔单抗,英文名称Zolbetuximab是由Astellas Pharma Europe Ltd.开发的一款靶向紧密连接蛋白18.2( claudin 18.2,CLDN18.2)的单克隆抗体(其部分序列信息见图4-6),该药物主要布局消化系统相关的肿瘤。2023年07月06日,针对HER2阴性胃癌、HER2阴性胃食管结合部腺癌,美国FDA将Zolbetuximab纳入优先审评类别。
药物解读
阅读时长 2分钟
Brogidirsen——靶向DMD 外显子44的反义寡核苷酸
2023-08-08
Brogidirsen是由Nippon Shinyaku Co., Ltd.开发的一款靶向DMD 外显子44的反义寡核苷酸,2023年7月,该药物同时获得FDA突破性疗法、孤儿药、罕见儿科疾病三种认证。
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。