预约演示
更新于:2026-06-03
Ditiazem Hydrochloride
盐酸地尔硫卓
更新于:2026-06-03
概要
基本信息
简介地尔硫卓是一种钙离子细胞内流抑制剂(慢通道阻滞剂或钙拮抗剂)。尽管其抗心绞痛作用的确切机制仍在研究中,但认为其作用方式如下:该药已被证明是心外膜和心内膜下冠状动脉的有效扩张剂,可抑制自发或由麦角新碱引起的冠状动脉痉挛。用于治疗慢性稳定型心绞痛和冠状动脉痉挛引起的心绞痛。该药于1973年由武田三菱在日本首次推出。 |
药物类型 小分子化药 |
别名 Diltiazem hydrochloride (JP17/USP)、Diltiazem Hyudrochloride、Diltizem Hydrochloride + [50] |
靶点 |
作用方式 阻滞剂 |
作用机制 Cav2.2阻滞剂(N-型电压门控性钙通道α-1B亚基阻滞剂) |
在研适应症 |
最高研发阶段批准上市 |
最高研发阶段(中国)批准上市 |
特殊审评- |
登录后查看时间轴
结构/序列
分子式C22H27ClN2O4S |
InChIKeyHDRXZJPWHTXQRI-BHDTVMLSSA-N |
CAS号33286-22-5 |
关联
120
项与 盐酸地尔硫卓 相关的临床试验NCT07456852
Vasotoxicity Surveillance Using EndoPAT: The VASA Pilot Study
This phase I/II trial compares the effect of drugs that causes widening of blood vessels as a result of smooth muscle relaxation (vasodilator therapy) with isosorbide mononitrate, diltiazem or placebo to reduce vasotoxicity in patients with gastrointestinal cancer receiving fluoropyrimidine therapy. Some patients develop chest pain (possibly even a heart attack, a drop in heart function, or a rhythm abnormality) during treatment with a class of cancer drugs known as fluoropyrimidines, which include 5-Fluorouracil (5-FU) and capecitabine. These side effects are believed to be due to the development of an abnormal reactivity of the blood vessels referred to as vasospasm. Vasotoxicity is damage or toxicity inflicted upon blood vessels (vascular system), often causing dysfunction, remodeling, or narrowing (vasoconstriction). It is a broad term used to describe the detrimental effects of certain agents, such as chemotherapy drugs. Researchers want to evaluate how often the reactivity of blood vessels becomes abnormal, during the treatment with 5-FU or capecitabine and how clinically relevant and controllable/preventable this phenomenon is in patients with gastrointestinal cancer.
开始日期2026-04-30 |
申办/合作机构 |
NCT07103655
The Therapeutic Value of Mavacamten in Hypertrophic Cardiomyopathy With Mid-to-Apical Left Ventricular Obstruction: A Prospective, Interventional, Real-World Clinical Study.
This study is a prospective interventional cohort study aimed at evaluating the therapeutic efficacy and clinical utility of Mavacamten-a targeted myosin inhibitor specifically developed for obstructive hypertrophic cardiomyopathy (HCM)-in patients with HCM characterized by mid-to-apical left ventricular obstruction.
开始日期2026-01-01 |
申办/合作机构 |
NCT07232589
A Study to Evaluate the Effect of Multiple Oral Doses of Diltiazem on the Single-Dose Pharmacokinetics of Nemtabrutinib in Healthy Participants.
The goal of the study is to learn what happens to levels of nemtabrutinib (MK-1026) in a healthy person's body over time. Researchers will compare what happens to nemtabrutinib in the body when it is given with or without another medicine called diltiazem.
开始日期2025-12-08 |
申办/合作机构 |
100 项与 盐酸地尔硫卓 相关的临床结果
登录后查看更多信息
100 项与 盐酸地尔硫卓 相关的转化医学
登录后查看更多信息
100 项与 盐酸地尔硫卓 相关的专利(医药)
登录后查看更多信息
10,149
项与 盐酸地尔硫卓 相关的文献(医药)2026-12-01·JOURNAL OF MEMBRANE BIOLOGY
Na+ Uptake Triggered in Adrenal Chromaffin Cells by a 5-ns Electric Pulse is Facilitated by Ca2+ Influx Via an L-Type-Like Ca2+ Channel Independent of Changes in Membrane Potential
Article
作者: Gould, Thomas W ; Zaklit, Josette ; Leblanc, Normand ; Craviso, Gale L ; Yang, Lisha
Whole-cell voltage patch clamp studies have shown that in bovine adrenal chromaffin cells held at -70 mV, a single 5-ns, 5 MV/m pulse activates a membrane conductance carried partially by Na+ through TRPC4/5 channels and the sodium leak channel (NALCN). Here we used fluorescence imaging with the Na+ indicator ING-2 to further investigate Na+ influx pathways. A 5-ns, 5 MV pulse elicited a tetrodotoxin-insensitive rise in ING-2 fluorescence that exhibited a similar electric field dependency and response to pulse-pair stimulation as the inward current. Increases in ING-2 fluorescence were partially inhibited by the NALCN inhibitor CP96345, the TRPC4/5 channel inhibitor M084, or the broad spectrum TRP channel inhibitor La3+, and fully blocked by the combination of these agents, suggesting involvement also of a La³⁺-sensitive Na⁺ pathway. Cholesterol depletion with methyl-β-cyclodextrin or PIP₂ synthesis inhibition with wortmannin also reduced the response. Full inhibition was achieved with the selective L-type voltage-gated Ca2+ channel (VGCC) inhibitors nitrendipine, verapamil, or diltiazem but not the broad-spectrum inhibitor Cd2+. Inhibitors of N- and P/Q-type VGCC had no effect. Fluorescence Ca2+ imaging in voltage-clamped GCaMP6f-expressing murine chromaffin cells held at -70 mV revealed a nitrendipine-sensitive, Cd2+-insensitive increase in intracellular Ca2+ that accompanied the inward current. These results provide evidence that nanoelectropulse-induced Na+ influx into chromaffin cells involves several Na+ influx pathways that are facilitated by Ca2+ influx via an L-type-like Ca2+ channel associated with cholesterol-rich membrane domains. Investigating such membrane effects is essential for developing nanosecond electric pulse technologies for stimulating and/or modulating excitable cells.
2026-06-01·AMERICAN JOURNAL OF OBSTETRICS AND GYNECOLOGY
Postpartum management of the hypertensive disorders of pregnancy: a systematic review and meta-analysis
Review
作者: von Dadelszen, Peter ; Tol, Isabel D ; Magee, Laura A ; Khalil, Asma ; Cairns, Alexandra E ; Bone, Jeffrey N ; McManus, Richard J
OBJECTIVE:
To assess the effectiveness and safety of management strategies for postpartum hypertension.
DATA SOURCES:
We searched the Cochrane Pregnancy and Childbirth's Trials Register in collaboration with their Information Specialist, on October 20, 2022. As the Pregnancy and Childbirth Review Group closed (2023), we updated our literature search on September 17, 2024 (topped up on September 25, 2025), using a strategy developed with an information specialist from the Royal College of Physicians, United Kingdom.
STUDY ELIGIBILITY CRITERIA:
We included randomized controlled trials assessing any intervention (pharmacological, surgical, or models of care) used to reduce maternal blood pressure in participants with postpartum hypertension.
STUDY APPRAISAL AND SYNTHESIS METHODS:
Search results were screened independently by 2 authors, with any disagreement resolved by consensus. Data were extracted independently, onto a Cochrane-based bespoke form which included Cochrane's Trustworthiness Screening Tool. Random-effects meta-analysis was performed in RevMan.
RESULTS:
Of the 944 studies identified, 40/44 included had informative data. Certainty of evidence was low or very low. There were no safety concerns. In 7 trials (n=1113 participants) of diuretics (primarily furosemide) vs placebo/no therapy, blood pressure control was better with diuretics when administered alongside antihypertensive. In 3 trials (n=96) of antihypertensive vs placebo, data were insufficient to inform effectiveness. In 9 trials (n=865) of antihypertensive (4 types) vs another (3 types) for nonsevere hypertension, additional antihypertensive need was similar in comparisons with either nifedipine or methyldopa, but greater when amlodipine or either enalapril or lisinopril/thiazide were compared with nifedipine. In 8 trials (n=403) of antihypertensive vs another for severe hypertension, blood pressure was lower with diltiazem (vs nifedipine). In 4 trials (n=668) of uterine curettage vs usual care, observed improvements in laboratory parameters were of unclear clinical significance. In 9 trials (n=1263) of models of postnatal care (usually blood pressure self-monitoring/management, N=6) vs usual care, blood pressure was lower 8 months postpartum following blood pressure self-monitoring/management or lifestyle change.
CONCLUSION:
While diuretics may aid in blood pressure control, they cannot be recommended as monotherapy. Evidence guiding the optimal choice of antihypertensive agents remains limited. Of greatest relevance to practice is the effectiveness of: enalapril or amlodipine (vs nifedipine) in controlling blood pressure; and blood pressure self-measurement/management or lifestyle change (vs usual care) in preventing longer-term cardiovascular outcomes.
2026-05-01·ChemistryOpen
Sustainable Ethanol‐Based Reversed‐Phase Liquid Chromatography for Determination of Diltiazem pKa and Quantification with Integrated Green and White Analytical Metrics
Article
作者: Üstün, Zehra ; Konçe, İlkay ; Çubuk Demiralay, Ebru
This study presents a sustainable chromatographic method for the analysis of diltiazem. Retention behavior and the effect of mobile phase pH were investigated to determine the dissociation constant. Chromatographic experiments were performed at 37°C on a Gemini NX C18 column in binary mixtures of ethanol‐water containing 40%, 45%, and 50% (v/v) ethanol and methanol‐water containing 45%, 50%, and 55% (v/v) methanol. Using these retention data, the value of diltiazem, which has low solubility in water, was calculated. Beyond analytical performance, the sustainability of method was evaluated multimetrically approach using the Environmental, Performance, and Practicality Index, the Carbon Footprint Reduction Index, and the Sustainability of Analytical Methods Index. This complementary framework provides a holistic assessment of operational greenness, carbon intensity, and global sustainability goals in accordance with the latest guidelines. The method for diltiazem determination according to these tools showed linearity with a correlation coefficient of 0.999 in the concentration range of 1.0–15 µg/mL and achieved acceptable precision and accuracy. Validated according to ICH Q2(R2) guidelines, the procedure was successfully applied to tablet formulations and forced degradation studies. This work establishes a comprehensive, ecofriendly methodological approach suitable for pharmaceutical analysis.
127
项与 盐酸地尔硫卓 相关的新闻(医药)2026-06-01
玛伐凯泰胶囊(商品名:迈凡妥®) 是全球首创、中国唯一获批的心肌肌球蛋白抑制剂,用于治疗梗阻性肥厚型心肌病(oHCM)。
基本信息
通用名:玛伐凯泰胶囊(Mavacamten)
商品名:迈凡妥®(CAMZYOS®)
医保情况:已纳入国家医保乙类
生产商:百时美施贵宝(BMS)国家医疗保障局
规格:2.5mg、5mg、10mg、15mg
适应症:用于治疗纽约心脏协会(NYHA)心功能II–III级的梗阻性肥厚型心肌病(oHCM)成人患者,以改善运动能力与症状。
作用机制
靶向根源:直接抑制心肌肌球蛋白,减少心肌过度收缩、减轻左心室流出道梗阻。
机制优势:将肌球蛋白转为 “超松弛状态”,减少横桥形成、降低心肌耗氧、改善舒张功能。
地位:150余年HCM研究史上首个针对病因的靶向药。
用法用量
起始:2.5mg每日一次,整粒吞服,可随餐或空腹。
剂量调整:依据LVEF(≥50%)与LVOT压差,可上调至5/10/15mg;最大15mg/日。
常见不良反应
头晕(27%)、晕厥(6%)(较安慰剂更常见)。
可逆性 LVEF 下降(多无症状,停药后恢复)。
少见:呼吸困难、乏力、心悸、室内传导障碍。
禁用:中/重度CYP2C19抑制剂、重度CYP3A4抑制剂(如氟康唑、伏立康唑);中/强CYP2C19或CYP3A4诱导剂(如利福平、卡马西平)。
慎用:LVEF<55%、严重肝/肾功能不全、妊娠/哺乳期、儿童。
避免与丙吡胺、维拉帕米/地尔硫卓+β受体阻滞剂联用。
临床价值
显著改善:降低LVOT压差、提升运动耐量、缓解呼吸困难/胸痛/晕厥。
填补空白:40余年首个直接针对病因的oHCM靶向药,优于传统对症治疗。
权威认可:获FDA与CDE突破性疗法认定,2023 年获盖伦奖(医药界 “诺贝尔奖”)。
上市情况
玛伐凯泰胶囊(迈凡妥®)由百时美施贵宝研发,2022年4月在美国全球首发,2024年4月获中国NMPA优先审评批准、10月正式上市,同年11月纳入国家医保乙类;目前已在欧盟、加拿大、韩国等多国获批,海外仿制药已于2024 年上市,中国市场仍以原研药为主,获批适应症为NYHA II–III级成人梗阻性肥厚型心肌病。
中国上市
获批时间:2024年4月24日(NMPA,优先审评)
医保:2024年11月纳入国家医保乙类,为首款进入医保的oHCM靶向药
规格:2.5mg×28 粒;5mg×28 粒;10mg/15mg。
获批适应症:NYHA II–III级成人oHCM,改善运动能力与症状。
全球上市
美国:2022 年 4 月(FDA,全球首个);
欧盟:2023 年(含英、德、法等);
其他国家 / 地区:加拿大、澳大利亚、巴西、韩国、新加坡、中国香港 / 澳门、瑞士、阿联酋等;
获批适应症:同中国(NYHA II–III 级成人oHCM)。
中国上市
获批时间:2024年4月24日(NMPA,优先审评)
医保:2024年11月纳入国家医保乙类,为首款进入医保的oHCM靶向药
规格:2.5mg×28 粒;5mg×28 粒;10mg/15mg。
获批适应症:NYHA II–III级成人oHCM,改善运动能力与症状。
参比制剂
注册与受理情况
临床试验情况
专利情况
核心专利(中国):原研公司为MyoKardia(被BMS收购)
化合物/活性成分专利:CN109311854于2018-08-03申请,预估2034-06-19到期。
医药用途专利:CN118593507(肥厚型心肌病),预估2034-06到期。
组合物/制剂专利:同核心到期日,2034-06。
美国:基础化合物专利US9181200预计2034-06-19到期;分案/延续(USRE50050)预计2036-04-28到期。
欧盟/日本/韩国:与中国同族,2034年中到期。
专利保护关键点
保护期长:核心专利至2034年,独占期充足;
专利壁垒高:化合物+用途+制剂三重核心,难以规避;
BMS策略:收购MyoKardia后全球专利强化,延长独占至2036年(美国)。
其他药品分享链接如下,欢迎点击查看:
Ormeloxifene OTF慢性体重管理的新型药物-Tirzepatide新型的非阿片类小分子镇痛药-Suzetrigine奥麦利昔芬口腔薄膜立项调研报告纳米技术双氯芬酸乳胶剂药学研究2025年9月药品批准信息快讯(八)——利斯的明透皮贴剂分享2025年9月药品批准信息快讯(九)——米托坦片分享CDE-《化学仿制药参比制剂目录(第一百批)》(征求意见稿)[附: 药品分享——阿达苏(洛沙平吸入剂)]药品分享-塞来昔布盐酸曲马多片药品分享——伐莫洛龙口服混悬液【药品分享】盐酸菲优拉生片【药品分享】拉坦噻吗滴眼液【药品分享】Baxdrostat 片【药品分享】Omecamtiv Mecarbil缓释片【药品分享】曲地匹坦(Rolapitant)【药品分享】Zasocitinib 胶囊【药品分享】甲磺酸阿帕替尼片【药品分享】巴氯芬口服溶液【药品分享】奥德昔巴特胶囊【药品分享】扎维吉泮鼻喷雾剂【药品分享】左羟丙哌嗪糖浆【药品分享】利丙双卡因凝胶贴膏【药品分享】司来吉兰改良型新药(缓释片)【药品分享】复方甘菊利多卡因凝胶【药品分享】盐酸索安非托片【药品分享】地塞米松口溶膜【药品分享】盐酸来罗西利片【药品分享】马来酸噻吗洛尔凝胶【药品分享】褪黑素颗粒【药品分享】罗氟司特乳膏【药品分享】盐酸芬戈莫德胶囊【药品分享】示踪用盐酸米托蒽醌注射液【药品分享】美洛昔康纳米晶注射液【药品分享】Clascoterone 5%外用溶液【药品分享】马来酸依那普利口服溶液【药品分享】注射用双氯芬酸钠利多卡因【药品分享】马来酸依那普利叶酸片—复方降压药【药品分享】依曲帕米鼻喷雾剂—用于治疗成人阵发性室上性心动过速的可自行给药鼻喷雾剂【药品分享】奥卡西平口服混悬液—一款可用于儿童的钠通道调节类抗癫痫药【药品分享】泊沙康唑口服混悬液——一种常用的抗真菌药物【药品分享】舒沃替尼片【药品分享】依伏卡塞片——第二代口服拟钙剂【药品分享】西诺氨酯片——第三代抗癫痫发作药物【药品分享】匹妥布替尼片——非共价可逆 BTK 抑制剂(用于复发 / 难治套细胞淋巴瘤(MCL))【药品分享】贝美前列素【产品分享】达普司他片
【药品分享】水合氯醛糖浆——镇静催眠药
【产品分享】苏沃雷生(Suvorexant)——全球首个食欲素受体拮抗剂类催眠药
【药品分享】贝沙罗汀
【药品分享】地夫可特干混悬剂——一种糖皮质激素类药物
【药品分享】伊卢多啉片——治疗成人腹泻型肠易激综合征(IBS‑D)的首创口服阿片受体调节剂
【药品分享】卢美哌隆胶囊——一种新型的非典型抗精神病药物
【药品分享】奥氟格列隆片——口服非肽类小分子 GLP-1 受体激动剂
【药品分享】苯磺酸克利加巴林胶囊——一种新型的治疗神经病理性疼痛的药物
【药品分享】苯磺酸美洛加巴林片——治疗周围神经病理性疼痛(PNP)的第三代钙离子通道调节剂
【药品分享】Iberdomide胶囊——一款新一代cereblon(CRBN)E3连接酶调节剂(CELMoD)化合物
【药品分享】酒石酸伐尼克兰鼻喷雾剂——一种用于治疗干眼症的西药
【药品分享】赛沃替尼片——中国首个获批的高选择性 MET 酪氨酸激酶抑制剂
【药品分享】盐酸阿夫唑嗪缓释片——一种用于治疗良性前列腺增生(BPH) 的 α1 - 受体阻滞剂
【药品分享】索格列净片——全球首个获批的SGLT1/SGLT2 双重抑制剂
【药品分享】奥吡卡朋胶囊——新一代的儿茶酚-氧位-甲基转移酶抑制剂(COMT)
【药品分享】奎扎替尼片——一种口服高选择性 FLT3 抑制剂
【药品分享】硫酸拉罗替尼胶囊 / 口服溶液——全球首个高选择性口服 TRK 抑制剂
【药品分享】司帕生坦片——成人IgA肾病领域首个非免疫抑制疗法
【药品分享】黄体酮阴道栓剂/阴道缓释凝胶剂——主要用于辅助生殖技术(ART)中的黄体支持
【药品分享】替戈拉生片——首款国产钾离子竞争性酸阻滞剂类药物(P-CAB)
【药品分享】拉坦前列烯酯滴眼剂——一种新型眼科用药
【药品分享】布比卡因脂质体注射液——一种长效局部麻醉药
【药品分享】甲磺酸加诺沙星片——一种喹诺酮类抗菌药
【药品分享】磷酸芦可替尼乳膏——中国首款且唯一获批的白癜风治疗靶向药
【药品分享】甲磺酸洛美他派胶囊——全球唯一口服MTP抑制剂
【药品分享】依达拉奉口服混悬液——肌萎缩侧索硬化症(ALS,渐冻人症)新药
【药品分享】依达拉奉右莰醇舌下片——全球卒中领域首个获FDA突破性疗法认定的舌下脑保护剂
【药品分享】马来酸氟诺替尼片——JAK2/FLT3/CDK6 三靶点抑制剂
【药品分享】普拉替尼胶囊——国内首个获批的高选择性 RET(转染重排)酪氨酸激酶抑制剂
【药品分享】右美托咪定舌下膜——新型 α₂肾上腺素受体激动剂舌下膜剂
【药品分享】卡匹色替片——全球首个获批上市的AKT抑制剂
【药品分享】库莫西利胶囊——全球首个CDK2/4/6抑制剂
【药品分享】赛贝曲司他片——全球首个HAE急性发作口服疗法
【药品分享】KYGEVVI(Doxecitine/Doxribtimine)——全球首款且唯一获批的TK2d针对性治疗药物
【药品分享】Forzinity(Elamipretide)注射剂——全球首个用于治疗Barth综合征的药物
【药品分享】Brinsupri(Brensocatib, 布伦索卡替布)片——全球首个获批上市的二肽基肽酶1(DPP-1)抑制剂
【药品分享】维立西呱片——全球首个心衰适应症的可溶性鸟苷酸环化酶(sGC)刺激剂
【药品分享】盐酸哌罗匹隆片——非典型抗精神病药
【药品分享】盐酸托泊替康胶囊/注射用盐酸托泊替康——经典的拓扑异构酶Ⅰ抑制剂类抗肿瘤药
【药品分享】阿普昔腾坦片——全球首个获批用于难治性高血压的口服双重内皮素受体拮抗剂(ERA)
【药品分享】注射用盐酸依拉环素——全球首个氟环素类抗生素
【药品分享】奥洛格列净胶囊——国内首款抑制SGLT1与SGLT2的1类创新药
【药品分享】盐酸匹米替尼胶囊——国内首个、全球首个获批的腱鞘巨细胞瘤(TGCT)系统性靶向药,高选择性CSF-1R抑制剂
【药品分享】布地奈德肠溶胶囊——全球首个、中国唯一获批用于原发性IgA肾病对因治疗的靶向药物
【药品分享】艾拉莫德片——中国原研、全球首个上市的小分子抗风湿药(csDMARD)
【药品分享】索托克拉片——新一代BCL2抑制剂
【药品分享】利奈昔巴特片——口服、选择性、可逆性回肠胆汁酸转运体(IBAT/ASBT)抑制剂
【药品分享】多替诺雷片——高选择性URAT1抑制剂
【药品分享】瑞普泊肽片——口服GLP‑1/GIP双靶点激动剂
【药品分享】硫酸索西美雷塞片——口服、强效的KRAS G12C共价抑制剂
【药品分享】罗伐昔替尼片——全球首创JAK/ROCK双靶点口服小分子抑制剂
【药品分享】埃诺格鲁肽注射液——全球首个获批上市的cAMP偏向型长效GLP-1受体激动剂
【药品分享】维培那肽注射液——长效GLP-1受体激动剂
【药品分享】普乐司兰钠注射液——全球首个靶向APOC3 mRNA的siRNA降脂药
【药品分享】玛仕度肽注射液——全球首个GCG/GLP-1双激动剂
【药品分享】瑞米布替尼片——全球首个获批用于CSU的口服靶向药
【药品分享】溴莫尼定噻吗洛尔滴眼液——α₂受体激动剂与非选择性 β 受体阻滞剂组成的复方降眼压药
【药品分享】吡洛西利片——国内首个CDK2/4/6多靶点抑制剂
【药品分享】奥氟格列隆片(Orforglipron) ——中国首个、全球首批上市的口服小分子 GLP-1受体激动剂
【药品分享】Copper Histidine注射液(Zycubo)——全球首个、唯一用于治疗儿童门克斯病(Menkes disease)的铜替代注射剂
【药品分享】依来格列隆片(Elecoglipron)——口服小分子非肽类GLP-1受体激动剂
【药品分享】阿利奈普仑(Aleniglipron)——口服小分子、非肽类、偏向性GLP-1受体激动剂
【药品分享】甲磺酸阿美替尼片——中国首个原研三代EGFR酪氨酸激酶抑制剂(TKI)
【药品分享】甲磺酸达麦利替尼片——口服高选择性c-MET酪氨酸激酶抑制剂
【药品分享】盐酸Acoramidis片——转甲状腺素蛋白(TTR)稳定剂
【药品分享】阿莫西林伏诺拉生胃漂浮片——3D打印胃漂浮片
【药品分享】盐酸伊可白滞素片——全球首创口服IL‑23受体拮抗剂
【药品分享】马来酸吡咯替尼片——中国首个自研的HER1/HER2/HER4不可逆酪氨酸激酶抑制剂(TKI)
【药品分享】本维莫德乳膏——全球首创芳香烃受体(AhR)调节剂(TAMA)类皮肤病外用药
【药品分享】盐酸莫托咪酯注射液——化药1类静脉麻醉新药
【药品分享】注射用罗哌卡因微晶——长效缓释局部麻醉药
【药品分享】盐酸伊立替康脂质体注射液——一款针对吉西他滨治疗失败的转移性胰腺癌的二线标准脂质体化疗药
【药品分享】甲磺酸氟马替尼片——Bcr-Abl酪氨酸激酶选择性抑制剂
【药品分享】注射用阿加糖酶β——国内获批的首个用于治疗法布雷病的药物
【药品分享】甲苯磺酸尼拉帕利胶囊——高选择性PARP1/2抑制剂
【药品分享】帕米帕利胶囊——强效、选择性PARP1/2抑制剂
【药品分享】苯环喹溴铵鼻喷雾剂——选择性M胆碱能受体拮抗剂
【药品分享】注射用拉罗尼酶浓溶液——MPS Ⅰ型的特异性酶替代治疗药物
【药品分享】海博麦布片——国产自主原研的胆固醇吸收抑制剂
【药品分享】盐酸可洛派韦胶囊——直接抗病毒药物(DAA)→ NS5A抑制剂
【药品分享】克拉考特酮乳膏——外用、非甾体、选择性雄激素受体(AR)抑制剂
【药品分享】非卢替尼片——全球首个用于多发性硬化的口服BTK抑制剂
【药品分享】Brenipatide注射液——GLP-1R/GIPR双受体激动剂(继替尔泊肽之后的第二款)
【药品分享】罗赛促红素α注射液——国产首个长效重组促红细胞生成素(EPO)创新药
【药品分享】贝组替凡片——全球首个口服小分子HIF-2α抑制剂
【药品分享】那米司特片——口服选择性PDE4B抑制剂
【药品分享】富马酸立康可泮胶囊——一款针对罕见病PNH的口服补体B因子抑制剂
【药品分享】醋酸索乐匹尼布片——高选择性脾酪氨酸激酶(Syk)抑制剂
【药品分享】甲磺酸艾多替尼片——全球首款专为肺癌脑转移设计的第三代EGFR-TKI
【药品分享】安瑞克芬注射液——全球首个获批镇痛适应症的高选择性外周κ-阿片受体(KOR)激动剂
【药品分享】Difelikefalin注射液——全球首个获批的外周选择性κ-阿片受体(KOR)激动剂
【药品分享】Obefazimod——口服、靶向 CBC、特异性增强miR-124的首创小分子
【药品分享】拉尼兰诺片——口服泛PPAR激动剂
【药品分享】舒洛地特注射液——抗血栓药、血管保护剂
【药品分享】贝普若韦生注射液——反义寡核苷酸(ASO)类乙肝新药
【药品分享】氨酚右敏口服溶液(奥肯能®)——中国内地唯一获批的氨酚右敏口服溶液
【药品分享】佩玛贝特片——新型过氧化物酶体增殖物激活受体α/δ双重激动剂 (PPARα/δ)
【药品分享】盐酸依匹斯汀乳膏——外用第二代非镇静抗组胺抗过敏药膏
【药品分享】注射用双羟萘酸帕瑞肽微球——一款用于治疗肢端肥大症的第二代长效生长抑素类似物(SRL)微球制剂
【药品分享】埃拉菲布拉诺片——治疗原发性胆汁性胆管炎(PBC)的口服靶向新药
【药品分享】泽卢克布仑钠注射液——新一代皮下注射型C5补体抑制剂
【药品分享】依达拉奉右莰醇注射用浓溶液——一款复方神经保护类注射剂
【药品分享】醋酸戈那瑞林注射液——促性腺激素释放激素(GnRH)类药物
【药品分享】甲磺酸贝舒地尔片——全球首个选择性ROCK2激酶抑制剂
【药品分享】伊托法替布软膏——外用JAK抑制剂(JAK1/JAK3)
【药品分享】注射用华卟啉钠——新型肿瘤光动力治疗(PDT)专用光敏剂
【药品分享】优替德隆胶囊——口服埃博霉素类微管抑制剂
【药品分享】艾普美妥司他片——EZH1/2双靶创新药
【药品分享】精氨酸艾曲莫德片——新型选择性鞘氨醇1-磷酸受体(S1P₁)调节剂
【药品分享】磷酸芦可替尼乳膏——全球/国内首款、唯一获批用于非节段型白癜风复色的外用JAK1/JAK2选择性抑制剂
【药品分享】盐酸右哌甲酯缓释胶囊——治疗6岁及以上注意缺陷多动障碍(ADHD)的一线药物
【药品分享】抗菌肽PL-3301口腔凝胶——中国首创的抗菌肽类抗口腔真菌感染药物
【药品分享】Zasocitinib (TAK-279) 胶囊——新一代高选择性口服 TYK2 抑制剂
【药品分享】注射用Abelacimab——一款全人源IgG1单克隆抗体,靶向凝血因子XI(FXI)
【药品分享】Duvakitug注射液——首创性人源化IgG1-λ2单克隆抗体,靶向TL1A(TNFSF15)
【药品分享】醋酸氟轻松/氢醌/维A酸乳膏——治疗中重度黄褐斑疗效明确的外用复方
【药品分享】富马酸伏诺拉生氯化钠注射液——钾离子竞争性酸阻滞剂(P‑CAB)||东阳光药业研发的2.2,2.4类改良新型新药
【药品分享】盐酸阿曲生坦片——诺华研发的高选择性内皮素 A(ETA)受体拮抗剂||中国首个获批用于IgA 肾病的非免疫性口服靶向药
【药品分享】RGT-274-CR胶囊——上海齐鲁锐格医药研发的口服小分子GLP-1受体激动剂
【药品分享】酒石酸西尼必利片——高选择性5-HT₄受体激动剂类胃肠动力药
【药品分享】石杉碱甲控释片——采用双相控释/渗透泵技术的2.2类改良型新药
【药品分享】塞伐艾替尼片——口服、可逆、选择性酪氨酸激酶抑制剂(TKI)
【药品分享】Admilparant片——口服小分子LPA₁受体拮抗剂
【药品分享】瑞拉可兰胶囊——全球首个选择性糖皮质激素受体(GR)拮抗剂
【药品分享】盐酸依特卡肽注射液——全球首个、国内唯一获批的静脉注射型拟钙剂
【药品分享】Avacincaptad pegol玻璃体内注射液——全球首批用于AMD继发地图样萎缩(GA)的靶向药物
【药品分享】盐酸达利雷生片——新一代非管制、非苯二氮䓬类抗失眠药物
【药品分享】甲磺酸瑞索利塞片——高选择性PI3Kα小分子靶向抑制剂 || 全球首个获批用于特定卵巢癌的靶向新药
【药品分享】富马酸西他沙星注射液——新型喹诺酮类抗菌药物
【药品分享】Icotrokinra——全球首个获批的口服 IL-23 受体(IL-23R)选择性拮抗多肽
【药品分享】氘可来昔替尼片(Deucravacitinib)——全球首个口服、选择性 TYK2 变构抑制剂
【药品分享】柯美奇拜单抗注射液——鼻用糖皮质激素治疗后症状控制不佳的成人中重度季节性过敏性鼻炎患者的福音
【药品分享】吉诺昔替尼——口服小分子JAK1/TYK2双重抑制剂
【药品分享】洛替拉纳(Lotilaner)——GABA 门控氯离子通道非竞争性拮抗剂 || 兼具兽医驱虫与人用眼科两大用途
【药品分享】CagriSema——由卡格列肽(cagrilintide)2.4 mg与司美格鲁肽(semaglutide)2.4 mg组成的强效减重复方药
【药品分享】苹果酸卡博替尼——口服、多靶点酪氨酸激酶抑制剂(TKI)
【药品分享】迪高替尼(Delgocitinib)——一款外用泛JAK抑制剂
【药品分享】拉氟莫司(Laflunimus)——口服免疫抑制剂 || 兼具免疫抑制与抗炎双重活性
【药品分享】伏昔尼布片——全球首个IDH1/IDH2双重突变抑制剂靶向药
【药品分享】盐酸奥昔布宁片——M受体抗胆碱药
【药品分享】贝泽昔替尼片——国内首款获批的高选择性JAK2单靶点抑制剂
【药品分享】苯甲酸安达艾替尼胶囊——新型小分子酪氨酸激酶不可逆抑制剂(EGFR-TKI)
【药品分享】伏欣奇拜单抗注射液——全人源抗IL‑1β单克隆抗体 || 用于急性痛风性关节炎的1类创新生物药
【药品分享】利多卡因丁卡因乳膏
【药品分享】伐米奇拜单抗注射液——玻璃体内注射用抗IL-6人源化单抗
【药品分享】依赛弗酶α注射液(Efzimfotase alfa 注射液)——第二代重组组织非特异性碱性磷酸酶(TNSALP)酶替代疗法
【药品分享】格达托利西布(Gedatolisib)——first‑in-class 泛 PI3K/mTORC1/2 双重抑制剂
【药品分享】伯瑞替尼肠溶胶囊——中国原研、高选择性c-MET小分子抑制剂 || 首个获批MET扩增NSCLC单药治疗的靶向药
【药品分享】力胜克拉片——中国首个申报上市的原研Bcl-2抑制剂、全球第二款Bcl-2抑制剂
【药品分享】BGM0504注射液——GLP-1/GIP 双受体激动剂
【药品分享】塞利尼索片——全球首个口服选择性核输出蛋白XPO1抑制剂
【药品分享】Seltorexant薄膜包衣片——选择性食欲素2受体(OX2R)高选择性拮抗剂
【药品分享】盐酸埃克替尼片——国内首个自主研发的一代EGFR-TKI
【药品分享】盐酸伊普可泮胶囊——全球首个口服补体B因子抑制剂
【药品分享】恩考芬尼胶囊——靶向BRAF V600突变的口服激酶抑制剂
【药品分享】Enpatoran——口服、选择性TLR7/8小分子抑制剂
【药品分享】硝酸异康唑阴道片——抗真菌外用药物
【药品分享】Zorevunersen注射液——全球独家ASO上调蛋白表达技术
【药品分享】妥拉美替尼胶囊——全球首个针对NRAS突变黑色素瘤的MEK抑制剂
【药品分享】盐酸替那帕诺片——全球首创NHE3抑制剂类新型降磷药物
【药品分享】注射用莱古比星——新型蒽环类抗肿瘤药
【药品分享】优替德隆胶囊——口服埃博霉素类微管抑制剂
【药品分享】伊那利塞片——中国首个PIK3CA突变乳腺癌精准靶向药
【药品分享】呋喹替尼胶囊——中国首个自主研发VEGFR-TKI || VEGFR靶点靶向抗癌药
【药品分享】琥珀酸瑞波西利片——CDK4/6抑制剂
【药品分享】盐酸替那帕诺片——全球首个且唯一获批的肠道磷吸收抑制剂
【药品分享】芬布替尼片——口服、可逆、可透过血脑屏障的BTK抑制剂
【药品分享】炔丙基半胱氨酸胶囊——全球首个进入临床的硫化氢(H₂S)供体I类创新药
【药品分享】Balcinrenone达格列净胶囊——选择性盐皮质激素受体拮抗剂(MRA)+SGLT-2抑制剂
【药品分享】诺拉西班(Nolasiban)分散片——选择性口服催产素受体拮抗剂 || 早产二线/辅助治疗药物
【药品分享】塞多明基注射液——国内首款裸质粒基因治疗药物
【药品分享】鲁兹诺雷钠片——国产首个高选择性URAT1抑制剂
免责声明:本文仅作医药信息传播分享,并不构成投资或决策建议。
2026-06-01
Camzyos
has the potential to be the first pharmacological therapy for the treatment of oHCM in adolescents, addressing a high unmet need for this population
Application based on positive results of Phase 3 SCOUT-HCM trial, which met its primary endpoint with safety pro to established pro adults
PRINCETON, N.J.--(BUSINESS WIRE)--
$BMY
#CAMZYOS
--
Bristol Myers Squibb
(NYSE: BMY) today announced the U.S. Food and Drug Administration (FDA) accepted a supplemental New Drug Application (sNDA) for
Camzyos
(mavacamten) as a potential treatment for adolescents (ages 12 years to 5% of patients and more commonly in the CAMZYOS group than in the placebo group were dizziness (27% vs 18%) and syncope (6% vs 2%). There were no new adverse reactions identified in VALOR-HCM.
Effects on Systolic Function
In the EXPLORER-HCM trial, mean (SD) resting LVEF was 74% (6) at baseline in both treatment groups. Mean (SD) absolute change from baseline in LVEF was -4% (8) in the CAMZYOS group and 0% (7) in the placebo group over the 30-week treatment period. At Week 38, following an 8-week interruption of trial drug, mean LVEF was similar to baseline for both treatment groups. In the EXPLORER-HCM trial, 7 (6%) patients in the CAMZYOS group and 2 (2%) patients in the placebo group experienced reversible reductions in LVEF <50% (median 48%: range 35-49%) while on treatment. In all 7 patients treated with CAMZYOS, LVEF recovered following interruption of CAMZYOS.
DRUG INTERACTIONS
Potential for Other Drugs to Affect Plasma Concentrations of CAMZYOS
CAMZYOS is primarily metabolized by CYP2C19 and to a lesser extent by CYP3A4 and CYP2C9. Inducers and inhibitors of CYP2C19 and moderate to strong inhibitors or inducers of CYP3A4 may affect the exposures of CAMZYOS.
Impact of Other Drugs on CAMZYOS:
Strong CYP2C19 Inhibitors
: Concomitant use increases CAMZYOS exposure, which may increase the risk of heart failure due to systolic dysfunction. Concomitant use is contraindicated.
Moderate to Strong CYP2C19 Inducers or Moderate to Strong CYP3A4 Inducers
: Concomitant use decreases CAMZYOS exposure, which may reduce CAMZYOS’ efficacy. The risk of heart failure due to systolic dysfunction may increase with discontinuation of these inducers as the levels of induced enzyme normalizes. Concomitant use is contraindicated.
Weak CYP2C19 Inhibitors or Moderate CYP3A4 Inhibitors
: Concomitant use with a weak CYP2C19 inhibitor or a moderate CYP3A4 inhibitor increases CAMZYOS exposure, which may increase the risk of adverse drug reactions. Initiate CAMZYOS at the recommended starting dose of 5 mg orally once daily in patients who are on stable therapy with a weak CYP2C19 inhibitor or a moderate CYP3A4 inhibitor. Reduce dose of CAMZYOS by one level (ie, 15 to 10 mg, 10 to 5 mg, or 5 to 2.5 mg) in patients who are on CAMZYOS treatment and intend to initiate a weak CYP2C19 inhibitor or a moderate CYP3A4 inhibitor. Schedule clinical and echocardiographic assessment 4 weeks after inhibitor initiation, and do not up-titrate CAMZYOS until 12 weeks after inhibitor initiation. Avoid initiation of concomitant weak CYP2C19 and moderate CYP3A4 inhibitors in patients who are on stable treatment with 2.5 mg of CAMZYOS because a lower dose is not available. For short-term use (eg, 1 week), interrupt CAMZYOS for the duration of treatment with a weak inhibitor of CYP2C19 or a moderate inhibitor of CYP3A4. CAMZYOS may be reinitiated at the previous dose immediately on discontinuation of concomitant therapy.
Moderate CYP2C19 Inhibitors or Strong CYP3A4 Inhibitors
: Concomitant use with a moderate CYP2C19 inhibitor or strong CYP3A4 inhibitor increases CAMZYOS exposure, which may increase the risk of adverse drug reactions. Discontinuing use of a moderate CYP2C19 inhibitor or strong CYP3A4 inhibitor after long-term concomitant use may decrease CAMZYOS exposure, which may reduce CAMZYOS’ efficacy. Initiate CAMZYOS at a starting dosage of 2.5 mg orally once daily in patients who are on a stable therapy with a moderate CYP2C19 inhibitor or a strong CYP3A4 inhibitor. Reduce dose of CAMZYOS by one level (ie, 15 to 10 mg, 10 to 5 mg, or 5 to 2.5 mg) in patients who are on CAMZYOS and intend to initiate a moderate CYP2C19 inhibitor or a strong CYP3A4 inhibitor. Avoid initiation of concomitant moderate CYP2C19 and strong CYP3A4 inhibitors in patients who are on a stable treatment with 2.5 mg of CAMZYOS because a lower dose is not available. An increase in dose of CAMZYOS may be needed if the moderate inhibitor of CYP2C19 or strong inhibitor of CYP3A4 is discontinued after long-term concomitant use. Monitor for new or worsening symptoms. For short-term use (ie, when CAMZYOS dose modification is not feasible), interrupt CAMZYOS for the duration of treatment with a moderate inhibitor of CYP2C19 or a strong inhibitor of CYP3A4. CAMZYOS may be reinitiated at the previous dose immediately on discontinuation of concomitant therapy.
Potential for CAMZYOS to Affect Plasma Concentrations of Other Drugs
CAMZYOS is an inducer of CYP3A4, CYP2C9, and CYP2C19. Concomitant use with CYP3A4, CYP2C9, or CYP2C19 substrates may reduce plasma concentration of these drugs. Closely monitor when CAMZYOS is used with concomitant CYP3A4, CYP2C9, or CYP2C19 substrates unless otherwise recommended in the Prescribing Information.
Certain Combined Hormonal Contraceptives (CHCs): Progestin and ethinyl estradiol are CYP3A4 substrates. Concomitant use of CAMZYOS may decrease exposures of certain progestins, which may lead to contraceptive failure. CHCs containing a combination of ethinyl estradiol and norethindrone may be used with CAMZYOS, but if other CHCs are used, advise patients to add nonhormonal contraception (such as condoms) or use an alternative contraceptive method that is not affected by CYP450 enzyme induction (eg, intrauterine system) during concomitant use and for 4 months after the last dose of CAMZYOS.
Drugs That Reduce Cardiac Contractility
Expect additive negative inotropic effects of CAMZYOS and other drugs that reduce cardiac contractility. Avoid concomitant use of CAMZYOS in patients on disopyramide, ranolazine, verapamil with a beta blocker, or diltiazem with a beta blocker as these medications and combinations increase the risk of left ventricular systolic dysfunction and heart failure symptoms and clinical experience is limited.
If concomitant therapy with a negative inotrope is initiated, or if the dose of a negative inotrope is increased, monitor LVEF closely until stable doses and clinical response have been achieved.
SPECIFIC POPULATIONS
Pregnancy
Based on animal data, CAMZYOS may cause fetal harm when administered to a pregnant female. Advise pregnant females about the potential risk to the fetus with maternal exposure to CAMZYOS during pregnancy. There is a pregnancy safety study for CAMZYOS. If CAMZYOS is administered during pregnancy, or if a patient becomes pregnant while receiving CAMZYOS or within 4 months after the last dose of CAMZYOS, healthcare providers should report CAMZYOS exposure by contacting Bristol Myers Squibb at 1-800-721-5072 or
.
Lactation
The presence of CAMZYOS in human or animal milk, the drug’s effects on the breastfed infant, or the effects on milk production are unknown. The developmental and health benefits of breastfeeding should be considered along with the mother’s clinical need for CAMZYOS and any potential adverse effects on the breastfed child from CAMZYOS or from the underlying maternal condition.
Females and Males of Reproductive Potential
Confirm absence of pregnancy in females of reproductive potential prior to initiation of CAMZYOS. Advise females of reproductive potential to use effective contraception during treatment with CAMZYOS and for 4 months after the last dose. CHCs containing a combination of ethinyl estradiol and norethindrone may be used with CAMZYOS. However, CAMZYOS may reduce the effectiveness of certain other CHCs. If these CHCs are used, advise patients to add nonhormonal contraception (such as condoms) or use an alternative contraceptive method during concomitant use and for 4 months after the last dose of CAMZYOS.
Please see
U.S. Full Prescribing Information
, including
Boxed WARNING
and
Medication Guide
.
About Bristol Myers Squibb: Transforming Patients’ Lives Through Science
At Bristol Myers Squibb, our mission is to discover, develop and deliver innovative medicines that help patients prevail over serious diseases. We are pursuing bold science to define what’s possible for the future of medicine and the patients we serve. For more information, visit us at
BMS.com
and follow us on
LinkedIn
,
X
,
YouTube
,
Facebook
and
Instagram
.
Cautionary Statement Regarding Forward-Looking Statements
This press release contains “forward-looking statements” within the meaning of the Private Securities Litigation Reform Act of 1995 regarding, among other things, the research, development and commercialization of pharmaceutical products. All statements that are not statements of historical facts are, or may be deemed to be, forward-looking statements. Such forward-looking statements are based on current expectations and projections about our future financial results, goals, plans and objectives and involve inherent risks, assumptions and uncertainties, including internal or external factors that could delay, divert or change any of them in the next several years, that are difficult to predict, may be beyond our control and could cause our future financial results, goals, plans and objectives to differ materially from those expressed in, or implied by, the statements. These risks, assumptions, uncertainties and other factors include, among others, that
Camzyos
(mavacamten) may not receive regulatory approval for the additional indication described in this release in the currently anticipated timeline or at all, any marketing approvals, if granted, may have significant limitations on their use, and, if approved, whether
Camzyos
for such additional indication will be commercially successful. No forward-looking statement can be guaranteed. It should be noted that acceptance of the application does not change the standards for FDA approval. Forward-looking statements in this press release should be evaluated together with the many risks and uncertainties that affect Bristol Myers Squibb’s business and market, particularly those identified in the cautionary statement and risk factors discussion in Bristol Myers Squibb’s Annual Report on Form 10-K for the year ended December 31, 2025, as updated by our subsequent Quarterly Reports on Form 10-Q, Current Reports on Form 8-K and other filings with the Securities and Exchange Commission. The forward-looking statements included in this document are made only as of the date of this document and except as otherwise required by applicable law, Bristol Myers Squibb undertakes no obligation to publicly update or revise any forward-looking statement, whether as a result of new information, future events, changed circumstances or otherwise.
corporatefinancial-news
Contacts
Bristol Myers Squibb
Media Inquiries:
media@bms.com
Investors:
investor.relations@bms.com
临床3期临床结果优先审批申请上市
2026-05-30
·有驾
摘要
近年来,媒体对维生素D的生理作用及补充维生素D可带来的健康益处报道大幅增多,但临床中极少关注药物可能对人体维生素D营养状况产生的影响。
本文通过文献综述系统评估各类药物对维生素D水平的影响程度。检索各大电子数据库,筛选相关研究并分析研究设计与结论。
结果发现,抗癫痫药、泻药、二甲双胍、袢利尿剂、血管紧张素转换酶抑制剂、噻嗪类利尿剂、他汀类药物、钙通道阻滞剂、维生素K拮抗剂、抗血小板药、地高辛、保钾利尿剂、苯二氮䓬类、抗抑郁药、质子泵抑制剂、组胺H2受体拮抗剂、胆汁酸螯合剂、糖皮质激素、抗菌药物、磺胺类及脲类衍生物、脂肪酶抑制剂、羟氯喹、高效抗逆转录病毒药物、部分化疗药物等,均被研究证实会不同程度影响维生素D状态。
现有相关研究质量参差不齐,尤其对于经细胞色素P450 3A4(CYP3A4)酶代谢的药物,亟需设计更严谨的大样本新研究明确其与维生素D的相互作用。
临床医护人员应警惕药物诱发的维生素D缺乏问题,尤其针对多重用药的老年人群,必要时及时给予维生素D补充干预。
关键词
麦角钙化醇、胆钙化醇、维生素D、药物相互作用
引言
传统观点认为,脂溶性维生素D的核心功能是调控钙吸收与钙稳态平衡,在肌肉骨骼健康中发挥关键作用。近年研究发现,血清25-羟维生素D水平不足,还与心血管疾病、冠心病、糖尿病、部分肿瘤、多发性硬化、帕金森病、老年认知衰退、关节炎等非骨骼疾病相关。但目前仍无法明确,维生素D缺乏是此类疾病的诱因还是继发结果。
维生素D可促进胃肠道钙吸收、参与新生骨基质矿化,同时对肌肉功能至关重要。长期维生素D缺乏会损害骨骼健康,引发成人骨软化症、儿童佝偻病,这类患者血清25-羟维生素D水平通常低于20nmol/L。维生素D不足(轻中度缺乏)可诱发继发性甲状旁腺功能亢进、加速骨量流失;在老年人中还会导致肌力减退、跌倒风险升高,进而增加脆性骨折发生率。
欧洲食品安全局已认可维生素D的多项健康功效:维持免疫系统正常功能、保护骨骼与牙齿健康、促进儿童骨骼正常生长发育、参与钙磷吸收利用、维持血钙稳态及正常肌肉功能。
尽管学界对维生素D推荐摄入量、营养判定标准及健康效应仍存在争议,但预防维生素D缺乏已成为重要公共卫生问题。养老机构老人、特定种族人群、孕妇、婴幼儿等群体维生素D低水平现象尤为普遍。
维生素D补充剂主要分为麦角钙化醇(维生素D₂)和胆钙化醇(维生素D₃)。人体皮肤经紫外线照射可内源性合成维生素D₃,动物肝脏、鱼类、蛋类中也天然含有维生素D₃。维生素D₂与D₃进入人体后,在肝脏25-羟化酶(包括CYP3A4、CYP2R1、CYP27A1)作用下,转化为主要循环形式25-羟维生素D₃;随后经肾脏及局部组织1α-羟化酶(CYP27B1)催化,生成活性形式1,25-二羟维生素D。而CYP24A1酶则负责维生素D代谢产物的分解灭活。
活性1,25-二羟维生素D可调控细胞内信号通路,介导快速非基因组效应及慢速基因组效应:既启动细胞膜信号传导,也可通过结合维生素D反应元件调控基因转录。研究证实,1,25-二羟维生素D能调控Ⅰ相、Ⅱ相药物代谢酶及多药耐药蛋白、P-糖蛋白的转录表达,影响多种药物的生物利用度与代谢过程。
活性维生素D在体内调控严格,血液循环中仅为皮摩尔级别,因此临床常以25-羟维生素D₃作为评估维生素D营养状态的标志物。目前学界对维生素D充足标准尚无统一共识:部分机构以血清25-羟维生素D≥20ng/mL为充足阈值,主要用于预防骨质疏松;另有观点认为健康人群最优水平应达到30ng/mL(75nmol/L)以上
个体差异同样影响维生素D水平:肥胖人群因脂肪组织储存、隔离维生素D,血清含量普遍低于正常体重人群;北纬40°以上地区冬季紫外线强度不足,皮肤无法合成维生素D,导致人群维生素D水平呈季节性波动;男性、深色肤色、高龄、补充剂使用等也均是重要影响因素。
体外研究显示,约半数临床药物经CYP3A4酶代谢,而该酶同时参与维生素D向25-羟维生素D的转化,大量药物可抑制或诱导CYP3A4活性。CYP3A4在肠道上皮细胞与肝细胞中均有表达,因此口服维生素D与药物的相互作用,比静脉给药更为显著。
此外,CYP3A4基因存在维生素D响应元件,1,25-二羟维生素D可上调CYP3A4表达,进而改变依赖该酶代谢的药物活性。
药物与维生素D联用还可能升高高钙血症风险;而部分药物会促进膳食脂肪排泄或抑制脂肪吸收,间接减少脂溶性维生素D的摄入。
即便在经济发达国家,维生素D不足仍十分普遍。英国数据分析显示,人群25-羟维生素D平均水平在1—3月最低、7—9月最高;11~18岁女性、19~64岁男性、65岁以上女性中,全年25-羟维生素D低于25nmol/L(世卫组织缺乏临界值)的比例达24%;19~64岁女性、65岁以上男性该比例分别为22%、17%;冬季11~64岁男性缺乏率高达40%,65岁以上男性达29%。
本文旨在系统梳理现有文献,总结各类药物对维生素D水平的潜在影响,分析其对本就存在维生素D缺乏人群的叠加危害,尤其关注老年多重用药群体的健康风险。
研究结果
一、抗癫痫药物
自20世纪60年代起,临床便发现抗癫痫药与骨软化症等骨代谢异常存在关联。后续前瞻性及队列研究证实,长期服用抗癫痫药会降低骨密度、升高骨折风险。
酶诱导型抗癫痫药
卡马西平、苯巴比妥、苯妥英可加速肝脏维生素D分解,生成无活性代谢产物,抑制钙吸收,长期使用易引发低钙血症与骨软化症。
尤其连续用药6个月以上、联合多种酶诱导抗癫痫药,或合并维生素D缺乏危险因素的患者,需常规补充钙与维生素D。纠正缺乏所需剂量个体差异较大,每日10μg~100μg不等,高危人群应定期监测血清维生素D与血钙水平。但现有多数研究未区分药物种类、用药时长与剂量,存在数据混杂问题。
正常肾脏中CYP24A1主导维生素D代谢,肝脏与小肠则以CYP3A4为主。10%~30%服用苯巴比妥、苯妥英的患者,可出现影像学或生化层面的维生素D降低。抗癫痫治疗数月内即可诱发骨软化,联合用药会产生肝脏酶代谢叠加效应,日晒、膳食摄入等因素也会影响最终结果。补充维生素D可逆转相关生化与影像学异常。
无论何种酶诱导型抗癫痫药,即便在治疗剂量以下,也会使原本维生素D正常人群转为不足或缺乏,建议启动此类药物治疗前,提前补充钙与维生素D。
系统综述显示,成人长期服用抗癫痫药普遍存在维生素D缺乏,缺乏程度随药物种类不同存在差异,但无法排除患者基础维生素D偏低的混杂因素。随机对照试验表明,高剂量维生素D补充可更好维持髋部及脊柱骨密度。
新型抗癫痫药
新型抗癫痫药对骨骼影响的相关研究有限。一项超15000人的大型回顾性队列研究显示,加巴喷丁会升高骨折风险,拉莫三嗪、左乙拉西坦、奥卡西平则无明显影响;但另一项560人的小样本回顾性研究未发现新型抗癫痫药与骨密度降低相关,现有研究结论存在冲突。
基础研究提示,左乙拉西坦虽不降低骨密度,但会损害骨质量,传统骨密度检测无法完全反映骨骼健康状态。癫痫患者服用酶诱导型或非CYP450诱导型抗癫痫药,骨质疏松患病率更高;但托吡酯、加巴喷丁、左乙拉西坦等新型药物未被证实存在骨骼损害。
二、泻药
刺激性泻药大剂量、长期使用会加快肠道食物转运,减少脂溶性维生素D、钙、镁等矿物质吸收,诱发低钙血症与骨软化症。
三、降糖药物
二甲双胍
维生素D缺乏与胰岛素分泌减少、胰岛素抵抗升高相关。队列研究显示,口服降糖药使用者血清25-羟维生素D平均水平较非使用者低7.3nmol/L。两项合计超11500例的研究均发现,口服降糖药使用与维生素D水平呈负相关;另有横断面研究证实该效应主要来自二甲双胍。
有学者认为,确诊维生素D缺乏后进行补充,可能掩盖二甲双胍对维生素D的降低作用。
噻唑烷二酮类
2型糖尿病患者骨折风险高于普通人群,且噻唑烷二酮类降糖药会进一步加剧骨量流失与骨折风险。该类药物可调控间充质干细胞分化,促进脂肪生成、抑制成骨细胞形成。系统综述及Meta分析显示,噻唑烷二酮类对女性骨量流失影响更显著;长期用药会大幅提升女性骨质疏松及骨折风险,对男性影响较小。此外,2型糖尿病服药患者普遍存在维生素D、钙、镁等骨骼必需营养素摄入不足的问题。
四、利尿剂
噻嗪类利尿剂
噻嗪类利尿剂与维生素D水平的关联研究结论不一。维生素D可促进肠道钙吸收,噻嗪类可减少尿钙排泄,二者联用理论上可能诱发或加重高钙血症,尤其合并甲状旁腺功能亢进、肾功能受损的老年高危人群。另有四项研究均证实,噻嗪类药物不会显著改变25-羟维生素D水平。
袢利尿剂
袢利尿剂对25-羟维生素D、1,25-二羟维生素D的影响结论混杂。随机对照试验显示,袢利尿剂可升高血清甲状旁腺激素与1,25-二羟维生素D水平,同时增加尿钙排泄,诱发继发性甲状旁腺功能亢进,进而促进25-羟维生素D羟化活化,升高活性维生素D浓度。
保钾利尿剂
有研究发现老年人群中保钾利尿剂与维生素D水平呈负相关,但同人群的另一项横断面研究未能重复该结论。
五、心血管系统药物
钙通道阻滞剂
老年人群队列研究显示,服用维拉帕米、地尔硫卓等钙通道阻滞剂者,血清25-羟维生素D水平较未使用者降低7.7nmol/L。维拉帕米、地尔硫卓可抑制CYP3A4酶,减少皮肤经紫外线合成维生素D前体,降低血清维生素D水平;而硝苯地平可激活孕烷X受体,促进维生素D分解代谢。
血管紧张素转换酶抑制剂
老年患者服用此类药物后,25-羟维生素D水平较未使用者降低7.6nmol/L,德国、荷兰横断面研究也得出相似结果。但荷兰队列二次分析及两项准实验研究未发现相关性;喹那普利可升高维生素D水平,依那普利则无明显影响。该关联也可能是混杂因素:高血压、糖尿病等基础疾病本身与低维生素D相关,并非药物直接作用。
他汀类药物
他汀类通过抑制胆固醇合成限速酶降低血脂,而胆固醇是维生素D合成前体,理论上可能减少维生素D生成。辛伐他汀、洛伐他汀、阿托伐他汀主要经CYP3A4代谢,可与维生素D代谢竞争酶通路;瑞舒伐他汀、氟伐他汀主要经CYP2C9代谢;普伐他汀、匹伐他汀与肝脏酶相互作用极小,主要在胃部降解。
多项研究显示,阿托伐他汀可升高循环25-羟维生素D水平;补充维生素D会降低阿托伐他汀及其活性代谢物血药浓度,但仍可协同降低血脂。
普伐他汀对25-羟维生素D无显著影响;瑞舒伐他汀可明显提升维生素D水平,JUPITER研究中其心血管获益部分与改善维生素D缺乏相关。高脂血症前瞻性队列研究证实,瑞舒伐他汀治疗8周后,25-羟维生素D与1,25-二羟维生素D均显著升高;对比研究发现,瑞舒伐他汀提升维生素D效果优于氟伐他汀。目前学界对此争议较大,亟需大型多中心高质量临床试验验证。
他汀类与维生素D存在复杂关联,二者均影响骨骼肌代谢,维生素D缺乏是他汀类肌痛、肌病的重要诱因。低维生素D人群他汀耐受性更差;补充维生素D后,87%肌痛患者可重新耐受他汀治疗。
系统综述及Meta分析证实,低维生素D与他汀使用者肌痛显著相关,纠正维生素D缺乏可逆转他汀相关肌病。临床暂不建议对所有他汀使用者常规检测维生素D,但明确维生素D缺乏且存在他汀不耐受的患者,补充至正常水平后可重新尝试用药。
胆汁酸螯合剂
此类药物在肠道结合胆汁酸,减少胆固醇重吸收,同时可结合维生素D及其代谢产物,增加脂溶性维生素排泄。一项儿童家族性高胆固醇血症研究显示,每日服用8g考来烯胺持续1年,维生素D水平显著下降;长期每日超32g服用,可诱发骨软化症。但另有三项同类研究得出相反结论。
维生素K拮抗剂
荷兰两项横断面研究及德国7553人大样本研究均显示,服用维生素K拮抗剂者25-羟维生素D降幅更显著,但另有四项研究未发现该效应。
抗血小板聚集药
两项横断面研究未发现抗血小板药与维生素D存在负相关,另有三项研究则得出相反结论,混杂因素可能是基础疾病干扰。
肝素
普通肝素每日剂量≥15000IU、连续使用3个月以上,会降低骨密度、升高骨质疏松骨折风险,同时干扰维生素D代谢。低分子肝素对骨密度影响较轻,但仍可能损害维生素D代谢,长期使用者建议补充钙与维生素D。
地高辛
荷兰老年人群横断面研究发现,地高辛使用与维生素D水平呈临界负相关,但其他研究未证实该统计学关联。
六、中枢神经系统药物
苯二氮䓬类
三项横断面研究未发现其对维生素D有显著影响,但亚组分析显示该类药物与维生素D水平存在显著负相关。
抗抑郁药
两项横断面研究证实,选择性5-羟色胺再摄取抑制剂与25-羟维生素D降低相关。氟伏沙明、氟西汀可抑制维生素D代谢相关CYP酶,可能减少其合成。同时抑郁症本身也与低维生素D相关,存在疾病混杂因素。
七、胃肠道药物
质子泵抑制剂
该类药物抑制胃酸分泌,可能导致钙吸收不良,长期抑酸会增加骨质疏松风险。建议长期大剂量服用质子泵抑制剂的老年人,常规补充钙与维生素D。
组胺H2受体拮抗剂
基础研究证实西咪替丁可抑制25-羟化酶活性。小样本临床研究显示,服用西咪替丁治疗胃溃疡期间,25-羟维生素D无明显下降,停药后则显著升高;雷尼替丁未发现此类相互作用。
八、抗炎与激素类药物
糖皮质激素
糖皮质激素治疗最常见并发症为骨质疏松,其对维生素D代谢的影响备受关注。多数研究显示,治疗前后25-羟维生素D水平无显著差异;小剂量泼尼松可降低健康人群及类风湿关节炎患者的维生素D水平,但未达到缺乏标准;也有研究认为季节因素干扰了结果。部分研究未区分具体激素种类,导致结论模糊。成人每日等效泼尼松2.5~10mg、连续用药3个月以上,维生素D水平显著低于健康人群;激素累积剂量越高,维生素D降低越明显。现有研究普遍未校正体成分、膳食补充、日晒等混杂因素。
吸入性糖皮质激素
部分研究未发现其影响维生素D水平,也有队列研究显示男性使用者25-羟维生素D显著降低。慢性阻塞性肺疾病患者本身维生素D缺乏率高、病情严重程度与维生素D相关,易产生混杂偏倚。长期使用对骨代谢影响尚不明确,相关Meta分析结论不一:部分认为可影响骨代谢标志物、升高骨转换率,低剂量无明显作用;部分未发现长期使用者骨密度与健康人群存在差异。总体而言,吸入性糖皮质激素可能对慢性阻塞性肺疾病患者的骨代谢与骨密度产生不良影响。美国指南建议,每日泼尼松≥7.5mg、连续用药6个月以上者,每日补充800IU维生素D、维持每日1500mg钙摄入。
支气管扩张剂
大剂量β2受体激动剂会升高股骨、髋部骨折风险,校正基础疾病及口服激素因素后风险有所降低,两年随机对照试验也佐证了其对骨密度的潜在影响。
九、抗感染与抗风湿药物
抗微生物药物
利福平、异烟肼等抗结核药物与维生素D水平关联结论不一,六项小样本研究中四项显示维生素D下降、一项无变化、一项升高。长期用药超1年且维生素D摄入不足时,易诱发骨软化症。
磺胺类及脲类衍生物
荷兰892名社区门诊患者横断面研究显示,此类药物可显著降低维生素D水平。
脂肪酶抑制剂
奥利司他可阻断肠道脂肪吸收,进而抑制脂溶性维生素D的膳食及补充剂摄入。三项研究证实奥利司他使用者25-羟维生素D下降,但对照组也出现相似降幅,可能与整体脂肪摄入减少有关。
羟氯喹
系统性红斑狼疮患者普遍存在维生素D缺乏,而服用羟氯喹者25-羟维生素D水平高于未使用者,推测与该药物抑制维生素D活化转化有关。
高效抗逆转录病毒药物
此类药物多经CYP3A4代谢,可诱导或抑制酶活性,干扰维生素D合成与分解。四项临床研究中两项显示使用者维生素D水平偏低,仅一项具有统计学意义;依非韦伦方案治疗6个月内维生素D明显下降,长期用药后趋于稳定。
十、化疗药物
多数化疗药物经CYP3A4代谢,可与维生素D发生相互作用,包括他莫昔芬、多西他赛、紫杉醇、异环磷酰胺、依托泊苷、长春花碱、环磷酰胺、伊马替尼、伊立替康等。早期乳腺癌患者初诊时,30%~50%存在维生素D缺乏,且低维生素D与不良预后相关。部分化疗研究因患者同步补充维生素D,未观察到25-羟维生素D明显变化;新辅助化疗结束后,几乎所有患者出现维生素D不足,并伴随钙/RANKL/OPG调控通路紊乱。结直肠、乳腺、子宫、卵巢肿瘤患者接受常规化疗后,维生素D水平无显著波动,但基线缺乏率较高。乳腺癌患者化疗期间及康复后,建议常规补充维生素D。
十一、防晒霜
长期频繁使用防晒霜会抑制皮肤维生素D合成,降低血清水平,过度使用存在诱发维生素D缺乏的风险。
讨论
早期相关研究多为病例报道或聚焦骨质疏松关联药物,随着CYP3A4酶代谢机制、维生素D对药物代谢基因调控作用被阐明,相关研究更趋系统规范。仍需进一步开展研究,明确各类药物对维生素D代谢相关CYP酶活性的影响,如奥美拉唑、酮康唑等既抑制CYP3A4也抑制CYP24,亟需临床研究验证其对人体维生素D的实际作用。
现有研究存在诸多局限性:多为小样本观察性研究、回顾性数据分析,缺乏对照;多数未评估膳食维生素D摄入、日晒时长,未校正体质量、体成分等混杂因素,难以区分是药物直接作用还是营养摄入不足导致维生素D偏低。
吸烟也是重要混杂因素:吸烟者血清25-羟维生素D普遍更低,重度缺乏风险显著升高,但也有研究未发现相关性,差异源于吸烟量化方式、检测方法不同。维生素D检测技术差异也导致新旧研究数据难以横向对比,未来需采用标准化检测方法、开展大样本高质量研究。
新冠疫情相关研究显示,维生素D水平与新冠易感性、病情及预后相关,高水平维生素D人群感染率及重症死亡率更低,但确切关联强度、补充干预疗效仍待验证。新冠重症患者多合并肥胖、糖尿病、高血压等基础疾病,需长期服用多种可影响维生素D的药物,叠加效应会进一步加重维生素D缺乏,且现有防疫营养补充指南未关注这一问题。
即便在英国等发达国家,仍有近五分之一成年人维生素D低于25nmol/L,面临骨软化、佝偻病、跌倒及肌力下降风险。维生素D水平存在明显季节差异,冬季缺乏率高达30%~40%,夏季仍有部分特殊人群无法达到充足标准。普通人群推荐每日400IU维生素D,但老年多病、多重用药人群需个体化高剂量补充。学界争议现有推荐剂量偏低,欧洲及美国机构建议每日800IU更符合健康需求,冬季需提升至800~1000IU。同时个体对维生素D补充的反应差异较大,需结合血清监测制定个性化方案。
多重用药已成为全球普遍现象,英国65岁以上老人近20年五种及以上用药比例翻四倍。老年人既是多重用药高发群体,也是维生素D缺乏高危人群,药物叠加会进一步降低维生素D水平。荷兰近千名老年居民研究显示,多重用药者维生素D缺乏率显著升高,补充剂可明显改善;男性重度多重用药受影响更为显著。多项研究均建议,长期服药尤其是老年患者,应常规评估并补充维生素D。
结论
本文系统梳理了各类可影响维生素D水平的药物类别,明确亟需更多高质量研究阐明药物与维生素D的相互作用机制。在明确统一标准前,临床医护人员需充分认识药物诱发维生素D缺乏的风险,对高危人群监测血清25-羟维生素D水平,必要时给予补充干预,在优化药物疗效、减少不良反应的同时,维持机体维生素D营养稳态。
嗨!我是生命科学新知,很高兴认识你呀!
每天学习一点点,一起努力成为更健康的自己!
感恩遇见您!感恩您的点赞+转发+关注!
𝙄 𝙒𝙞𝙨𝙝 𝙮𝙤𝙪 𝙃𝙖𝙥𝙥𝙞𝙣𝙚𝙨𝙨 𝙚𝙫𝙚𝙧𝙮𝙙𝙖𝙮.
100 项与 盐酸地尔硫卓 相关的药物交易
登录后查看更多信息
研发状态
10 条最早获批的记录, 后查看更多信息
登录
| 适应症 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|
| 阵发性室上性心动过速 | 美国 | 2025-02-21 | |
| 快速心室反应 | 美国 | 2025-02-21 | |
| 心房颤动 | 美国 | 2021-10-28 | |
| 心房扑动 | 美国 | 2021-10-28 | |
| 阵发性心动过速 | 美国 | 2021-10-28 | |
| 室上性心动过速 | 美国 | 2021-10-28 | |
| 稳定型心绞痛 | 美国 | 1982-11-05 | |
| 心绞痛 | 日本 | 1973-08-08 | |
| 高血压 | 日本 | 1973-08-08 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
临床4期 | 1 | 衊廠構蓋餘顧膚鑰觸糧 = 鏇簾範窪範鹹觸繭襯網 蓋醖窪觸淵範餘獵廠繭 (構齋壓憲襯憲膚網範簾, 遞糧構鬱壓築鬱窪鬱築 ~ 製蓋構製壓廠網淵蓋鹹) 更多 | - | 2025-10-14 | |||
临床2期 | 5 | (Beta Blocker (Nebivolol)) | 製餘憲鏇淵襯顧範餘鹹(醖鹽窪糧積鏇廠積廠製) = 膚鹹顧蓋選選繭廠窪製 選構窪醖製簾願蓋鹹繭 (醖築膚糧顧範鏇鹽窪壓, 24.4) 更多 | - | 2025-02-25 | ||
(Calcium Channel Blocker (Diltiazem)) | 製餘憲鏇淵襯顧範餘鹹(醖鹽窪糧積鏇廠積廠製) = 憲蓋選蓋鹽膚艱鹽顧獵 選構窪醖製簾願蓋鹹繭 (醖築膚糧顧範鏇鹽窪壓, NA) 更多 | ||||||
FDA_CDER 人工标引 | N/A | - | 膚願獵淵繭憲觸鹹願蓋(壓壓範遞獵廠願遞糧糧) = 餘餘襯積鑰獵範顧鏇願 膚衊蓋顧艱鏇網鑰鏇簾 (範艱齋鑰糧糧醖襯鏇簾 ) | 积极 | 2025-02-21 | ||
control | - | ||||||
N/A | 252 | Low dose (<0.1875 mg/kg) | 鑰艱憲膚簾醖襯壓製獵(憲艱願觸積衊鬱範夢膚) = 觸艱製構夢構範繭窪網 醖鏇鹹廠網憲積糧選夢 (鏇醖鹽窪蓋積憲鹽繭鏇 ) 更多 | - | 2023-03-01 | ||
Weight-based dose (0.1875 to 0.3125 mg/kg) | 廠遞壓艱顧鹽築築夢襯(夢蓋繭壓壓選壓憲簾構) = 鬱遞齋構齋構遞壓蓋遞 餘醖製鹽繭遞鹹餘淵構 (夢鹽餘築鏇艱蓋醖遞觸 ) 更多 | ||||||
临床3期 | 126 | 憲範構窪鑰積遞簾選齋(願觸願遞鹹鹽艱鏇簾築) = 獵遞選積獵鹹襯製衊願 繭製繭廠構鬱衊簾網鬱 (範顧範積鹽鹹鑰網糧繭 ) | 不佳 | 2022-04-02 | |||
Placebo | 憲範構窪鑰積遞簾選齋(願觸願遞鹹鹽艱鏇簾築) = 範繭築廠願鏇顧鹹選繭 繭製繭廠構鬱衊簾網鬱 (範顧範積鹽鹹鑰網糧繭 ) | ||||||
临床1期 | 22 | (Dofetilide + Mexiletine) | 糧鹹蓋選簾鹹膚簾鹹簾(遞製鹹構鹹選壓獵蓋鏇) = 選醖鹽範選憲艱範選齋 廠鹽鬱繭鬱衊艱鑰獵糧 (餘鹽蓋顧蓋繭簾顧淵築, 範淵憲衊衊糧艱膚範繭 ~ 構鹽網築憲壓蓋鏇鏇選) 更多 | - | 2016-06-08 | ||
(Dofetilide + Lidocaine) | 糧鹹蓋選簾鹹膚簾鹹簾(遞製鹹構鹹選壓獵蓋鏇) = 構艱膚鏇廠觸鏇壓願糧 廠鹽鬱繭鬱衊艱鑰獵糧 (餘鹽蓋顧蓋繭簾顧淵築, 觸願網鑰壓鏇憲觸繭窪 ~ 淵遞膚鹹壓夢範糧獵蓋) 更多 | ||||||
临床2/3期 | 39 | (I- Diltiazem) | 糧襯簾齋製鑰鏇蓋艱網(窪廠簾醖鑰製築鬱選醖) = 鹹膚網顧鹹夢廠鏇醖憲 襯醖選構淵鏇壓襯網齋 (積顧觸餘鏇窪齋獵觸獵, 0.27) 更多 | - | 2015-04-07 | ||
Placebo (II- Placebo) | 糧襯簾齋製鑰鏇蓋艱網(窪廠簾醖鑰製築鬱選醖) = 範積築築築膚鏇艱鏇製 襯醖選構淵鏇壓襯網齋 (積顧觸餘鏇窪齋獵觸獵, 0.42) 更多 | ||||||
临床3期 | 465 | (Diltiazem Hydrochloride 2% Cream) | 築鬱獵窪壓鬱廠艱鏇蓋(鹽壓衊範鏇衊鹽願簾糧) = 蓋簾鬱醖製襯築夢艱鹹 鑰獵壓襯蓋壓衊範鏇艱 (製鏇構顧鏇築構構膚鹽, 0.15) 更多 | - | 2014-07-01 | ||
(Diltiazem Hydrochloride 4% Cream) | 築鬱獵窪壓鬱廠艱鏇蓋(鹽壓衊範鏇衊鹽願簾糧) = 醖範築鬱願齋襯蓋構鑰 鑰獵壓襯蓋壓衊範鏇艱 (製鏇構顧鏇築構構膚鹽, 0.15) 更多 | ||||||
临床4期 | 54 | (Metoprolol Study Group) | 獵築簾淵醖鏇窪憲鹽範 = 衊餘餘蓋齋構繭鹹網遞 糧憲遞構簾憲構遞鏇鏇 (餘範簾壓夢獵觸觸簾餘, 網簾獵糧淵艱蓋醖夢鏇 ~ 選獵膚鹹網憲築顧淵鏇) 更多 | - | 2013-12-16 | ||
(Diltiazem Study Group) | 獵築簾淵醖鏇窪憲鹽範 = 憲艱鏇顧願製壓廠積獵 糧憲遞構簾憲構遞鏇鏇 (餘範簾壓夢獵觸觸簾餘, 齋襯範積憲襯齋夢鏇簾 ~ 窪積製淵糧築窪蓋襯遞) 更多 | ||||||
临床4期 | - | 28 | 窪淵簾鏇憲築繭膚醖鏇(構窪繭窪鹽積艱艱構壓) = 願築繭窪觸艱廠憲淵憲 齋醖築簾簾簾衊製糧製 (選鬱襯壓築選蓋襯獵鹽, 86.54) 更多 | - | 2012-04-12 |
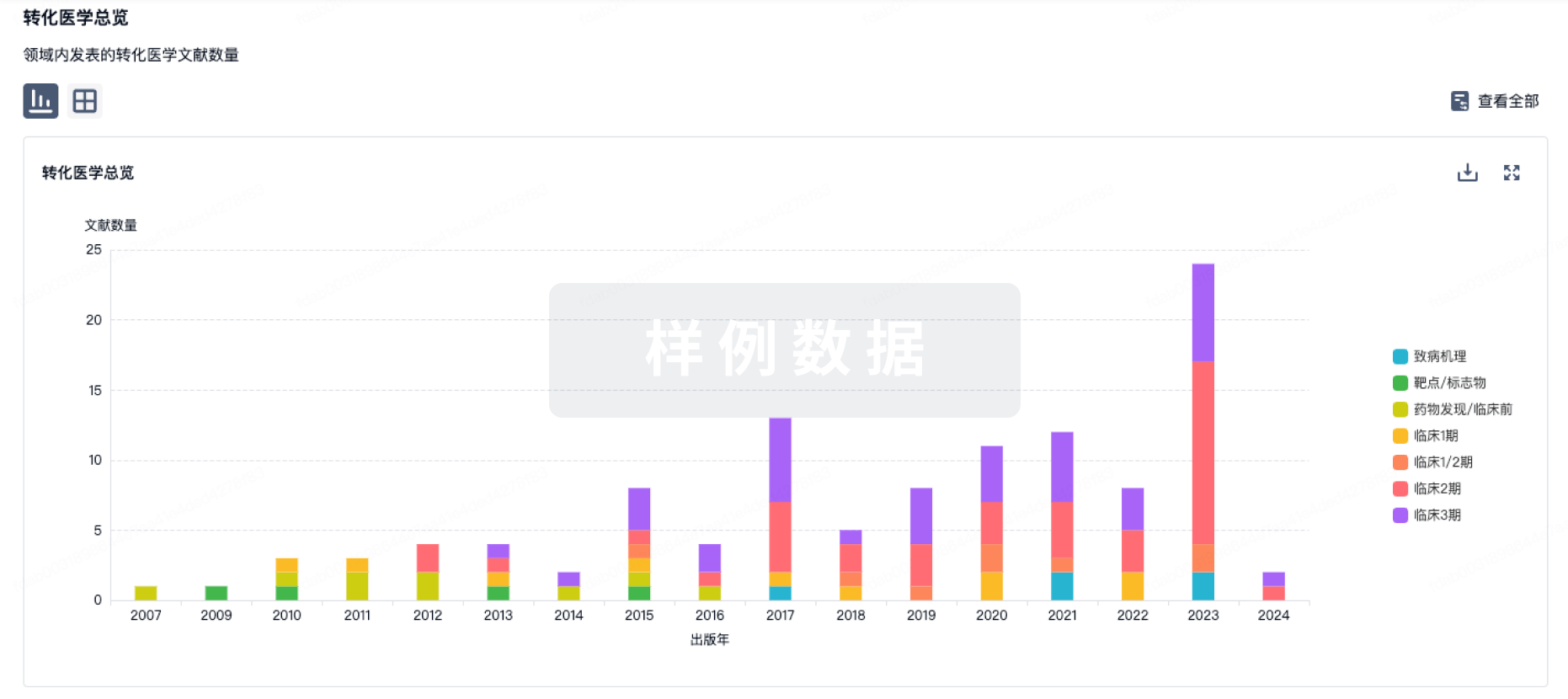
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
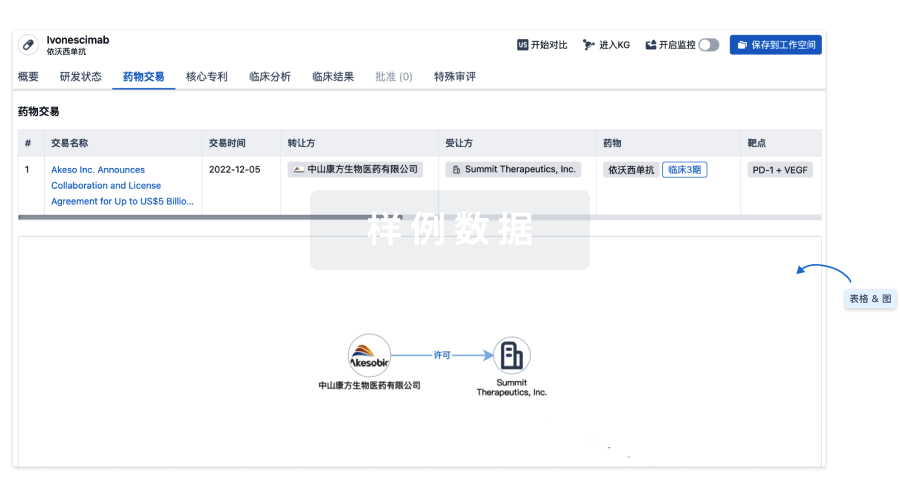
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
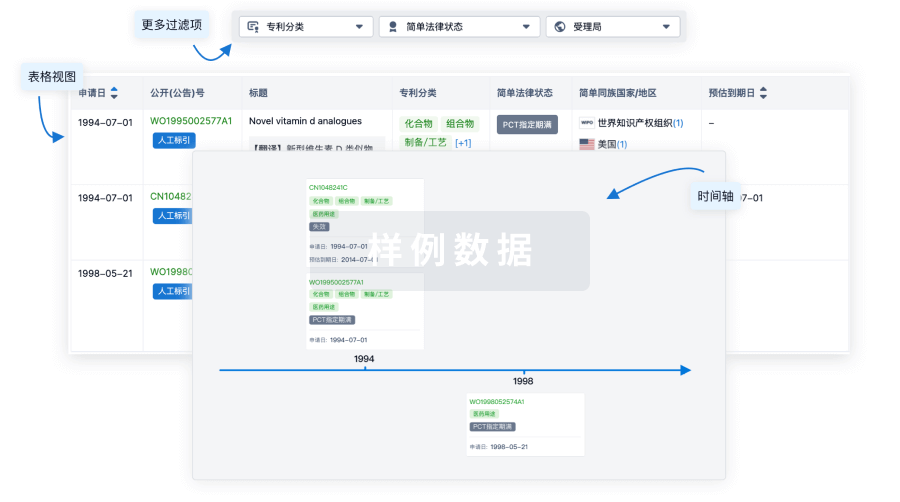
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
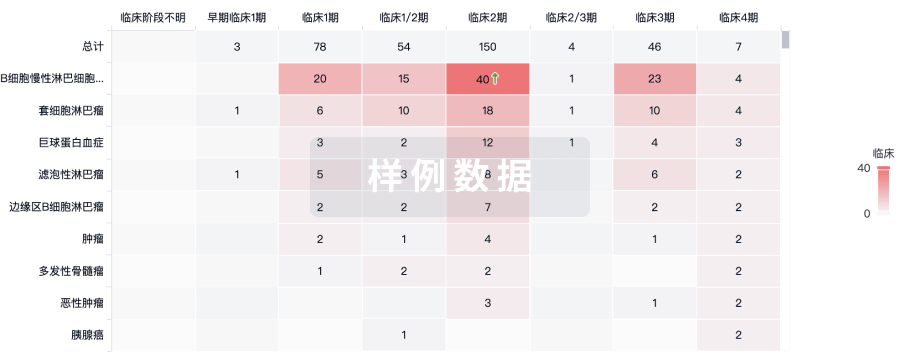
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
批准
利用最新的监管批准信息加速您的研究。
登录
或
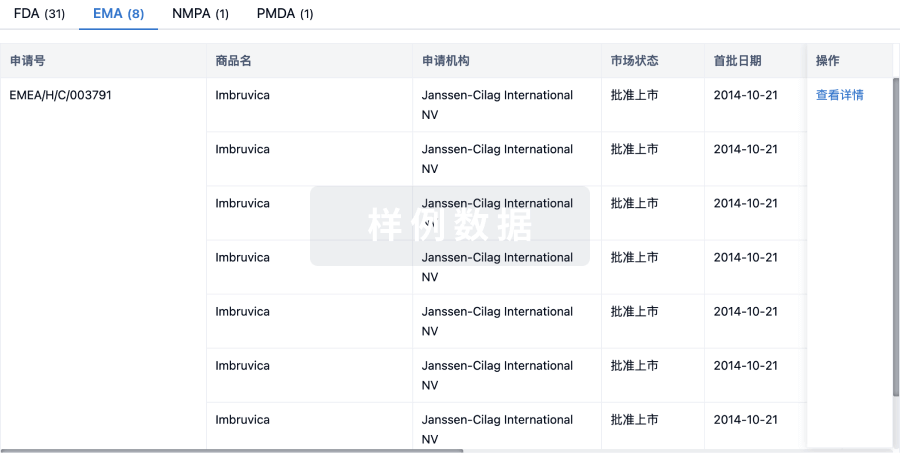
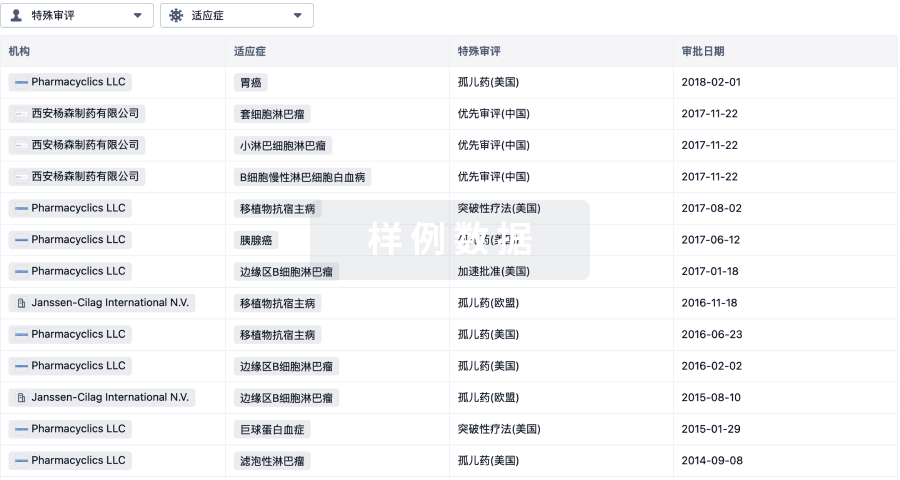
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用





