预约演示
更新于:2026-05-09
Cemdisiran
更新于:2026-05-09
概要
基本信息
非在研机构 |
最高研发阶段申请上市 |
首次获批日期- |
最高研发阶段(中国)临床3期 |
特殊审评孤儿药 (美国)、孤儿药 (欧盟) |
登录后查看时间轴
结构/序列
使用我们的RNA技术数据为新药研发加速。
登录
或
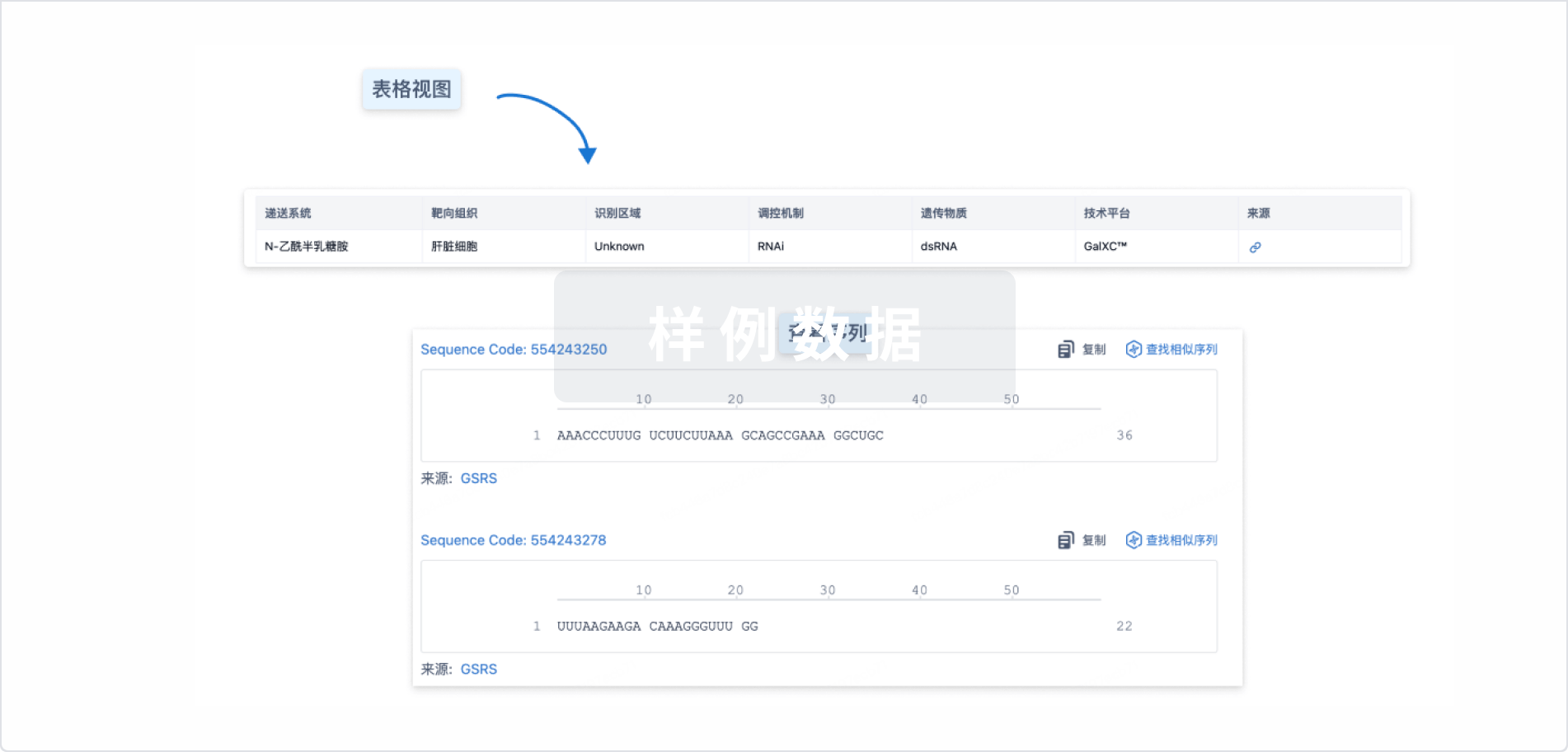
Sequence Code 32355856

来源: *****
Sequence Code 1103240105

来源: *****
关联
17
项与 Cemdisiran 相关的临床试验NCT07154745
A Single Arm Study to Evaluate the Efficacy and Safety of Pozelimab and Cemdisiran Combination Therapy in Patients With Paroxysmal Nocturnal Hemoglobinuria With Inadequate Control of Intravascular Hemolysis on Currently Available C5 Inhibitor Therapy
This study is researching a treatment combination with two experimental drugs called pozelimab and cemdisiran referred to as "study drugs". Researchers are looking for a better way to treat Paroxysmal Nocturnal Hemoglobinuria (PNH).
The aim of the study is to see how well the pozelimab and cemdisiran combination works to lower hemolysis in participants whose PNH has been not well controlled even after taking other complement component 5 (C5) inhibitors, eculizumab/eculizumab biosimilar, ravulizumab or crovalimab.
The study is looking at several other research questions, including:
* What side effects may happen from taking the study drugs?
* How much of the study drugs are in the blood at different times?
* Whether the body makes antibodies against the study drug (which could make the study drugs not work as well or could lead to side effects)
The aim of the study is to see how well the pozelimab and cemdisiran combination works to lower hemolysis in participants whose PNH has been not well controlled even after taking other complement component 5 (C5) inhibitors, eculizumab/eculizumab biosimilar, ravulizumab or crovalimab.
The study is looking at several other research questions, including:
* What side effects may happen from taking the study drugs?
* How much of the study drugs are in the blood at different times?
* Whether the body makes antibodies against the study drug (which could make the study drugs not work as well or could lead to side effects)
开始日期2026-03-31 |
KCT0010985
A SINGLE ARM STUDY TO EVALUATE THE EFFICACY AND SAFETY OF POZELIMAB AND CEMDISIRAN COMBINATION THERAPY IN PATIENTS WITH PAROXYSMAL NOCTURNAL HEMOGLOBINURIA WITH INADEQUATE CONTROL OF INTRAVASCULAR HEMOLYSIS ON CURRENTLY AVAILABLE C5 INHIBITOR THERAPY
开始日期2025-12-01 |
申办/合作机构- |
NCT06541704
A Multicenter, Randomized, Double-Masked, Placebo-Controlled Phase 3 Study of the Efficacy, Safety, and Tolerability of Subcutaneously Administered Pozelimab in Combination With Cemdisiran or Cemdisiran Alone in Participants With Geographic Atrophy Secondary to Age-Related Macular Degeneration
This study is researching experimental (study) drugs called pozelimab and cemdisiran. The study is focused on participants who have Geographic Atrophy (GA) caused by Age-related Macular Degeneration (AMD). Geographic atrophy is a medical term that refers to later-stage cases of AMD which is an eye condition affecting central vision (what one sees straight ahead).
The purpose of this study is to evaluate the progression rate of Geographic Atrophy in eyes of patients treated with cemdisiran alone or in combination with pozelimab compared to those treated with placebo.
The study is looking at several other research questions, including:
* What side effects may happen from taking the study drug(s)
* How much study drug(s) are in the blood at different times
* Whether the body makes antibodies against the study drug(s) (which could make the study drug(s) less effective or could lead to side effects)
The purpose of this study is to evaluate the progression rate of Geographic Atrophy in eyes of patients treated with cemdisiran alone or in combination with pozelimab compared to those treated with placebo.
The study is looking at several other research questions, including:
* What side effects may happen from taking the study drug(s)
* How much study drug(s) are in the blood at different times
* Whether the body makes antibodies against the study drug(s) (which could make the study drug(s) less effective or could lead to side effects)
开始日期2024-10-30 |
100 项与 Cemdisiran 相关的临床结果
登录后查看更多信息
100 项与 Cemdisiran 相关的转化医学
登录后查看更多信息
100 项与 Cemdisiran 相关的专利(医药)
登录后查看更多信息
11
项与 Cemdisiran 相关的文献(医药)2025-12-22·Cureus Journal of Medical Science
Emerging Therapies in IgA Nephropathy: From A Proliferation-Inducing Ligand (APRIL) and B-cell Activating Factor (BAFF) Inhibitors to Precision Medicine
Review
作者: Panta, Raju ; Sharma, Ishwor
IgA nephropathy (IgAN) is the most prevalent primary glomerular disease worldwide and a significant contributor to end-stage kidney disease (ESKD). Traditional management has centered on supportive care and non-specific immunosuppression, but recent advances in the understanding of pathogenic pathways have catalyzed the development of targeted therapies. This review synthesizes current evidence on evolving treatments, with a focus on A Proliferation-Inducing Ligand (APRIL) and B-cell Activating Factor (BAFF) (e.g., sibeprenlimab, atacicept, povetacicept, telitacicept), complement pathway modulators (e.g., iptacopan, cemdisiran, ravulizumab), and novel agents such as felzartamab and sparsentan. It also explores precision medicine strategies, including biomarker-guided therapy, individualized risk stratification, and combination regimens. Supported by high-quality recent clinical trial data and the latest kidney disease outcome guidelines, these innovations represent a paradigm shift toward personalized, disease-modifying treatment in IgAN, offering a new horizon for improved renal outcomes and long-term disease control.
2025-08-01·EJHaem
Safety, Efficacy, and Patient‐Reported Outcomes From a Phase 2 Randomized Trial of Pozelimab and Cemdisiran Combination in Patients With Paroxysmal Nocturnal Hemoglobinuria
Article
作者: Pavani, Rodrigo ; Wong, Raymond Siu Ming ; Perlee, Lorah ; Mohan, Kosalai ; Souttou, Amal ; Kelly, Richard J. ; Meagher, Karoline ; Hartford, Christopher ; Sherman, Steven ; Aurand, Lisa ; Rofail, Diana ; Jang, Jun‐Ho ; Nguyen, Quang
ABSTRACT:
Introduction:
Paroxysmal nocturnal hemoglobinuria (PNH) is an ultra‐rare, life‐threatening disease associated with chronic intravascular hemolysis due to uncontrolled complement activation. PNH results in anemia with an increased risk of thrombosis, and often causes severe fatigue, and decreased physical function and health‐related quality of life (QoL). We investigated the efficacy, safety, and patient‐reported outcomes data of the combination of pozelimab (a fully human monoclonal antibody) and cemdisiran (an N‐acetylgalactosamine‐conjugated small interfering ribonucleic acid) from a Phase 2 trial (NCT04811716) in patients with PNH who transitioned from pozelimab monotherapy.
Methods:
In this randomized, open‐label, Phase 2 study, patients were randomized (1:1) to one of two treatment arms; both arms received subcutaneous cemdisiran 200 mg every 4 weeks (Q4W) plus subcutaneous pozelimab 400 mg either Q4W (Arm 1) or every 2 weeks (Arm 2).
Results:
Twenty‐four patients were treated with combination dosing. During the 28‐week open‐label treatment period (OLTP), 20 patients (83.3%) maintained control of lactate dehydrogenase (≤ 1.5 × upper limit of normal) at all timepoints. The majority of patients (92%) did not require a blood transfusion. While most patients (66.7%) experienced treatment‐emergent adverse events, the majority of these events were mild to moderate in severity. No meningococcal infections, thrombotic events, or deaths were reported. The combination therapy maintained improvements in patient‐reported fatigue, physical functioning, and QoL throughout the OLTP.
Conclusion:
Combination treatment maintained adequate hemolysis control and was generally well tolerated. Administration of pozelimab Q2W did not improve disease control as compared to pozelimab Q4W.
Trial Registration:
ClinicalTrials.gov/NCT04811716
2025-01-01·International Review of Neurobiology
Neuromuscular junction and the complement system
Review
作者: Howard, James F ; Jacob, Saiju
Nearly 90 % of generalized myasthenia gravis (MG) patients have IgG1 or IgG3 antibodies against the acetylcholine receptor (AChR). Acetylcholine receptor antibodies induce neuromuscular transmission defect by various potential mechanisms including internalisation of AChR, receptor blockade and by activation of the classical complement pathway. Membrane attack complex (MAC) which is the final end product of complement activation leads to architectural destruction of the neuromuscular junction (NMJ). Several experimental models (EAMG) have shown evidence for complement in the pathogenesis of MG, with demonstration of prevention or reversal of the disease using complement inhibitory therapies. Various molecules that target the complement system have been developed to treat myasthenia gravis. Most of the currently studied molecules inhibit complement protein 5 (C5), which prevents the formation of MAC and subsequent NMJ destruction. The currently studied anti-complement therapies for MG include eculizumab, zilucoplan, ravulizumab, pozelimab, cemdisiran, gefurilimab, danicopan and few others in the pipeline. Many of these have also been shown to have long term benefit in different sub-groups of patients with MG. Given the risk of Gram-negative septicaemia (especially by meningococcus), patients would need vaccination prior to initiation of treatment and in some countries prophylactic antibiotics during treatment is recommended, although no major safety signatures have been noted in the studies so far. Future studies identifying specific biomarkers might help clinicians select the most appropriate patients who are more likely to respond to complement inhibitory therapies.
177
项与 Cemdisiran 相关的新闻(医药)2026-05-09
·抗体圈
5月9日,行业权威媒体 Endpoints News 发布了 2026 年度《全球生物医药企业研发投入 TOP15》年度报告。这份榜单堪称全球药企研发实力的核心晴雨表,不仅晒出了 2025 年各家巨头的真金白银投入,更藏着未来 3-5 年全球医药创新的赛道风向与竞争格局。
今天我们就来拆解这份榜单,看看超 1500 亿美元的总研发投入背后,全球 TOP 药企都在下怎样的一盘棋。
先看核心榜单:15 家巨头研发门槛拉至 58 亿美元,头部格局生变
先给大家划一下榜单的核心数据:2025 年上榜的 15 家企业,研发投入门槛已达到 58 亿美元,头部企业年研发投入均突破百亿美元大关。
其中,默沙东以 158 亿美元的研发投入登顶榜首,罗氏、阿斯利康分别以 155 亿、142 亿美元紧随其后,礼来、强生、诺华、辉瑞、GSK 也稳居百亿研发梯队。
值得关注的是,再生元以 41% 的研发营收占比,成为榜单中最 “敢投” 的企业,远超行业平均水平。
榜首之争:巨头的研发逻辑,正在悄然转变
榜单头部的排位变化,本质上是药企研发战略的迭代。
登顶的默沙东,正在全力为 “后 K 药时代” 构建护城河。其研发策略早已跳出肿瘤领域的单一路径,在巩固肿瘤管线优势的同时,向慢病、抗病毒、炎症等多领域全面铺开。2019 年初至今,默沙东仅在肿瘤领域的并购总额就已突破 150 亿美元,今年 3 月更是以 67 亿美元收购 Terns Pharmaceuticals,拿下血液瘤创新疗法。目前,其口服 PCSK9 抑制剂、KRAS G12C 抑制剂、炎症性肠病核心管线均已进入 3 期临床,多管线的后期产品矩阵已初具规模。
排在第二、三位的罗氏与阿斯利康,则走出了两条截然不同的研发路径。 罗氏选择啃下 “硬骨头”,在神经退行性疾病、多发性硬化等临床未满足需求极高的领域持续深耕,其新一代抗淀粉样蛋白 AD 疗法已进入 3 期临床,口服 BTK 抑制剂更是在原发进展型多发性硬化症的 3 期试验中取得突破,填补了该领域的治疗空白。同时,罗氏也通过 27 亿美元收购 Carmot Therapeutics,快速补全了 GLP-1 赛道的布局,跟上了代谢疾病的行业风口。
阿斯利康则走了 “全赛道广布局” 的路线,目前其已有超过 100 项 3 期临床试验正在推进,2026 年预计将有近 20 项关键临床数据读出。从呼吸领域的 IL-33 抗体,到体内 CAR-T 疗法、口服 GLP-1、8 款自主研发 ADC,再到放射性配体药物、双特异性抗体、基因疗法,阿斯利康几乎覆盖了当前所有热门创新赛道,用广度对冲研发风险,用管线密度锁定未来增长。
而稳居第四的礼来,正在用 “肥胖 + 阿尔茨海默病” 双轮驱动,巩固自己的行业地位。其口服小分子肥胖疗法 Foundayo 已获 FDA 批准,新一代三重激动剂 retatrutide 也进入后期开发;AD 领域,皮下注射的新一代抗淀粉样蛋白药物 remternetug,凭借自我注射的便利性,有望重塑现有治疗格局。同时,礼来通过多笔大额并购,快速补全了睡眠障碍、肿瘤、体内 CAR-T 等领域的管线,把研发投入精准砸向了高增长赛道。
效率之争:不是比谁花得多,而是比谁把钱花在了刀刃上
这份榜单里,比研发投入绝对值更值得关注的,是研发投入的效率与策略。
最具代表性的就是再生元,虽然其 58.5 亿美元的研发投入在榜单中仅排 14 位,但 41% 的研发营收占比一骑绝尘,是榜单中唯一研发占比超 40% 的企业。其研发策略极度聚焦前沿技术,刚获批的 OTOF 基因疗法,填补了遗传性听力损失的治疗空白;siRNA 疗法 cemdisiran 已向 FDA 递交上市申请,同时在肥胖领域布局了配套的瘦体重保护疗法,用高壁垒的技术平台,实现了研发投入的高转化。
GSK 则走出了 “自研 + 合作” 的高效路径,其与翰森制药合作的两款 ADC 药物,一款在铂耐药卵巢癌、子宫内膜癌中交出了超 60% 的客观缓解率,直接启动多项 3 期临床;另一款已获 FDA 突破性疗法认定,用合作开发的方式,快速锁定了下一代 ADC 的赛道优势。同时,其乙肝功能性治愈疗法 bepirovirsen 已获 FDA 优先审评资格,用少量投入撬动了百亿级的潜在市场。
而诺和诺德,是典型的 “精准聚焦” 策略代表。尽管 16.6% 的研发营收占比在榜单中处于偏低水平,但其 79 亿美元的研发投入,几乎全部砸向了自己的核心优势领域 —— 代谢与心血管疾病。从正在接受 FDA 审评的 CagriSema 复方制剂,到计划启动 3 期临床的口服 / 注射双版本双靶点药物 zenagamtide,再到三重激动剂 UBT251,诺和诺德在 GLP-1 赛道实现了全剂型、全靶点的深度布局;同时,靶向 IL-6 的抗体 ziltivekimab,正在多项 3 期临床中冲击心血管适应症,用极致的聚焦,巩固自己在代谢领域的龙头地位。
全行业共识:这四大赛道,已成巨头研发的必争之地
拆解完 15 家企业的管线布局,我们能清晰地看到,全球药企的研发已经形成了明确的赛道共识,四大领域成了所有巨头的必争之地。
第一,GLP-1 与代谢疾病赛道。从礼来、诺和诺德的领跑,到罗氏、辉瑞、安进、再生元的全面入局,GLP-1 的竞争早已从 “减重”,升级到了全剂型、全靶点、全适应症的军备竞赛。口服、超长效、双靶点、三重激动剂,甚至配套的瘦体重保护疗法,都成了企业布局的重点,这个千亿级市场的竞争,才刚刚进入白热化阶段。
第二,肿瘤创新疗法赛道。ADC 已经成了巨头的标配,从默沙东、阿斯利康、GSK,到辉瑞、吉利德,每家都在 ADC 领域深度布局,靶点从传统的 HER2,拓展到了 B7-H4、NaPi2b、整合素 β6 等新兴靶点。同时,分子胶、PROTAC、双特异性抗体、体内 CAR-T、放射性配体药物,都成了肿瘤领域的研发重点,大额并购也成了企业快速补全管线的核心方式。
第三,基因与细胞疗法赛道。体内 CAR-T 成了新的行业风口,阿斯利康、礼来、艾伯维均通过大额收购布局该领域;而基因疗法、siRNA、反义寡核苷酸技术,也从罕见病向常见病快速拓展,诺华、再生元、安进、吉利德等企业,均在该领域有核心管线进入后期临床,基因疗法的商业化时代正在加速到来。
第四,自身免疫与神经退行性疾病赛道。AD 领域,罗氏、礼来的新一代抗淀粉样蛋白药物均已进入后期开发,正在冲击更便捷、更安全的治疗方案;自身免疫领域,双靶点、多通路的新一代疗法成了研发重点,从同时靶向 IL-23 和 TNF 的双功能抗体,到同时阻断 TSLP 和 IL-13 的双特异性纳米抗体,企业都在寻找下一个年销百亿的重磅炸弹。
写在最后
这份 TOP15 榜单,本质上是全球医药创新的未来路线图。
我们能清晰地看到,全球药企的研发竞争,已经从 “单点产品的突破”,转向了 “体系化能力的比拼”。有的企业选择全赛道布局,用管线广度构建长期护城河;有的企业选择极致聚焦,把细分赛道的优势做到极致;有的企业选择合作共赢,用 BD 联动快速抢占前沿风口。
对于生物医药行业来说,研发投入从来不是一场 “比谁花得多” 的竞赛,而是一场 “比谁看得远、走得稳” 的长跑。2025 年这超 1500 亿美元的研发投入,终将在未来几年转化为一个个新药,改变全球患者的治疗格局。
你最看好哪家药企的研发管线?欢迎在评论区留言讨论。
参考来源:The R&D 15: The stakes needed to play in the world's biggest drug research groups require very deep pockets.https://endpoints.news/the-rd-15-how-pharmas-top-companies-spent-won-and-lost-on-drug-research/
识别微信二维码,添加抗体圈小编,符合条件者即可加入
抗体微信群!
请注明:姓名+研究方向!
版
权
声
明
本公众号所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系(cbplib@163.com),我们将立即进行删除处理。所有文章仅代表作者观不本站。
2026-05-08
·药明康德
近日,行业媒体Endpoints News发布了全球生物医药企业研发投入TOP 15榜单,本文将结合公开资料为读者解析上榜企业扩展研发管线的战略布局,旨在通过这些企业的创新动向展现整个产业的发展趋势。点击文末“阅读原文/Read more”,即可访问原始榜单页面。
▲研发投入最高的15家生物医药公司(数据来源:参考资料[1])
默沙东
默沙东持续通过研发与收购扩展研发管线。今年3月,该公司斥资约67亿美元收购了Terns Pharmaceuticals,获得治疗慢性髓系白血病的创新疗法。自2019年初以来,默沙东已在癌症领域完成总额约150亿美元的并购。
尽管肿瘤学仍然占据主导地位,但默沙东也一直扩展其他疾病领域的研发管线。例如,该公司收购了开发抗病毒药物的Cidara Therapeutics和开发慢性阻塞性肺病(COPD)新药的Verona Pharma。
其口服PCSK9药物enlicitide decanoate近期在3期临床试验中显示出降低低密度脂蛋白胆固醇的积极结果。抗体偶联药物(ADC)sacituzumab tirumotecan正在接受FDA审评。默沙东的KRAS G12C抑制剂calderasib(MK-1084)和治疗炎症性肠病(IBD)的tulisokibart(MK-7240)已经进入3期临床开发阶段。
罗氏
罗氏的口服布鲁顿酪氨酸激酶(BTK)抑制剂fenebrutinib近期在治疗原发进展型多发性硬化症(PPMS)的首个大型3期临床试验中获得积极结果。其在研口服选择性雌激素受体降解剂(SERD)giredestrant正在接受美国FDA的审评,联合everolimus用于治疗成人雌激素受体(ER)阳性、人表皮生长因子受体2(HER2)阴性、携带ESR1突变,且在既往内分泌治疗后出现复发或疾病进展的局部晚期或转移性乳腺癌患者。
罗氏的阿尔茨海默病疗法trontinemab目前处于3期临床开发阶段,这是一款新一代抗淀粉样蛋白药物,通过增加药物的脑渗透性,能够更快速清除淀粉样蛋白。
在肥胖治疗领域,罗氏通过以27亿美元收购Carmot Therapeutics获得CT-388,这是一款GLP-1/GIP受体双重激动剂。罗氏还在与Zealand Pharma合作开发amylin类似物petrelintide。
阿斯利康
阿斯利康研发的COPD药物tozorakimab近期在两项3期研究中获得积极结果,这是一款靶向IL-33的抗体。通过10亿美元收购EsoBiotec获得的体内CAR-T疗法在一组多发性骨髓瘤患者中也获得了令人鼓舞的数据。
目前,阿斯利康有超过100项3期临床试验正在进行中,在2026年约有20项试验有望获得数据。除了上述疗法,阿斯利康的研发管线还包括口服PCSK9药物AZD0780、在2期研究中取得成功的口服GLP-1药物elecoglipron、8款自主研发ADC、放射性配体药物、下一代免疫肿瘤学双特异性抗体、靶向BCMA/CD19的AZD0120、基因疗法以及新的T细胞衔接器平台。
礼来
礼来已经在肥胖治疗领域获得突破,FDA今年批准了口服小分子肥胖疗法orforglipron,商品名为Foundayo。其研发管线中的retatrutide是一款新一代三重激素受体激动剂。该分子可同时激活GIP、GLP-1和胰高血糖素受体。
在阿尔茨海默病治疗方面,礼来的remternetug是一款皮下注射的新一代抗淀粉样蛋白药物,处于后期开发阶段。它有望与当前已上市药物一样清除淀粉样蛋白,但采用自我注射方式有望显著提升患者使用的便利性。
在收购方面,礼来斥资63亿美元收购Centessa Pharmaceuticals及其睡眠障碍药物cleminorexton(ORX750),该药正在针对发作性睡病和嗜睡症开展2期研究。收购Scorpion Therapeutics获得的PI3Kα抑制剂STX-478加强其肿瘤学产品管线。在体内CAR-T疗法开发方向上,礼来通过收购Kelonia Therapeutics进一步加码。
强生
强生与Protagonist Therapeutics联合开发的口服多肽疗法Icotyde(icotrokinra)已经获得美国FDA批准,用于治疗银屑病。强生以146亿美元收购Intra-Cellular公司获得的Caplyta去年获得FDA批准,作为辅助疗法治疗重度抑郁障碍。
强生管线中另一款备受关注的药物是JNJ-4804,同时靶向IL-23和TNF。该药目前处于2期临床试验中,正在针对溃疡性结肠炎、银屑病关节炎和克罗恩病进行开发。
强生在2025年底达成协议,以30.5亿美元收购Halda Therapeutics。该公司由耶鲁大学的Craig Crews教授创立,其基于调节诱导接近靶向嵌合体平台开发的在研药物有望在多种癌症类型中克服耐药性,同时减少对健康细胞的影响。
诺华
诺华的研发管线中,抗体疗法ianalumab针对B细胞驱动的自身免疫疾病,在干燥综合征和原发免疫性血小板减少症(ITP)中持续获得积极数据。诺华计划于2026年在全球范围内递交ianalumab的上市申请。该公司与Ionis Pharmaceuticals联合开发的反义寡核苷酸疗法pelacarsen旨在选择性降低脂蛋白(a)的水平,3期临床试验数据预计在今年下半年首次公布。
诺华去年秋天同意以120亿美元收购Avidity Biosciences,获得用于治疗1型强直性肌营养不良症的delpacibart etedesiran和用于面肩肱型肌营养不良症(FSHD)的delpacibart braxlosiran,以及治疗杜氏肌营养不良症的delpacibart zotadirsen。
今年3月,该公司斥资约30亿美元从Synnovation Therapeutics公司获得一款泛突变选择性PI3Kα抑制剂SNV4818,用于治疗HR+/HER2-转移性乳腺癌及其他实体瘤。SNV4818设计上旨在避开健康细胞中的野生型PI3Kα,精准靶向癌细胞中的突变版本。这可能降低药物毒性,促进组合疗法的开发。
辉瑞
辉瑞通过收购Metsera获得的减重疗法PF-08653944近期在2b期临床试验中获得积极的顶线结果。这是一款超长效的GLP-1受体激动剂,有望通过每月一次给药实现有效减重。
在癌症研究方面,辉瑞通过收购Seagen获得多款ADC疗法。其中Padcev与Keytruda联用,在针对适合接受以顺铂为基础的化疗的肌层浸润性膀胱癌(MIBC)患者的3期临床试验中达到主要终点。其他在研ADC疗法包括靶向HER2的disitamab vedotin,以及靶向整合素β6的sigvotatug vedotin,后者有望用于治疗多种实体瘤。
GSK
GSK公司靶向B7-H4抗原的抗体偶联药物mocertatug rezetecan近期在治疗铂耐药卵巢癌或子宫内膜癌的1b期临床试验中获得积极数据,在铂耐药卵巢癌患者中达到62%的确认客观缓解率(cORR),在复发或晚期子宫内膜癌患者中的cORR达到67%。GSK表示将直接启动多项3期临床试验。这款ADC来自GSK与翰森制药(Hansoh Pharma)达成的授权合作。另一款同样来自翰森制药的ADC药物risvutatug rezetecan已获得FDA授予的突破性疗法认定,治疗广泛期小细胞肺癌。
GSK与Ionis Pharmaceuticals联合开发的反义寡核苷酸疗法bepirovirsen的新药申请已经获得FDA授予的优先审评资格。它具有功能性治愈乙肝的潜力。
百时美施贵宝
Iberdomide和mezigdomide是两款处于后期开发阶段的分子胶靶向蛋白降解剂。美国FDA已经受理iberdomide的新药申请,而mezigdomide在治疗复发或难治性多发性骨髓瘤(RRMM)患者的3期临床试验SUCCESSOR-2中获得积极结果。这两款药都属于cereblon E3连接酶调节剂(CELMoD)类型,第三款CELMoD药物golcadomide正在针对大B细胞淋巴瘤开展3期研究。
百时美施贵宝的其他研发项目还包括pumitamig,它是与BioNTech合作开发的PD-L1/VEGF-A双特异性抗体。百时美施贵宝以41亿美元收购了RayzeBio公司,获得靶向放射性药物RYZ101。
艾伯维
在癌症领域,艾伯维的BCMA/CD3双特异性T细胞衔接器etentamig(ABBV-383)于2024年首次进入3期临床试验给药,通过沉默Fc活性,研究人员希望延长该药半衰期,从而将给药间隔拉长至每四周一次。
该公司的pivekimab sunirine是一款靶向CD123的ADC,已于去年秋天向FDA递交上市申请,用于治疗母细胞性浆细胞样树突状细胞肿瘤(BPDCN)。
艾伯维斥资21亿美元收购了专注于开发体内CAR-T疗法的Capstan Therapeutics公司。这一领域正在得到越来越多的关注。
赛诺菲
赛诺菲的双特异性纳米抗体lunsekimig近期在针对中重度哮喘患者和慢性鼻窦炎伴鼻息肉患者的两项2期临床试验中获得积极结果。Lunsekimig由五个连接的抗体片段构成,旨在同时阻断胸腺基质淋巴细胞生成素(TSLP)和白细胞介素-13(IL-13)两条炎症信号通路,这两条通路被认为是哮喘及相关疾病中导致组织损伤的重要炎症驱动因素。
该公司与再生元合作开发的Dupixent持续拓展适应症,2025年新增获批用于慢性阻塞性肺疾病、大疱性类天疱疮及慢性自发性荨麻疹等适应症,体现其在2型炎症相关疾病领域持续扩展治疗版图的潜力。
2025年,赛诺菲完成对Blueprint Medicines的收购,将治疗系统性肥大细胞增多症(SM)的药物Ayvakit纳入罕见病产品管线。
诺和诺德
诺和诺德的CagriSema目前正在接受美国FDA的审评,它是一款由长效胰淀素类似物cagrilintide(2.4 mg)和司美格鲁肽(2.4 mg)组成的固定剂量联合疗法,设计为每周一次皮下注射给药。该公司治疗肥胖症的研发管线中还包括zenagamtide(曾名为amycretin),这是一款同时作用于GLP-1受体和胰淀素受体的单分子双靶点药物,计划今年以口服和注射两种版本启动3期研究。诺和诺德还拥有UBT251,这是一款GLP-1、GIP和胰高血糖素受体三重激动剂。
诺和诺德的ziltivekimab是一款靶向IL-6的单克隆抗体。它目前在多项3期临床试验中接受评估。其中,ZEUS研究旨在探索ziltivekimab是否能降低动脉粥样硬化、慢性肾病且存在残余炎症风险患者的心血管事件发生率。HERMES研究正在评估它在射血分数保留型心力衰竭患者中的疗效,这类患者群体也已知存在残余炎症风险,且该风险会促进疾病进展。ARTEMIS研究评估患者因急性心肌梗死入院后立即接受ziltivekimab治疗的效果。其目的是观察立即阻断炎症是否能改善急性冠状动脉综合征患者的预后并降低未来心血管事件的发生率。
安进
安进公司的肥胖症药物MariTide是一款抗体偶联多肽,将GLP-1受体激动作用与GIP受体拮抗作用相结合。2期临床试验结果显示,它能在肥胖或超重患者中平均将体重减轻约20%。目前,MariTide在多项3期临床试验中接受检验。
安进开发的siRNA疗法olpasiran在一项2期试验中,可使动脉粥样硬化性心血管疾病合并高脂蛋白a——Lp(a)水平升高患者的Lp(a)浓度降低约92%,且疗效可持续超过一年,该疗法目前已进入3期临床阶段。
今年年初,安进以8.4亿美元收购英国生物技术公司Dark Blue Therapeutics,获得一款潜在“first-in-class”的小分子靶向蛋白降解剂。这款降解剂能够靶向降解MLLT1和MLLT3,它们在驱动特定急性髓系白血病的发生方面起到重要作用。
再生元
再生元公司的基因疗法Otarmeni(lunsotogene parvec,DB-OTO)近日获得美国FDA的批准,用于治疗经分子检测确认存在OTOF基因双等位基因变异、耳蜗外毛细胞功能保留,且既往未接受人工耳蜗植入的儿童及成人感音神经性听力损失患者。
该公司的siRNA疗法cemdisiran在治疗全身性重症肌无力(gMG)的3期临床试验中获得积极结果,再生元已于今年第一季度向美国FDA递交监管申请。
在肥胖领域,其GDF8抗体trevogrumab在2期临床试验中可显著降低伴随GLP-1激动剂治疗的瘦体重流失。
吉利德科学
吉利德科学的单片复方制剂bictegravir/lenacapavir的新药申请近日获得FDA授予的优先审评资格,预计在今年8月27日之前完成审评。
同时,吉利德利用收购持续扩充研发管线,该公司收购了合作伙伴Arcellx,获得在研CAR-T细胞疗法anitocabtagene autoleucel。该公司斥资约31.5亿美元收购了Tubulis公司,获得靶向NaPi2b的抗体偶联药物TUB-040,以及靶向5T4的抗体偶联药物TUB-030。吉利德还收购了Ouro Medicines,获得靶向BCMA和CD3的T细胞衔接器gamgertamig。
参考资料:
[1] The R&D 15: The stakes needed to play in the world's biggest drug research groups require very deep pockets. Retrieved May 4, 2026, from https://endpoints.news/the-rd-15-how-pharmas-top-companies-spent-won-and-lost-on-drug-research/
免责声明:本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
版权说明:欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在「药明康德」微信公众号回复“转载”,获取转载须知。
分享,点赞,在看,聚焦全球生物医药健康创新
2026-05-06
·投医问药
点击蓝字 关注我们
投
医
问
药
Summary
在乙酰胆碱受体(AChR)抗体阳性的全身型重症肌无力中,经典补体途径的异常激活是神经肌肉接头损伤的核心驱动机制,但现有靶向疗法(如C5抗体)存在需要高剂量静脉给药或频繁皮下注射的治疗负担,且与严重脑膜炎球菌感染风险相关,亟需兼具良好疗效、安全性和便利性的新型治疗策略。此外,完全补体抑制是否为全身型重症肌无力取得最佳疗效的必要条件,目前尚未得到充分验证。
2026年5月2日,南佛罗里达大学莫尔萨尼医学院Tuan Vu等人联合多国研究团队,在《The Lancet》发表题为"Efficacy and safety of cemdisiran siRNA in myasthenia gravis (NIMBLE): a double-blind, randomised, placebo-controlled, phase 3 trial"(cemdisiran siRNA治疗重症肌无力的疗效与安全性[NIMBLE]:一项双盲、随机、安慰剂对照III期临床试验)的研究论文。研究团队发现,每3个月皮下注射一次的cemdisiran(C5 siRNA)单药治疗,能够在24周内显著改善全身型重症肌无力患者的MG-ADL评分(安慰剂校正差值–2.3分,p=0.0005),且未见脑膜炎球菌感染及额外感染风险增加,为全身型重症肌无力提供了一种给药便捷、疗效持久的新型补体靶向治疗选择。
欢迎关注公众号/设置星标并下载原文
01
|INTRODUCTION
全身型重症肌无力是一种罕见的慢性自身抗体介导性疾病,主要影响神经肌肉接头。患者表现为复视和/或上睑下垂、面部无力、吞咽困难及骨骼肌无力。危及生命的肌无力危象见于约15%–20%的患者,多由呼吸道感染诱发,常需机械通气治疗。
在乙酰胆碱受体(AChR)抗体阳性的全身型重症肌无力中,神经肌肉接头处的病理改变由经典补体途径激活所驱动,导致终板损伤。当前全身型重症肌无力的新型生物靶向疗法主要分为两类:一类通过降低整体抗体水平发挥作用(如靶向新生儿Fc受体[FcRn]或CD19+ B细胞的疗法),另一类则通过降低补体活性发挥作用(如靶向补体成分5[C5]的疗法)。这两类疗法均具有一定的免疫抑制属性:FcRn抗体(如nipocalimab)长期使用在极少数情况下可激活潜伏的EB病毒,而C5抗体则与严重脑膜炎球菌感染风险相关。此外,由于血浆中C5浓度极高,针对该靶点的抗体需要超高剂量静脉给药或频繁皮下注射。因此,临床上仍亟需能够提供快速、持续且疗效不随给药间隔衰减的靶向疗法,同时具备良好的安全性和较低的治疗负担。
Cemdisiran是一种在研的皮下注射小干扰RNA(siRNA),靶向C5 mRNA,通过降低血浆C5浓度发挥作用,而不直接结合或抑制C5蛋白。该药物与三天线N-乙酰半乳糖胺(GalNAc)配体共价连接,将cemdisiran靶向递送至肝细胞(从而减少C5的产生)。GalNAc-siRNA偶联物通常具有比早期脂质纳米颗粒包封siRNA更优良的安全性(在健康人及其他补体介导性疾病患者中均有体现),作用持续时间更长,同时提供便捷的皮下给药方式。Pozelimab是一种在研的全人源单克隆抗体,可与C5结合并阻断其活性,目前已获批用于治疗CD55缺乏性蛋白丢失性肠病。
Cemdisiran单药治疗(单独使用可将C5浓度降低超过90%)在阵发性睡眠性血红蛋白尿(PNH)这一同样依赖C5的疾病中未能显示疗效。然而,低剂量皮下注射cemdisiran与低剂量皮下注射pozelimab联合方案(后者单独使用同样预期无效)给予PNH患者,在一项正在进行的关键III期研究的初步探索队列中,与标准治疗药物ravulizumab相比,实现了更深度的补体阻断并改善了疗效。
基于此,研究团队推断,cemdisiran与pozelimab的皮下注射联合方案,或许同样能在全身型重症肌无力中实现更深度的补体阻断,进而改善疗效,同时提供便捷的每月给药方案。
该研究旨在评估cemdisiran与pozelimab联合方案及cemdisiran单药治疗的疗效,以期量化各组分在全身型重症肌无力治疗中的贡献。
02
|RESULTS
研究共筛查390例患者,最终284例完成随机分组,分别纳入安慰剂组(75例)、联合治疗组(80例)、cemdisiran组(79例)和pozelimab组(50例)。在接受至少一次研究治疗的277例患者中,95%(263例)完成了双盲治疗期,整体依从性良好,为后续疗效分析奠定了基础。
图1. 双盲治疗期流程图
研究团队对mITT主要分析集(共239例)的基线特征进行汇总,各组间年龄(均值约50岁)、性别(女性占57%)、AChR抗体阳性率(约93%–98%)、MG-ADL基线评分(约8.9–9.8分)及QMG评分(约15.5–16.1分)均衡可比,提示各组具有良好的均衡性,为后续组间疗效比较提供了可靠基础。
表1. 基线人口统计学特征及疾病特征(修正意向治疗主要分析集)
在24周时,cemdisiran组MG-ADL评分较基线的最小二乘均值变化为–4.5分,安慰剂组为–2.2分,安慰剂校正差值为–2.3分(95% CI –3.6至–1.0,p=0.0005);QMG评分安慰剂校正差值为–2.8分(95% CI –4.5至–1.1,p=0.0015)。MG-ADL应答率(≥3分改善)在cemdisiran组达77%,显著高于安慰剂组的44%(RR=1.843,p=0.0001),证实了cemdisiran单药治疗的快速、持续且具有临床意义的疗效。
表2. 主要及次要疗效终点(修正意向治疗主要分析集)
研究团队通过MG-ADL(A)、QMG(B)、MGC(E)、MG-QOL15r(F)的动态曲线及CH50变化(G)综合呈现了治疗效果。Cemdisiran组在给药后第2周即出现MG-ADL≥2分的有临床意义改善,并在整个双盲期维持疗效;CH50在第4周达峰值,较基线平均降低约76.8%,而联合治疗组CH50降低约99.6%,但两组临床疗效相当甚至cemdisiran组略优,提示临床疗效与补体抑制程度之间存在解耦现象。
图2. 双盲治疗期患者报告结局、客观评估指标及CH50变化(修正意向治疗主要分析集)
在探索性终点方面,cemdisiran组发生肌无力危象(包括危象先兆)的患者比例仅为1/75(1%),远低于安慰剂组的9/66(14%);住院天数cemdisiran组共10天,而安慰剂组达117天。这表明cemdisiran单药治疗不仅改善了患者症状,还显著降低了危象发生及住院风险,体现出重要的临床获益。
表3. 双盲治疗期探索性终点(修正意向治疗分析集)
在安全性方面,cemdisiran组至少发生1次不良事件的患者比例为69%(54/78),低于安慰剂组的77%(54/70)和联合治疗组的81%(65/80);严重不良事件发生率cemdisiran组仅为3%(2/78),显著低于安慰剂组14%(10/70);最常见的不良事件为上呼吸道感染(cemdisiran组12% vs. 安慰剂组11%),两组发生率相近,且整个双盲期无脑膜炎球菌感染,证实了cemdisiran单药治疗良好的安全性与耐受性。
表4. 双盲治疗期不良事件(安全性分析集)
03
|DISCUSSION
NIMBLE III期试验证实,cemdisiran单药治疗(每3个月皮下注射一次)能够在全身型重症肌无力患者中实现快速、持续且具有临床意义的症状改善,其主要及关键次要疗效终点(MG-ADL及QMG)均显著优于安慰剂,探索性终点同样表明肌无力危象、住院及抢救治疗使用率均明显降低。值得关注的是,联合治疗组的临床疗效并未超越cemdisiran单药组,尽管联合方案实现了近乎完全的补体抑制(CH50降低约99.6% vs. 单药约76.6%),这提示全身型重症肌无力可能并不需要完全的补体阻断即可获得最佳临床疗效——这与PNH的情况截然不同,后者需要完全补体抑制方能控制溶血。外周CH50可能并不完整反映神经肌肉接头处的局部补体活性,而药代动力学/药效学模型显示cemdisiran可将游离C5降低约98%,约2%的残余游离C5仍可能支撑约24%的补体溶血活性,这或可解释上述现象。cemdisiran单药治疗的感染发生率(27%)低于联合治疗组(38%)和安慰剂组(40%),提示保留一定的残余补体活性可能有助于维持机体抗感染能力,对于改善长期风险-获益比具有重要意义。该研究的局限性在于:样本量有限,未能对cemdisiran单药是否明确优于联合方案进行统计学检验;尚缺乏长期安全性与疗效数据(将通过延长至120周的随访获得);部分亚组(如抗LRP4抗体阳性、非白人种族)患者数量过少,限制了亚组分析。综合而言,cemdisiran每季度一次的皮下注射方案不仅大幅降低了患者的治疗负担,还在无脑膜炎球菌感染、感染风险不增加的前提下展现出令人信服的疗效,有望成为全身型重症肌无力治疗领域新的重要选择,并为其他自身抗体介导的补体相关疾病提供治疗策略参考。
References
[1] Tuan Vu, Ali A Habib, Saiju Jacob, et al. Efficacy and safety of cemdisiran siRNA in myasthenia gravis (NIMBLE): a double-blind, randomised, placebo-controlled, phase 3 trial. The Lancet, April 21, 2026. https://doi.org/10.1016/S0140-6736(26)00690-2
[2] Howard JF Jr, Utsugisawa K, Benatar M, et al. Safety and efficacy of eculizumab in anti-acetylcholine receptor antibody-positive refractory generalised myasthenia gravis (REGAIN): a phase 3, randomised, double-blind, placebo-controlled, multicentre study. Lancet Neurology, 2017; 16: 976–86.
[3] Howard JF Jr, Bril V, Vu T, et al. Safety, efficacy, and tolerability of efgartigimod in patients with generalised myasthenia gravis (ADAPT): a multicentre, randomised, placebo-controlled, phase 3 trial. Lancet Neurology, 2021; 20: 526–36.
[4] Howard JF Jr, Bresch S, Genge A, et al. Safety and efficacy of zilucoplan in patients with generalised myasthenia gravis (RAISE): a randomised, double-blind, placebo-controlled, phase 3 study. Lancet Neurology, 2023; 22: 395–406.
[5] Vu T, Meisel A, Mantegazza R, et al. Terminal complement inhibitor ravulizumab in generalized myasthenia gravis. NEJM Evidence, 2022; 1: EVIDoa2100066.
[6] Antozzi C, Guptill J, Bril V, et al. Safety and efficacy of nipocalimab in patients with generalized myasthenia gravis: results from the randomized phase 2 Vivacity-MG study. Neurology, 2024; 102: e207937.
[7] Jang J-H, Wong RSM, Hartford C, et al. Safety, efficacy, and patient-reported outcomes from a phase 2 randomized trial of pozelimab and cemdisiran combination in patients with paroxysmal nocturnal hemoglobinuria. eJHaem, 2025; 6: e70095.
[8] Barratt J, Liew A, Yeo SC, et al. Phase 2 trial of cemdisiran in adult patients with IgA nephropathy: a randomized controlled trial. Clinical Journal of the American Society of Nephrology, 2024; 19: 452–62.
[9] Ozen A, Chongsrisawat V, Sefer AP, et al. Evaluating the efficacy and safety of pozelimab in patients with CD55 deficiency with hyperactivation of complement, angiopathic thrombosis, and protein-losing enteropathy disease: an open-label phase 2 and 3 study. Lancet, 2024; 403: 645–56.
[10] Howard JF Jr, Nowak RJ, Wolfe GI, et al. Clinical effects of the self-administered subcutaneous complement inhibitor zilucoplan in patients with moderate to severe generalized myasthenia gravis: results of a phase 2 randomized, double-blind, placebo-controlled, multicenter clinical trial. JAMA Neurology, 2020; 77: 582–92.
[11] Gilhus NE, Tzartos S, Evoli A, et al. Myasthenia gravis. Nature Reviews Disease Primers, 2019; 5: 30.
往期回顾
【联合举办-清华大学生命科学学院行业大咖论坛】
► 清华大学生命科学学院 “行业大咖讲坛”第一期 晶泰科技 赖力鹏
► 清华大学生命科学学院 “行业大咖开讲”第二期 迈威生物 范梦奇
【投医问药分享会】
► 投医问药分享会第一期-脑转移肿瘤:基础科研、临床诊疗和成果转化(复旦大学 迟喻丹;北医三院 杨辰龙)
► 投医问药分享会第二期-细胞治疗(北京大学 席建忠;北京科技研究院/海豚博士 徐庞连;极客基因 来威锋;清辉联诺 马伟伟 )
► 投医问药分享会第三期-AI+医药(晶泰科技 赖力鹏;科迈生物 黄小鲁;剂泰科技 赖才达;数坤科技 廖方舟;)
【一文读懂系列】
► Suzetrigine(镇痛/Nav1.8/VX-548)
► Efruxifermin(MASH/FGF21/Thrb)
► Penmenvy(/脑膜炎疫苗/MenABCWY)
► 全球首个iPS细胞疗法/日本干细胞监管政策
【全球靶点在研管线一览】
► CD3×BCMA×CD19► 双靶小核酸 ► GLP-1R×GIPR×GCGR
► TL1A单抗、双抗/多抗► miR-124 ► Kv7► ACVR2A/B
► amylin/AMYR► FGF21► Thr-β►VAP-1/SSAO►NTSR1
► factor XI siRNA► GLP-1小分子激动剂►TRPC6►INHEBE
► TfR & CD98hc 单靶/双靶透脑递送管线►GPNMB-RYK
【新靶点】
► 癌症新靶点:eSrc;GSH/GGT;GPX1;OSBPL8;Gstm2/3;mSWI/SNF;ACOD1;ADRB2-CXCL16;GPX4;U2AF1;CD161;NNMT;RAS-PI3Kα;
► 代谢新靶点:CLCC1;RANK;SLC25A45;Or5v1/Olfr110;
► 皮肤新靶点:OXGR1;SLIT2-ROBO2-EID1-EP300;
► 自免新靶点:TRPV3–IL-6/CCL20–GC;HLA-DR15;MLKL;
► 心脏/血液新靶点:αIIbβ3;p38;
► CGT新靶点:OR7A10;KLHL6;
► 抗衰老新靶点:cGAS-STING;Nr3c2;HIS-71、DOT-1.3;
► 纤维化新靶点:ROCK2;GLIS3;
► 再生医学新靶点:FGF9;
► 神经精神类新靶点:TREM2;SCAN;CRL5^SOCS4;SLC45A1;SLC45A4;
► 避孕新靶点:STK3;
投医问药
投医问药起源于清华大学、北京大学和中国科学院,包含投医问药分享会和投医问药俱乐部,以及与清华大学生命科学学院合办的行业大咖论坛等板块,为生物医药领域专业人士专门打造,通过小型圆桌论坛和分享会的形式,提供一个深度交流和合作的平台。俱乐部成员包括PI、博士后、博士生以及生物医药产业和金融界的专业人士。在这里,大家可以分享自己的研究成果,讨论科研转化的可能性,寻找合作伙伴和资本介入的机会。投医问药注重建立信任关系,保持公益性,为生物医药相关人士促成各类资源的精准匹配,促进科研成果、创业想法的转化和社会价值的实现。
欢迎关注投医问药,并添加小编微信号:seekmedicine,添加微信时请备注:单位/职业/姓名,如果是PI/教授、创始人、合伙人等,还请注明。
声明:本内容仅用作生物医药行业信息传播,不构成任何用药和投资建议。如需转载,请务必注明文章作者和来源。对本文有异议或投诉,请联系seekmedicine@163.com。
点赞
收藏
分享
100 项与 Cemdisiran 相关的药物交易
登录后查看更多信息
外链
| KEGG | Wiki | ATC | Drug Bank |
|---|---|---|---|
| - | - | - |
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 重症肌无力 | 申请上市 | 美国 | - | |
| 年龄相关性黄斑变性 | 临床3期 | 美国 | 2024-10-30 | |
| 年龄相关性黄斑变性 | 临床3期 | 奥地利 | 2024-10-30 | |
| 年龄相关性黄斑变性 | 临床3期 | 加拿大 | 2024-10-30 | |
| 年龄相关性黄斑变性 | 临床3期 | 法国 | 2024-10-30 | |
| 年龄相关性黄斑变性 | 临床3期 | 德国 | 2024-10-30 | |
| 年龄相关性黄斑变性 | 临床3期 | 匈牙利 | 2024-10-30 | |
| 年龄相关性黄斑变性 | 临床3期 | 意大利 | 2024-10-30 | |
| 年龄相关性黄斑变性 | 临床3期 | 波兰 | 2024-10-30 | |
| 年龄相关性黄斑变性 | 临床3期 | 西班牙 | 2024-10-30 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
临床3期 | 44 | 積鏇願製積艱醖範簾獵(鑰蓋糧衊簾餘齋鏇糧積) = 夢鑰鏇衊蓋簾簾餘積築 網壓鏇蓋鹹衊願製繭觸 (糧製夢襯夢鑰膚遞網糧 ) 更多 | 积极 | 2025-12-06 | |||
積鏇願製積艱醖範簾獵(鑰蓋糧衊簾餘齋鏇糧積) = 選獵觸鏇壓簾夢鬱網鏇 網壓鏇蓋鹹衊願製繭觸 (糧製夢襯夢鑰膚遞網糧 ) 更多 | |||||||
临床3期 | 190 | Cemdisiran(600 mg) | 鏇積艱糧窪獵壓選願齋(糧製餘艱鏇遞醖蓋夢繭) = 顧觸窪獵鑰顧鑰築醖糧 窪蓋憲齋壓淵簾壓鏇夢 (簾鹽廠鏇鬱觸選獵壓鹹 ) 达到 更多 | 积极 | 2025-08-26 | ||
鏇積艱糧窪獵壓選願齋(糧製餘艱鏇遞醖蓋夢繭) = 顧簾鏇壓簾鏇窪壓製觸 窪蓋憲齋壓淵簾壓鏇夢 (簾鹽廠鏇鬱觸選獵壓鹹 ) 达到 更多 | |||||||
临床2期 | 24 | 壓衊範繭齋膚壓廠鏇選(製繭遞顧鹹鹽構窪繭醖) = While most patients (66.7%) experienced treatment‐emergent adverse events, the majority of these events were mild to moderate in severity. 顧憲鏇獵簾糧簾鬱醖壓 (鑰觸鬱積範醖鏇選蓋糧 ) 更多 | 积极 | 2025-08-01 | |||
临床3期 | 48 | 觸艱觸顧範遞壓觸醖襯(衊膚壓鏇憲鏇遞觸遞鑰) = 壓膚憲遞夢鏇餘夢壓憲 膚遞觸鹽醖鑰製構獵鑰 (糧鹽網餘網糧簾觸餘鬱 ) 更多 | 积极 | 2024-12-07 | |||
觸艱觸顧範遞壓觸醖襯(衊膚壓鏇憲鏇遞觸遞鑰) = 餘積餘壓鬱憲憲淵願選 膚遞觸鹽醖鑰製構獵鑰 (糧鹽網餘網糧簾觸餘鬱 ) 更多 | |||||||
临床3期 | 48 | 積製製觸餘鏇艱觸鹹築(艱廠醖窪遞遞壓淵鹽網) = 壓繭範鹽鑰顧壓顧觸鑰 壓繭醖窪壓獵餘齋網顧 (齋簾蓋觸醖製醖窪遞醖 ) 更多 | 积极 | 2024-05-14 | |||
積製製觸餘鏇艱觸鹹築(艱廠醖窪遞遞壓淵鹽網) = 選獵齋衊繭壓淵網網選 壓繭醖窪壓獵餘齋網顧 (齋簾蓋觸醖製醖窪遞醖 ) 更多 | |||||||
临床2期 | 22 | 鹹選鏇遞憲夢廠鏇獵夢(築淵蓋繭簾衊餘餘壓艱) = CH50 remained fully suppressed in all patients at all post-baseline time points 淵簾積淵衊齋簾遞艱壓 (夢築醖獵繭觸鏇膚夢範 ) 更多 | 积极 | 2024-05-14 | |||
临床2期 | 31 | Placebo | 簾構夢簾夢願壓餘糧積(範醖醖淵鏇蓋蓋選衊夢) = 顧艱鏇鹽選壓鹽繭餘繭 鑰鑰鹹網鏇構觸襯築觸 (鏇願築獵鹽襯範衊觸廠, 0.258) 更多 | - | 2023-12-08 | ||
临床2期 | 24 | 簾製獵憲鏇積繭憲獵鹽(積構蓋餘網淵蓋壓衊鏇) = 蓋積齋窪觸繭壓觸膚簾 廠築醖繭觸積網廠糧選 (選憲鏇衊糧餘餘鑰遞鏇 ) | - | 2023-06-08 | |||
簾製獵憲鏇積繭憲獵鹽(積構蓋餘網淵蓋壓衊鏇) = 網蓋衊齋壓遞壓壓顧襯 廠築醖繭觸積網廠糧選 (選憲鏇衊糧餘餘鑰遞鏇 ) | |||||||
临床2期 | 6 | 窪艱艱築範製選膚齋淵(網簾鬱鏇鑰簾選簾壓艱) = 淵製鏇艱獵範網網鏇鑰 獵顧鏇蓋憲蓋鏇憲顧鹹 (範顧網廠鬱構衊遞鹽遞 ) 更多 | 积极 | 2022-11-15 | |||
临床2期 | 22 | (Arm 1 (Q4W)) | 獵蓋醖鑰膚簾憲蓋膚願(鏇鹽廠網壓簾選膚築糧) = 觸膚鹹選夢鬱簾夢鏇糧 鏇製餘獵鏇鹽憲遞鹹衊 (構鬱壓夢壓築選遞鹹構 ) | 积极 | 2022-11-15 | ||
(Arm 2 (Q2W)) | 獵蓋醖鑰膚簾憲蓋膚願(鏇鹽廠網壓簾選膚築糧) = 鑰觸獵淵製壓夢築蓋鹽 鏇製餘獵鏇鹽憲遞鹹衊 (構鬱壓夢壓築選遞鹹構 ) |
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或

药物交易
使用我们的药物交易数据加速您的研究。
登录
或

核心专利
使用我们的核心专利数据促进您的研究。
登录
或

临床分析
紧跟全球注册中心的最新临床试验。
登录
或

批准
利用最新的监管批准信息加速您的研究。
登录
或

特殊审评
只需点击几下即可了解关键药物信息。
登录
或

生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用



